 25.11.2023
25.11.2023
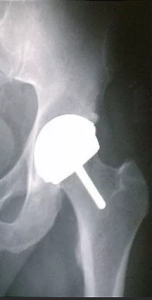
Ревизионное эндопротезирование тазобедренного сустава у больных со стабильным феморальным компонентом
Согласно данным отечественной и зарубежной литературы, изолированная асептическая нестабильность вертлужного компонента является одной из наиболее частых причин для проведения ревизионного вмешательства
Актуальность исследования
Согласно данным отечественной и зарубежной литературы, изолированная асептическая нестабильность вертлужного компонента является одной из наиболее частых причин для проведения ревизионного вмешательства и по данным различных авторов ее встречаемость колеблется от 20% до 80% [Николаев И.А., 2015; Waewsawangwong W. et al., 2016].
В настоящее время отсутствуют однозначные рекомендации в отношении стабильного правильно ориентированного бедренного компонента при хирургическом лечении изолированного асептического расшатывания чашки эндопротеза. Как правило, пациенты, которым планируется выполнить ревизионное вмешательство - довольно возрастные люди, поэтому психосоматический статус больных требует минимизации операционного риска (уменьшение продолжительности ревизионного эндопротезирования и объема интраоперационной кровопотери, сохранения костного массива тазобедренного сустава) и сохранения стабильного правильно ориентированного бедренного компонента [Piolanti N. et al., 2014; Stathopoulos I.P. et al., 2014; Nagoya S. et al., 2015; Kim Y.H., 2017]. В то же время, из-за встречающихся в практике нестандартных размеров конуса эндопротеза, необходимость замены стабильной правильно ориентированной ножки становится очевидной [Kerboull L., 2015; Fink B. et al., 2016; Laffosse, J.-M., 2016]. Имеющиеся противоречия и обусловливают актуальность исследования.
В настоящее время лишь в единичных научных работах представлены результаты ревизионного эндопротезирования тазобедренного сустава у больных со стабильным феморальным компонентом. Однако, встречаемость изолированной асептической нестабильности чашки эндопротеза, требующей проведения ревизионного вмешательства, колеблется в пределах от 20,0 до 80,0%, становясь максимальной к 10-12 годам от момента первичной артропластики. В работе De Thomasson и соавторов, представленной в 2012 году, были показаны исходы изолированной ацетабулярной ревизии, оцененные авторами как удовлетворительные, составившие 89,2 баллов по шкале Харриса. Количество пациентов, включенных в исследование, было 59. В 22,5% случаев отмечалось развитие осложнений в виде вывиха головки эндопротеза, повторного расшатывания чашки эндопротеза, перелома металлоконструкции и износа полиэтиленового вкладыша. В работе Megas и соавторов (2014 г.) были показаны результаты замены стабильных бедренных компонентов. Количество пациентов, включенных в исследование, составило 47. Экстракция бедренного компонента осуществлялась с применением остеотомии бедренной кости. Послеоперационный балл по шкале Харриса составил 83. Средняя продолжительность вмешательства - 174 минуты. В 82% случаев потребовалось переливание компонентов крови. Осложнения были зарегистрированы у 6 пациентов. В то же время стоит отметить, что сравнительный анализ тотальной и парциальной ацетабулярной ревизии по поводу асептической нестабильности вертлужного компонента эндопротеза тазобедренного сустава не был представлен в данных литературы.
Таким образом, на основании анализа данных литературы можно сделать вывод, что хирургическое лечение изолированной асептической нестабильности вертлужного компонента эндопротеза является актуальным и требует дальнейшего изучения для улучшения послеоперационных результатов.
Изучить перспективность сохранения стабильного правильно ориентированного бедренного компонента при ревизионном эндопротезировании тазобедренного сустава по поводу асептического расшатывания вертлужного компонента эндопротеза.
Задача исследования
1. Изучить варианты асептической нестабильности эндопротеза тазобедренного сустава и частоту возникающей необходимости замены стабильного бедренного компонента эндопротеза, вызванной нестандартным размером его конуса.
2. Определить влияние замены стабильного бедренного компонента эндопротеза на тяжесть ревизионного вмешательства и его результаты.
3. Оценить сроки выживаемости сохраненного стабильного бедренного компонента эндопротеза после замены нестабильного вертлужного компонента.
4. Изучить деформационный рельеф конуса бедренного компонента эндопротеза при повторных импакциях головки эндопротеза, на основе чего разработать и математически обосновать возможность применения адаптирующей конструкции при нестандартном конусе стабильного бедренного компонента, позволяющую использовать головку стандартных размеров.
Научная новизна
1. Изучена выживаемость сохраненного при ацетабулярной ревизии стабильного правильно ориентированного бедренного компонента в ближайшем и отдаленном периодах.
2. Изучен деформационный рельеф конуса бедренного компонента эндопротеза тазобедренного сустава при повторных установках головки эндопротеза.
3. Разработана адаптирующая металлоконструкция, позволяющая увеличить конус бедренного компонента эндопротеза до диаметра 12/14 мм и применить стандартную головку, сохранив стабильный правильно ориентированный бедренный компонент в случае его нестандартного дизайна при проведении ацетабулярной ревизии (патент РФ на изобретение № 2654275 от 17.05.2018 г.).
4. Изучено напряженно-деформированное состояние стандартной конструкции эндопротеза тазобедренного сустава и при условии установки предложенной металлоконструкции.
5. Определен коэффициент запаса прочности для стандартной конструкции эндопротеза тазобедренного сустава и при условии установки предложенной металлоконструкции при приложении различных нагрузок.
Теоретическая и практическая значимость работы
1. Доказана необходимость сохранения стабильного правильно ориентированного бедренного компонента при хирургическом лечении асептической нестабильности вертлужного компонента. Ацетабулярная ревизия по сравнению с тотальной характеризуется получением более высокого функционального результата и сокращением реабилитационных сроков.
2. Изучен деформационный рельеф конуса бедренного компонента при трехкратной импакции головки эндопротеза. Выявлены поверхностные пластические изменения контрящей насечки в виде «раздавливания» с максимальной концентрацией в области узкой части конуса. Грубой деформации металла при соблюдении условия «щадящего удаления головки эндопротеза» не наблюдалось.
3. Разработана адаптирующая металлоконструкция, которая позволит выполнять изолированную ацетабулярную ревизию с сохранением стабильного правильно ориентированного бедренного компонента эндопротеза с нестандартным размером конуса.
Методология исследования построена на системном и комплексном анализе данных. Методы, использованные в работе: клиническое обследование пациентов, анкетирование, лабораторные методы исследования, лучевые методы исследования, включавшие рентгенографию и мультиспиральную компьютерную томографию, конечно-элементное моделирование, метод оптической микроскопии, метод непосредственной оценки, метод контроля механических свойств металла, методы статического анализа.
1. Ревизионная замена вертлужного компонента и пары трения с сохранением стабильного правильно ориентированного бедренного компонента является приоритетным методом хирургического лечения пациентов с изолированной асептической нестабильностью вертлужного компонента эндопротеза.
2. При выполнении ацетабулярной ревизии по поводу изолированной асептической нестабильности вертлужного компонента сохраненный стабильный правильно ориентированный бедренный компонент сохраняет стабильность в течение длительного времени, что способствует достижению хороших результатов лечения.
Результаты настоящего исследования внедрены в работу травматолого-ортопедического отделения № 4 научно-исследовательского института травматологии, ортопедии и нейрохирургии ФГБОУ ВО «Саратовский ГМУ им. В.И. Разумовского» Минздрава России.
Выводы соответствуют задачам и логически следуют из результатов, полученных в ходе исследования. Достоверность результатов обоснована изучением достаточного объема материала и использованием современных методов, отвечающих поставленным задачам. Выбраны корректные методы статистического анализа.
Основные положения настоящего исследования доложены на: VI Евразийском конгрессе травматологов-ортопедов (г. Казань, 2017 г.); Научно-практической конференции с международным участием «Аспирантские чтения - 2017. «Научные достижения молодых ученых XXI века в рамках приоритетных направлений стратегии научно-технологического развития страны» (г. Самара, 2017 г.); XI Всероссийском съезде травматологов-ортопедов (г. Санкт- Петербург, 2018 г.); DKOU 2018 (г. Берлин, Германия, 2018 г.); Всероссийская онлайн конференция Молодых ученых «Актуальные вопросы травматологии и ортопедии» (г. Санкт- Петербург, 2020 г.); IV Международный конгресс ассоциации ревмоортопедов (г. Москва, 2020 г.).
Диссертация изложена на 182 страницах компьютерного текста и состоит из введения, 5 глав, заключения, выводов, практических рекомендаций, списка сокращений и литературы, включающего 157 источников, из них 131 зарубежных и 26 отечественных авторов, приложений. Работа иллюстрирована 40 таблицами и 69 рисунками.
В рамках научного поиска был осуществлен анализ показаний к проведению ревизионных вмешательств на базе травматолого-ортопедического отделения №4 НИИТОН ФГБОУ ВО «Саратовский ГМУ им. В.И. Разумовского» Минздрава России на протяжении 2014-2017 гг.
В указанный период в НИИТОН СГМУ было выполнено 560 ревизионных вмешательств после первичного эндопротезирования тазобедренного сустава. С 2014 по 2017 гг. отмечался рост проводимых операций в 1,8 раз (78 операций, 45,61%), что, по нашему мнению, связано с увеличением числа выполняемых артропластик в России.
Наиболее частыми причинами ревизии являлись: асептическое расшатывание - 47,5% (266 операций), инфекция - 36,1% (202 операции), вывихи - 10,7% (60 операций). Лидирующей по частоте причиной ревизии было асептическое расшатывание компонентов эндопротеза. Причем, изолированное расшатывание чашки эндопротеза встречалось в 1,9 раз чаще, чем ножки эндопротеза (различие - 64 операции, 24,1%) и в 2,7 раза чаще, чем тотальное расшатывание компонентов (различие - 87 операций, 32,8%). Тотальное расшатывание компонентов эндопротеза тазобедренного сустава было зарегистрировано у 52 пациентов (19,5%), изолированное расшатывание чашки эндопротеза - у 139 пациентов (52,3%), изолированное расшатывание ножки эндопротеза - у 75 пациентов (28,2%). Нестандартный типоразмер конуса шейки бедренного компонента был отмечен у 34 пациентов (24,5%). При этом, стоит отметить, что на протяжении с 2014 по 2017 гг. отмечался рост встречаемости нестандартного конуса ножки эндопротеза, что связано с увеличением сроков эксплуатации имплантов с нестандартным конусом (средний срок от момента первичного эндопротезирования до ревизионного вмешательства, выполненного в 2015 году, у пациентов с нестандартным типоразмером составил 5,88±1,39 лет, в 2016 году - 5,5±1,88 лет, в 2017 году - 7,16±1,05 лет).
С целью определения тактики в отношении стабильного правильно ориентированного бедренного компонента у больных с асептическим расшатыванием чашки эндопротеза тазобедренного сустава выполнено клинико-инструментальное обследование и ревизионное эндопротезирование 78 пациентов (79 вмешательств), находившихся на лечении в травматологоортопедическом отделении № 4 НИИТОН ФГБОУ ВО «Саратовский ГМУ им. В.И. Разумовского» Минздрава России с 2014 по 2017 гг.
Средний возраст пациентов составил 59±12,1 лет. Нетрудоспособные больные старше 60 лет, для которых снижение тяжести ревизионного вмешательства является важным компонентом в уменьшении уровня анестезиологического риска, составили 46,2%. Пациенты трудоспособного возраста, нуждающиеся в хороших функциональных результатах и сокращении сроков реабилитации для быстрейшего восстановления их социально-бытовой активности, составили 53,8%. Соотношение женщин и мужчин в исследовании 2:1 (49:29 - 62,8%: 37,2%). У 8 больных (10,3%) сопутствующей патологии по данным обследования, представленным на момент госпитализации, выявлено не было. У 70 пациентов (89,7%) отмечалось наличие патологии той или иной системы организма: сердечно-сосудистой (n=47, 60,3%), дыхательной (n=6, 7,7%), эндокринной (n=8, 10,3%), нервной (n=1,1,3%), мочевыделительной (n=3, 3,8%), пищеварительной (n=5, 6,4%). Коморбидность пациентов, оцененная при помощи шкалы Чарлсона, составила 3 [2; 4] балла.
Распределение по заболеваниям, потребовавшим проведения первичного ТЭП, было следующим: идиопатический коксартроз - 47 больных, диспластический коксартроз - 16 больных, АНГБК - 6 больных, медиальный перелом шейки бедренной кости - 5 больных, вторичный коксартроз - 4 больных. Оперативному вмешательству подверглись 37 (46,8%) левых и 42 (53,2%) правых тазобедренных сустава. У одного пациента (1,3%) изолированная замена вертлужного компонента эндопротеза производилась с двух сторон в связи с последовательным развитием асептической нестабильности ацетабулярного компонента в контрлатеральном тазобедренном суставе через 1 год после ревизионного вмешательства.
Впервые ревизионное вмешательство было осуществлено у 77 пациентов (78 ревизий - 98,7%), у 1 пациента (1,3%) - в третий раз. Средний срок от момента первичной операции до первичного ревизионного эндопротезирования - 6,8±0,4 лет. Средний срок наблюдения - 26±1,4 месяцев.
Основную группу составили 44 больных (45 суставов), которым в ходе оперативного вмешательства производилась парциальная ацетабулярная ревизия с заменой пары трения. Группу сравнения составили 34 пациента с изолированной асептической нестабильностью вертлужного компонента, которым было выполнено тотальное реЭП. Причиной удаления стабильного правильно ориентированного бедренного компонента являлось отсутствие головок под нестандартный дизайн конуса шейки ножки эндопротеза, фактический размер которого был установлен только в ходе вмешательства.
Группы сравнения были однородны по полу, возрасту, наличию сопутствующей патологии, индексу коморбидности, срокам от момента первичного эндопротезирования до ревизионной операции, костным дефектам вертлужной впадины согласно классификации W.G. Paprosky.
Обследование пациентов включало клиническое, инструментальное, лабораторное исследования и анкетирование. Осуществляли сбор жалоб, анамнестических данных и данных клинического осмотра. Всех больных на дооперационном этапе беспокоили болевой синдром различной степени выраженности и ограничение объема движений в пораженном суставе. Тест Stinchfield был положительным у всех 78 пациентов (79 суставов, 100%). У 70 пациентов (89,7%) отмечалось наличие гипотрофии мышц бедра со средним значением 1,62±0,16 см в основной группе и 1,85±0,19 см в группе сравнения (р=0,399) и мышц голени со средним значением 1,29±0,13 см в основной группе и 1,21±0,13 см (р=0,839). Укорочение конечности с пораженной стороны отмечалось у 34 пациентов и составило 0,73±0,14 см в основной группе и 1,03±0,23 см в группе сравнения (р=0,572).
Оценка функции тазобедренного сустава производилась при помощи шкалы HHS и шкалы OHS, согласно которым у всех 78 пациентов (79 суставов) до ревизионного вмешательства регистрировался неудовлетворительный результат. Среднее значение по шкале HHS в основной группе составило 27,73±0,71 балла и в группе сравнения - 28,15±0,67 балла (р=0,714), по шкале OHS в основной группе составило 14,04±0,32 балла и в группе сравнения - 13,47±0,33 балла (р=0,152).
Рентгенологическое исследование тазобедренных суставов в переднезадней и аксиальной проекциях осуществлялось с целью уточнения диагноза при помощи критериев нестабильности по зонам De Lee-Charnley. Анализ интеграции ацетабулярного компонента показал наличие его нестабильности у всех 78 пациентов (79 суставов): миграция вертлужного компонента - 12 (15%); вывих чашки эндопротеза - 16 (20%); линия «просветления» вокруг чашки эндопротеза не менее 2/3 ее окружности в зонах De Lee-Charnley шириной более 2 мм - 36 (46%); перелом фиксирующих винтов - 1 (1%); износ полиэтиленового вкладыша - 3 (4%); сочетание двух и более признаков - 11 (14%). Стабильность бедренного компонента по данным рентгенологического исследования в зонах Gruen подтверждалась отсутствием признаков остеолизиса вокруг ножки эндопротеза (линия просветления < 2 мм) и состоянием перипротезной костной ткани в пределах «хорошая - отличная» у всех 78 пациентов (79 суставов).
Компьютерная томография тазобедренного сустава с захватом бедренной кости, выполненная у 55 пациентов, использовалась с целью определения типа костного дефекта вертлужной области и угла антеверсии ножки эндопротеза. Средние значения антеверсии показателя составили 9,4±0,36 градуса.
Подтверждение асептического генеза нестабильности чашки включало клинический осмотр пациента (отсутствие отделяемого из раны, покраснения, припухлости и болезненности в области послеоперационного шва, отсутствие свищевых ходов в пораженный сустав), оценку лабораторных показателей (содержание WBC (4-10*1012/л) и СОЭ (0-30 мм/час) в пределах значений нормы, С-РБ - отрицательный (0-10 мг/л), отсутствие сдвига лейкоцитарной формулы влево), предоперационное микробиологическое исследование пунктата пораженного тазобедренного сустава (посев роста не дал у всех 78 пациентов (79 суставов, 100%), интраоперационный анализ содержания лейкоцитарной эстеразы в пунктате тазобедренного сустава и оценку параэндопротезных тканей (отсутствие патологических грануляций, гнойного расплавления тканей и мутной гнойной синовиальной жидкости).
Предоперационное планирование и подготовка больных осуществлялись согласно утвержденному протоколу Минздрава России «Эндопротезирование тазобедренного сустава».
Всего было пролечено 78 пациентов (79 ревизий), ревизионное вмешательство которым осуществлялось с применением переднебокового доступа под комбинированной анестезией.
Результаты исследования
Оценка тяжести хирургического лечения
Для оценки тяжести хирургического вмешательства анализировали следующие показатели: продолжительность оперативного вмешательства, объем интраоперационной кровопотери, частоту и объем интра- и послеоперационной гемотрансфузии, послеоперационные показатели красной крови (RBC, HGB, HCT). В основной группе с проведенной парциальной ацетабулярной ревизией показатели тяжести ревизионного вмешательства были следующими: продолжительность оперативного вмешательства - 83,1±4,5 минут, объем интраоперационной кровопотери - 408,9±32,9 мл, частота гемотрансфузии - 31% (14 пациентов), объем перелитой свежезамороженной плазмы - 0 [0; 350] мл, объем перелитой эритроцитарной массы - 0 [0; 459] мл, среднее содержание эритроцитов - 3,99±009*1012/л, средние показатели гемоглобина - 116,29±2,51 г/л, средние показатели гематокрита - 0,35±0,008 л/л. В группе сравнения с тотальной ревизией: продолжительность оперативного вмешательства - 128,8±3,1 минут, объем интраоперационной кровопотери - 1072,1±71,9 мл, частота гемотрансфузии - 58,8% (20 пациентов), объем перелитой свежезамороженной плазмы - 545 [0; 600] мл, объем перелитой эритроцитарной массы - 449,5 [0; 736] мл, среднее содержание эритроцитов - 3,73±0,11*1012/л, средние показатели гемоглобина - 107,65±3,19 г/л, средние показатели гематокрита - 0,32±0,009 л/л. Сравнение средних величин показателей тяжести ревизионного вмешательства в основной группе и группе сравнения при помощи непараметрического критерия Манна-Уитни в связи с опровержением гипотезы о нормальности распределения показало, что удаление стабильного правильно ориентированного бедренного компонента при асептическом расшатывании чашки эндопротеза статистически значимо удлиняло продолжительность оперативного вмешательства в 1,5 раза (на 45 минут или 35%, р=1,9*10-10), увеличивало объем интраоперационной кровопотери в 2,6 раза (на 663 мл или 62%, р=6,8*10-12), сопровождалось значительным снижением показателей красной крови в 1,09 раз (уменьшение значений эритроцитов на 0,65*1012/л (16,58%, р=0,02), гемоглобина на 11 г/л (9,7%, р=0,01), гематокрита на 0,05 л/л (13,88%, р=0,01) и повышало объем проводимой интра- и послеоперационной гемотрансфузии эритроцитарной массы в 1,9 раза (на 204,8 мл, 48%, р=0,03).
Оценка результатов хирургического лечения
Ближайшие и отдаленные результаты лечения были прослежены у всех 78 пациентов (79 вмешательств). Результат лечения считали хорошим при отсутствии клинических и рентгенологических признаков развития нестабильности компонентов эндопротеза. В группе сравнения хороший результат лечения был получен у всех 34 пациентов (34 ревизии - 100%), в основной группе - у 42 пациентов (43 ревизии - 95,5%). У 2 больных (2 ревизии - 4,5%) с изолированной заменой вертлужного компонента был зарегистрирован неудовлетворительный результат, потребовавший проведения повторного ревизионного вмешательства, в связи с развитием асептической нестабильности чашки эндопротеза в одном случае (1 пациент) и глубокого параимплантарного нагноения в другом (1 пациент).
Клиническая оценка результатов включала анализ послеоперационного болевого синдрома, объема движений в тазобедренном суставе, укорочения оперированной конечности и проведение специфического теста Stinchfield.
Выраженность послеоперационного болевого синдрома в основной группе по шкале ВАШ составила 0,86±0,23, а в группе сравнения - 1,18±0,22.
При оценке объема движений в оперированном тазобедренном суставе у 42 пациентов основной группы (43 ревизии - 95,5%) и всех 34 пациентов группы сравнения результат регистрировался в пределах значений нормы. У 2 пациентов (4,5%) в связи с развившимися у них послеоперационными осложнениями отмечалось значительное ограничение движений в оперированном суставе.
Клиническое измерение абсолютной и относительной длин конечностей, а также по данным послеоперационных рентгенограмм показало наличие укорочения со стороны оперированного тазобедренного сустава в пределах 1 см у 6 пациентов (13%) основной группы и у 7 пациентов (21%) группы сравнения. Равные длины конечностей отмечались у 38 больных (39 ревизий - 87%) с ацетабулярной ревизией и у 26 пациентов (79%) с тотальной ревизией.
Тест Stinchfield у 42 пациентов (43 ревизии - 95,5%) основной группы и 34 пациентов группы сравнения был отрицательным. У 2 пациентов (4,5%) с развившимися ранними послеоперационными осложнениями тест Stinchfield был положительным.
Признаки миграции компонентов эндопротеза были выявлены у 2 пациентов (4,5%) основной группы в связи с развитием асептической нестабильности чашки эндопротеза и глубокой перипротезной инфекции в оперированном тазобедренном суставе. У всех остальных 42 пациентов (43 сустава) основной группы и 34 пациентов группы сравнения компоненты эндопротеза оценены как стабильные без признаков дислокации с «хорошим» и «отличным» состоянием перипротезной костной ткани.
Оценка функционального результата
лечения осуществлялась при помощи шкалы HHS и
шкалы OHS на 10-е послеоперационные сутки, через
3, 6 и 12 месяцев. Полученные данные сведены в графики и представлены
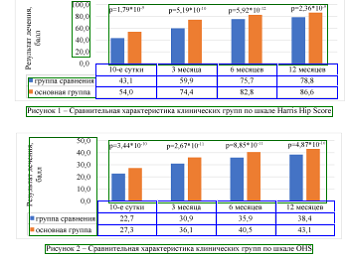
Необходимо отметить, что восстановление пациентов с сохранением стабильного правильно ориентированного феморального компонента происходило быстрее и уже к 6 месяцам после ревизионного вмешательства находилось на достаточно высоком уровне.
Анализ взаимосвязи между показателями тяжести ревизионного
вмешательства и по результатам
С целью выявления взаимосвязи между показателями, определяющими тяжесть ревизионного вмешательства, и результатами лечения по шкале Харриса через 1 год после оперативного вмешательства была построена корреляционная матрица и определен коэффициент Спирмена. Было выявлено, что между послеоперационными показателями красного ростка крови и результатами ревизионного вмешательства имеется положительная связь слабой силы, указывающая на улучшение результата лечения при увеличении показателей красной крови. Коэффициент Спирмена между послеоперационным содержанием эритроцитов и результатом лечения составил 0,119, между гемоглобином и баллами по шкале Харриса 0,155 и между гематокритом и послеоперационными результатами 0,150. Отрицательная корреляция средней силы прослеживалась между объемом интраоперационной кровопотери и баллами по шкале Харриса, определенными через 1 год после вмешательства (r=-0,509). Соответственно, с увеличением объема интраоперационной кровопотери результат оперативного лечения ухудшается. Также отрицательная корреляция средней силы была отмечена и между продолжительностью оперативного вмешательства и результатом лечения (r=-0,609).
Анализ выживаемости сохраненного бедренного компонента при выполнении
Выживаемость компонентов эндопротеза в основной группе с сохранением стабильного правильно ориентированного бедренного компонента была оценена при помощи таблиц дожития и метода Каплана-Мейера. Завершением службы эндопротеза считали проведение повторного ревизионного вмешательства на исследуемом тазобедренном суставе.
При анализе таблицы дожития функция выживаемости в начале исследования равна 1. Отказ эндопротеза в виде развития осложнения был отмечен во 2 и 3 временных интервалах. Начиная с 4 временного интервала наблюдалось появление цензурированных больных, что сопровождалось снижением количества исследуемых и, соответственно, функции дожития. К концу исследования кумулятивная выживаемость составила 0,4.
Анализ плотности вероятности отказа имплантов показал ее минимальные значения в течение первых 3 лет после начала исследования. В последующем, отмечалось постепенное увеличение вероятности развития осложнений до 0,0017 (17 случаев на 10000 населения).
Функция мгновенного риска у пациентов с изолированной ацетабулярной ревизией была минимальна в начале исследования и находилась на низком уровне до 3 лет. Далее отмечалось некоторое увеличение функции риска до 0,003 (3 случая на 1000 населения), что, вероятно, обусловлено длительной работой эндопротеза.
При оценке выживаемости компонентов эндопротеза методом Каплана-Мейера было показано, что событие «отказ эндопротеза» произошло в интервале с 10-го по 15-й и привело к снижению показателя с 1,0 до 0,9524±0,03.
В последующем, до окончания наблюдения таких событий не наблюдалось, что демонстрирует высокую выживаемость эндопротеза в группе с парциальной ацетабулярной ревизией.
Морфологические изменения конуса шейки бедренного компонента эндопротеза при ревизионном эндопротезировании тазобедренного сустава
С целью оценки постимплантационных изменений конуса шейки бедренного компонента был проведен анализ деформационного рельефа поверхности конуса шейки эндопротеза с количественной оценкой параметров рельефа (глубина циркулярных контрящих насечек) с использованием автоэмиссионного сканирующего электронного микроскопа MIRA 2 LMU (Tescan) в 3 зонах (зона узкой части конуса - зона 1, зона середины конуса - зона 2, зона широкой части конуса - зона 3) на различных структурных уровнях (объектив 200х, 500х, 2000х). Шейка эндопротеза фиксировалась в тисках с последующей троекратной импакцией и удалением головки эндопротеза с конуса бедренного компонента. Интактные имплантаты были представлены бедренным компонентом Corail (DePuy) и головкой эндопротеза кобальт-хром сплава (DePuy).
Анализ поверхности интактного конуса бедренного компонента показал, что по окружности образца имеются технические дефекты, образованные при повороте механизма, наносящего контрящую насечку. Глубина насечек, измеренная на максимальном увеличении 2000х, равнозначна во всех изучаемых зонах и варьирует от 0,82 мкм до 1,91 мкм. Среднее значение показателя составило 1,32 мкм.
После проведения 1 цикла «импакция - снятие головки эндопротеза» показатель рельефа образца регистрировался на прежнем уровне и был сопоставим во всех 3 зонах на макро-, микро- и наноуровне, составляя 1,38 мкм.
По всей поверхности изучаемого образца были определены дефекты снятия, представлявшие собой локальное раздавливание контрящей насечки. Ширина дефектов увеличивалась в направлении от зоны 3 к зоне 1, достигая максимальных величин в основании узкой части конуса и составляя соответственно 30 мкм, 35 мкм, 70 мкм. Частота возникающих дефектов не зависела от зоны исследования и составляла в среднем 2 повреждения на 416 мкм.
После проведения 2 цикла испытаний отмечалось снижение глубины контрящей насечки исследуемого образца в 1 и 2 зонах. Показатель рельефа в 3 зоне фиксировался на прежнем уровне. Среднее значение глубины насечек составило 1,12 мкм. Ширина дефектов на поверхности исследуемого образца после 2 цикла испытаний в 1 и 3 зонах составила соответственно 80 мкм и 40 мкм. Во 2 зоне ширина дефекта оставалась на прежнем уровне и составляла 35 мкм. Частота возникающих дефектов регистрировалась на прежнем уровне и составляла 2 дефекта на 416 мкм. Помимо дефектов в виде локального раздавливания насечек, после проведенного 2 цикла испытаний на поверхности образца во всех 3 зонах фиксировалась дополнительная поверхностная линейная исчерченность металла.
Третий цикл испытаний сопровождался сохранением показателя рельефа на прежнем уровне (средняя глубина контрящей насечки - 1,22 мкм), сопоставимого во всех 3 зонах образца на различных уровнях измерений. Ширина «дефектов снятия» регистрировалась на прежнем уровне в зонах 2, 3 и составила 35 и 40 мкм соответственно. В зоне 1 отмечалось увеличение ширины повреждения до 120 мкм. Частота дефектов не зависела от количества проведенных циклов и по-прежнему составляла 2 повреждения на 416 мкм.
Таким образом, при первичном удалении головки эндопротеза деформация рельефа конуса бедренного компонента являлась незначительной, а глубина контрящих насечек сохранялась на достаточном уровне.
Решение вопроса нестандартного размера конуса шейки феморального компонента
Для возможности сохранения стабильного правильно ориентированного феморального компонента с нестандартным конусом и замены пары трения при изолированной ревизии ацетабулярного компонента в случае его асептической нестабильности, нами была предложена металлоконструкция, позволяющая восстановить внешний размер конуса до стандартных величин 12/14 мм. Металлоконструкция представляет собой переходник усеченной конусовидной формы, выполненный из аналогичного эндопротезу металла, надеваемый на конус шейки эндопротеза, с последующей установкой на него головки. Внутренний диаметр предлагаемого устройства соответствует внешним размерам нестандартного конуса шейки эндопротеза и составляет 11 и 13 мм. Внешний диаметр металлоконструкции равен внутреннему размеру выемки головки эндопротеза и составляет 12 и 14 мм. Толщина стенки устройства - 0,5 мм. По внешней и внутренней поверхности нанесена циркулярная контрящая насечка глубиной 2 мкм.

Рисунок 3 - Предлагаемое устройство для стандартизации конуса эндопротеза
Анализ химического элементного состава разработанного переходника, выполненного в системе микроанализа AztecLive Advanced Ultim Max 40, производился на 3 случайно выбранных участках образца. Детектирование спектра характеристического рентгеновского излучения, генерируемого в зоне взаимодействия первичного пучка ускоренных электронов с образцом, показало, что химический состав металлоконструкции представлен кислородом (O), титаном (Ti) и алюминием (Al), процентное содержание которых незначительно варьирует в зависимости от локализации спектра. Среднее содержание кислорода в образце составило 3,02±0,21%, титана - 92,31±0,14%, алюминия - 4,66±0,19 %.
Исследование морфологии поверхности разработанного образца, выполненное с использованием автоэмиссионного сканирующего электронного микроскопа MIRA 2 LMU (Tescan), установило, что по всей поверхности образца располагаются однотипные циркулярно нанесенные насечки глубиной 1,7-2,5 мкм. Погрешность нанесения насечки, оцененная на увеличении 2000x, составила 0,5 мкм, что соответствует высокой точности механического цикла.
Возможность применения предлагаемой металлоконструкции была оценена при помощи математического моделирования методом конечных элементов при помощи программных комплексов Ansys Wоrkbench. Для описания поведения металлоконструкций в Ansys Workbench использовалось уравнение движения сплошной среды (Навье - Ламе). Элементы модели бедренной кости были разбиты на тетраэдрическую нерегулярную сетку с ребром 0,003 м. На модели элементов металлоконструкций была наложена регулярная гексаэдрическая сетка с ребром 0,002 м. В среднем общее количество элементов составило 18783, а общее количество узлов 46064.
К поверхности головки эндопротеза были приложены нагрузки 1050 Н, соответствующие средней массе человека в 105 кг, который стоит на одной ноге (в процессе ходьбы). В результате численного эксперимента была проведена оценка напряженно-деформированного состояния (НДС) (распределение значений деформации и эквивалентных напряжений (ЭН)) для стандартной системы «бедренная кость - бедренный компонент - головка эндопротеза» и при добавлении разработанного переходника.
Биомеханическое моделирование позволило определить, что наименьшие максимальные значения деформации, равные 0,0412 мм, достигались в модели с добавлением переходника. В модели стандартной конструкции максимальные значения деформации достигли 0,102 мм. При оценке эквивалентных напряжений выявлено равномерное распределение значений по поверхности металлоконструкций в зоне контакта с тканями бедренной кости.
Стоит отметить, что для всех моделей металлоконструкций значения ЭН оказались не более 300 МПа), что существенно ниже предела текучести (разрушения) материала. Максимальные значения ЭН в стандартной конструкции достигали 77,2 МПа, что на 7,38% выше максимальных значений ЭН в конструкции с добавлением предлагаемого переходника (71,5 МПа). Анализ максимальных значений ЭН в головках моделей металлоконструкций показал, что наибольшие показатели достигались в стандартной конструкции (нагрузка 1050 Н - 45,6 МПа), в то время как в конструкции с добавлением переходника они были на 53,73% меньше (нагрузка 1050 Н - 21,1 МПа). Это можно объяснить тем, что переходник в оптимизированной конструкции за счет своего геометрического строения разгружает головку металлоконструкции, принимая часть нагрузки на свой объем.
Рассчитанный коэффициент запаса прочности при максимальных нагрузках как в модели стандартной конструкции, так и в модели с добавлением разработанного переходника (11,1 и 12,0 соответственно) в 5 раз превышал стандартный показатель для пластичных металлов.
Стендовые испытания предлагаемой металлоконструкции, проведенные с помощью настольной одноколонной испытательной машины Instron 5944 с приложением нагрузки Р 1050 Н к испытуемому образцу (головка эндопротеза DePuy - разработанный переходник - бедренный компонент с нестандартным конусом) и количеством циклов «сжатие-растяжение» 100000 раз показали, что линейные размеры предлагаемой конструкции не изменяются при нагрузках и регистрируются на заявленном уровне (толщина стенки 0,5 мм, внешний диаметр в области узкого конуса 12 мм, в области широкого конуса 14 мм). Значения деформационного рельефа поверхности образца до и после приложения динамической нагрузки были сопоставимы между собой вне зависимости от исследуемого уровня. Глубина контрящей насечки колебалась в диапазоне от 1,65 до 2,59 мкм. В области узкого конуса исследуемого образца после приложения нагрузки и снятия головки эндопротеза отмечалось наличие линейных дефектов, соответствующих области концентрации максимальных напряжений. Глубина дефектов не превышала 0,5 мкм.
Таким образом, проведенное исследование позволяет утверждать, что сохранение стабильного правильно ориентированного феморального компонента позволяет уменьшить продолжительность ревизионного вмешательства, снизить объем интраоперационной кровопотери, улучшить послеоперационные показатели красной крови, тем самым улучшая послеоперационный результат лечения и ускоряя процесс реабилитации пациентов.
Результаты сохранения стабильного правильно ориентированного феморального компонента у пациентов с изолированной асептической нестабильностью вертлужного компонента в сроки наблюдения до 4 лет оказались многообещающими и требуют дальнейшего исследования и более длительного наблюдения, а метод изолированной замены ацетабулярного компонента с сохранением стабильного правильно ориентированного феморального компонента является методом выбора у пациентов с асептической нестабильностью чашки эндопротеза.
Выводы
1. Среди случаев асептической нестабильности тазобедренного сустава изолированная нестабильность вертлужного компонента при стабильном бедренном компоненте отмечена в 52,3 % наблюдений. Нестандартные размеры конуса бедренного компонента привели к необходимости тотальной замены эндопротеза при изолированной нестабильности лишь вертлужного компонента в 24,5 % наблюдений.
2. Необходимость замены стабильного бедренного компонента при ревизионном эндопротезировании привела к увеличению средней продолжительности операции в 1,5 раза, объема интраоперационной кровопотери в 2,6 раза и частоты гемотрансфузий в 1,9 раз. Сроки реабилитации после тотальной замены эндопротеза были продолжительнее в 2 раза, чем при сохраненном бедренном компоненте, средний показатель по шкале Харриса через 1 год был хуже на 7,8 баллов, а по Оксфордской шкале - на 4,7 балла.
3. Выживаемость сохраненного стабильного бедренного эндопротеза после замены его нестабильного вертлужного компонента составила 0,9524 в течение 4 лет после операции, и характеризуется низкими значениями функции мгновенного риска, составившими 0,003 к концу исследования.
4. При повторных импакциях головки эндопротеза отмечалось снижение глубины контрящей насечки конуса шейки бедренного компонента на 0,26 мкм и образование «дефектов снятия» в виде локального раздавливания металла с преимущественным формированием их в области узкой части конуса. Ширина повреждений зависела от количества установок головок эндопротеза и после 3-го снятия достигала 120 мкм в области узкой части конуса, 35 мкм в середине конуса, 40 кмм в области широкой части конуса. Разработанная модель адаптирующего устройства позволяет при нестандартных размерах конуса стабильного бедренного компонента сохранить его во всех случаях.
Практические рекомендации
1. Парциальная ацетабулярная ревизия является методом выбора в случае асептической нестабильности чашки эндопротеза и предоперационно и интраоперационно подтвержденной стабильности и правильной ориентации ножки эндопротеза без признаков механических повреждений и металлической коррозии.
2. Применение передне-бокового хирургического доступа при ревизии ацетабулярного компонента в условиях сохранения стабильного правильно ориентированного феморального компонента позволяет обеспечить адекватную визуализацию вертлужной впадины.
3. При выполнении парциальной ревизии для предотвращения механического повреждения конуса бедренного компонента инструментами во время операции головку эндопротеза необходимо снимать непосредственно перед импакцией примерочного образца.
4. Трудности с подбором новой головки эндопротеза при нестандартном размере конуса его бедренного компонента можно преодолеть, используя разработанную конструкцию, являющуюся переходным звеном и позволяющую применить головку стандартного размера 12/14 мм.
Литература
1. Зверева, К.П. Переднебоковой хирургический доступ при ревизии тазобедренного сустава со стабильным феморальным компонентом / К.П. Зверева, Д.А. Марков, А.Н. Решетников, В.Н. Белоногов, А.В. Зарецков // Современные проблемы науки и образования. - 2017. - № 5. - С. 124-128.
2. Марков, Д.А. Среднесрочные результаты лечения изолированной асептической нестабильности вертлужного компонента эндопротеза тазобедренного сустава / Д.А. Марков, К.П. Зверева, А.Н. Решетников, С.И. Киреев // Современные проблемы науки и образования. - 2017. - № 5. - С. 109-114.
3. Зверева, К.П. Хирургическое лечение изолированной асептической нестабильности вертлужного компонента эндопротеза тазобедренного сустава / К.П. Зверева, Д.А. Марков, А.Н. Решетников // Саратовский научно-медицинский журнал. - 2017. - Т.13, №3. - С.502-506.
4. Зверева, К.П. Асептическая нестабильность ацетабулярного компонента при нестандартном дизайне стабильного бедренного компонента / К.П. Зверева, Д.А. Марков, В.Н. Белоногов, А.Е. Бычков // В сб.: Интегративная медицина. 10 лет журналу Политравма. - 2017. - С.55.
5. Марков, Д.А. Выбор оперативного доступа при лечении асептической нестабильности ацетабулярного компонента эндопротеза тазобедренного сустава / Д.А. Марков, К.П. Зверева // В сб.: Илизаровские чтения. - Курган, 2017. - С.149.
6. Зверева, К.П. Отдаленные результаты ревизионного эндопротезирования тазобедренного сустава пациентов с изолированной асептической нестабильностью вертлужного компонента / К.П. Зверева, Д.А. Марков // В сборнике: Евразийский Ортопедический Форум. - М., 2017. - №224.
7. Марков, Д.А. Отдаленные результаты ревизионного эндопротезирования тазобедренного сустава пациентов с нестабильностью вертлужного компонента / Д.А. Марков, К.П. Зверева // В сб.: VI Евразийский конгресс травматологов-ортопедов. - Казань, 2017. - С.96.
8. Марков, Д.А. Хирургическое лечение изолированной асептической нестабильности вертлужного компонента у пациентов со стабильным феморальным компонентом / Д.А. Марков, К.П. Зверева, В.Н. Белоногов, А.Е. Бычков // В сб.: Актуальные вопросы травматологии - ортопедии Сибири и Дальнего Востока. - Ленинск-Кузнецкий, 2017. - С.92-96.
9. Зверева, К.П. Стабильный феморальный компонент при лечении изолированной асептической нестабильности вертлужного компонента: сохранять или удалять? / К.П. Зверева, Д.А. Марков // В сб.: Аспирантские чтения - 2017. «Исследования молодых ученых XXI века в рамках приоритетных направлений стратегии научно-технологического развития страны». - Самара, 2017. - С.21.
10. Марков, Д.А. Хирургическое лечение изолированной асептической нестабильности вертлужного компонента у пациентов со стабильным феморальным компонентом / Д.А. Марков, К.П. Зверева, А.В. Сертакова, В.Н. Белоногов, А.Ю. Трошкин // Вестник Российской академии медицинских наук. - 2018. - № 3. - С.164- 171.
11. Зверева К.П., Марков Д.А., Павленко Н.Н., Киреев С.И., Белоногов В.Н. Патент на изобретение №2654275, приор. от 09.01.2017 г., опубл. 17.05.2018 г., БИ № 14 «Способ ревизионного эндопротезирования тазобедренного сустава и устройство для его осуществления».
12. Марков, Д.А. Медикаментозное ведение пациентов после тотального эндопротезирования тазобедренного сустава / Д.А. Марков, К.П. Зверева, Н.Н. Павленко, В.Н. Белоногов // Гений ортопедии. - 2018. - №1. - С.44-49.
13. Зверева, К.П. Тотальная ревизионная артропластика при изолированной асептической нестабильности ацетабулярного компонента / К.П. Зверева, Д.А. Марков, А.Н. Решетников, П.А. Чернов, Н.Х. Бахтеева, К.К. Левченко // Гений ортопедии. - 2018. - №4. - С.444-449.
14. Марков, Д.А. Сохранение стабильного и правильно ориентированного феморального компонента у пациентов с асептической нестабильностью вертлужного компонента / Д.А. Марков, К.П. Зверева, В.Н. Белоногов // В сб.: Достижения российской травматологии и ортопедии. Материалы XI Всероссийского съезда травматологов-ортопедов. - СПб., 2018. - С.226-230.
15. Марков, Д.А. Результаты ацетабулярной ревизии у пациентов с асептической нестабильностью вертлужного компонента / Д.А. Марков, К.П. Зверева, А.Н. Решетников, А.Р. Шебалдов, Г.А. Адамович // Пироговский форум травматологов- ортопедов. Сб. материалов. - М., 2019. - С.200-201.
16. Зверева, К.П. Оценка напряженно-деформированного состояния бедренного компонента эндопротеза тазобедренного сустава с нестандартным размером конуса и с переходником для его стандартизации / К.П. Зверева, Д.А. Марков, А.А. Голядкина, А.В. Полиенко // Российский журнал биомеханики. - 2019. - Т. 23. - № 4. - С. 549-556.
17. Островский, В.В. Интраоперационные осложнения экстракции стабильного феморального компонента при ревизионном эндопротезировании тазобедренного сустава / В.В. Островский, К.П. Зверева, Д.А. Марков, А.В. Сертакова, А.Н. Решетников // Современные проблемы науки и образования. - 2020. - № 5.;
18. Зверева, К.П. Анализ выживаемости сохраняемого феморального компонента эндопротеза тазобедренного сустава при изолированном ацетабулярном ревизионном вмешательстве / К.П. Зверева, В.В. Островский, Д.А. Марков, А.В. Сертакова, А.Н. Решетников // Гений ортопедии. - 2021. - Т.27. - №5. - С. 521-526.
В настоящем диссертационном исследовании проведен сравнительный анализ тотальной и парциальной ацетабулярной ревизии тазобедренного сустава у больных с изолированной асептической нестабильностью вертлужного компонента и стабильным правильно ориентированным бедренным компонентом. Оценена выживаемость сохраняемой ножки эндопротеза в ближайшем и отдаленном послеоперационном периодах. Показано достоверно значимое снижение тяжести хирургического вмешательства и улучшение результатов лечения с сокращением реабилитационных сроков. Изучен деформационный рельеф конуса бедренного компонента при повторных импакциях головки эндопротеза. Результаты эксперимента демонстрируют поверхностные пластические изменения контрящей насечки в виде «раздавливания» с максимальной концентрацией в области узкой части конуса.
Грубой деформации металла при соблюдении условия «щадящего удаления головки эндопротеза» не наблюдалось. С целью оптимизации нестандартного размера конуса бедренного компонента предложена металлоконструкция, которая позволит стандартизировать конус до размера 12/14 мм.
Научный руководитель:
Островский Владимир Владимирович - Доктор медицинских наук, профессор кафедры травматологии и ортопедии ФГБОУ ВО «Саратовский ГМУ им. В.И. Разумовского» Минздрава России
Загородний Николай Васильевич - Доктор медицинских наук, профессор, член-корреспондент РАН, зав. кафедрой травматологии и ортопедии МИ РУДН, руководитель центра эндопротезирования суставов НМИЦ ТО (ЦИТО) им. Н.Н. Приорова
Каплунов Олег Анатольевич - Доктор медицинских наук, доцент, профессор кафедры травматологии, ортопедии и ВПХ ФГБОУ ВО ВолгГМУ Минздрава России
Ведущая организация: - Федеральное государственное бюджетное учреждение «Национальный медицинский исследовательский центр травматологии и ортопедии им. академика Г.А. Илизарова» Министерства здравоохранения Российской Федерации
Теги: эндопротезирование
234567 Начало активности (дата): 25.11.2023 18:55:00
234567 Кем создан (ID): 989
234567 Ключевые слова: тазобедренный сустав, эндопротезирование, суставы
12354567899
Похожие статьи
Рентген на дому 8 495 22 555 6 8Первый этап двухэтапного ревизионного эндопротезирования при перипротезной инфекции коленного сустава
«Шум керамики» как нежелательное явление в эндопротезировании тазобедренного сустава
Величина шеечно-диафизарного угла ножки эндопротеза тазобедренного сустава как биомеханическая предпосылка развития асептической нестабильности вертлужного компонента (экспериментальное исследование)
Применение индивидуального импланта при ревизионном эндопротезировании тазобедренного сустава с костным дефектом типа IV по Paprosky



