 09.09.2023
09.09.2023
Величина шеечно-диафизарного угла ножки эндопротеза тазобедренного сустава как биомеханическая предпосылка развития асептической нестабильности вертлужного компонента (экспериментальное исследование)
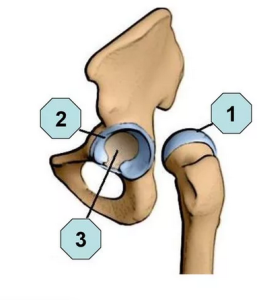
По данным компьютерной томографии построена биомеханическая модель таза и имплантат с различными вариантами величины шеечно-диафизарного угла бедренного компонента
ВВЕДЕНИЕ
Хирургическое лечение пациентов с асептическим расшатыванием эндопротезов тазобедренного сустава является одним из краеугольных камней современной ортопедии.
Несмотря на существенные различия в структуре ревизионных операций и их зависимость от множества факторов, асептическое расшатывание компонентов эндопротеза и остеолиз являются наиболее частыми причинами повторных оперативных вмешательств [1].
Одним из путей уменьшения количества ревизионных эндопротезирований и увеличения срока эксплуатации искусственного сустава после первичной артропластики является совершенствование биомеханических характеристик и дизайна имплантатов [2].
По мнению N. Ramaniraka с соавт. (2000), эндопротез тазобедренного сустава должен быть максимально адаптирован к индивидуальной анатомии конкретного пациента, а предпочтительным является восстановление функций тазобедренного сустава, приближенных к физиологическим. При этом на срок службы имплантата оказывают большое влияние как качество первичной фиксации, так и остеогенетические процессы на границе контакта имплантат - кость [3].
Традиционно с целью уменьшения эксцентрических изгибающих нагрузок, испытываемых ножкой эндопротеза, отдается предпочтение бедренным компонентам с вальгусными шеечно-диафизарными углами (ШДУ) [4]. При этом C. Shidlo с соавт. (1999) выявили, что ШДУ ножек искусственных суставов в среднем на 18° больше индивидуальных анатомических значений ШДУ пациента [5]. Также после тотальной артропластики тазобедренного сустава достаточно часто имеет место разница в длине конечностей [6-8]. Эти же исследователи изучали различные сочетания геометрических параметров бедренного компонента (ШДУ, антеверсия, длина шейки), от которых зависит распределение напряжений и контактного давления на границе ацетабулярного компонента и кости. Авторы пришли к выводу о существенном влиянии величины антеверсии ножки искусственного сустава на параметры напряженно-деформированного состояния контактной пары.
L. Quagliarella с соавт. (2006) в своем трехэтапном биомеханическом исследовании, базирующемся на изучении трехмерной модели A. Iglic с соавт. (2002) [9], собственной конечно-элементной модели и измерении контактного давления чашки по методу A. Strozzi с соавт. (1999) [10], оценивали влияние геометрических параметров ножки эндопротеза на распределение напряжений в шейке бедренного компонента и характеристики контактного давления на границе чашка - кость [1]. Авторами было установлено, что по мере возрастания ШДУ значения напряжений в шейке уменьшаются, однако контактное давление возрастает. По мнению авторов, величина ШДУ может влиять на стабильность имплантата, так как использование более варусных ножек будет способствовать снижению контактного давления и износа [1].
Цель исследования: провести сравнительный анализ результатов биомеханического моделирования бесцементного эндопротезирования тазобедренного сустава имплантатами с различными шеечно-диафи- зарными углами ножек применительно к изучению предпосылок развития асептического расшатывания ацетабулярного компонента.
МАТЕРИАЛЫ И МЕТОДЫ
На основе компьютерной томограммы (КТ) конкретного пациента, обработанной в программном комплексе Mimics, была построена твердотельная трехмерная геометрическая модель таза. Далее была использована программа 3Matic. Также по представленным реальным имплантатам были построены виртуальные твердотельные модели эндопротеза тазобедренного сустава бесцементной фиксации с клиновидной ножкой трех типов: с шеечно-диафизарными углами, равными 125°, 135° и 145°.
В дальнейшем в системе автоматизированного проектирования SolidWorks построенные модели эндопротеза тазобедренного сустава были размещены в модели таза в соответствии с общепринятой технологией их имплантации, применяемой в хирургической практике (расположение ацетабулярного компонента в анатомическом центре ротации с инклинацией 45°, антеверси- ей 15° и полным покрытием; расположение бедренного компонента с антеверсией 10°). Таким образом было получено три твердотельных трехмерных модели комплекса таз - тотальный бесцементный эндопротез тазобедренного сустава с различными ШДУ бедренного компонента.
Во всех моделях диаметр ацетабулярного компонента был равен 50 мм, диаметр головки - 28 мм.
Конечно-элементное моделирование нагружения построенных моделей выполнялось в системе Ansys 19.0.
Для каждой модели решалась статическая задача механики деформируемого твердого тела [12]. В качестве граничных условий к построенной модели прикладывалась осевая нагрузка, соответствующая весу человека при условии двухопорного стояния (к ножке эндопротеза прикладывалась нагрузка величиной 450 Н). Гребень подвздошной кости таза жестко фиксировали (рис. 1).
Все материалы считали идеально упругими, изотропными. Свойства материалов представлены в таблице 1. Модуль Юнга губчатой костной ткани рассчитывался индивидуально на основе данных КТ с помощью разработанной методики [13]. Свойства остальных материалов, представленных в таблице 1, брались из литературы [11, 12].
Таблица 1
Механические свойства тканей таза и материалов имплантата
|
Материал |
Модуль Юнга, МПа |
Коэффициент Пуассона |
|
Кортикальная кость |
11000 |
0,3 |
|
Губчатая кость |
200 |
0,3 |
|
Связка |
50 |
0,4 |
|
Вкладыш эндопротеза |
1100 |
0,33 |
|
(полиэтилен) |
||
|
Титановый сплав |
96000 |
0,36 |
Из-за сложности геометрии модели таза для расчета параметров его напряженно-деформированного состояния была создана нерегулярная тетраэдрическая вычислительная сетка (рис. 2). На моделях эндопротеза создавали более густую гексаэдрическую вычислительную сетку, позволившую получить результаты моделирования, мало зависящие от ее размера.
Полученные результаты биомеханического моделирования сопоставляли с результатами клинического и дополнительного инструментального исследования пациентов после первичного эндопротезирования тазобедренного сустава в отдаленном послеоперационном периоде.
РЕЗУЛЬТАТЫ
В результате расчетов были получены поля перемещений и эквивалентных напряжений в моделях, имеющих различные варианты шеечно-диафизарного угла клиновидного бедренного компонента эндопротеза. Типовые поля полных перемещений и эквивалентных напряжений представлены на рисунке 3.
Показательными являются характеристики эквивалентных напряжений, возникающих в полиэтиленовом вкладыше (табл. 2). Так, для моделей с ШДУ, равным 125°, его значение составило 1,3 МПа, для 135° - 2,7 МПа, а для 145° - 4,8 МПа. Эти данные свидетельствуют о не
избежном возрастании нагрузок на вкладыш при использовании типов ножек с большими значениями ШДУ.
Анализ значений контактного давления между головкой искусственного сустава и поверхностью его вкладыша коррелировал со значениями эквивалентных напряжений в нем.
Он также свидетельствует, что при использовании бедренного компонента с ШДУ 125° значения рассматриваемого параметра являлись наименьшими и составляли 1,2МПа. В то же время для ножек с ШДУ 135° и 145° они были равны 2,6 и 4,5 МПа соответственно.
Таблица 2
Эквивалентные напряжения во вкладыше и контактное давление между вкладышем и головкой эндопротеза
|
ШДУ бедренного компонента |
Эквивалентные напряжения, МПА |
Контактное давление, Мпа |
|
125° |
1,3 |
1,2 |
|
135° |
2,7 |
2,6 |
|
145° |
4,8 |
4,5 |
Далее были оценены эквивалентные напряжения, возникающие на поверхности костного ложа, контактирующего с поверхностью ацетабулярного компонента искусственного сустава. Для моделей с бедренным компонентом, имеющим шеечно-диафизарный угол, равный 125°, наибольшие эквивалентные напряжения на границе тазовая кость - чашка составили 0,56 МПА. Аналогичные значения рассматриваемого параметра для эндопротезов с ножками 135° и 145° градусов были равны, соответственно, 0,6 и 1,5 МПа (табл. 3).
Таблица 3
Наибольшие эквивалентные напряжения и контактное давление на поверхности контакта чашки эндопротеза и кости
|
ШДУ бедренного компонента |
Эквивалентные напряжения, МПА |
Контактное давление, МПа |
|
125° |
0,56 |
0,83 |
|
135° |
0,60 |
0,84 |
|
145° |
1,50 |
1,60 |
Изучение зависимости контактного давления от чашки эндопротеза на поверхности костного ложа от величины ШДУ ножки также свидетельствовало об увеличении значений изучаемой характеристики при имплантации более «вальгусных» бедренных компонентов. При использовании ножки эндопротеза с ШДУ 125° контактное давление составило 0,83 МПа, при ШДУ 135° - 0,84 МПа, а в случае применения бедренного компонента с ШДУ 145° возрастало до 1,60 МПа.
Анализ полученных данных убедительно свидетельствовал о скачкообразном увеличении значений эквивалентных напряжений и контактного давления на костную ткань таза на границе с поверхностью ацетабулярного компонента эндопротеза в случае использования ножки с ШДУ, равным 145°.
Особое внимание в нашем исследовании было уделено изучению локализации так называемого пятна контакта на сформированном для фиксации ацетабулярного компонента эндопротеза полусферической формы костном ложе, а также особенностям распределения внутри него эквивалентных напряжений и контактного давления.
Результаты моделирования продемонстрировали, что распределение изучаемых характеристик напряженно-деформированного состояния системы костьацетабулярный компонент эндопротеза происходит неравномерно и эксцентрично. Близкими к оптимальным являются локализация пятна контакта и распределение эквивалентных напряжений и контактного давления, характерные для эндопротезов с ножками, имеющими шеечно-диафизарные углы, равные 125° и 135° (рис. 4, 5).
Для модели эндопротеза, в которой был применен бедренный компонент с ШДУ, равный 145°, локализация пятна контакта на границе кость - поверхность ацетабулярного компонента, а также распределение эквивалентных напряжений и контактного давления внутри него оказались эксцентричными и характеризовались смещением кверху и кпереди, концентрируясь по краю чашки (рис. 6).
ДИСКУССИЯ
В случае применения в составе эндопротеза бесцементной фиксации бедренного компонента с шееч- но-диафизарным углом 145° эквивалентные напряжения, возникающие в полиэтиленовом вкладыше, а также контактное давление на границе поверхности вкладыша и головки искусственного сустава оказываются значительно выше, чем при использовании ножек с меньшими ШДУ. Полученные данные согласуются с результатами биомеханических исследований L. Ouagliarella с соавт. (2006). Однако, несмотря на высокие значения рассматриваемых параметров в искусственных суставах с более варусными ножками, нельзя говорить о том, что они могут приводить к усталостному разрушению полиэтилена, так как эти значения далеки от предела его прочности.
При этом существенный рост эквивалентных напряжений и контактного давления, характерный для имплантатов, бедренный компонент которых имеет ШДУ 145°, может стать предпосылкой к потере стабильности в системе кость - ацетабулярный компонент и привести к его асептическому расшатыванию.
Полученные данные полностью согласуются с результатами биомеханических исследований L. Ouagliarella с соавт. (2006) [4]. По мнению этих авторов, влияние ШДУ на параметры контактного давления имеет существенное значение, так как с уменьшением шеечно-диафизарного угла снижается износ и дебрис-ассоциированный остеолиз. Исследователи высказывают предположение, что применение ножек с ШДУ, равными 125°, показано у молодых пациентов с хорошим качеством костной ткани при условии достижения одинаковой длины нижних конечностей [4].
По данным нашего исследования, еще более важной предпосылкой к развитию нестабильности чашки эндопротеза представляется эксцентричная локализация пятна контакта на границе кости и ацетабулярного компонента, а также распределение контактного давления и эквивалентных напряжений внутри этого пятна, характерные для искусственных суставов с ножками, имеющими ШДУ 145°. Смещение пятна контакта вверх и вперед, а также концентрация напряжений в костной ткани по краю чашки являются механическими предпосылками к развитию асептической нестабильности имплантата. Эти данные, с нашей точки зрения, дополняют результаты исследования L. Ouagliarella с соавт. (2006) [4].
Сопоставление полученных данных, которые обосновывают потенциально более благоприятные условия для функционирования эндопротезов с меньшими ШДУ ножки, с анализом выживаемости таких имплантатов подтверждает результаты выполненного биомеханического исследования. Так, N. Edwards с соавт. (2017), проанализировавшие данные датского регистра эндопротезирования тазобедренного сустава, описывают, что ножки эндопротеза Symax, обладающие ШДУ, близким к изучаемому (128°), демонстрируют среднюю 6,5-летнюю выживаемость в более чем 97,5 % наблюдений [16]. Проведенный нами анализ данных австралийского регистра эндопротезирования тазобедренного сустава также показал высокую выживаемость эндопротезов, в которых использованы бедренные компоненты с ШДУ в диапазоне 125-135°. Так, для имплантатов с ножкой MS 30 (ШДУ124-135°) доля ревизий по поводу асептической нестабильности в течение 10 лет наблюдений варьировала в пределах 2,7-3,8 %. Для эндопротезов с ножкой Natural hip (ШДУ 130°) ревизии при асептической нестабильности в течение 10 лет достигали 2,4-4,1 %; для ножки Omnifit (ШДУ 127-132°) - 3,8-9,9 %; для бедренного компонента Secur-fit (ШДУ 127-132°) - 3,2-4,6 %; для ножки Summit (ШДУ 130°) - 3,4-8,9 %; для ножки Synergy (ШДУ 131°) - 2,9-3,9 %; для бедренного компонента Antology (ШДУ 131°) - 3,5-4,4 % соответственно [17].
ЗАКЛЮЧЕНИЕ
Таким образом, результаты биомеханического моделирования свидетельствуют, что величина шееч- но-диафизарного угла бедренного компонента эндопротеза может являться одной из биомеханических предпосылок к развитию асептического расшатывания ацетабулярного компонента искусственного сустава бесцементной фиксации. В частности, при использовании клиновидных ножек с ШДУ 145° имеет место смещение пятна контакта на границе чашки эндопротеза и кости вверх и вперед с неравномерным распределением эквивалентных напряжений и контактного давления по периферии ацетабулярного компонента.
Эндопротезы тазобедренного сустава с ножками, имеющими ШДУ 125° и 135°, характеризуются хорошо центрированным пятном контакта и равномерным распределением внутри него изучаемых параметров напряженно-деформированного состояния.
Вместе с тем, следует отметить, что представленное экспериментальное биомеханическое исследование имеет ряд ограничений. Последние связаны с моделированием нагрузки только в статическом вертикальном положении с опорой на обе нижние конечности без учета сокращения мышц, смещения центра тяжести тела и позиции компонентов эндопротеза при ходьбе. Также следует отметить, что сопоставление полученных результатов с информацией из регистров о выживаемости эндопротезов не учитывает возможное влияние на нее ряда других факторов [17].
СПИСОК ИСТОЧНИКОВ
1. National Joint Registry for England and Wales: 8th Annual Report // UK: NJR Centre Hemel Hemstead. 2011.
2. Kavanagh B.F., Ilstrup D.M., Fitzgerald R.H. Jr. Revision total hip arthroplasty // J. Bone Joint. Surg. Am. 1985. Vol. 67, No 4. P. 517-526.
3. Arthoplastie totale non cimentee de la anche: influence des parametres extra-medullaires sur la stabilite primaire de l’implant et sur les con- traintes a l’interfcace os/implant / N.A. Ramaniraka, L.R. Rakotomanana, PJ. Rubin, P. Leyvraz // Rev. Chir. Orthop. Reparatrice Appar. Mot. 2000. Vol. 86, No 6. P. 590-597.
4. Biomechanical effects of prosthesis neck geometries to contrast limb lengthening after hip replacement / L. Quagliarella, A. Boccaccio, L. Lamberti, N. Sasanelli // J. Appl. Biomater. Biomech. 2006. Vol. 4, No 1. Р. 45-54.
5. Anderung des CCD-Winkels sowie des femoralen Antetorsionswinkels durch Huftprothesenimplantation / C. Schidlo, C. Becker, V. Jansson, J. Refior // Z. Orthop. Ihre Grenzgeb. 1999. Vol. 137, No 3. Р 259-264. DOI: 10.1055/s-2008-1037404.
6. Surgical treatment of limb-length discrepancy following total hip arthroplasty / J. Parvizi, P.F. Sharkey, G.A. Bissett, R.H. Rothman, W.J. Hozack // J. Bone Joint. Surg. Am. 2003. Vol. 85, No 12. Р. 2310-2317.
7. Theruvil B., Kapoor V. Surgical treatment of limb-length discrepancy following total hip arthroplasty // J. Bone Joint Surg. Am. 2004. Vol. 86, No 8. Р. 1829. DOI: 10.2106/00004623-200408000-00039.
8. Maloney W.J., Keeney J.A. Leg length discrepancy after total hip arthroplasty // J. Arthroplasty. 2004. Vol. 19, No 4, Suppl. 1. Р. 108-115. DOI: 10.1016/j.arth.2004.02.018.
9. Computer determination of contact stress distribution and size of weight bearing area in the human hip joint / A. Iglic. V. Kralj-Iglic, M. Daniel, A. Macek-Lebar // Comput. Methods Biomech. Biomed. Engin. 2002. Vol. 5, No 2. P. 185-192. DOI: 10.1080/10255840290010300.
10. Strozzi A. Analytical modelling of the elastomeric layer in soft layer hip replacements // Proc. Inst. Mech. Eng. H. 2000. Vol. 214, No 1. P. 69-81. DOI: 10.1243/0954411001535255.
11. Biomechanical analysis of limited-contact plate used for osteosynthesis / M. Pochrz^st, M. Basiaga, J. Marciniak. M. Kaczmarek // Acta Bioeng. Biomech. 2014. Vol. 16, No 1. Р. 99-105. DOI: 10.5277/abb140112.
12. Доль А.В., Доль Е.С., Иванов Д.В. Биомеханическое моделирование вариантов хирургического реконструктивного лечения спондилолистеза позвоночника на уровне L4-L5 // Российский журнал биомеханики. 2018. Т. 22, № 1. С. 31-44.
13. Constructing the dependence between the Young’s modulus value and the Hounsfield units of spongy tissue of human femoral heads / L.V. Bessonov, A.A. Golyadkina, P.O. Dmitriev, A.V. Dol, VS. Zolotov, D.V Ivanov, I.V Kirillova, L. Yu. Kossovich, Yu. I. Titova, VYu. Ulyanov, A.V. Kharlamov // Izvestiya of Saratov University. A New Series. Series: Mathematics. Mechanics. Informatics. 2021. Vol. 21, No 2. Р. 182-193. DOI: 10.18500/1816- 9791-2021-21-2-182-193.
14. Primary total hip reconstruction with a titanium fiber-coated prosthesis inserted without cement / J.M. Martell, R.H. Pierson 3rd, J.J. Jacobs, A.G. Rosenberg, M. Maley, J.O. Galante // J. Bone Joint Surg. Am. 1993. Vol. 75, No 4. Р. 554-571. DOI: 10.2106/00004623-199304000-00010.
15. DeLee J.G., Charnley J. Radiological demarcation of cemented sockets in total hip replacement // Clin. Orthop. Relat. Res. 1976. No 121. P. 20-32.
16. Edwards N.M., Varnum C., Kj^rsgaard-Andersen P. Up to 10-year follow-up of Symax stem in THA: a Danish single-centre study // Hip Int. 2018. Vol. 28, No 4. P. 375-381. DOI: 10.5301/hipint.5000578.
17. Australian Orthopaedic Association National Joint Replacement Registry (AOANJRR). 2019 Annual Report. South Australia: Adelaide. 2019.
Информация об авторах:
1. Алексей Леонидович Кудяшев - доктор медицинских наук, доцент;
2. Владимир Васильевич Хоминец - доктор медицинских наук, профессор;
3. Дмитрий Валерьевич Иванов - кандидат физико-математических наук, доцент
4. Ирина Васильевна Кириллова - кандидат физико-математических наук;
5. Леонид Юрьевич Коссович - доктор физико-математических наук;
6. Павел Анатольевич Метленко - кандидат медицинских наук;
7. Виталий Викторович Чернышев.
Теги: эндопротезирование тазобедренного сустава
234567 Начало активности (дата): 09.09.2023 12:29:00
234567 Кем создан (ID): 989
234567 Ключевые слова: биомеханика, биомеханическое моделирование, метод конечных элементов, эндопротезирование тазобедренного сустава, асептическое расшатывание, эквивалентные напряжения, контактное давление
12354567899
Похожие статьи
Возможности хирургической коррекции деформаций позвоночника у пациентов с синдромом Ehlers-Danlos. Несистематический обзор«Синдромокомплекс» идиопатического сколиоза
Рентген на дому 8 495 22 555 6 8
Остеопороз в ракурсе оказания профильной травматолого-ортопедической помощи при низкоэнергетических переломах проксимального отдела бедренной кости
Экстренное гистологическое исследование в диагностике перипротезной инфекции при ревизионном эндопротезировании коленного сустава



