 11.12.2024
11.12.2024
Результаты лечения больных с осложнениями переломов костей предплечья
Несращения, ложные суставы, дефекты и посттравматические деформации являются сравнительно частыми осложнениями диафизарных переломов костей предплечья
Несращения, ложные суставы, дефекты и посттравматические деформации являются сравнительно частыми осложнениями диафизарных переломов костей предплечья. Их лечение представляет крайне сложную задачу для хирурга. Частота несращений костей предплечья в больших сериях наблюдений колеблется от 2 до 10% [1]. Часто имеются грубые анатомические и функциональные нарушения, связанные с изменением взаимоотношения костей, повреждением межкостной мембраны, что влечет за собой снижение ротационной функции предплечья и функции смежных суставов. Функциональные результаты оставляют желать лучшего и неудовлетворительны в 20–34% случаев [1, 2]. Это связано с необходимостью применения длительной внешней иммобилизации после операции и ограничением активной реабилитации из-за риска развития нестабильности или усталостного перелома конструкции [3, 4]. Реконструктивные операции у этих больных нередко выполняются на фоне выраженных контрактур вследствие предшествующего лечения, что также является крайне неблагоприятным прогностическим фактором для восстановления функции сегмента [5, 6, 7].
Наиболее распространенным вариантом остеосинтеза при лечении больных с осложнениями переломов костей предплечья является накостная фиксация отломков и трансплантата пластиной с винтами [8–10]. Следует отметить, что накостный остеосинтез обладает жесткой фиксацией и отсутствием амортизации при нагрузке, характеризуется большей травматичностью операции (обнажение отломков на большом протяжении, сверление отломков, дырчатые дефекты). Это, безусловно, нарушает кровоснабжение и негативно отражается на заживлении перелома [10]. При реабилитации все вышесказанное может скомпрометировать результат реконструкции (развитие нестабильности, отсутствие ассимиляции трансплантата с материнским ложем), поэтому проведение активного восстановительного лечения сразу после операции при этом виде фиксации рискованно. Использование интрамедуллярных стержней приводит к меньшему повреждению мягких тканей и сосудов, его удаление является малотравматичной процедурой и не требует обнажения области трансплантата. В отличие от компрессионных пластин, стержень распределяет нагрузку по длине, что способствует образованию периостальной мозоли и приводит к предсказуемому более прочному сращению перелома [2, 3].
Блокирующий интрамедуллярный остеосинтез (БИОС) является наиболее функциональным методом при минимальной операционной травме, позволяющим начать реабилитацию сразу после операции. Метод обеспечивает фиксацию c родственной стабильностью (relative fixation), то есть модуль упругости имплантата приближается к модулю упругости интактной кости, что обеспечивает свойство амортизации и нивелирует риски несостоятельности фиксации. Механический аспект микроподвижности между отломками и трансплантатом положительно сказывается на остеогенезе и заживлении перелома. Ось фиксатора совпадает с осью кости, в отличие от кортикального остеосинтеза, при котором ось фиксатора располагается сбоку от оси фиксируемой кости. БИОС широко используется при лечении несращений бедренной, большеберцовой и плечевой костей [9, 10]. Однако публикации по использованию блокируемых штифтов при несращениях костей предплечья немногочисленны [5, 6, 7], как и данные о тактических и технических аспектах хирургического лечения. Высокая частота неудовлетворительных результатов лечения данной патологии побудила нас к разработке комплекса лечебных мероприятий и новых решений для лечения этой сложной патологии.
Цели исследования: разработка алгоритма хирургического лечения больных с осложнениями диафизарных переломов костей предплечья и клиническая апробация предложенного комплекса.
Материал и методы исследования
Исследование ретроспективное. Изучались и анализировались исходы оперативного лечения больных с нарушениями консолидации переломов и посттравматическими деформациями костей предплечья в отделении травматологии и ортопедии СПб ГБУЗ «Городская Мариинская больница» за период 2006–2021 гг.
В группу исследования были отобраны пациенты, соответствовавшие следующим критериям включения: возраст старше 18 лет; несращение, псевдоартроз, дефект или посттравматическая деформация диафиза одной или обеих костей.
Критерии невключения: инфекционно-воспалительные процессы в области поврежденного предплечья в анамнезе; психическая неадекватность. Также исключены пациенты с невозможностью или нежеланием активного осознанного сотрудничества в процессе лечения.
Согласно этим критериям, в исследование были включены 22 пациента, возрастные характеристики представлены в таблице 1.
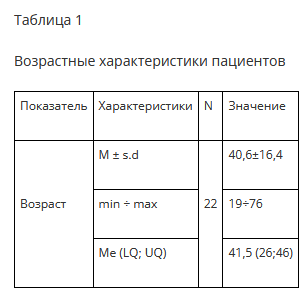
Женщин было 7 (31,8%), мужчин – 15 (68,2%). С последствиями переломов обеих костей было 8 (36,4%) пациентов, лучевой кости – 4 (18,2%), локтевой – 7 (31,8%) и переломовывихов – 3 (13,6%).
Осложнения переломов костей предплечья явились исходом консервативного и различных видов оперативного лечения:
- консервативного лечения у 4 (18,2%) пациентов;
- чрескостного остеосинтеза – у 3 (13,6%), в том числе у 2 реконструкция была вторым этапом лечения при открытых переломах III типа (Gustillo-Anderson);
- накостного остеосинтеза – 10 (45,5%), из них у 4 был отмечен перелом пластины, у 4 – нестабильность кортикального остеосинтеза и у 2 – рефрактура после удаления пластины;
- несращения на фоне интрамедуллярного остеосинтеза без блокирования – 3 (13,6%);
- периимплантного перелома при наличии несросшегося предшествовавшего – 2 (9,1%).
Комплекс лечебных мероприятий при осложнениях переломов костей предплечья в себя включает:
1) установление срока хирургического вмешательства;
2) предоперационное планирование, в том числе измерение дефекта по данным рентгенографии контрлатерального предплечья;
3) моделирование стержней и оценку нарушений взаимоотношений между костями;
4) определение очередности реконструирования и остеосинтеза костей;
5) технику устранения и контроля смещений;
6) забор аутотрансплантата;
7) замещение имеющихся костных дефектов с созданием биологических условий для сращения отломков;
8) фиксацию отломков и трансплантата и последовательность интраоперационных действий;
9) реабилитационный протокол.
При определении сроков оперативного вмешательства обращали внимание на выраженность имеющихся контрактур в локтевом, кистевом суставах, степень ограничения ротационных движений. При наличии таковых прекращали все виды иммобилизации и проводили курс активного реабилитационного лечения длительностью от 2 до 8 недель, направленного на восстановление движений, несмотря на имеющиеся несращения, дефекты костей и т.д. В редких случаях использовали иммобилизацию в пределах сегмента для исключения патологической подвижности без захвата смежных суставов. При внеочаговом остеосинтезе аппарат наружной фиксации должен быть снят с последующим курсом восстановительного лечения. Цель подобной тактики – добиться максимума восстановления функции конечности с устранением значительной доли контрактур до операции. При этом облегчается выполнение самой реконструктивной операции.
Моделирование стержней производили по рентгенограммам здорового предплечья. Имплантация моделированных стержней приводила к восстановлению кривизны костей [3].
Восстановлению взаимоотношений между костями уделяли самое пристальное внимание. Наш опыт показывает, что одной из причин несращений костей предплечья после остеосинтеза являются недостаточная репозиция и выпрямление кривизны костей и, как следствие, нарушение биомеханических взаимоотношений между лучевой и локтевой костями.
Последовательность реконструкции костей. Считается, что оптимальным подходом при остеосинтезе «свежих» переломов обеих костей предплечья является следующий: сначала более простой перелом, затем более сложный.
Еще один принятый ранее принцип: вначале остеосинтез локтевой, затем лучевой кости. Оба вышеуказанных подхода не всегда применимы при осложнениях переломов. Авторами использована следующая тактика. Первым этапом выполняли мобилизацию отломков обеих костей и производили релиз межкостной мембраны. Вторым этапом производили реконструкцию и остеосинтез локтевой кости с восстановлением ее физиологического изгиба.
После анатомического восстановления локтевой кости последняя оказывает шинирующее действие на лучевую, что упрощает манипуляции на ней. Третьим этапом реконструировали лучевую кость, также с восстановлением ее физиологического изгиба и длины.
Техника устранения смещений. Для устранения смещений отломков выполняли открытую репозицию отломков для контроля их положения. Рассматривая отдельно все виды смещений, следует отметить, что при правильном моделировании стержней при их имплантации происходит автоматическое устранение угловых смещений и смещений по ширине. Поскольку производится открытая репозиция и отломки визуализированы, контроль ротационного смещения достаточно легко осуществить по местам прикрепления межкостной мембраны к межкостному краю лучевой и локтевой костей. Для этого необходимо сопоставить межкостный край одного отломка межкостному краю другого. В случае затруднения их визуализации еще одним ориентиром для выравнивания ротации служат анатомические образования на проксимальных и дистальных отделах костей, которые можно отследить при интраоперационной рентгеноскопии.
На локтевой кости в строго боковой проекции венечный отросток расположен на 1800 по отношению к шиловидному. На лучевой кости в строго прямой проекции ее бугристость находится на 1800 по отношению к шиловидному отростку. Для выравнивания костей по длине использовали следующий алгоритм. При реконструкции измерялась длина дефекта при максимальной ручной или аппаратной тракции отломков. Трансплантат формировали на 2–3 мм длиннее имеющегося дефекта. При необходимости возможна коррекция (укорочение трансплантата). Первой реконструировали локтевую кость в положении максимальной тракции. При измерении имеющегося дефекта на лучевой кости ориентиром служит взаимоотношение костей в дистальном радиоульнарном сочленении, т.е. длину трансплантата необходимо формировать таким образом, чтобы при его имплантации соотношения в дистальном радиоульнарном сочленении были восстановлены.
«Краеугольные вопросы» замещения дефектов костей. Успех замещения дефектов костей предплечья заключается в соблюдении следующих принципов: выбор остеозамещающего материала с наиболее выраженными остеоиндуктивными и остекондуктивными свойствами; максимальный контакт трансплантата с материнским ложем и стабильность фиксации трансплантата и отломков. По нашему мнению, наилучшим материалом является аутотрансплантат из гребня подвздошной кости. Анатомически диаметр костей предплечья соответствует размерам гребня подвздошной кости.
Выполнение периостальной декортикации отломков является важным хирургическим приемом при восстановлении биологических условий консолидации при осложненных переломах любой локализации. Этот прием дает хороший остеоиндуктивный эффект. Рубцовый процесс в зоне осложненного перелома приводит к изменению межкостной мембраны. Для восстановления функции ротации необходимо произвести ее релиз с рассечением рубцовых спаек. Кроме того, эта манипуляция визуализирует место прикрепления мембраны к кости, которое служит ориентиром для восстановления ротационных взаимоотношений периферического и центрального отломков.
Расправление межкостной мембраны положительно сказывается на восстановлении трофики мягких тканей и восстановлении ротации предплечья.
Экономная резекция торцов отломков с удалением патологически измененной (склерозированной) костной ткани крайне важна для восстановления биологических условий сращения кости. Известно, что при комплексном исследовании кровоснабжения поврежденного сегмента конечности у пациентов с разными видами ложных суставов нарушение микроциркуляции является одной из главных причин нарушения сращения отломков. В условиях стабильной фиксации и удовлетворительного стояния отломков плохие исходы лечения находятся в прямой зависимости от выраженности склероза костной ткани в зоне ложного сустава. Рассверливание костномозгового канала при реконструкции костей предплечья преследует две цели: первая – подготовка канала к имплантации стержня, вторая – улучшение эндостального кровоснабжения вдоль стержня.
Техника хирургического вмешательства. Авторами были разработаны и запатентованы способы замещения дефектов костей предплечья, которые могут использоваться практически при большинстве ложных суставов, дефектов и несращений (приоритет № 2006119595, бюллетень № 36 от 27.12.2007 г.; патент RU2555117; патент RU2577937) [2]. Способы заключаются в замещении дефекта кости трансплантатом, помещенным в дефект, и проведении блокируемого остеосинтеза. Такой вид фиксации трансплантата исключает его миграцию и обеспечивает необходимую стабильность. Блокирующий стержень с винтами, проходящий через проксимальный, дистальный отломки и аутотрансплантат, действуют как единая система, при этом исключены риски несостоятельности при раннем активном функциональном лечении. Для точной адаптации трансплантата и отломков костей предплечья предложена и использована обработка торцов сферическими фрезами, что обеспечивает полный контакт между ними (RU2555117). Еще один способ заключается в краевой резекции кортикального слоя аутотрансплантата с торцов, при этом происходят сминание губчатой костной ткани и самоадаптация отломков и трансплантата (RU2577937).
Техника и последовательность манипуляций при реконструкции костей предплечья авторами строго определены и описаны ранее.
Реабилитационный протокол. После операции дополнительной фиксации не применяли, движения в суставах разрешали после хирургического этапа лечения операции. Несомненное значение это имеет при предшествовавшей длительной иммобилизации. При этом наблюдается развитие выраженных контрактур, в том числе ротационных. В случаях предшествовавших оперативных вмешательств проводили антибиотикопрофилактику в течение 3 дней.
Медикаментозная терапия: назначали прием препарата остеогенона (1 табл. – 830 мг) по 2–4 табл. 2 раза в сутки на срок от 2 до 6 месяцев.
Оценка результатов
Осмотр и рентгенографию в динамике выполняли на нескольких этапах. Это были 4, 6, 12, 18–24 месяцев от момента выполнения реконструктивной операции. Сроки наблюдения были от 12 до 36 месяцев (Ме – 12 месяцев). Пациентов наблюдали до полной консолидации отломков. Консолидации верифицировали рентгенологически.Таким образом, было запланировано 4 визита для осуществления этапного контроля, из которых обязательными являлись первые три.
1-й визит (4 месяца) – минимальный срок ожидаемой перестройки трансплантата и сращения перелома; 2-й визит (6 месяцев) – оценка предварительных результатов лечения и контрольная рентгенография; 3-й визит (1 год) – завершающий, окончание наблюдения и оценка результата лечения.
Результаты оценивали по следующим признакам: наличие сращения, наличие болевых ощущений, функция конечности и наличие осложнений. Оценку боли производили по Визуальной аналоговой шкале (ВАШ). Наличие сращения и восстановление взаимоотношений костей оценивали по данным контрольной рентгенографии или компьютерной томографии. Для оценки функциональных результатов использовали вопросник неспособности верхней конечности DASH (The Disabilities of the Arm, Shoulder and Hand Score) и сравнивали ротационные движения предплечья (пронация/супинация) с контрлатеральным предплечьем. Функциональный результат при оценке по DASH считали хорошим – от 0 до 20 баллов, удовлетворительным – от 20 до 50 и неудовлетворительным – более 50 баллов.
Статистический анализ
Полученные в исследовании клинические результаты для группы из 22 пациентов с осложнениями переломов костей предплечья были проанализированы с использованием программной системы STATISTICA for Windows (версия 10 Лиц. BXXR310F964808FA-V).
При проведении статистического анализа рассчитывали традиционные статистические показатели. Абсолютные значения и процентные доли в соответствующих задачам работы в группах определяли для качественных параметров.
Для сопоставления частотных характеристик (ротация, осложнения) с целью подтверждения достоверного превалирования положительного эффекта использовали критерий Фишера. Оценку динамики ВАШ выполняли с помощью критерия знаков.
Результаты исследования и их обсуждение
Результаты лечения отслежены у всех 22 (100%) больных.
Анатомические результаты представлены в таблице 2.
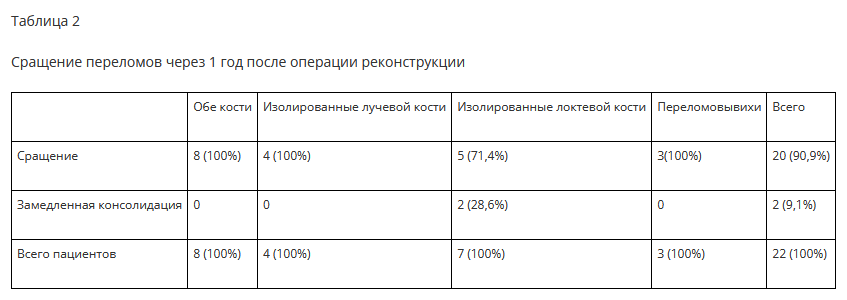
Консолидация достигнута у всех 22 (100%) больных. Достичь восстановления взаимоотношения между лучевой и локтевой костями удалось у всех больных. У 20 пациентов консолидация достигнута в срок от 4 месяцев до 1 года после операции.
У 2 больных с неоднократными ревизиями с применением накостного остеосинтеза до поступления в нашу клинику отмечался выраженный склероз костной ткани на протяжении пластины, что отрицательно повлияло на сроки консолидации, которые составили 18 и 24 месяцев соответственно.
Показатели оценки результатов по шкалам ВАШ и DASH представлены в таблице 3.
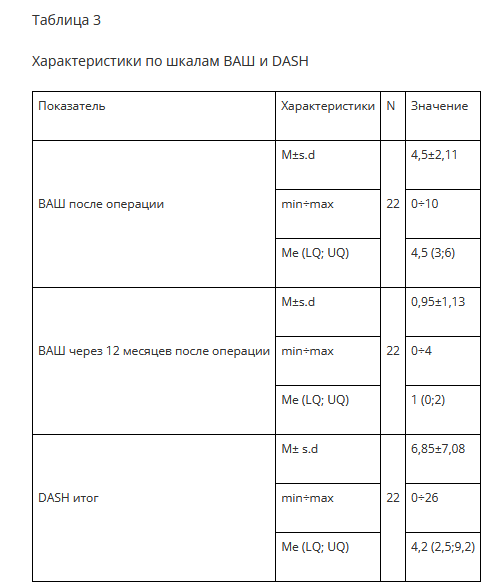
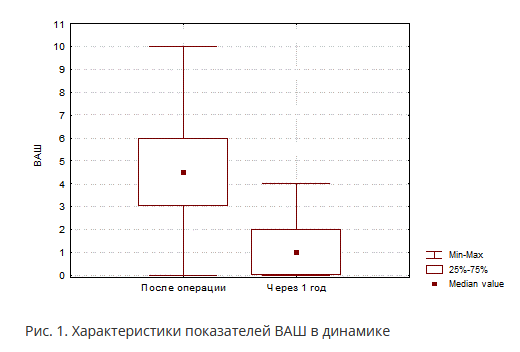
Средняя оценка боли по 10-балльной шкале ВАШ при оценке результатов лечения через 12 месяцев составила 0,96±0,24 балла, минимум – 0, максимум – 4 балла (рис. 1). По критерию знаков показатели ВАШ через 1 год после операции достоверно значительно снизились (р<0,001).
При субъективном изучении функциональных исходов использовали шкалу DASH. Минимальное значение – 0 баллов, максимальное – 20,6 балла, среднее – 6,9±1,5 балла (рис. 2). Функциональные результаты отличные и хорошие в 21 (95,5%) наблюдении, в 1 (4,5%) удовлетворительный. Неудовлетворительных результатов не было. По критерию Фишера хорошие и отличные результаты доминируют достоверно (р<0,001).
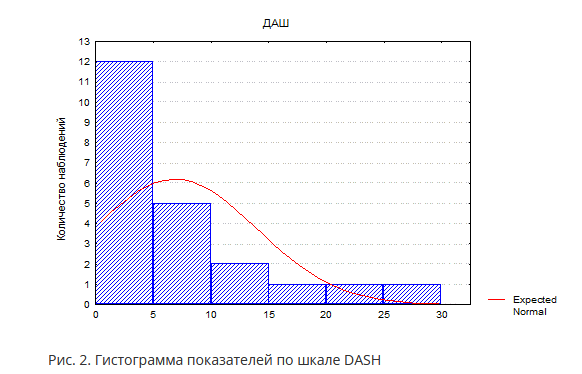
При анализе ротационной функции предплечья согласно критерию Фишера подтверждено достоверное превалирование ее восстановления (р=0,039). У 12 из 22 больных до операции имелись выраженные контрактуры, что потребовало длительного реабилитационного лечения после реконструкции. При исследовании ротационной функции предплечья у 14 из 22 больных ротация была восстановлена полностью, у 8 выявлена остаточная ротационная контрактура, 6 из них имели ограничения пронации или супинации в пределах 30–400, субъективно при этом ограничения функции пациенты не отмечали. У 3 больных ротационная контрактура имела клинически значимый характер – ротация была ограничена более чем на 50%. В 2 из них имело место развитие гетеротопической оссификации. В анамнезе одного из них проводилось лечение в аппарате наружной фиксации по поводу открытого перелома с порочным стоянием отломков в течение 5 месяцев. Развитие гетеротопической оссификации произошло в месте порочного стояния отломка. У второго имел место перелом пластины. После реконструкции отмечено образование обширной костной мозоли. Синостозирования костей при окончательной оценке результата лечения у них не отмечено. Инфекционных осложнений не было. У 1 больного констатирована постжгутовая нейропатия, явления которой купированы через 6 месяцев после операции.
Несращения и дефекты костей при лечении переломов предплечья – достаточно частое осложнение. Причинами несращений могут быть такие факторы, как оскольчатый или сегментарный характер перелома, костные дефекты, интерпозиция мягких тканей, нарушение кровоснабжения фрагментов кости, некачественный остеосинтез и местная инфекция [9, 10, 11].
Перестройка аутотрансплантатов, ассимиляция их с материнским ложем происходят в период от 4 до 6 месяцев. Используемый фиксатор должен стабильно фиксировать отломки и аутотрансплантат в течение всего срока ассимиляции трансплантата с материнским ложем при условии проводимого активного восстановительного лечения.
Успех лечения зависит от многих клинических параметров, таких как: время, прошедшее от момента травмы, предшествующие операции, присутствие инфекции, размер костного дефекта, метод остеосинтеза [11].
Авторы одной из работ сообщили о результатах лечения 15 больных, имевших 26 несросшихся переломов костей предплечья, которым были выполнены открытое рассверливание, костная пластика дефектов аутотрансплантатом из гребня подвздошной кости и фиксация блокирующими стержнями ForeSight. Протяженность дефектов костей составила в среднем 20 (от 10 до 30) мм. Сращение переломов констатировано у 14 (93%) больных. Среднее время консолидации было 15 недель. Однако хорошая функция сегмента отмечена только у 2 больных, удовлетворительная – у 6 и неудовлетворительная – у 7 пациентов [1].
В 8 наблюдениях других авторов, которые применили блокирующие стержни в комбинации с техникой Nikoll, ни у одного пациента не наблюдалось разрушения импланта или аутотрансплантата, во всех случаях наступило заживление переломов. Длина аутотрансплантатов была от 0,5 до 3 см. Авторам удалось достичь восстановления анатомии и, как следствие, хороших функциональных результатов, все пациенты вернулись к повседневной деятельности. У всех пациентов амплитуда движений и сила хвата кисти стали лучше, чем до реконструкции [5]. Данные этих авторов коррелируют с нашими результатами.
В серии 14 пациентов исследователи использовали фиксацию пластинами Loking Compression Plate. Размер замещаемого дефекта был не более 50 мм. Перестройка трансплантатов и их сращение с отмечены на сроке от 6 до 8 месяцев в случаях изолированных несращений, при несращениях обеих костей – более 8 месяцев. Отмечено, что функция смежных суставов у всех больных была хорошая [6].
Одним из важных факторов для восстановления функции является восстановление лучевой кривизны [5]. По полученным данным авторов статьи, в исследовании на кадаверах установлена зависимость амплитуды ротации при выпрямлении кривизны костей. Выпрямление лучевой кривизны приводит к ограничению пронации от 10 до 350, в среднем (ошибка средней) 20,750 (±2,60). Выпрямление локтевой кривизны приводит к ограничению пронации от 5 до 200, в среднем 10,630 (±1,50). Выпрямление кривизны обеих костей ограничивает пронацию от 15 до 450, в среднем 31,750 (±2,90). Ограничения супинации при этом не наблюдали. При угловой деформации костей на угол больший, чем выпрямление физиологической кривизны, наблюдали резкое ограничение ротационных движений. Поэтому, на взгляд авторов данной статьи, необходимы педантичное восстановление как лучевой, так и локтевой кривизны, строгий контроль ротационных смещений и выравнивание костей по длине, поскольку именно это обеспечивает восстановление ротационной функции предплечья.
При анализе причин несращений при первичном кортикальном остеосинтезе в наших наблюдениях установлено, что практически во всех случаях имели место неустраненные смещения, в первую очередь угловые и ротационные.
Это позволяет сделать вывод, что анатомические и функциональные нарушения, которые при этом возникают, препятствуют сращению. Подобного мнения придерживаются и другие авторы: «игнорирование физиологической кривизны лучевой кости может негативно сказаться на сращении перелома» [7].
Костная аутопластика рутинно выполняется в ортопедической практике при лечении несращений. Гребень подвздошной кости является наиболее частым донорским участком для получения аутотрансплантатов. Этот материал не имеет риска возникновения иммунологических реакций. Несращения костей предплечья с дефектами до 60 мм можно успешно лечить с применением губчатых костных аутотрансплантатов, но их применение менее эффективно при лечении длинных дефектов, особенно более 60 мм, так как при этом затруднены компрессия и адаптация аутотрансплантата к торцам отломков из-за его кривизны.
Ряд исследователей провели сравнение ауто- и аллотрансплантатов. Ими были изучены результаты лечения 34 больных, где у 20 пациентов был применен аутотрансплантат, у 14 – аллотрансплантат. Все переломы срослись, среднее время консолидации составило 16 недель, а результаты отмечены как удовлетворительные в обеих группах. Авторы пришли к выводу об эффективности обоих материалов [11].
Также при анализе источников были найдены сведения, что при изолированных несращениях авторы применяли васкуляризированный аутотрансплантат у 7 больных. В качестве «донора» использована дистальная часть лучевой кости, в качестве фиксатора – кортикальный остеосинтез пластинами с винтами, сращение было достигнуто у всех пациентов с удовлетворительным функциональным результатом. Из недостатков необходимо отметить, что данный метод нельзя использовать при патологии обеих костей и затруднительно его применение при больших дефектах кости [12].
Также по данным литературы была найдена работа, где применяли васкуляризированный аутотрансплантат из малоберцовой кости у 27 больных. Для фиксации костей и аутотрансплантата использованы пластины Loking Compression Plate по оригинальному разработанному способу, который позволил предотвратить ошибки кортикального остеосинтеза пластинами. Было показано преимущество применения пластин Loking Compression Plate над аппаратами наружной фиксации в обеспечении стабильности трансплантата. Оценка по DASH составила 33,7±3,61 балла [13]. Надо отметить, что значительная разница по шкале DASH в сравнении с результатами (6,5±1,78), изложенными в данной статье, обусловлена тем, что в вышеописанном исследовании авторов 41% пациентов имели последствия огнестрельных ранений, при которых имеется значительное повреждение мягких тканей сегмента.
Важным является то, что при наличии инфекции рекомендуется этапное лечение. Методика индуцированных мембран, известная как техника Masquelet, подразумевает двухэтапное лечение. Первый этап: стабилизация отломков и установка спейсера из костного цемента с добавлением антибактериальных препаратов между отломками. Второй этап выполняется на сроке не менее 2 месяцев от момента установки спейсера. Он подразумевает удаление спейсера, при этом образовавшаяся фиброзная капсула вокруг него максимально сохраняется. Сформированная полость заполняется костными аутотрансплантатами. Данная методика также рекомендована при обширных костных дефектах. И есть исследование, где авторы применили методику индуцированных мембран у 9 пациентов, где 5 случаев были последствиями открытых переломов III типа, 1 – псевдоартроз и 3 случая связаны с инфекцией. Протяженность дефектов составила от 17 до 54 мм, в среднем 47 мм, и консолидация была констатирована во всех случаях, кроме одного, где потребовалась ревизия в связи с переломом фиксатора [14].
При невозможности восстановления целостности костей необходимо рассмотрение альтернативных хирургических техник. При массивных дефектах костей предплечья спасательным решением является реконструкция в виде конверсии костей. Суть методики заключается в соединении между собой лучевой и локтевой костей. При этом полностью блокируется ротация предплечья. Однако конечность становится функциональной и безболезненной.
Так, авторами статьи были описаны исходы лечения 38 больных. У всех имелись массивные дефекты костей, в основном вследствие тяжелых травм:
· после реплантаций – 16;
· потеря костной массы, обусловленная инфекцией, – 16;
· опухоли лучевой кости – 2;
· псевдоартроз – 4 пациента.
Оперативное вмешательство заключалось в:
· соединении периферической части лучевой кости и центральной локтевой – 29;
· артродезировании дистального лучезапястного сустава – 4;
· артродезировании локтевой кости с костями запястья – 5.
У 22 пациентов был отмечен хороший функциональный результат, у 11 – хороший и у 5 – неудовлетворительный. Авторы пришли к выводу, что реконструкция предплечья на одной кости (конверсия) может быть эффективной альтернативой хирургическому лечению. Это сложная реконструкция, но она обеспечивает функциональность руки и косметически более привлекательна, чем ампутация предплечья. При этом надо отметить, что у данного исследования было несколько ограничений, включая относительно небольшое количество больных, различные импланты, использованные при первичном остеосинтезе, и относительно небольшая длина используемого аутотрансплантата, а в перспективе для окончательных выводов авторы отметили, что требуется дальнейшее изучение техник и материалов для замещения дефектов костей, биомеханических и биологических аспектов применения различных имплантатов [15].
Заключение
Интрамедуллярный блокируемый стержень – перспективная альтернатива при лечении несращений предплечья. Разработанные комплекс лечения и способы фиксации отломков и трансплантата при осложненных переломах предплечий позволяют получить отличные и хорошие анатомо-функциональные исходы.Литература:
1. Hong G., Cong-Feng L., Hui-Peng S., Cun-Yi F., Bing-Fang Z. Treatment of diaphyseal forearm nonunions with interlocking intramedullary nails // Clin. Orthop. Relat. Res. 2006. Vol. 450. P. 186-192.
3. Неверов В.А., Черняев С.Н. Хирургическая техника блокирующего интрамедуллярного остеосинтеза переломов костей предплечья // Вестник хирургии им. И.И. Грекова. 2015. № 174 (5). C. 35-39.
4. Kamrani R.S., Mehrpour S.R., Sorbi R., Aghamirsalim M., Farhadi L. Treatment of nonunion of the forearm bones with posterior interosseous bone flap // J. Orthop. Sci. 2013. Vol. 18 (4). P. 563-568. DOI: 10.1007/s00776-013-0395-0.
5. Saka G., Saglam N., Kurtulmus T., Avc? C.C., Akp?nar F. Treatment of diaphyseal forearm atrophic nonunions with intramedullary nails and modified Nicoll's technique in adults // Acta Orthop. Traumatol. Turc. 2014. Vol. 48 (3). P. 262-270.
7. Yorukoglu A.C., Demirkan A.F., Akman A., Kitis A., Usta H. The effects of radial bowing and complications in intramedullary nail fixation of adult forearm fractures // Eklem. Hastalik. Cerrahisi. 2017. Vol. 28 (1). P. 30-34.
8. Boussakri H., Elibrahimi A., Bachiri M., Elidrissi M., Shimi M., Elmrini A. Nonunion of Fractures of the Ulna and Radius Diaphyses: Clinical and Radiological Results of Surgical Treatment // Malays. Orthop. J. 2016. Vol. 10 (2). P. 27-34.
10. Regan D.K., Crespo A.M., Konda S.R., Egol K.A. Functional Outcomes of Compression Plating and Bone Grafting for Operative Treatment of Nonunions About the Forearm // J. Hand Surg. Am. 2018. Vol. 43 (6). P. 564-569.
11. Faldini C., Traina F., Perna F., Borghi R., Nanni M., Chehrassan M. Surgical treatment of aseptic forearm nonunion with plate and opposite bone graft strut. Autograft or allograft? // Int. Orthop. 2015. Vol. 39 (7). P. 1343-1349.
13. Середа А.П., Ефименко Н.А., Грицюк А.А., Васютык Б.М. Лечение огнестрельных дефектов костей предплечья // Травматология и ортопедия России. 2007. № 3 (45). C. 17.
14. Walker M., Sharareh B., Mitchell S.A. Masquelet Reconstruction for Posttraumatic Segmental Bone Defects in the Forearm // J. Hand Surg. Am. 2019. Vol. 44 (4). P. 341-348. DOI: 10.1016/j.jhsa.2018.07.003.
15. Devendra A., Velmurugesan P.S., Dheenadhayalan J., Venkatramani H., Sabapathy S.R., Rajasekaran S. One-Bone Forearm Reconstruction: A Salvage Solution for the Forearm with Massive Bone Loss // J. Bone Joint Surg. Am. 2019. Vol. 101 (15). P. 74-79. DOI: 10.2106/JBJS.18.01235.
Авторы:
1 СПб ГБУЗ «Городская Мариинская больница»
2 ФГБОУ ВО «Санкт-Петербургский государственный педиатрический медицинский университет» Министерства здравоохранения Российский Федерации
3 ФГБОУ ВО «Северо-Западный государственный медицинский университет имени И.И. Мечникова» Министерства здравоохранения Российский Федерации
4 СПб ГБУЗ «Городская больница Святого Великомученика Георгия»
Теги: кости предплечья
234567 Начало активности (дата): 11.12.2024
234567 Кем создан (ID): 989
234567 Ключевые слова: кости предплечья, переломы предплечья, остеосинтез, перелом, лучевая кость, локтевая кость, ложный сустав, несращение, дефект кости
12354567899
Похожие статьи
Алгоритм выбора метода хирургического лечения диафизарных переломов костей предплечьяРентген на дому 8 495 22 555 6 8
Многоэтапное лечение открытого перелома бедра с дефектом кости, мягких тканей и бедренной артерии
Поиск лабораторных тестов для прогнозирования замедленного сращения переломов костей у пациентов с политравмой (пилотное исследование)
Клиническое наблюдение хирургического лечения рецидивирующего вывиха костей предплечья



