 16.05.2024
16.05.2024
Возможности лечения методом радиочастотной денервации при коксартрозе различных стадий
Радиочастотная денервация — это современное интервенционное эффективное воздействие на основной симптом многих заболеваний — боль
Введение
Хронический болевой синдром в тазобедренном суставе является весьма распространённым симптомокомплексом при обращении пациентов к врачам разных специализаций. Большинство из них испытывают боль в бедре, паховой и ягодичной области с характерными ограничениями при нагрузке в поражённой конечности и движениях в суставе. При этом хронический болевой синдром может быть вызван группой различных нозологий (асептический некроз головки бедренной кости, остеоартрит, ревматоидный артрит, инфекционный артрит и др.), объединённых в одно распространённое полиэтиологическое заболевание — коксартроз [1-4]. Многочисленные факторы риска, такие как пожилой возраст, женский пол, ожирение, травматизм, повторяющиеся перегрузки, слабость мышечного аппарата, курение [5], играют определённую роль в его развитии и прогрессировании.
Наиболее распространённой на сегодняшний день является основанная на рентгенологических показателях классификация коксартроза по J. Kellgren и J. Lawrence (1957) [6], в которой выделены четыре стадии патологии.
Традиционное комплексное консервативное лечение коксартроза любой стадии (лечебная физкультура, физиотерапия, приём нестероидных противовоспалительных средств, внутрисуставное введение глюкокортикостероидов и гиалуроновой кислоты) часто не в состоянии полностью устранить хроническую боль в суставах, к тому же большинству пациентов с III-IV стадией противопоказан золотой стандарт хирургического лечения — эндопротезирование сустава — из-за тяжести сопутствующих заболеваний. Нельзя не отметить и тот факт, что у 15-20% прооперированных боль сохраняется и при отсутствии нарушения техники операции (асептическая нестабильность компонентов, инфекционно-воспалительные осложнения) [7].
Радиочастотная денервация (РЧД) описана в 1998 году как альтернативный способ лечения хронической боли в тазобедренных суставах на основе положительного опыта широко применяемой методики воздействия на боль при фасет-синдроме в вертебрологии группой отечественных учёных во главе с О.В. Акатовым [8]. РЧД может быть выполнена с помощью различных режимов — обычного, импульсного и охлаждённого [9].
РАДИОЧАСТОТНАЯ ДЕНЕРВАЦИЯ: АЛЬТЕРНАТИВНЫЙ СПОСОБ ЛЕЧЕНИЯ ХРОНИЧЕСКОЙ БОЛИ В ТАЗОБЕДРЕННЫХ СУСТАВАХ
Методология поиска источников Информационный поиск научной литературы производился с помощью открытых электронных баз данных PubMed за временной интервал с 1990 по 2023 год.
Критериями включения служили исследования разной степени доказательности: клинические случаи и серии клинических случаев, когортные и рандомизированные исследования. Критерии исключения: исследования на животных, отдельные мнения и правки.
На втором этапе исключены дублирующие статьи, статьи без полнотекстовой версии, а также работы, не удовлетворяющие в полной мере критериям включения.
Вопрос эффективности методики РЧД напрямую зависит от особенностей иннервации тазобедренного сустава для максимального воздействия на нервные окончания, передающие болевой импульс с периферического отдела.
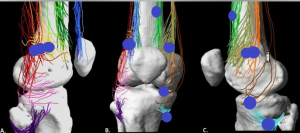
При изучении особенностей иннервации с позиции анатомии отмечено превалирующее участие в формировании боли суставных ветвей запирательного и бедренного нервов [24]. Проведено множество исследований иннервации тазобедренного сустава. Так, в работе канадских учёных во главе с A. Alzaharani [25] показано, что чувствительная иннервация капсулы тазобедренного сустава происходит главным образом от пояснично-крестцового сплетения и периферических нервных ветвей, включающих бедренный, запирательный, седалищный и верхний ягодичный нервы. Переднемедиальную область иннервирует суставная ветвь запирательного нерва, а суставная ветвь бедренного нерва отвечает за переднюю область, соответственно, задняя иннервация осуществляется за счёт суставной ветви от седалищного нерва, а ветви верхнего ягодичного нерва иннервируют заднебоковую капсулу тазобедренного сустава [26-28].
Исследования анатомии показали, что большая часть тазобедренного сустава получает чувствительную иннервацию за счёт многочисленных нервных окончаний запирательного и бедренного нервов, а седалищный и верхний ягодичный — только дополняют их. Пусковые очаги боли могут возникать во внутри- и внесуставных структурах (связки, хрящ, синовиальная оболочка, суставная губа, сумки, сухожилия и др.). Так, согласно исследованию Y.T. Kim и H. Azuma [29], суставная губа содержит значительное количество рецепторов — тельца Фатера-Пачини и тельца Гольджи-Маццо- ни, а тельца Руффини и колбы Краузе сосредоточены в передневерхней и задневерхней части губы. Данные результаты могут объяснить наблюдения с различным направлением боли у пациентов с коксартрозом тазобедренного сустава, преимущественно в пах и переднемедиальную часть бедра, в редких случаях — в ягодицу, коленный сустав и даже в голень [30].
Обсуждения
Большой интерес специалистов вызывает выбор доступа и расположение точек-мишеней для направления радиочастотной канюли с целью денервации. Последние данные анатомии иннервации и доли нервов в развитии общего болевого синдрома в тазобедренном суставе, согласно систематическому обзору по технике РЧД P. Kumar и соавт. [31], свидетельствуют, что боль в паху и медиальной части бедра может быть уменьшена путём воздействия на суставную ветвь запирательного нерва, поместив кончик иглы передним или переднелатеральным доступом под рентгенконтролем в месте соединения седалищной и лобковой кости с установкой в область запирательной борозды. Боль по наружной поверхности бедра и области трохантера блокируется воздействием на суставную ветвь бедренного нерва, когда кончик иглы проводится ниже передней подвздошной ости рядом с переднелатеральным краем тазобедренного сустава.
Коллектив авторов под руководством S. Locher [27] провёл в 2008 году анатомическое исследование на трупном материале, а также с помощью МРТ-моделирования для оценки оптимального доступа игл-канюль к запирательному нерву. В заключении авторы предложили косое направление игл с приближением к параллельному расположению относительно нервного волокна для минимизации повреждений сосудов (бедренный нерв и артерия) и максимальной площади воздействия коагуляции на нерв с возможностью 2-3 повторений, в том числе сообщили о необходимости дальнейших клинических испытаний, однако данная методика не нашла дальнейшего практического применения.
Начиная с работы M. Kawaguchiи соавт. (2001) [12], все последующие публикации включают в методику денервации воздействие на суставную ветвь бедренного нерва. Уже в первом исследовании [12] показано снижение показателей боли более чем на 50% в период от 1 до 11 месяцев у 86% пациентов. Кроме наблюдения K. Okada[10], в клинических исследованиях обсуждается только денервация передней капсулы, а область задней иннервации сустава нуждается в дальнейшем изучении, чтобы определить расположение и количество суставных ветвей седалищного и верхнего ягодичного нервов, а также их проецирование относительно костных ориентиров.
Характеристика и эффективность методики
Протокол денервации описывается с использованием обычного, импульсного или охлаждённого режима радиочастотного генератора и введением иглы-канюли под рентгенологическим интраоперационным контролем; в нескольких случаях сообщалось о дополнительном использовании ультразвука для исключения повреждения сосудов и окружающих тканей [20, 32, 33]. Заслуживает внимания ретроспективный анализ лечения 136 пациентов с 235 случаями РЧД со сроком наблюдения более 12 месяцев, проведённый американскими учёными из Института боли под руководством L. Kapural (2021) [22]. Ультразвуковое сопровождение проводилось для точной локализации канюли с целью предотвращения повреждения бедренной артерии и вены, при этом не было зарегистрировано ни одного такого случая.
Во всех отобранных нами исследованиях используется радиочастотная игла-канюля размером от 18G до 22G c активным рабочим наконечником иглы 5-10 мм и общей длинной 100 мм или 150 мм. Температурный режим стандартной методики РЧД — от 60°C до 90°C и продолжительностью воздействия от 90 до 300 секунд.
Отдельной группой выделяются работы с использованием радиочастотного генератора в импульсном режиме. В своих публикациях C.L. Chye [18], A. Tinnirello и соавт. [19] применяют короткоимпульсный режим с температурой не более 42°C и длительность 180-300 секунд у 29 и 14 пациентов соответственно для сравнения с консервативным лечением и уменьшением риска развития таких осложнений, как неврит и невринома. При этом только в исследовании L. Kapural (2018) по РЧД тазобедренного сустава [20] упоминается единственный случай осложнения в виде неврита, проявившегося чувством местного жжения с самостоятельным разрешением в течение недели, который, по опыту лечения вертеброгенного болевого синдрома, имеет распространённость в 0,5% случаев [34]. Нельзя не обратить внимания на технику денервации с использованием охлаждаемого режима, плюсом которого авторы считают большую площадь повреждения относительно обычной методики, но данное направление подлежит дальнейшему изучению в аспекте сопоставления с обычным режимом [20, 22].
Согласно обзору американских учёных C.W. Cheney и соавт. (2021) [35] по РЧД тазобедренного сустава, в 10 научных работах продемонстрировано достоверное снижение показателей боли от 30 до 80% с общим периодом наблюдений от 3 месяцев до 3 лет, в 6 — значительное уменьшение боли на срок не менее 6 месяцев. Указывается и положительное изменение функциональных характеристик по системам оценки WOMAC (Western Ontario and McMaster Universities Osteoarthritis Index), Harris Hip Score, OHS (Oxford Hip Score), несмотря на неоднородность показателей. Сокращение использования анальгетических препаратов после РЧД отмечено в работах S. Jaramillo [36] и G. Gupta [15]. С позиции доказательной медицины, Американское общество боли и неврологии (American Society of Pain and Neuroscience, ASPN) с 2021 года рекомендует РЧД направленного воздействия на запирательный и бедренный нерв для лечения боли GRADE II-1 B [37].
Обсуждение
В настоящее время в общедоступных научных электронных базах представлено небольшое количество работ по тематике РЧД тазобедренного сустава. В имеющихся исследованиях используется как обычная методика РЧД, так и импульсная, с охлаждённой канюлей или поддержкой ультразвукового контроля. Авторы сообщают о преимуществах своей методики в сравнении со стандартной:
• использование ультразвука обеспечивает отсутствие повреждений сосудов (бедренной вены и артерии) и точную установку иглы к нерву [20, 22, 32, 33];
импульсная техника предполагает минимальное разрушение нервного волокна при длительном подавлении боли за счёт синаптической активности, что снижает риск неврита, при этом требуется точное перпендикулярное расположение• техника с использованием охлаждённой канюли обеспечивает значительно больший размер очага поражения, чем обычный радиочастотный электрод того же размера [20-22].
По результатам исследований, только в 3 работах получены осложнения в виде послеоперационных местных гематом паховой области (у 4 пациентов) с быстрым разрешением без дополнительных лечебных мероприятий [18, 19, 23], а развитие неврита, также разрешившегося самостоятельно в течение недели, описано в одном случае [20]. Все осложнения носят единичный характер и не являются статистически значимыми, что свидетельствует о малотравматичности и высокой безопасности метода в целом.
Срок наблюдения пациентов в данном обзоре колебался от 1 до 36 месяцев и в большинстве случаев составил не более 6 месяцев.
Только в двух отечественных работах применялось воздействие исключительно на запирательный нерв, а исследование особенностей иннервации тазобедренного сустава и зон болевого синдрома (13 источников) демонстрирует эффективность денервации за счёт воздействия как на запирательный, так и бедренный нерв.
В связи с вышеизложенным невозможно говорить о преимуществе или недостатке использования импульсного или охлаждённого режима в сравнении с обычным ввиду малого количества наблюдений, низкого качества исследований, редко используемых функциональных систем оценки тазобедренного сустава до и после РЧД (WOMAC, Harris Hip Score, OHS и др.). Группа контрольного сравнения с консервативным лечением имеется лишь в одном исследовании [18], но и там отсутствует рандомизация, пациенты выбирали способ лечения самостоятельно, что ставит результаты и выводы под сомнения. Однако в последние годы прослеживается устойчивая тенденция к увеличению количества наблюдений и изменению качества дизайна исследований (не только описание клинических примеров).
Заключение
Вопрос целесообразности применения методики РЧД в лечении болевого синдрома при коксартрозе получает в последние годы всё большее распространение в связи с неудовлетворённостью пациентов и врачей периодом ремиссии консервативного лечения, наличием противопоказаний к эндопротезированию, а в некоторых случаях и сохранением боли после операции. Данные литературы подтверждают высокую эффективность РЧД с длительным периодом ремиссии и сокращением сроков нетрудоспособности.
Перспективность методики не подлежит сомнению, но требует дальнейших исследований с современным дизайном для тщательного анализа безопасности и эффективности при каждой стадии коксартроза, разработки единого протокола вмешательства, определения показаний и противопоказаний.
Авторы:
1. Helmick CG, Felson DT, Lawrence RC, et al. Estimates of the prevalence of arthritis and other rheumatic conditions in the United States. Part I. Arthritis Rheum. 2008;58(1):15-25. doi: 10.1002/art.23177
2. Lawrence RC, Felson DT, Helmick CG, et al. Estimates of the prevalence of arthritis and other rheumatic conditions in the United States. Part II. Arthritis Rheum. 2008;58(1):26-35. doi: 10.1002/art.23176
3. Johnson VL, Hunter DJ.
The epidemiology of osteoarthritis. Best Pract Res Clin
Rheumatol.
4. Балабанова Р.М., Дубинина Т.В., Демина А.Б., Кричевс-
кая О.А. Заболеваемость болезнями костно-мышечной системы в Российской
Федерации за 2015-2016 гг. // Научно-практическая
ревматология. 2018. Т.
56, № 1. С. 15-21. [Balabanova RM, Dubinina TV, Demina
AV, Krichevskaya OA. The incidence of musculoskeletal diseases in the Russian
Federation over 2015-2016. Rheumatology Science and
Practice. 2018;56(1):15-21. (In Russ).]
5. Barbour KE, Helmick CG, Boring M, Brady TJ. Vital signs: Prevalence of doctor-diagnosed arthritis and arthritis- attributable activity limitation — United States, 2013-2015. MMWR Morb Mortal Wkly Rep. 2017;66(9):246-253. doi: 10.15585/mmwr.mm6609e1
6. Kellgren JH, Lawrence JS. Radiological assessment of osteoarthrosis. Ann Rheum Dis. 1957;16(4):494-502. doi: 10.1136/ard.16.4.494
7. Глемба К.Е., Макаров М.А., Каратеев А.Е. Хроническая боль после эндопротезирования крупных суставов у больных остеоартритом // Opinion Leader. 2019. № 3. С. 70-75. [Glemba KE, Makarov MA, Karateev AE. Chronic pain after endoprosthetics of large joints in patients with osteoarthritis. Opinion Leader. 2019;(3):70-75. (In Russ).]
8. Акатов О.В., Древаль О.Н., Гринев А.В. Новый метод лечения болевого синдрома при коксартрозе // Вопросы нейрохирургии. 1998. № 1. С. 37-39. [Akatov OV, Dreval ON, Grinev AV. A new method of treating pain syndrome in coxarthrosis. Questions Neurosurgery. 1998;(1):37-39. (In Russ).]
9. Hernandez-Gonzalez L, Calvo CE, Atkins-Gonzalez D. Peripheral nerve radiofrequency neurotomy: Hip and knee joints. Phys Med Rehab Clin. 2018;29(1):61-71. doi: 10.1016/j.pmr.2017.08.006
10. Okada K. New approach to the pain of the hip joint: Percutaneous sensory nerve electrocoagulation of the hip joint. Pain Res. 1993;8:125-135.
11. Шпилевой В.В., Худяев А.Т., Шатохин В.Д. Отдаленные результаты лечения хронического болевого синдрома при коксартрозе методом чрескожной радиочастотной деструкции запирательного нерва // Гений ортопедии. 2001. № 3. С. 72-75. [Shpilevoy VV, Khudyaev AT, Shatokhin VD. Long-term results of treatment of chronic pain syndrome in coxarthrosis by percutaneous radiofrequency destruction of the occlusive nerve. Genius Orthopedics. 2001;(3):72-75. (In Russ).]
12. Kawaguchi M, Hashizume K, Iwata T, Furuya H. Percutaneous radiofrequency lesioning of sensory branches of the obturator and femoral nerves for the treatment of hip joint pain. Reg Anesth Pain Med. 2001;26:576-581. doi: 10.1053/rapm.2001.26679
13. Malik A, Simopolous T, Elkersh M, et al. Percutaneous radiofrequency lesioning of sensory branches of the obturator and femoral nerves for the treatment of non-operable hip pain. Pain Physician. 2003;6(4):499-502.
14. Rivera F, Mariconda C, Annaratone G. Percutaneous radiofrequency denervation in patients with contraindications for total hip arthroplasty. Orthopedics. 2012;35(3):e302-305. doi: 10.3928/01477447-20120222-19
15. Gupta G, Radhakrishna M, Etheridge P, et al. Radiofrequency denervation of the hip joint for pain management: Case report and literature review. US Army Med Dep J. 2014;41-51.
16.. Cortinas-Saenz M, Salmeron-Velez G,
Holgado-Macho IA. Joint and sensory branch block of the obturator and femoral
nerves in a case of femoral head osteonecrosis and arthritis. Rev
Esp Cir Ortop Traumatol. 2014;58(5):319-324.
17. Kasliwal P, Iyer V, Kasliwal S. Percutaneous radio frequency ablation for relief of pain in a patient of hip joint avascular necrosis. Ind J Pain. 2014;28:121-123.
18. Chye CL, Liang CL, Lu K, et al. Pulsed radiofrequency treatment of articular branches of femoral and obturator nerves for chronic hip pain. Clin Interv Aging. 2015;10:569-574. doi: 10.2147/CIA.S79961
19. Tinnirello A, Todeschini M, Pezzola D, Barbieri S. Pulsed radiofrequency application on femoral and obturator nerves for hip joint pain: Retrospective analysis with 12-month follow-up results. Pain Physician. 2018;21(4):407-414.
20. Kapural L, Jolly S, Mantoan J, et al. Cooled radiofrequency neurotomy of the articular sensory branches of the obturator and femoral nerves--combined approach using fluoroscopy and ultrasound guidance: Technical report, and observational study on safety and efficacy. Pain Physician. 2018;21(3): 279-284. doi: 10.1097/AAP.0000000000000690
21. Naber J, Lee N, Kapural L. Clinical efficacy assessment of cooled radiofrequency ablation of the hip in patients with avascular necrosis. Pain Manag. 2019;9:355-359. doi: 10.2217/pmt-2018-0083134
22. Kapural L, Naber J, Neal K, Burchell M. Cooled radiofrequency ablation of the articular sensory branches of the obturator and femoral nerves using fluoroscopy and ultrasound guidance: A large retrospective study. Pain Physician. 2021;24(5):611-617.
23. пациентов с дегенеративным остеоартрозом тазобедренного сустава 3-4 стадии // Гений ортопедии. 2021. Т. 27, № 2. С. 209-213. [Fishchenko IV, Vladimirov AA, Roy IV, et al. Treatment of coxalgia in patients with grades 3-4 hip osteoarthritis. Genius Orthopedics. 2021;27(2):209-213. (In Russ).] doi: 10.18019/1028-4427-2021-27-2-209-213
ОБ АВТОРАХ
Автор, ответственный за переписку:
Горохов Михаил Аркадьевич;
Соавторы:
Загородний Николай Васильевич, д.м.н., чл.-корр. РАН;
Кузьмин Вячеслав Иванович, д.м.н.;
Шарамко Тарас Георгиевич, к.м.н.;
Теги: тазобедренный сустав
234567 Начало активности (дата): 16.05.2024 13:01:00
234567 Кем создан (ID): 989
234567 Ключевые слова: тазобедренный сустав; радиочастотная денервация; коксартроз; боль в тазобедренном суставе
12354567899
Похожие статьи
Отдалённые результаты профилактики лечения перипротезной инфекции в онкоортопедииРентген на дому 8 495 22 555 6 8
Шкалы оценки морфометрической готовности культи конечности к протезированию и технического состояния эксплуатируемого протеза
Особенности лечения переломов бедра у детей с тяжёлыми формами детского церебрального паралича
Парентеральное использование транексамовой кислоты при тотальном эндопротезировании тазобедренного сустава



