 25.02.2024
25.02.2024
Оценка результатов органосохраняющего хирургического лечения травмы дистальной фаланги пальцев кисти и обоснование алгоритма лечения травм пальцев кисти
Установлено, что применение разработанного метода хирургического лечения травмы дистальной фаланги пальцев кисти обеспечивает меньшую (по сравнению с использованием стандартных методов) выраженность болевого синдрома
ВВЕДЕНИЕ
Доля повреждений кисти в последние десятилетия составляет в структуре травматизма от 30 до 50 % [1-4]. При этом отмечается высокая частота выхода пострадавших на инвалидность после данной травмы [2, 5-7].
Одним из тяжёлых повреждений является травматическое отчленение сегментов кисти, при этом в структуре причин инвалидности доля ампутационной культи составляет 54-67 % [6, 8, 9].
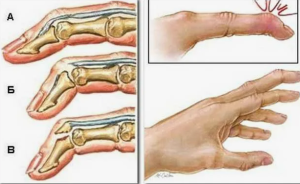
После ампутации дистальной фаланги может развиться ряд осложнений, в том числе нарушения сроков заживления раны, гиперчувствительность, болевые ощущения, непереносимость холодовых воздействий, ретракция рубца, сгибательная контрактура, хронические язвы, инфекционные осложнения и т. п. [10-14]. Необходимость комплексного лечения, включающего восстановление десмомио-артроостеогенного компонента, обусловливает, в первую очередь, важность адекватного восстановления дерматогенного компонента, так как нормальная функция кисти возможна лишь при обеспечении це¬лостности кожных покровов, особенно ладонной (опорной) поверхности [3, 9, 15, 16]. Однако принципы выбора тактики и методов кожно-пластических операций при травмах дистальных фаланг пальцев кисти изучены недостаточно, представленные в литературе сведения практически не систематизированы, не разработаны общепринятые алгоритмы ведения данной категории пострадавших.
До настоящего времени ряд авторов считает, что формирование культи (пусть и с некоторым укорочением фаланги), сохраняющее основные виды захвата и оптимизирующее сроки реабилитации, является мето¬дом выбора при травматическом разрушении и ампутации фаланг пальцев кисти [17-22]. В связи с этим актуальным представляется совершенствование подходов к выбору оптимальных вариантов кожной пла¬стики у больных с глубокими ожогами, с обширными рвано-скальпированными ранами и послеожоговыми деформациями кисти, обеспечивающих сохранение анатомической целостности и функции пальцев.
Цель работы - сравнительный анализ клинической эффективности различных методов хирургического лечения травмы дистальной фаланги пальцев кисти.
МАТЕРИАЛЫ И МЕТОДЫ
Выполнено обследование и лечение 47 пострадавших (18 мужчин и 29 женщин), средний возраст которых составил 36,3 ± 14,2 года (от 22 до 52 лет), поступивших в клинику термических поражений Военно-медицинской академии им. С.М. Кирова с травмами ногтевых фаланг пальцев кисти.
Пациенты были разделены на 2 группы:
- в группе 1 (сравнения) - 25 пациентов, в лечении которых использованы стандартные методы формирования культей пальцев при травме или термическом поражении, им выполняли укорочение костной части фаланги, формирование встречных лоскутов и наложение нескольких узловых швов;
- в группе 2 (основной) - 22 пострадавших, в лечении которых использована предложенная хирургическая тактика, включающая реконструктивно-пластическое восстановление мягкотканных структур концевой части ногтевой фаланги без укорочения ее костной составляющей.
Группы пациентов сопоставимы по половозрастному распределению и по морфологическим особенностям повреждений дистального отдела трехсуставных пальцев кисти.
В качестве критериев включения пациентов в исследование рассматривали:
- возраст от 18 до 50 лет;
- наличие посттравматических торцевых дефектов концевых фаланг трехсуставных пальцев кисти в остром, подостром и отдаленном периодах после травмы.
Критерии невключения в исследование:
- наличие декомпенсированной соматической патологии;
- инфекционные осложнения в области повреждения;
- сахарный диабет 2 типа в стадии суб- и декомпенсации.
В исследование не включали пострадавших с мягкотканными дефектами площадью до 10 мм2, по¬скольку раны таких размеров могут быть закрыты путем краевой эпителизации с восстановлением целостности покровных тканей.
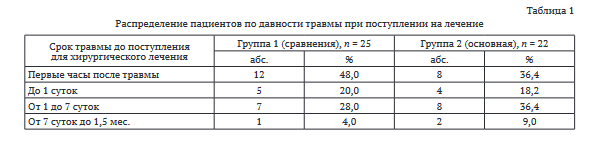
Распределение пациентов по давности травмы приведено в таблице 1. При поступлении у 20 пострадавших была травма, полученная несколько часов назад, остальные 27 пациентов поступали с травмой давностью до 1 суток - 9 человек (19,1 %), до 7 суток - 15 человек (31,9 %), 3 пострадавших поступили в срок от 7 дней до 1,5 месяцев (6,4 %).
Статистически значимых различий по срокам травмы концевой фаланги пальцев кисти выявлено не было.
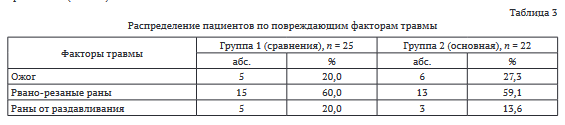
Клиническую картину у пациентов, включенных в исследование, определяли повреждающие факторы: термический и механический. Ожог как причина утраты мягких тканей части пальца зафиксирован был у 11 (23,4 %) пострадавших, в том числе у 6 (27,3 %) - в основной группе и 5 (20,0 %) - в группе сравнения (табл. 2).
Всем пациентам проведено рентгенологическое исследование.
Высокая вариабельность формы и размеров травматических повреждений усложняла планирование оперативных вмешательств в стандартном исполнении, тем не менее, в основу предложенного нами подхода к хирургическому лечению данного контингента пострадавших был положен принцип сохранения костной части культи ногтевой фаланги.
Другим фактором, усложнявшим клинический этап исследования, было разнообразие векторов отчленения фаланги, в первую очередь, с утратой матрицы и основания ногтевой пластинки. Таких пациенов в общей выборке было 3 (6,4 %), при этом размозжение мягких тканей наблюдали у двух пострадав¬ших основной группы (9,1 %) и у трех пациентов группы сравнения (11,1 %). Косая линия отчленения фаланги с сохранением части ногтя (1-2 мм) и ногтевой матрицы отмечена у 9 пострадавших основной группы (40,9 %) и в 12 случаях (54,5 %) в группе сравнения.
На рисунке 1 виден практически циркулярный дефект покровных тканей V пальца при сохраненной части ногтевой фаланги. Сохранилась также ногтевая пластинка V пальца. IV палец интактен.
Основной целью применения разработанного варианта реконструктивно-пластического замещения дефектов ногтевых фаланг трехсуставных пальцев, апробированного при лечении пострадавших основной группы, являлось пластическое замещение дефекта ногтевой фаланги с визуальным эффектом ее удлинения, который обеспечивается выполнением местной или перекрестной пластики кожно-фасциальными лоскутами.
Выкраивание этих лоскутов определяется формой и размерами дефекта, подлежащего закрытию.
Принципиальным отличием предлагаемого подхода от стандартной методики формирования культи пальца является отказ от укорочения костной части ногтевой фаланги, осуществление выкраивания лоскута кожно-фасциального лоскута для того, чтобы обеспечить не только закрытие дефекта, но и визуальное удлинение ногтевой фаланги путем применения особой формы выкройки лоскута.
Операцию проводили под сочетанной анестезией (проводниковая с седативной поддержкой); выпол¬няли фигурный разрез кожи, подкожной жировой клетчатки и поверхностной фасции в форме прямоугольника, косоугольника или в виде «ракетки». Формирование комплекса тканей во всех трех случаях выполнялось таким образом, чтобы в него, по возможности, была включена поперечная ветвь собственной ладонно-боковой артерии пальца.
Выделяемый кровоснабжаемый кожно-фасциальный лоскут брали на держалки, разворачивали в сторону дефекта так, чтобы на периферической части перемещенного комплекса тканей оставался небольшой избыток тканей, из которых впоследствии формировали кончик пальца. Два первых фиксирующих шва накладывали в области матрицы ногтя по её краям, остальные - по окружности торцевого дефекта.
В качестве пластического материала использовали кожу локтевого сгиба или подмышечной зоны у женщин и кожу предплечья у мужчин. Подобный подход позволял скрыть образующийся косметический дефект - рубец кожных покровов. Забор лоскута осуществляли с помощью электродерматома при заданной толщине лоскута 0,2-0,3 мм (тонкий лоскут). Донорский дефект ушивали в линию после отсепаровывания краев кожи на 5-8 мм от краев разреза.
Размеры комплекса тканей зависели от размеров дефекта, но не превышали (36 ± 5) х (16 ± 3) мм для бо-ковых лоскутов и (32 ± 3) х (15 ± 2) мм - для прямоугольных и косоугольных лоскутов.
На рисунке 2 представлен вид после перемещения лоскута с IV пальца на ногтевую фалангу V пальца. Донорский дефект не закрыт.
Перемещенный комплекс тканей фиксировали отдельными узловыми швами с оставлением длинных концов нитей. Далее накладывали 2 слоя марлевой салфетки, заворачивали в них несколько (5-7) мелких марлевых шариков, заготовленных для этой цели. Края салфетки подворачивали, образуя компрессирующую повязку, фиксировали её, попарно связывая отдельные длинные нити. Повязка плотно удерживала комплекс тканей от смещения в течение 7-9 дней, после чего её снимали.
Вторым разрезом подготавливали реципиентное поле, освежали края кожно-фасциального дефекта и, при необходимости, резецировали 1-2 мм культи ногтевой фаланги. При этом остатки ногтевой фаланги не иссекали.
Послеоперационное ведение пациентов проводили по общепринятым стандартам, которые предусматривали профилактическое введение антибиотиков и антикоагулянтов в терапевтических дозах для профилактики осложнений.
Для снижения выраженности болевого синдрома проводили медикаментозное лечение; назначали анальгетики, витамины; использовали местные охлаждающие повязки; конечности придавали возвышенное положение для уменьшения выраженности отёка.
Особенностью проводимого лечения было использование обездвиживания оперированных пальцев и всей кисти в целом на протяжении продолжительного срока (до 4-5 недель).
Иммобилизацию осуществляли с помощью гипсовой повязки или повязки из современных материалов (турбокаст, целлакаст и т.п.). Эти меры были направлены на профилактику нарушений кровоснабжения перемещенных комплексов тканей, создание благоприятных условий для качественного приживления тканей на раневой поверхности торца культи.
После заживления ран с пострадавшими проводили тренировки по восстановлению объема движений, по-степенному увеличению нагрузки от сгибания пальцев без отягощений до удерживания 2-3 кг гантелей в течение 3-х недель. Длительная иммобилизация неизбежно приводила к возникновению комбинированной контрактуры пястно-фаланговых и межфаланговых суставов, но при этом обеспечивала возможность правильного приживления и перестройки тканевых лоскутов без грубых рубцов. Пациенты регулярно вы-полняли движения, направленные на разработку пальца; начинали сразу после окончания иммобилизации, постепенно увеличивая амплитуду сгибания, и доводили ее до полной в течение 1-2 месяцев.
Поскольку у пациентов, включенных в исследование, были различные виды травм, подходы к их лечению также дифференцировали. В частности, при закрытии послеожоговых дефектов покровных тканей пальцев кисти требовалось выполнение от 1 до 3 корректирующих операций (обезжиривание лоскутов, удаление избытков кожи при формировании культи), в отличие от травм режущими предметами.
В процессе анализа результатов лечения пострадавших проводили сравнение данных, полученных при обследовании пациентов в группах исследования, в раннем послеоперационном периоде, а также спустя 3, 6, 12 месяцев после проведения реконструктивно-восстановительных операций.
На 10-21 сутки после вмешательства оценивали выраженность болевого синдрома по 10-балльной визуально-аналоговой шкале (ВАШ), в последующие сроки было выполнено изучение функционального состояния верхней конечности и кисти, активности пациента в обычной жизни на основе шкалы DASH (Disability of the Arm, Shoulder and Hand outcome measure).
Также исследовали наличие и выраженность рубцовых изменений кожи в области хирургического вмешательства с использованием модифицированной Ванкуверской шкалы оценки признаков рубцовой деформации (Vancouver scar scale) П1 (тип рубца), П2 (консистенция), П3 (цвет), П4 (чувствительность рубца).
Статистический анализ результатов исследования был выполнен с помощью пакетов программного обеспечения Statsoft. STATISTICA 10 и Microsoft Excel 2016. Рассчитывали средние значения со стандартной ошибкой среднего, в то время как качественные параметры представляли в виде частот встречаемости признаков в процентах от общего числа пациентов в соответствующих группах.
На заключительном этапе хирургического лечения на рану накладывали салфетки с антисептиком, изолировали смежные пальцы ватно-марлевыми салфетками или ватными дисками, после чего накладывали гипсовую повязку с фиксацией пальца-донора и пальца-реципиента для исключения случайных смещений, на 18-21 день. По истечении этого срока лоскут отсекали, выполняли его окончательное моделирование, ориентируясь на форму ногтевой фаланги соседнего пальца (рис. 4).
Межгрупповые сравнения по количественным показателям проводились с использованием рангового непараметрического критерия Манна - Уитни в случае непараметрического распределения значений показателей и/или значительной разницы дисперсий в группах. Для анализа различий по качественным параметрам применялись критерий хиквадрат или точный критерий Фишера. Различия считались достоверными при недостижении р порогового значения уровня статистической значимости нулевой гипотезы (альфа), равного 0,05.
РЕЗУЛЬТАТЫ
Осмотр области вмешательства в послеоперационном периоде показал, что у большинства пациентов отёк и венозный застой в перемещенных тканях лоскута купировались в течение 7-9 суток, в абсолютном большинстве случаев приживление было полным. При использовании разработанного нами подхода к хирургическому лечению первичное приживление было достигнуто у всех 22 пациентов основной группы. При этом не отмечено каких-либо осложнений на всем протяжении лечения. Кожные швы снимали в среднем через 12-14 суток после выполнения операций. В эти же сроки снимали повязку в области донорского дефекта. Отсечение лоскута и окончательное моделирование комплекса мягких тканей выполняли, как правило, не ранее 21 суток после выполнения операции, что гарантировало успешный исход лечения в целом.
Анализ проявлений болевого синдрома в раннем послеоперационном периоде в группах исследования показал, что, если на первые сутки после вмешательства его величины оценки по шкале ВАШ достоверно не различались, то в дальнейшем в основной группе значение этого показателя было статистически значимо ниже (p < 0,05) относительно соответствующего показателя в группе сравнения (табл. 3).
Оценка динамики показателя шкалы Quick DASH показала, что, если до операции и через 1 месяц значения этого параметра были примерно на одном уровне, то спустя 3 месяца после проведенного лечения и в последующие сроки значения параметров данной шкалы в основной группе были статистически значимо ниже (р < 0,05), чем в группе сравнения (рис. 5). Эти данные свидетельствовали о более высоком функциональном результате лечения при использовании предложенного нами подхода.
Анализ удовлетворенности пострадавших результатами проведенного лечения по¬казал, что в основной группе доли пациентов, оценивших результаты как «отличный» и «хороший», были статистически значимо больше (р < 0,05), чем в группе сравнения (табл. 4). При этом группе 1 было 10 пациентов (40,0 %), которые оценили результат лечения как «неудовлетворительный», в то время как в группе 2 был только один (4,6 %) такой пациент (р < 0,05).
Следует отметить, что основной причиной низкой субъективной оценки анатомических, функциональных и эстетических результатов лечения является остаточная асимметрия в сравнении со здоровыми пальцами контралатеральной кисти. Отсутствие косного фрагмента ногтевой фаланги, поддерживающего мягкие ткани подушечки пальца, также сопровождалось более низкими уровнями удовлетворенности части пациентов результатами лечения. Доля таких лиц из числа пациентов с дефектами торца культи пальца, прооперированных в соответствии с предложенными хирургическими подходами, была статистически значимо ниже, чем в группе сравнения.
Выраженность рубцовых изменений кожи оценивали через 6 и 12 месяцев после проведенного хирургического лечения. Как видно из таблицы 5, через 6 месяцев после проведенного лечения у пациентов основной группы значение показателя Ванкуверской шкалы было статистически значимо ниже (р < 0,05), чем в группе сравнения. Через 12 месяцев после операции отмечалось уменьшение выраженности объективных
составляющих этой шкалы и снижение значений оценки субъективных ощущений у большинства пациентов, при этом снизилась выраженность собственного отношения к сохраняющимся дефектам пальцев кисти.
Наиболее выраженное уменьшение показателя Ванкуверской шкалы было характерно для пациентов основной группы. В этот срок исследования величина данного параметра у пациентов, в лечении которых применяли предложенный нами подход, была статистически значимо ниже (р < 0,05) соответствующего значения в группе 1.
ОБСУЖДЕНИЕ
В целом сравнение достигнутых результатов в исследуемых группах продемонстрировало более высокую (по сравнению с традиционными методами лечения) клиническую эффективность предложенного подхода к хирургическому лечению травм концевых фаланг пальцев кисти, основанного на выполнении пластики торцевых дефектов периферических отделов трехсуставных пальцев кисти, относительно результатов, полученных в группе сравнения.
Итоги исследования свидетельствуют, что применение предлагаемой хирургической тактики у рассматриваемой категории пострадавших позволяет достоверно улучшить результаты лечения пациентов с травмой дистальных отделов трехсуставных пальцев кисти, сопровождающейся утратой части кости ногтевой фаланги и мягких тканей подушечки пальца.
Полученные нами данные согласуются с результатами, представленными в работах других авто¬ров [15, 16, 23-26]. Так, T. Yildirim et al. анализировали долгосрочные функциональные и косметические результаты применения однопальцевого сосудисто-нервного островкового лоскута при выполнении реконструкции обширных дефектов пульпы с обнажением кости у детей.
У 23 детей (средний возраст 4.8 года, от 1 до 10 лет) с травмами кончиков пальцев были выполнены реконструированные вмешательства с использованием однопальцевого лоскута на ножке. Авторы проводили оценку чувствительности кожи травмированных участков пальцев, непереносимости холода, образования рубцов, деформации ногтей, диапазона движений и общей длины пальцев в течение наблюдения, в среднем составившем 7.8 года (от 2 до 13 лет). Одиннадцать пациентов сообщили о чувствительности к холоду в оперированном кончике пальца, а у 15 была выявлена деформация в виде крючковидного ногтя. Объем суммарных актив¬ных движений поврежденного пальца был значительно ниже, чем на неповрежденной стороне (p < 0,001). Тем не менее, было продемонстрировано, что использованный в работе подход является эффективным и надежным методом реконструктивного лечения при травмах кончиков пальцев у детей [15].
J. Schultz et al. в рамках своего исследования разработали и испытали силиконовый колпачок, который надевается на поврежденный палец, образуя влажную камеру, окружающую область травмы. В работе были проанализированы данные пациентов с повреждениями кончиков пальцев на всю толщину, которым невозможно было выполнить простое первичное закрытие дефекта. Пострадавшие были рандомизированы в 2 группы, на области повреждения им была либо наложена повязка, либо использовался силиконовый колпачок для пальца. Авторы включили в исследование 11 пациентов в возрасте от 2 до 72 лет в каждую из двух групп. Все пациенты были удовлетворены косметическим результатом лечения, у 88,9 % не было отмечено изменений чувствительности кожи пальцев, у 73,7 % не было деформации пальца. Длительность эпителизации - от 5 недель. Не было отмечено серьезных побочных явлений при применении использованных в работе устройств. Авторами сделан вывод о высокой эффективности апробированного подхода [16].
По результатам нашего исследования удалось провести успешную апробацию разработанного метода пластики торцевых дефектов ногтевых фаланг трехсуставных пальцев кисти путем перемещения ладонно-боковых и тыльно-боковых кровоснабжаемых лоскутов с одноименного и соседних пальцев без укорочения костных культей ногтевых фаланг с одновременным достижением косметического результата в виде визуального удлинения концевой фаланги. Полученные данные
позволили нам предложить алгоритм лечебно-диагностических мероприятий
при травмах пальцев кисти, представленный на рисунке 6.
Мы полагаем, что диагностика повреждений структур дистальной фаланги трехсуставных пальцев должна быть основана на оценке размеров и тяжести повреждения мягких тканей и костного компонента. При этом следует также учитывать состояние пограничных тканей с уровнем отчленения [23-28].
Размозженный характер повреждения может поставить под сомнение успешность хирургического лечения. В этом случае необходимо выполнить экономную первичную хирургическую обработку раны с удалением заведомо нежизнеспособных тканей. Богатая капиллярная сеть дистальных отделов фаланг пальцев позволяет сохранять мягкие ткани, которые через 2-3 суток при соответствующем лечении будут выглядеть вполне жизнеспособными [29-33]. Основой окончательный диагностики, определяющей степень тяжести повреждения изучаемых структур, должен быть результат рентгенологического исследования, который дает возможность выявить или исключить наличие костных отломков и степень их связи с проксимальным отделом костной части фаланги [25, 34, 35]. В случае выявления свободно лежащего отломка, как показывает наш опыт, его следует удалить, поскольку его жизнеспособность мала, и это может вызвать нагноение в отдаленном периоде (остеомиелит). При выявлении сосудистой патологии у пострадавшего проводят её лечение, что обеспечивает условия для выполнения реконструктивно-пластического вмешательства [36-39].
ЗАКЛЮЧЕНИЕ
Разработан метод закрытия торцевых дефектов ногтевых фаланг II-V пальцев кисти, при реализации которого осуществляется формирование косого П-образного разреза на тыловой поверхности соседнего пальца на уровне средней фаланги с возможностью закрытия дефекта и создания избытка мягких тканей при повороте лоскута в сторону пальца-реципиента. Применение разработанного метода обеспечивает меньшую (по сравнению с использованием стандартных методов хирургического лечения) выраженность болевого синдрома на 10-21 сутки после операции, более низкий уровень показателя шкалы Quick DASH через 3-12 мес., снижение показателя Ванкуверской шкалы выраженности рубцовых изменений кожи через 6-12 мес., более высокую удовлетворенность пациентов результатами проведенного лечения.
1. Kawaiah A, Thakur M, Garg S, et al. Fingertip Injuries and Amputations: A Review of the Literature. Cureus. 2020;12(5):e8291. doi: 10.7759/cureus.8291
2. Березуцкий С.Н. Особенности лечения травматических ампутаций части дистальных фаланг пальцев кисти у детей. Детская хирургия. 2022;26(1):23.
3. Кокарев В.А., Шалин В.В. Травмы пальцев кисти: Ампутация или артропластика? Кремлевская медицина. Кли-нический вестник. 2022;(4):81-83.
4. Маликов М.Х., Артыков К.П., Карим-Заде Г.Д. и др. Отсроченные реконструктивные операции при тяжёлых травмах кисти. Вестник Авиценны. 2022;24(3):404-412. doi: 10.25005/2074-0581-2022-24-3-404-412
5. Петрушин А.Л. Травматические ампутации сегментов кисти, анализ лечебных мероприятий на различных эта¬пах оказания медицинской помощи в сельском районе. Казанский медицинский журнал. 2013; 94 (3): 327-334.5.
6. Jerome JTJ, Malshikare VA. Fingertip Injuries Outcome Score. Plast Reconstr Surg Glob Open. 2022;10(6):e4386. doi: 10.1097/GOX.0000000000004386
7. Wang J, Zhou X, Qiang L, Xue M. Thumb fingertip injuries reconstruction using a dorsoulnar flap of the thumb combined with relay V-Y flaps for donor site repair. J Orthop Surg (Hong Kong). 2022;30(2):23094990211025089.
9. Wang K, Sears ED, Shauver MJ, Chung KC. A systematic review of outcomes of revision amputation treatment for fingertip amputations. Hand (N Y). 2013;8(2):139-45. doi: 10.1007/s11552-012-9487-0
10. Braga Silva J. Fingernail injury. Hand SurgRehabil. 2023:S2468-1229(23)00027-0. doi: 10.1016/j.hansur.2023.01.002
11. Ng HJH, Yuan J, Rajaratnam V. Management of Fingertip Injuries: A Survey of Opinions of Surgeons Worldwide. J Hand Microsurg. 2020;14(1):64-70. German. doi: 10.1055/s-0040-1713072
12. James V, Heng TYJ, Yap QV, Ganapathy S. Epidemiology and Outcome of Nailbed Injuries Managed in Children's Emergency Department: A 10-Year Single-Center Experience. PediatrEmerg Care. 2022;38(2):e776-e783.
13. Woo SH, Kim YW, Cheon HJ, et al. Management of complications relating to finger amputation and replantation. Hand Clin. 2015;31(2):319-38. doi: 10.1016/j.hcl.2015.01.006
14. Samantaray SA, Oommen J, Thamunni CV, et al. Fingertip injury epidemiology: an Indian perspective. J Plast Surg Hand Surg.. 2022;56(4):224-228. doi: 10.1080/2000656X.2021.1962332
15. Yildirim T, Gunturk OB, Erol K, Toros T. Long-term outcomes of homodigital neurovascular island flap reconstruction of fingertip injuries in children. J Hand Surg Eur Vol. 2022;47(8):845-850. doi: 10.1177/17531934221108470
16. Schultz J, Wruck JE, Trips E, et al. Semi-occlusive management of fingertip injuries with finger caps: A randomized controlled trial in children and adults. Medicine (Baltimore). 2022;101(27):e29324.
17. Pastor T, Hermann P, Haug L, et al. Semi-occlusive dressing therapy versus surgical treatment in fingertip amputation injuries: a clinical study. Eur J Trauma Emerg Surg. 2023;49(3):1441-1447. doi: 10.1007/s00068-022-02193-6
18. Koh SH, Park I, Kim JS, et al. Fingertip reconstruction with a subcutaneous flap and composite graft composed of nail bed and volar pulp skin. Arch Plast Surg. 2022;49(1):70-75. doi: 10.5999/aps.2021.01200
19. Mohsen I, Mahmoud M, Shaheen A. Modified Bilateral V-Y Rotation Advancement Flap for Coverage of Fingertip Amputations. J Hand Surg Asian Pac Vol. 2022;27(6):1013-1020. doi: 10.1142/S2424835522500977
20. Balde FB, Mukenge T, Benmassaoud Z, et al. Local or distal flap in the management of digital trauma in children. Afr JPaediatr Surg. 2022;19(1):5-8. doi: 10.4103/ajps.AJPS_56_21
21. Hao R, Wang H, Huo Y, et al. Fingertip degloving injury coverage with homodactyle bipedicled dorsal island flap. Hand Surg Rehabil. 2023;42(2):134-140. doi: 10.1016/j.hansur.2023.01.009
22. Yang S, Li Z. Finger-shaped dressing for fingers and toes after nail surgeries. J Am Acad Dermatol. 2023;88(2):e83-e84. doi: 10.1016/j.jaad.2019.07.020
23. Hunt TJ, Powlan FJ, Renfro KN, et al. Common Finger Injuries: Treatment Guidelines for Emergency and Primary Care Providers. Mil Med. 2023:usad022. doi: 10.1093/milmed/usad022
24. Xu J, Cao JY, Graham DJ, et al. Clinical Outcomes and Complications of Primary Fingertip Reconstruction Using a Reverse Homodigital Island Flap: A Systematic Review. Hand (N Y). 2023;18(2):264-271.
26. Moellhoff N, Throner V, Frank K, et al. Epidemiology of hand injuries that presented to a tertiary care facility in Germany: a study including435 patients. Arch Orthop Trauma Surg. 2023;143(3):1715-1724.
27. Delle Femmine PF, Bruno E, Tosi D, et al. Reversed distal laterodigital adipofascial flap for nail-bed reconstruction. Microsurgery. 2023. doi: 10.1002/micr.31048
28. Ji Z, Nie R, Li S, et al. Clinical effects of resurfacing fingertip amputations in long fingers using homodigital dorsal neurofascial broaden pedicle island flaps. J Plast Surg Hand Surg. 2023;57(1-6):453-458.
29. Martin-Playa P, Foo A. Approach to Fingertip Injuries. Clin Plast Surg. 2019;46(3):275-283. doi: 10.1016/j.cps.2019.02.001
30. Neustein TM, Payne SH Jr, Seiler JG 3rd. Treatment of Fingertip Injuries. JBJSRev. 2020;8(4):e0182. doi: 10.2106/JBJS. RVW.19.00182
31. Venkatesh A, Khajuria A, Greig A. Management of Pediatric Distal Fingertip Injuries: A Systematic Literature Review. Plast Reconstr Surg Glob Open. 2020;8(1):e2595. doi: 10.1097/GOX.0000000000002595
32. Golinvaux NS, Maslow JI, Hovis JP, Lee DH. Fingertip Injury and Management. JBJS Essent Surg Tech. 2019;9(3):e30. doi: 10.2106/JBJS.ST.19.00008
33. Mak WK, Cheah JM, Chua DT, et al. Outcomes of Surgically Treated Fingertip Injuries in Migrant Workers. Ann Acad Med Singap. 2020;49(6):405-407.
34. Gunasagaran J, Sian KS, Ahmad TS. Nail bed and flap reconstructions for acute fingertip injuries - A case review and report of a chemical burn injury. J Orthop Surg(Hong Kong). 2019;27(2):2309499019839278.
36. Zhang JF, Wang L, Hao RZ, et al. Treatment of fingertip avulsion injuries using two periposition pedicled flaps. JPlast ReconstrAesthet Surg. 2019;72(4):628-635. doi: 10.1016/j.bjps.2018.12.051
37. Tang JB. Fingertip repair methods: choices for different fingers and sides emphasizing sensation. J Hand Surg Eur Vol. 2019;44(10):1109-1111. doi: 10.1177/1753193419876496
38. Petrella G, Tosi D, Sapino G, Adam R. Fingertip defect reconstruction with a modified pivot flap. J Hand Surg Eur Vol. 2021;46(1):75-79. doi:
Информация об авторах:
Игорь Владимирович Чмырев - доктор медицинских наук, доцент, начальник кафедры
Николай Григорьевич Губочкин - доктор медицинских наук, доцент
Теги: травма пальцев кисти
234567 Начало активности (дата): 25.02.2024 19:22:00
234567 Кем создан (ID): 989
234567 Ключевые слова: травма пальцев кисти, ногтевая фаланга, торцевой дефект, пластика кожным лоскутом, болевой синдром, рубец кожи
12354567899
Похожие статьи
Оценка состояния стопы после заимствования некровоснабжаемых фаланг пальцев для аутотрансплантации на кистьРевизионная реконструкция шейного отдела позвоночника у пациента с ранней глубокой инфекцией области хирургического вмешательства, осложненной угловым кифозом: клинический случай и краткий обзор литературы
Рентген на дому 8 495 22 555 6 8
Лечение пациента с ятрогенным повреждением лучевого нерва после остеосинтеза плечевой кости: клинический случай
Выживаемость несвязанных керамических эндопротезов лучезапястного сустава



