 23.11.2023
23.11.2023
Первичное тотальное эндопротезирование коленного сустава с применением активной роботической системы
Тотальное эндопротезирование коленного сустава (ТЭКС) признано наиболее эффективным методом лечения тяжёлых форм остеоартроза, позволяющим устранить болевой синдром, улучшить физическую активность и качество жизни пациентов
Актуальность темы исследования
Тотальное эндопротезирование коленного сустава (ТЭКС) признано наиболее эффективным методом лечения тяжёлых форм остеоартроза, позволяющим устранить болевой синдром, улучшить физическую активность и качество жизни пациентов. В России в 1994 г. было выполнено всего 3000 вмешательств, в 2013 г. уже 54 тыс., а в 2019 г. 70 тыс. операций ТЭКС [Р.М.Тихилов, 2013, Т.М.Андреева, 2017], при этом отмечено, что постепенно увеличивается количество артропластик у пациентов молодого возраста [RRavi, 2012].
В то же время, по данным литературы, лишь 80% пациентов довольны результатами этой операции [Г.М.Кавалерский, 2016], при этом число ревизионных артропластик коленного сустава превышает 10 % [S.Kurtz, 2007; А.Khlopas, 2019].
Успех ТЭКС зависит от множества факторов: планирования, дизайна и материала имплантата, хирургической техники и подхода, метода фиксации, реабилитации, опыта хирурга и его команды.
Ошибки планирования и неточности резекции кости приводят к неправильной позиции имплантата, что влияет на функциональный результат, проявляется выраженным болевым синдромом, ограничением амплитуды движения и может привести к раннему расшатыванию и износу компонентов эндопротеза [Г.М.Кавалерский, 2015, 2016; D.Arbab, 2018; C.W.Kim, 2020]. В значительной мере на результат лечения влияет и коморбидный фон пациента, в котором особую роль играет избыточная масса тела. У пациентов с высоким индексом массы тела (ИМТ) функциональный результат после ТЭКС, как правило, ниже, чем у пациентов с нормальным весом, что обусловлено трудностями как при доступе и позиционировании имплантата, так и при активизации пациента [
В то же время, ТЭКС остается методом выбора в лечении пациентов с тяжелыми формами гонартроза. Поиск путей совершенствования операционной техники привел к появлению роботизированных хирургических систем, призванных обеспечить прецизионное выполнение плана операции, оптимальное позиционирование имплантата и безопасность пациента [А.В.Лычагин, 2016; B.Kayani, 2020].
Особое место среди пациентов, нуждающихся в ТЭКС, занимают лица с избыточной массой тела, доля которых среди кандидатов на такую операцию весьма высока, достигая 50 и более процентов. Многие авторы считают ожирение противопоказанием к выполнению ТЭКС, причем в зависимости от величины ИМТ эти противопоказания варьируются от относительных до абсолютных [Н.Н.Корнилов, 2015; В.С.Приходько, 2015; R.S.Namba, 2005]. Эти ограничения фирма-разработчик активной роботической системы TSolution-One распространила и на робот-ассистированные операции, определив возможность выполнения ТЭКС по данной технологии при ИМТ, не превышающем 35 кг/м . Основанием для таких ограничений, помимо вышеуказанных, послужили технические сложности, не позволяющие у ряда пациентов с избыточным ИМТ соблюсти в полной мере технологию позиционирования.
Опыт роботической ассистенции при ТЭКС еще небольшой, в связи с чем, до сих пор нет единого мнения о том, способны ли эти дорогостоящие технологии помочь добиться улучшения результатов лечения пациентов в сравнении с традиционными операционными методиками. Не решенным остается также вопрос, насколько доступны новые возможности лечения пациентам с высоким ИМТ, которым часто отказывают в ТЭКС. Поэтому вопрос изучения эффективности робот-ассистированных операций ТЭКС в сравнении с традиционными методиками, а также уточнение противопоказаний к таким операциям для лиц с повышенным ИМТ, является актуальной задачей травматологии и ортопедии.
Цель работы - улучшить результаты лечения пациентов, страдающих гонартрозом, путем использования активной роботизированной хирургической системы.
Задачи работы:
1. Изучить точность позиционирования компонентов эндопротеза коленного сустава при его первичном эндопротезировании с применением мануальной техники и компьютерной навигации в сравнении с активной роботизированной системой.
2. Провести сравнительный анализ результатов лечения пациентов после первичного ТЭКС, выполненного с применением распространенных методик и роботизированной техники.
3. Оценить уровень тревожности пациентов и их оценку комфортности лечения при применении различных техник ТЭКС.
4. Изучить основания для существующих ограничений применения активной роботизированной системы при выполнении ТЭКС у пациентов с избыточной массой тела.
5. Обосновать возможность расширения показаний к первичному ТЭКС у пациентов с избыточной массой тела с применением активной роботизированной системы.
6. Провести анализ результатов робот-ассистированных операций ТЭКС у пациентов с избыточной массой тела и на этом основании скорректировать показания к первичной артропластике у данного контингента.
Вид работы: Тема относится к плановой работе кафедры травматологии, ортопедии и хирургии катастроф ФГАОУ ВО Первый МГМУ им. И.М.Сеченова МЗ РФ (Сеченовский Университет) «Первичное тотальное эндопротезирование коленного сустава с применением активной роботической системы» по специальности 14.01.15 - «травматология и ортопедия» и утверждена на Ученом совете (протокол № 10/18-у от 10.10.2018 г.).
Научная новизна
1. Впервые проведен пошаговой сравнительный анализ всех основных этапов операции первичной артропластики коленного сустава с использованием различных техник, на основе чего показаны преимущества использования активной роботической системы.
2. Впервые уточнена возможность применения активной роботической системы при артропластике коленного сустава у пациентов с избыточной массой тела, за счет чего расширены показания к выполнению таких операций у данного контингента.
Практическая значимость
1. Внедрение активной ортопедической роботической хирургической системы в клиническую практику позволит улучшить позиционирование компонентов эндопротеза коленного сустава, снизить риск технической ошибки и асептического расшатывания по сравнению с традиционными техниками.
2. Уточнение противопоказаний к выполнению ТЭКС с применением активной роботической системы позволит повысить доступность таких операций для пациентов с избыточной массой тела.
Положения, выносимые на защиту
1. Операции ТЭКС, выполненные с применением активной роботической системы «TSolution-One» (THINK Surgical Inc., Фримонт, Калифорния, США), имеют преимущество в точности навигации перед традиционными техниками, в том числе компьютерной навигацией, что способствует улучшению результатов лечения.
2. Непосредственным противопоказанием к использованию активной роботической системы для пациентов с ожирением следует считать не показатель индекса массы тела, а расстояние от дальнего кортикального слоя большеберцовой кости до поверхности кожи как фактор, определяющий возможность интраоперационного установления фиксатора большеберцовой кости в соответствии с определенными методикой технологическими параметрами.
Внедрение в практику
Предложенные методы внедрены в практику клиники травматологии, ортопедии и патологии суставов УКБ № 1 Первого МГМУ им. И.М.Сеченова г. Москвы, являющейся клинической базой кафедры травматологии, ортопедии и хирургии катастроф ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет).
6
Материалы исследования использованы в преподавании цикла травматологии и ортопедии студентам, клиническим ординаторам и аспирантам, проходящим обучение в ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет) Личный вклад автора
Автор лично сформулировал цель и задачи исследования. Он лично проводил отбор пациентов, их предоперационное планирование и подготовку, принял участие во всех операциях, осуществлял динамическое послеоперационное наблюдение пациентов. Автор проводил пошаговый сравнительный анализ основных этапов операции первичной артропластики коленного сустава, уточнил возможность применения активной роботической системы при артропластике коленного сустава у пациентов с избыточной массой тела. Им проведен сбор и анализ полученных результатов, их статистическая обработка, сформулированы выводы и практические рекомендации.
Публикации
По материалам диссертации опубликовано 8 работ, в том числе 1 научная статья в журнале, включенном в Перечень рецензируемых научных изданий Сеченовского Университета / Перечень ВАК при Минобрнауки России, в которых должны быть опубликованы основные научные результаты диссертаций на соискание ученой степени кандидата наук; 2 статьи в изданиях, индексируемых в международных базах Web of Science, Scopus; иные публикации - 1 (обзорная статья); публикаций в сборниках материалов международных и всероссийских научных конференций - 4.
Апробация работы
Результаты диссертационной работы доложены:
• «Ассоциация травматологов-ортопедов России» (06.12.2019 г. Грозный);
• онлайн-конференция клуба «Евразийский Ортопедический Форум» (26.01.2021 г.Москва);
• онлайн-конференция клуба «Евразийского Ортопедического Форума» (25.05.2021 г.Москва);
• «Илизаровские чтения» (16-18.06.2021 г. Курган);
• «Евразийский Ортопедический Форум 2021» (25-26.06.2021 г. Москва);
• «III Научно-практическая конференция Пироговские курсы 2021 «От гипсовой повязки к высокотехнологичному остеосинтезу»» (14-15.10.2021 Крым, г. Севастополь);
• «VI Пироговский Форум травматологов-ортопедов, посвященный 50-летию кафедры травматологии, ортопедии и медицины катастроф МГМСУ имени А. И. Евдокимова» (2122.10.2021 г. Москва);
• «Вреденовские чтения 2021» (28-30.10.2021 г. Санкт-Петербург);
• онлайн-конференция клуба «Евразийский Ортопедический Форум» (13.12.2021 г.Москва).
Соответствие диссертации паспорту научной специальности
Диссертационная работа соответствует паспорту специальности 14.01.15 - Травматология и ортопедия», а именно посвящена улучшению результатов лечения пациентов, страдающих гонартрозом, путем использования активной роботизированной хирургической системы при тотальном эндопротезировании, что будет способствовать сохранению здоровья населения, восстановлению трудоспособности, сокращению продолжительности и улучшению качества лечения. Области исследования: разработка и усовершенствование методов диагностики и лечения заболеваний и повреждений опорно-двигательной системы, и внедрение их в клиническую практику. Задачи и положения, выносимые на защиту диссертации, соответствуют формуле специальности 14.01.15 - Травматология и ортопедия. Результаты проведенного исследования соответствуют пунктам 1, 3, 4 паспорта специальности
«Травматология и ортопедия».
Диссертация изложена на 218 страницах машинописного текста и состоит из введения, 5 глав собственных наблюдений, заключения, выводов, практических рекомендаций, приложения и списка литературы из 176 источников (58 отечественных и 118 иностранных авторов). Работа иллюстрирована 123 рисунками, 12 таблицами.
В клинике травматологии, ортопедии и патологии суставов Университетской клинической больницы №1, ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава России (Сеченовский Университет) с 2018 по 2021г. выполнено проспективное, рандомизированное исследование 99 пациентов старше 18 лет с остеоартрозом коленного сустава 3-4 степени по классификации Kellgren-Lowrence и болевым синдромом выше 5 баллов по 10-балльной ВАШ. Всем пациентам выполнено ТЭКС эндопротезом коленного сустава фирмы Zimmer® (NexGen, Persona).
В первом этапе исследования приняли участие 92 пациента, имевшие ИМТ не выше 35 кг/м ; они рандомизированы методом случайных чисел в отношении 1:1:1 на три равные группы. После окончания обследования пациентам сообщали результаты рандомизации, разъясняли особенности планируемого хирургического лечения, и пациенты подписывали согласие на операцию. Всем выполнили операцию ТЭКС с использованием:
• пациентам группы «А» (n = 29) - активной роботической системы TSolution One;
• пациентам группы «В» (n = 32) - стандартного набора инструментов и мануальнойтехники;
• пациентам группы «С» (n = 31) - компьютерной навигации.
На втором этапе исследования была дополнительно сформирована группа «D», в которую включили 7 пациентов, соответствующих основным критериям включения, однако имеющим индекс массы тела свыше 35 кг/м2; им выполнили ТЭКС с применением активной роботической системы TSolution One по той же технологии, что и в группе «А».
Среди всех пациентов преобладали женщины (82,6 %). Возраст составил от 39 лет до 91 года, в среднем 66,3 ± 13,2 года. Индекс массы тела в среднем равен 31,6 кг/м2. Большинство пациентов (66,3 %) имели идиопатический остеоартроз. Коморбидный статус оценивали по классификации American Society of Anesthesiologists (ASA): ASA-I встречалось в 38,0 % случаев, ASA- II в 53,3 %, и ASA III - в 8,7% наблюдений.
В предоперационном периоде и после операции оценивали болевой синдром по 10- балльной шкале ВДШ, функциональное состояние сустава по шкалам OKS, WOMAC. Оценивали также качество жизни (по SF-36), степень тревожности пациентов (тест Спилбергера), комфортность лечения (из 10 баллов). Оценивали время всех этапов проведения операции, объем кровопотери. Проводили анализ амплитуды движений, окружности бедра в нижней трети и голени в верхней трети в послеоперационном периоде. По данным лучевой диагностики определяли положение имплантата, механическую ось конечности, уровень щели коленного сустава относительно надколенника, угол наклон бедра во фронтальной плоскости (LDFA), угол наклона бедра в сагиттальной плоскости, угол ротации бедренного компонента относительно надмыщелков бедренной кости, угол наклона плато большеберцовой кости (имплантата) во фронтальной плоскости (MPTA) и в сагиттальной плоскости, угол ротации тибиального компонента относительно бугристости большеберцовой кости, степень деформации, механическую ось конечности, ротационное смещение компонентов эндопротеза. Для этого выполняли стандартную рентгенографию, телерентгенографию с осевой нагрузкой и компьютерную томографию.
Сроки плановых визитов пациентов для контрольного осмотра были определены через 3, 6 и 12 месяцев после операции, и далее раз в год для наблюдения в динамике.
Общим для всех наблюдавшихся нами пациентов были следующие ключевые моменты лечения:
S Антибиотикопрофилактику инфекционных осложнений проводили за 30 мин до операции внутривенно цефалоспоринами третьего поколения, которую продолжали в течение 24 ч. после операции и далее до 3 дней после операции. Перед разрезом кожи выполняли внутривенное введение транексамовой кислоты.
S Все вмешательства были выполнены в условиях субарахноидальной анестезии с внутривенной седацией и стандартным интраоперационным мониторингом.
•S Операционный доступ осуществляли по средней линии с рассечением капсулы и
медиального удерживателя надколенника с его латеральным вывихом. Турникет не применяли, гемостаз во время операции выполняли электрокоагуляционным инструментом.
S Всем пациентам устанавливали эндопротез коленного сустава фирмы Zimmer® (NexGen, Persona) с сохранением и с замещением задней крестообразной связки с цементной фиксацией и фиксированным вкладышем.
Пластику надколенника не производили, выполняли только удаление остеофитов и циркулярную денервацию.
S В послеоперационном периоде всем пациентам проводили системную мультимодальную аналгезию, антикоагулянтную и антибактериальную терапию.
•S Протокол реабилитации включал начало пассивного движения колена через 2 часа
после операции, активные движения и вставание с кровати через 24 ч после операции, ходьбу с ограниченной нагрузкой (при помощи костылей) до 3 недель после операции, после чего разрешали полную нагрузку на оперированную ногу.
В группах В и С основной этап операции выполняли по стандартным технологиям.
Проведение операции включало 3 этапа.
Этап 1. Предоперационное обследование и планирование.
Выполняли КТ нижней конечности с калибровочным стержнем (рисунок 1).
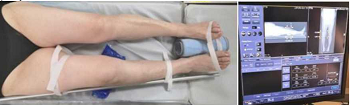
Рисунок 1 - Выполнение КТ пациенту: укладка пациента с калибровочным стержнеми отображение данных на мониторе компьютерного томографа
Данные КТ вводили в специальную установку трехмерного планирования TPLAN, с помощью которой вначале выполняли сегментирование бедренной и большеберцовой костей на всем протяжении - от тазобедренного до голеностопного суставов (рисунки 2,3).
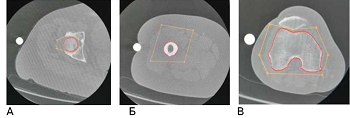
Рисунок 2 - Сегментирование на установке TPLAN: головки бедренной кости (А),диафиза бедренной кости (Б), мыщелков бедренной кости

Рисунок 3 - Сегментирование на установке TPLAN: тибиального плато (А), голеностопногосустава (Б)
Виртуально проводили подбор и позиционирование имплантата (рисунок 4).
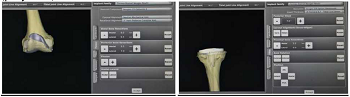
Рисунок 4 - Позиционирование бедренного компонента (А), и тибиального компонента (Б), на мониторе TPLAN
После завершения позиционирования проводили окончательное согласование и утверждение плана операции и записывали его на компакт-диск, который впоследствии относили в операционную для введения в роботическую систему.


Рисунок 5 - Установка TSolution One, подготовленная к операции (внешний вид робота -А, и набор инструментов -Б)
Этап 2. Интраоперационная подготовка роботизированной установки.
Нестерильная подготовка. Устанавливали нестерильные инструменты и проводили кинематические испытания установки.
Стерильная подготовка. Робота драпировали стерильным бельем, устанавливали стерильные инструменты, проводили повторный кинематический тест стерильных узлов (рисунок 5).
Этап 3. Выполнение операции.
Во время операции после осуществления хирургом стандартного доступа устанавливали маркеры, пины, датчики смещения кости, проводили регистрацию виртуальных точек. Далее роботическая рука самостоятельно высокооборотистой фрезой проводила поэтапные резекции бедренной и большеберцовой костей (рисунок 6).

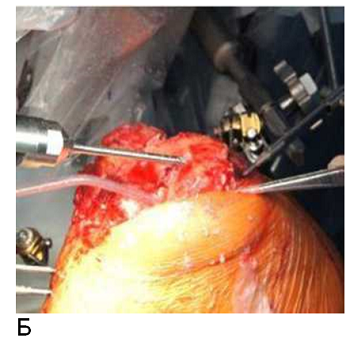
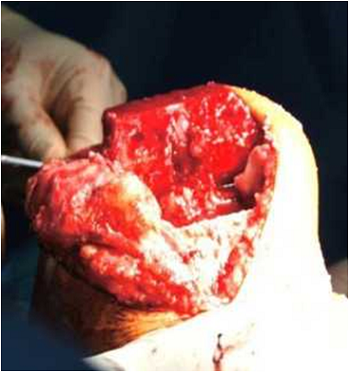
Рисунок 6 - Выполнение роботом резекции бедренной кости (А, Б), окончательный вид раны коленного сустава после фрезерования и доработки кости (В)
Анализ всех этапов проведения операции непосредственно в операционной, без учета предоперационного планирования, показал, что в группе А тратится больше времени (около 45 мин) на выполнение нестерильной и стерильной фаз настройки робота, однако этот этап выполняют без присутствия пациента. Время же пребывания пациента непосредственно на операционном столе в группе А составило в среднем 76,7 мин, что всего на 7,4 мин больше, чем в группе С, и на 16,3 мин больше, чем в группе В. Хотя эти отличия являются статистически значимыми (р < 0,01), клинического значения эта разница, особенно с группой С, не имеет. Можно отметить, что среднее время, затраченное на непосредственное выполнение костных опилов, в группе А было меньше, чем в группах В и С соответственно на 2,3 и 5,3 мин, что, впрочем, также не имеет клинической значимости (таблица 1).
Таблица 1 - Затраты времени на выполнение этапов операции (средние значения в мин)
|
Этапы операции |
Гр. А (n=29) |
Гр. В (n=32) |
Гр. С (n=31) |
Сравнение А и В |
Сравнение А и С |
Сравнение В и С |
|
Подготовка робота |
45,0 ± 10 |
- |
- |
+45,0 |
+45,0 |
- |
|
Доступ |
9,6 ± 3,1 |
9,0 ± 4,3 |
10,1 ± 3,2 |
ю 9 + II |
-0,5 (p=0,284) |
-1,1 (p<0,01) |
|
Костная регистрация |
14,2 ± 6,1 |
- |
5,5 ± 3,6 |
+14,2 (p<0,001) |
+8,7 (p<0,001) |
о о |
|
Резекция кости |
12,7 ± 3,4 |
15,0 ± 5,7 |
18,0 ± 4,2 |
-2,3 (p<0,01) |
-5,3 (p<0,001) |
-3,0 (p<0,001) |
|
Примерка |
10,1 ± 2,3 |
5,3 ± 2,0 |
5,7 ± 2,3 |
+4,7 (p<0,001) |
+4,4 (p<0,001) |
-0,4 (p<0,01) |
|
Цементирование |
13,6 ± 1,5 |
13,7 ± 2,3 |
13,0 ± 2,8 |
-0,1 (p=0,312) |
+0,6 (p=0,225) |
+0,7 (p=0,125) |
|
Ушивание |
16,5 ± 3,8 |
17,4 ± 6,0 |
17,0 ± 2,7 |
-0,9 (p=0,45) |
-0,5 (p=0,278) |
+0,4 (p=0,301) |
|
Время без учета подготовки робота |
76,7 ± 3,3 |
60,4 ± 20,3 |
69,3 ± 15,6 |
+16,3 (p<0,01) |
+7,4 (p<0,01) |
-8,9 |
|
Общее время |
121,7 ± 30,2 |
60,4 ± 20,3 |
69,3 ± 15,6 |
+61,2 |
+52.4 |
-8,9 |
Наименьший объем кровопотери был зафиксирован в группе А (971,4 мл), что на 124,5 мл меньше, чем в группе С и на 152,7 мл меньше, чем в группе В (р = 0,001).
После операции выполняли контрольные рентгенограммы, телерентгенографию и КТ нижней конечности (рисунок 7).
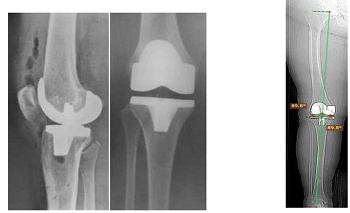
Рисунок 7 - Послеоперационная рентгенография коленного сустава (А), телерентгенография нижней конечности (Б)
В группах В и С, в отличие от группы А, этап планирования был менее кропотливый, не было необходимости в долгой укладке и калибровке, однако в ходе операции нельзя гарантировать идеальное расположение имплантата и точное воспроизведение предоперационного плана. Слишком много факторов, включая возможность неточных действий или ошибки хирурга, могут повлиять на качество выполняемых костных опилов, в отличие от робот-ассистированной операции, где уровни резекции загружены в систему и воспроизводятся с прецизионной точностью.
В отличие от группы А, где режущим инструментом являлась высокооборотистая фреза, при выполнении операций пациентам групп В и С использовали щелевидный направитель и стандартный мануальный инструмент (осцилляторную пилу), что повышало риск погрешности при выполнении костных опилов и ожога кости.
Так, в группе А отклонение механической оси конечности отмечено в 27,6 % наблюдениях и не превысило 1°, что является допустимым, тогда как в группе С отклонения встретились у 51,6 % (в 1,9 раза чаще) и доходили до 2°, а в группе В они встречались у всех 32 пациентов (чаще, чем в группе А, в 3,6 раза), причем в 15,6 % случаев это отклонение превысило 3° (таблица 2).
14
Таблица 2 - Изменения механической оси нижней конечности во фронтальной плоскости (средние значения в градусах)
|
Группа (n) |
До операции |
После операции |
1 год после |
норма |
|
Группа А- (n=29) |
170,5 ± 1,8 |
179,6 ± 0,5 |
179,7 ± 0,5 |
180° |
|
Группа В- (n=32) |
169,9 ± 1,9 |
177,8 ± 1,1 |
177,8 ± 1,1 |
180° |
|
Группа С- (n=31) |
170,4 ± 1,8 |
179,1 ± 0,6 |
179,2 ± 0,6 |
180° |
|
Всего |
170,3 ± 1,8 |
178,8 ± 1,1 |
178,8 ± 1,1 |
180° |
|
Р |
0,369 |
<0,001 |
<0,001 |
|
Послеоперационное ротационное расположение бедренного компонента относительно межнадмыщелковой линии в группе А имело незначительный разброс (0,72°), тогда как в группе С он составил 1,74°, а в группе В - 2,44° (соответственно, больше в 2,4 и 3,4 раза, р < 0,01). При планировании положения тибиального компонента мы выставляли ориентиры на медиальную треть бугристости, гребень большеберцовой кости, ориентировались на линию Akagi. Ротационное расположение тибиального компонента в группе А составило 3° наружной ротации, в группе С - 3,97° и в группе В - 4,03° (в этой группе значение человеческого фактора было наиболее значимо).
Послеоперационный болевой синдром в группе А снижался быстрее, чем в других группах, и на 5 сутки наблюдения его среднее значение составило 3,5±1,7 баллов по ВАШ, что на 0,5 балла меньше, чем в группе С и на 0,7 балла, чем в группе В (рисунок 8).
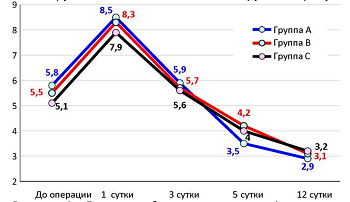
Рисунок 8 - Динамика болевого синдрома (средние значения в баллах по ВАШ)
Измерения окружности области коленного сустава в группах А и С показали примерно одинаковые средние значения, и на 8 % меньше, чем в группе В.
Средний показатель амплитуды активных движений в оперированном коленном суставе (сгибание-разгибание) через 1 год после операции в группе А составил 127,5 ± 1,6°, что на 2,8° больше, чем в группе С, и на 11,1°, чем в группе В (р < 0,01) (рисунок 9).
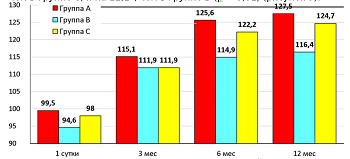
Рисунок 9 - Средняя амплитуда активных движений в коленном суставе (в градусах)
При отличных ранних послеоперационных результатах, через 1 год наблюдения статистически значимых различий в результатах оперативного лечения по шкалам KSS, OKS, WOMAC не получено, пациенты возвращались к привычному образу жизни уже через 3 месяца (рисунок 10).
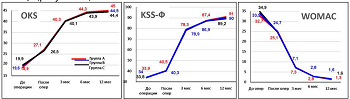
Рисунок 10 - Оценка функции коленного сустава по шкалам OKS, KSS-Ф, WOMAC -средние значения в баллах
По результатам FJS-12 через 1 год, средняя оценка лучше в группе А на 4 %, чем в группе В, и на 2,7 %, чем в группе С (рисунок 11).
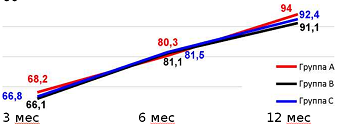
Рисунок 11 - Оценка коленного сустава по FJS-12 (средние значения в баллах)
При анализе средних показателей по STAI, отмечено, что уровень тревоги в группе А был до операции на 9,4 % выше чем в группе В и на 5,4 % - чем в группе С, что можно объяснить не вполне достаточной информацией о предстоящей операции и пугающим многих словом «робот» применительно к предстоящему хирургическому вмешательству.
В то же время, общие впечатления пациентов о комфортности проведенного в стационаре лечения после того, как рассеялись страхи, в группе А уже к 5 суткам послеоперационного периода были лучше, чем в группах В и С, где отмечены абсолютно идентичные результаты (рисунок 12).
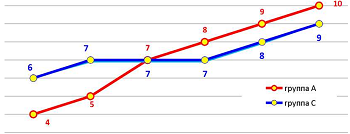
до операции 1 сутки после 3 сутки после 5 сутки после 7 сутки после 12 сутки после
Рисунок 12 - Оценка пациентами комфортности лечения (в баллах по 10-балльной шкале)
Таким образом, наши результаты выполнения ТЭКС с использованием активной роботической техники показали очевидное преимущество такой техники, однако существенным противопоказанием к ее применению оставался ИМТ, превышающий 35 кг/м , в то время как такие высокие значения ИМТ отмечались у 41 % пациентов, обращавшихся к нам за консультативной помощью. Морбидное ожирение влечет за собой ряд соматических заболеваний, в свою очередь, существенно повышающих операционный риск и ставящих под сомнение достижение положительного результата ТЭКС, однако мы поставили задачу разобраться, всем ли без исключения пациентам с ИМТ > 35 кг/м действительно невозможно выполнить робот-ассистированную операцию.
Мы исходили из того, что ограничение относительно возможности выполнения операции с использованием активной роботической системы не напрямую связано с ожирением, а основано на невозможности у лиц с большой толщиной подкожно-жирового слоя в области верхней трети голени установить тибиальный фиксирующий пин с соблюдением всех технических требований. Измерение этого слоя проводили по компьютерным томограммам.
КТ коленного сустава оценивали в двух проекциях. На сагиттальной проекции от передних отделов мыщелков большеберцовой кости откладывали дистально 8 см. Далее на этом уровне в аксиальной проекции размечали сектор проведения фиксирующего пина от 30 до 45°. В этом коридоре отмеряли стандартную длину пина (12,5 см) и разбивали линию на отрезки: от внутреннего до наружного кортикального слоя кости (пин должен быть фиксирован в оба этих слоя) - X, от наружного кортикального слоя кости до кожи - Y, от кожи до универсального зажима - Z, длина универсального зажима - F (рисунок 13).
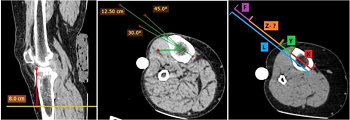
Рисунок 13 - Измерение параметров тканей пациента в верхней трети голени: уровень проведения пина на сагиттальной проекции (А); сектор проведения пина на аксиальной проекции (Б); зоны вдоль стандартной длины пина в соответствии с формулой (В)
Таким образом, L=X+Y+Z+F.
В этой формуле фиксированными величинами являются: длина пина (L=12,5 см), ширина универсального фиксирующего зажима (F=2 см), а также расстояние от поверхности кожи до фиксирующего зажима, для которого фирма-производитель в своих технических условиях определила минимальное значение 3 см (Z > 3 см). Отсюда имеем индивидуальные параметры пациента:
(X+Y) = L - (Z + F)
(X+Y) < 12,5 - 2 - 3 (X+Y) < 7,5 см
По нашим наблюдениям, расстояние между двумя кортикальными слоями большеберцовой кости составляет обычно от 3 до 4,5 см (в среднем 3,7 см), а, значит, допустимая толщина мягких тканей (и прежде всего - подкожно-жировой клетчатки) для соблюдения технических условий робот-ассистированной операции ТЭКС также не должна превышать 3-4,5 см (в среднем - 3,8 см).
Основываясь на этих расчетах, на втором этапе исследования у 18 человек, обратившихся для проведения ТЭКС, и имеющих в качестве единственного противопоказания к робот-ассистированной операции ИМТ >35 кг/м , были проведены расчеты по нашей формуле на основе данных КТ, и из тех 7 пациентов (38,8 %), у кого параметр Z был больше или равен 3 см, создана дополнительная группа «D». Среднее значение ИМТ у пациентов этой группы составило 40,4 кг/м (от 35,2 до 46,5 кг/м ), а среднее значение Z - 5,1 см, что позволяло соблюсти технические условия робот- ассистированной операции (рисунок 14).
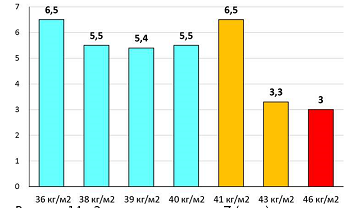
Рисунок 14 - Значение параметра Z (в см) у пациентов группы D
Всем пациентам группы D выполнили робот-ассистированную операцию по тому же техническому протоколу, что и в группе А.
Результаты операции по всем исследованным параметрам были сопоставимы с аналогичными данными, полученными в группе А (таблица 3).
По сравнению с группой А среднее общее время операции увеличилось в группе D на 8,9 мин, прежде всего за счет выполнения хирургического доступа (+4,4 мин), примерки (+2,6 мин) и костной регистрации (+2,5 мин), что связано с большей толщей мягких тканей у пациентов с морбидным ожирением. Однако, эти отличия незначительны и не являются клинически значимыми.
Таблица 3 - Затраты времени на выполнение этапов операции (средние значения в мин) - группы А и D
|
Этапы операции: |
Гр. D (n=7) |
Гр. А (n=29) |
Сравнение группы D и А |
|
Подготовка робота |
42,2 ± 8,9 |
45,0 ± 10,0 |
-2,8 (p<0,001) |
|
Доступ |
14,0 ± 4,3 |
9,6 ± 3,1 |
+4,4 (p<0,001) |
|
Костная регистрация |
16,7 ± 4,2 |
14,2 ± 6,1 |
+2.5 (p<0,001) |
|
Резекция кости |
14,4 ± 2,4 |
12,7 ± 3,4 |
+1,7 (p<0,01) |
|
Примерка |
12,7 ± 2,6 |
10,1 ± 2,3 |
+2,6 (p<0,001) |
|
Цементирование |
12,5 ± 2,1 |
13,6 ± 1,5 |
+1,1 (p<0,01) |
|
Ушивание |
18,4 ± 5,2 |
16,5 ± 3,8 |
+1,9 (p<0,001) |
|
Общее время |
130,6 ± 10,3 |
121,7 ± 30,2 |
+8,9 (p<0,001) |
Сравнение таких показателей как точность позиционирования имплантата, выравнивание механической оси конечности, объем интраоперационной кровопотери, болевой синдром, динамика послеоперационного отека, амплитуда движения в суставе, оценка функции конечности по шкалам опросникам, комфортность лечения и качество жизни между группами А и D за все время наблюдения не имело статистически значимых отличий.
Преимущества применения активной ортопедической роботической хирургической установки (АОРХС) при выполнении ТЭКС заключаются в следующем:
S Возможность цифрового детального предоперационного планирования на основе персонифицированных данных КТ-обследования пациента;
S Минимизация влияния на ход операции «человеческого фактора»;Прецизионная резекция и точное позиционирование имплантата в соответствии с планом;
S Возможность интраоперационной оценки стабильности сустава, амплитуды движения и выравнивания оси конечности;
S Возможность добиться баланса мягкотканых структур коленного сустава после примерки имплантатов ориентируясь на данные монитора, где указана информация о выравнивании оси конечности.
Таким образом, несмотря на то, что предоперационное планирование РаТЭКС занимает до 3 часов на одного пациента, а после этого требуется около 45 минут для непосредственной подготовки робота уже в операционной, пациент не замечает этих подготовительных этапов, так как для него длительность пребывания в операционной ограничивается временем непосредственно выполняемой операции, и превышает длительность выполнения операций с применением традиционных техник не более, чем на 16 минут. Вместе с тем, РаТЭКС имеет ряд преимуществ, важнейшим из которых является максимально точное выполнение костных опилов в соответствии с предоперационным планом, исключающее отклонения или ошибки, связанные с «человеческим фактором», максимально точно расположить имплантаты и свести к минимуму послеоперационные отклонения оси оперированной конечности. Кроме того, проведенное нами исследование показало, что использование АОРХС по сравнению с традиционными хирургическими техниками позволяет статистически значимо снизить объем интраоперационной кровопотери, увеличить амплитуду активных движений в оперированном суставе, повысить оценку пациентами комфортности лечения.
Важным направлением дальнейших исследований в отношении операций ТЭКС с использованием АОРХС должно явиться сокращение времени предоперационного планирования за счет совершенствования системы TPLAN, а также расширение показаний (а точнее, сокращение противопоказаний) к выполнению таких операций - прежде всего среди полиморбидных пациентов, страдающих избыточной массой тела, и пациентов с выраженными деформациями нижней конечности.
1. Применение активной роботической системы при первичном тотальном эндопротезировании коленного сустава позволило добиться 100 % точности положения имплантата, превысив точность операций с применением компьютерной навигации на 10,2
% и мануальной техники - на 20,5 %.
2. Робот-ассистированная операция требует в 1,2 раза больше времени, чем при применении компьютерной навигации и в 1,4 раза при мануальной технике, однако позволяет уже в раннем послеоперационном периоде достичь лучших результатов по показателям боли (соответственно на 6,5 % и 12,0 %), кровопотери (на 11,4% и 15,2 %) и амплитуды движений в оперированном суставе (на 3,7 % и 9,8 %)
3. По данным лучевой диагностики ротационное расположение бедренного компонента после РаТЭКС лучше на 38 %, а тибиального компонента - на 43 % в сравнении с другими техниками, а отклонение оси нижней конечности отмечено реже в 1,9 раза, чем после операции с применением компьютерной навигации, и чем при мануальной технике - в 3,6 раза. Это позволило получить к 1 году наблюдения лучшие результаты, добившись большей амплитуды движений в оперированном суставе на 3,7 %, чем после применения компьютерной навигации, и на 9,8 % больше, чем после применения мануальной техники.
4. Уровень тревожности перед операцией при планировании РаТЭКС у пациентов был выше на 7,4 % по сравнению с традиционными методиками, тогда как оценка ими степени комфортности лечения была выше на 10 %.
5. Противопоказанием к РаТЭКС является не наличие у пациента ИМТ > 35 кг/м , а расстояние от дальнего кортикального слоя большеберцовой кости до поверхности кожи в области проведения фиксирующего пина. Это расстояние не должно превышать 7,5 см.
6. Среди пациентов, нуждающихся в артропластике коленного сустава, имеющих ИМТ > 35 кг/м2, операция с применением активной роботической техники, в соответствии с уточненными противопоказаниями, возможна в 38,8 % случаев.
7. Результаты РаТЭКС, выполненной по расширенным показаниям у пациентов с ИМТ > 35 кг/м2 не имеют статистически значимых отличий от аналогичных показателей среди пациентов с ИМТ, соответствующим официальным рекомендациям.
1. Учитывая повышенный уровень тревожности пациентов перед применением активной роботической системы, следует уделить повышенное внимание проведению с пациентами разъяснительных бесед в предоперационном периоде.
2. Получение необходимой персонифицированной информации для загрузки в систему TPLAN требует соблюдения специального протокола предоперационного обследования пациента с использованием компьютерной томографии.
3. Предоперационное планирование и этапы непосредственной подготовки роботической системы к операции (нестерильный и стерильный) требуют значительного времени и трудозатрат, в связи с чем целесообразно поручить их выполнение специально обученному вспомогательному персоналу (врачу-ассистенту и медицинским сестрам) под контролем оперирующего хирурга.
4. Противопоказанием к тотальной артропластике коленного сустава с применением активной роботической системы TSolution One у пациентов с избыточной массой тела является расстояние от дальнего кортикального слоя большеберцовой кости до поверхности кожи в области проведения направляющего пина на расстоянии 8 см от суставной щели. Эту толщину можно измерить по компьютерным томограммам; для соблюдения необходимых технических условий выполнения операции она не должна превышать 7,5 см.
5. За исключением технической подготовки и непосредственного выполнения оперативного вмешательства, другие аспекты работы с пациентом (общая предоперационная подготовка, анестезия, медикаментозная терапия, профилактика осложнений, послеоперационное ведение и реабилитация) не имеют отличий в сравнении с применением традиционных хирургических техник.
Литература
1. Елизаров М.П. Первый опыт роботизированного эндопротезирования коленного сустава. / Лычагин А.В., Грицюк А.А., Рукин Я.А., Елизаров М.П. // Кафедра травматологии и ортопедии. 4 (38) 2019, С. 27-33, doi: 10.17238/issn2226-2016.2019.4 [ВАК].
2. Елизаров М.П. История развития робототехники в хирургии и ортопедии (обзор). / Лычагин А.В., Грицюк А.А., Рукин Я.А., Елизаров М.П. // Кафедра травматологии и ортопедии. 1 (39) 2020, С. 13-19, doi: 10.17238/issn2226-2016.2020.1
3. Елизаров М.П. Ранние результаты эндопротезирования тазобедренного сустава с применением индивидуальных аугментов при диспластическом коксартрозе. / Рукин Я.А., Лычагин А.В., Мурылев В.Ю., Гаркави А.В., Тарасов ДА., Елизаров М.П. // Травматология и ортопедия России. 2020;26(2), С. 50-59, doi.org/10.21823/2311-2905- 2020-26-2-50-59 [WoS].
4. Елизаров М.П. Морфологические изменения слюнных желез крыс в условиях экспериментальной гипосаливации./Сирак А.Г., Сирак С.В., Елизаров М.П., Диденко Н. Н. // Медицинский вестник Северного Кавказа. 2021;16(1), С.71-72, doi:10.14300/mnnc.2021.16019 [Scopus].
5. Елизаров М.П. Особенности робот-ассистированного тотального эндопротезирования коленного сустава. / Лычагин А.В, Грицюк А.А., Рукин Я.А., Грицюк А.Анд. // Сборник материалов конференции «Вреденовские чтения 2021» 28-30.10.2021 г. Санкт-Петербург.
6. Елизаров М.П. Ранние послеоперационные результаты тотальногоэндопротезирования коленного сустава с применением активной роботической установки tsolution one. / Лычагин А.В., Грицюк А.А., Рукин Я.А., Грицюк А.Анд. // сборник материалов конференции «Илизаровские чтения» 16-18.06.2021 г. Курган.
7. Елизаров М.П. Новые аспекты робот-ассистированных операций на коленном суставе. / Лычагин А.В., Грицюк А.А., Рукин Я.А., Грицюк А.Анд. // Сборник материалов конференции «VI Пироговский форум травматологов-ортопедов, посвященный 50-летию кафедры травматологии, ортопедии и медицины катастроф МГМСУ имени А. И. Евдокимова» 21 - 22.10.2021 г. Москва.
8. Елизаров М.П. Преимущества Робот-ассистированной артропластики коленного сустава. / Лычагин А.В., Грицюк А.А., Рукин Я.А., Грицюк А.Анд. // Сборник материалов III научно-практическая конференция Пироговские курсы 2021 «От гипсовой повязки к высокотехнологичному остеосинтезу» 14-15.10.2021 г. Крым, г. Севастополь.
Научный руководитель:
доктор медицинских наук, профессор Лычагин Алексей Владимирович
Брижань Леонид Карлович - доктор медицинских наук, профессор, Федеральное государственное бюджетное учреждение «Г лавный военный клинической госпиталь имени Н. Н. Бурденко» Министерства обороны Российской Федерации, заместитель начальника госпиталя по научной работе
Загородний Николай Васильевич - член-корреспондент РАН, заслуженный деятель науки, заслуженный врач РФ, доктор медицинских наук, профессор, федеральное государственное автономное образовательное учреждение высшего образования «Российский университет дружбы народов», Медицинский институт, кафедра травматологии и ортопедии, заведующий кафедрой; главный внештатный травматолог- ортопед ДЗМ; Федеральное Государственное Бюджетное Учреждение «Национальный медицинский исследовательский центр травматологии и ортопедии имени Н.Н. Приорова» Министерства здравоохранения Российской Федерации, отделение эндопротезирования №2, заведующий отделением
Ведущая организация: Федеральное государственное автономное образовательное учреждение высшего образования «Российский национальный исследовательский медицинский университет имени Н. И. Пирогова» Министерства здравоохранения Российской Федерации
Теги: эндопротезирование
234567 Начало активности (дата): 23.11.2023 22:10:00
234567 Кем создан (ID): 989
234567 Ключевые слова: эндопротезирование, коленный сустав, ТЭКС
12354567899
Похожие статьи
Лазерные технологии в лечении пациентов с хроническим синовитом коленного суставаРентген на дому 8 495 22 555 6 8
«Шум керамики» как нежелательное явление в эндопротезировании тазобедренного сустава
Применение индивидуального импланта при ревизионном эндопротезировании тазобедренного сустава с костным дефектом типа IV по Paprosky
Гематологические маркеры перипротезной инфекции при ревизионном эндопротезировании тазобедренного сустава



