 11.11.2023
11.11.2023
Сравнительный анализ результатов применения различных хирургических методик у пациентов с закрытыми повреждениями седалищного нерва после тотального эндопротезирования тазобедренного сустава
Введение
Одним из наиболее грозных осложнений тотального эндопротезирования (ТЭП) тазобедренного сустава кает у 0,17-8 % пациентов [1-3], а в 50-70 % случаев (ТБС) является закрытое повреждение седалищного носит преходящий характер и может не сопровождаться развитием выраженной клинической картины [4, 5]. Учитывая активный рост количества хирургических вмешательств на ТБС, увеличивается и распространенность ЗПСН, особенно среди пациентов трудоспособного возраста [6]. Ряд авторов в своих исследованиях отмечает, что удлинение конечности в ходе операции, женский пол, повторные хирургические вмешательства, цементная фиксация, а также задний доступ к ТБС коррелируют с ростом числа осложнений, что можно отнести к факторам риска [7-10]. При развитии нейропатии седалищного нерва (СН) после ТЭП ТБС у пациентов отмечается быстрое формирование болевого синдрома и выраженное нарушение сократительной функции мышц нижней конечности, что приводит в дальнейшем к атрофии и контрактурам суставов и отрицательно влияет на исходы лечения [11, 12].
Сложность хирургического лечения ЗПСН обусловлена высоким уровнем повреждения ствола нерва на уровне подгрушевидного и большого седалищного отверстий во время выполнения операции на ТБС, что может потребовать выполнения высокотравматичного доступа, связанного с массивной диссекцией мягкотканных структур, в ряде случаев приводящей к развитию выраженного рубцово-спаечного процесса в зоне операции, что повышает число неудовлетворительных результатов лечения [13, 14]. В качестве стандарта лечения подобных пациентов, как правило, выполняется микрохирургический невролиз (МН), а в качестве рекомендаций и опций рассматриваются различные способы прямой электростимуляции (ЭС) СН [13, 15, 16]. Однако использование данных методик не всегда приводит к восстановлению полезной функции нижней конечности и сопровождается частым возникновением рецидивов комплексного регионарного болевого синдрома (КРБС) в нижней конечности [17-19]. Некоторые авторы применяют в своей работе комбинированную стимуляцию как периферического нерва, так и сегментарного аппарата спинного мозга, при этом демонстрируют улучшение ближайших и отдаленных результатов лечения [20]. Несмотря на обилие различных методик ЭС, в литературе нет единого мнения по поводу показаний, сроков и применяемых режимов, а большинство работ, исследующих ее влияние на регенераторные процессы, происходящие в мионев-ральном комплексе, выполнялись только на экспериментальных моделях [21-25].
Таким образом, высокая распространённость ЗПСН после ТЭП ТБС и частота неудовлетворительных результатов обусловливает актуальность данного исследования, направленного на поиск наиболее эффективной методики хирургического лечения.
Цель - сравнить результаты применения различных методов хирургического лечения пациентов с ЗПСН после ТЭП ТБС.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование явилось продольным, открытым, проспективным с исторической группой контроля. Критерии включения пациентов в исследование: трудоспособный возраст, изолированный характер травмы СН после ТЭП ТБС (идиопатический коксартроз 3 стадии, индекс массы тела от 18,5 до 24,99, использование во время хирургического вмешательства только переднебокового доступа к ТБС и эндопротезов с бесцементной фиксацией), степень повреждения нервных стволов, соответствующая II, III, IV по классификации Sunderland [26], КРБС в заинтересованной конечности, предшествующее неэффективное консервативное лечение в сроке не менее 3 месяцев с момента получения травмы, подписанное добровольное информированное согласие пациента на участие в исследовании.
В исследование вошли 94 пациента с ЗПСН, находившихся на стационарном лечении в НИИТОН СГМУ с 2005 по 2022 г., 41 (43,6 %) из которых мужского пола, 53 (56,4 %) - женского. Половых различий между исследуемыми группами выявлено не было (р = 0,785). Исследование проведено в трёх группах, однородных по тяжести повреждения нерва.
При этом в I группе (n = 29) выполняли МН ствола СН на уровне его по микрохирургический невролиз (МН), а в качестве рекомендаций и опций рассматриваются различные способы прямой электростимуляции (ЭС) СН [13, 15, 16]. Однако использование данных методик не всегда приводит к восстановлению полезной функции нижней конечности и сопровождается частым возникновением рецидивов комплексного регионарного болевого синдрома (КРБС) в нижней конечности [17-19]. Некоторые авторы применяют в своей работе комбинированную стимуляцию как периферического нерва, так и сегментарного аппарата спинного мозга, при этом демонстрируют улучшение ближайших и отдаленных результатов лечения [20]. Несмотря на обилие различных методик ЭС, в литературе нет единого мнения по поводу показаний, сроков и применяемых режимов, а большинство работ, исследующих ее влияние на регенераторные процессы, происходящие в мионев-вреждения, во II группе (n = 32) - МН в сочетании с одноуровневой ЭС (непосредственно на ствол СН), в III группе (n = 33) выполняли МН в сочетании с двухуровневой ЭС (установку стимулирующих электродов как на ствол СН, так и на сегментарный аппарат СМ).
Анализ результатов лечения производили по шкалам и опросникам: визуально-аналоговой шкале (ВАШ) [27], пятибалльной шкале оценки мышечной силы [28], пятибалльной шкале оценки чувствительности [29], шкале функциональной недостаточности Oswestry Disability Index (ODI)
В качестве объективных методов исследования использовали электронейромиографию (ЭНМГ) нижних конечностей в динамике. Статистический анализ полученных результатов осуществляли с применением программ Statistica 13,0, Microsoft Office Excel 2019. В связи с тем, что распределение данных не соответствовало закону нормального распределения, использовали непараметрические методы статистики с вычислением медианы и межквартильного интервала (Me (Q1; Q3)), критерия Вилкоксона для связанных выборок, критерия Краскелла - Уоллиса. Различия между группами считали статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ
До момента выполнения хирургического вмешательства интенсивность болевого синдрома у всех пациентов (n = 94) была высокой и составила 7,0 (6,0; 8,0) баллов, степень двигательных нарушений в заинтересованной конечности составила 1,0 (0; 2) балл, степень чувствительных расстройств составила 1,0 (0; 2) балл, при этом по данным показателям группы были однородны (критерий Краскелла - Уоллиса рваш = 0,949, р = 0,452, р = 0,950).
Функциональная недостаточность по шкале ODI до операции в группе I составила 31,0 (25,0; 40,0) балл, в группе II - 27,0 (21,0; 36,0) баллов, в группе III - 29,5 (21,5; 41,0), при этом оценка однородности трех групп показала отсутствие отличий (р = 0,579).
ЭНМГ-данные в дооперационном периоде свидетельствовали о высоком повреждении СН, при этом наиболее часто отмечали повреждение обеих его порций, что показано в таблице 1.
Таблица 1
Дооперационные показатели электронейромиографии нижней конечности у пациентов с закрытым повреждением седалищного нерва после тотального эндопротезирования тазобедренного сустава
|
Нерв |
Показатель |
Группа I Me (Q1; Q3) |
Группа II Me (Q1; Q3) |
Группа III Me (Q1; Q3) |
|
Малоберцовый |
М-ответ (мА) |
0,7 (0,1; 1,5) |
0,7 (0,0; 1,3) |
1,0 (0,4; 1,3) |
|
ЛП (мс) |
3,3 (3,1; 4,4) |
3,3 (0,0; 4,4) |
4,8 (4,2; 5,1) |
|
|
Большеберцовый |
М-ответ (мА) |
2,0 (1,0; 4,6) |
1,3 (1,0; 2,2) |
1,1 (0,6; 1,6) |
|
ЛП (мс) |
4,3 (3,5; 5,5) |
5,6 (4,6; 6,7) |
5,3 (4,6; 6,5) |
Примечание: Me - медиана (25 и 75 процентили), p > 0,05.
В соответствии с таблицей 1 во всех случаях (n = 94) показатели ЭНМГ характеризовались снижением амплитуды и увеличением латентного периода М-ответа, что соответствовало тяжелому аксонально- демиелинизирующему повреждению СН.
При контрольном обследовании через 6 месяцев после операции у всех пациентов было отмечено снижение выраженности болевого синдрома, при этом полный его регресс отмечали только у пациентов группы III (р < 0,05) (рис. 1).
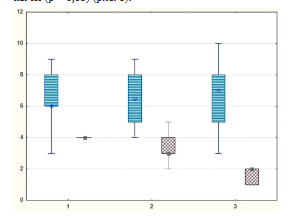
Рис. 1. Динамика интенсивности болевого синдрома
Динамика показателей чувствительности и мышечной силы во всех исследуемых группах была выражена слабо, и статистически значимых различий вышеуказанных показателей за период наблюдения выявлено не было (p > 0,05).
Послеоперационная динамика функциональной недостаточности у пациентов в группах I и II была менее выражена по сравнению с пациентами группы III, что было обусловлено снижением степени выраженности болевого синдрома и, как следствие, приводило к улучшению показателей самообслуживания, при этом результаты тестирования по шкале ODI в группе I составили 28,0 (20,0; 34,0) баллов, в группе II - 16,5 (9,0; 21,5) баллов, в группе III - 5,9 (4,3; 8,5), p < 0,05.
При оценке показателей ЭНМГ было отмечено восстановление проводимости по волокнам малоберцового и большеберцового нервов, что коррелировало с положительной клинико-неврологической динамикой показателей и заключалось в увеличении амплитуды М-ответа и снижении его латентности. Это свидетельствовало об активизации регенераторных процессов в периферических сенсомоторных структурах нижней конечности. При этом медианные показатели амплитуд М-ответа в дистальной точке стимуляции малоберцового нерва составили в группе I - 1,2 (0,3; 2,6), в группе II - 1,6 (1,2; 2,2), в группе III - 1,7 (0,7; 2,4) (р < 0,05) (рис. 2).
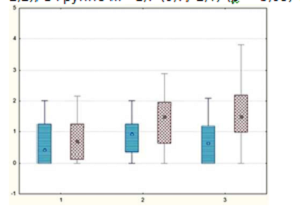
Рис. 2. Динамика показателей М-ответа малоберцового нерва
Показатели амплитуды М-ответа большеберцового нерва в послеоперационном периоде составили в группе I - 2,1 (1,1; 2,9), в группе II - 2,2 (1,4; 2,6), в группе III-3,2 (1,3; 5,60) (р < 0,01) (рис. 3).
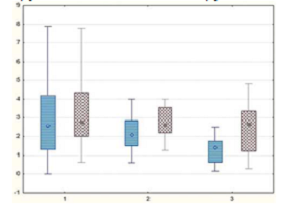
Рис. 3. Динамика показателей М-ответа большеберцового нерва
Таким образом, наиболее отчетливую положительную динамику клинико-неврологических и электрофизиологических параметров в виде регресса болевого синдрома, функциональной недостаточности нижней конечности, увеличения амплитуды и снижения латентности М-ответа выявили у пациентов в изучаемой группе III, что свидетельствовало о преимуществе сочетания методики МН и двухуровневой ЭС в лечении пациентов с ЗПСН после ТЭП ТБС.
Данное исследование явилось продолжением работы по изучению результатов лечения пациентов с ЗПСН после ТЭП ТБС [31], при этом отмечали, что восстановление функции СН происходило у всех пациентов, однако наиболее выраженный эффект регистрировали в III исследуемой группе. При анализе литературных данных отмечено незначительное количество печатных работ, посвященных лечению данной патологии [32, 33], что усложняет достоверное сравнение полученных данных в оригинальном исследовании с данными отечественной и зарубежной литературы.
Позитивный эффект от применения методики МН в сочетании с двухуровневой ЭС связан с одновременным электроимпульсным воздействием как на ствол периферического нерва, так и на сегментарный аппарат спинного мозга, что оказывает взаимоусиливающее влияние на образования периферической нервной системы.
В литературных источниках имеются указания на применение подобной методики в комплексном лечении пациентов с повреждениями периферических нервов, что продемонстрировано в работах Мещеряги- ной И.А. и соавт. [20, 33], при этом полученные данные схожи с настоящим исследованием, несмотря на некоторые отличия в технике установки стимулирующих электродов, заключающейся в использовании миниинвазивных технологий [34].
На текущий момент до сих пор не определены четкие критерии, показания и оптимальный алгоритм выбора конкретной методики хирургического лечения у пациентов с ЗПСН после ТЭП ТБС. Также, несмотря на бурное развитие функциональной нейрохирургии и появление различных методик ЭС, до конца не установлены сроки, длительность, режимы электронейромодуляции [11, 35], что обусловливает необходимость проведения дальнейших исследований, которые позволят определить наиболее эффективный метод, а в перспективе - и установить персонализированный подход к лечению пациентов с ЗПСН после ТЭП ТБС.
Сравнительный анализ различных методов хирургического лечения пациентов с ЗПСН после ТЭП ТБС продемонстрировал достоверную эффективность методики применения МН в сочетании с ЭС стволов ПС и сегментарного аппарата СМ, что позволило достоверно улучшить результаты лечения и проявилось более быстрым темпом снижения болевого синдрома в заинтересованной нижней конечности и улучшением электрофизиологических показателей.
СПИСОК ЛИТЕРАТУРЫ
1. Schmalzried TP, Amstutz HC, Dorey FJ. Nerve palsy associated with total hip replacement. Risk factors and prognosis. J Bone Joint Surg Am. 1991;73(7):1074-80.
2. Hasija R, Kelly JJ, Shah NV, Neet al. Nerve injuries associated with total hip arthroplasty. J Clin Orthop Trauma. 2018;9(1):81-86. doi: 10.1016/j. jcot.2017.10.011
3. DeHart MM, Riley LH Jr. Nerve injuries in total hip arthroplasty. J Am Acad Orthop Surg. 1999;7(2):101-11. doi: 10.5435/00124635-199903000- 00003
4. Толкачев В.С., Бажанов С.П., Коршунова Г.А. и др. Ближайшие клинические результаты хирургического лечения пациентов с повреждениями седалищного нерва после тотального эндопротезирования тазобедренного сустава. Гений ортопедии. 2022;28(6):774-777. doi: 10.18019/1028-4427-2022-28-6-774-777
5. Mangual D, Valentin J, Acevedo J, et al. The Effect of Total Hip Arthroplasty on the Sciatic Nerve: an Electrodiagnostic Evidence Study. P R Health Sci J. 2020;39(3):254-259.
6. Park JH, Hozack B, Kim P, et al. Common peroneal nerve palsy following total hip arthroplasty: prognostic factors for recovery. J Bone Joint Surg Am. 2013;95(9):e55. doi: 10.2106/JBJS.L.00160
7. De Fine M, Romagnoli M, Zaffagnini S, Pignatti G. Sciatic Nerve Palsy following Total Hip Replacement: Are Patients Personal Characteristics More Important than Limb Lengthening? A Systematic Review. Biomed Res Int. 2017;2017:8361071.
8. Patel N, Golwala P. Approaches for Total Hip Arthroplasty: A Systematic Review. Cureus. 2023;15(2):e34829. doi: 10.7759/cureus.34829
9. Devlieger BK, Drees P, Mattyasovszky S, et al. Impingement of the Sciatic Nerve due to a Protruding Acetabular Cage Rim. Arthroplast Today. 2020;6(4):825-829. doi: 10.1016/j.artd.2020.08.005
10. Shemesh SS, Robinson J, Overley S, et al. Novel technique for intraoperative sciatic nerve assessment in complex primary total hip arthroplasty: a pilot study. Hip Int. 2018;28(2):210-217. doi: 10.5301/hipint.5000553
11. Gordon T. Peripheral Nerve Regeneration and Muscle Reinnervation. Int J Mol Sci. 2020;21(22):8652. doi: 10.3390/ijms21228652
12. Gronholdt-Klein M, Altun M, Becklen M, et al. Muscle atrophy and regeneration associated with behavioural loss and recovery of function after sciatic nerve crush. Acta Physiol (Oxf). 2019;227(3):e13335. doi: 10.1111/apha.13335
13. Декопов А.В., Томский А.А., Исагулян Э.Д. и др. Лечение посттравматической невропатии седалищного нерва с использованием хронической нейростимуляции и эндоскопической техники. Журнал «Вопросы нейрохирургии» имени Н.Н. Бурденко. 2020;84(5):64-71. doi: 10.17116/neiro20208405164
14. Беляк Е.А., Пасхин Д.Л., Лазко Ф.Л., и др. Эндоскопический невролиз седалищного нерва. Хирургия. Журнал им. Н.И. Пирогова. 2021;(11):66 75. DOI: 10.17116/hirurgia202111166
15. Haastert-Talini K, Grothe C. Electrical stimulation for promoting peripheral nerve regeneration. Int Rev Neurobiol. 2013;109:111-124. doi: 10.1016/ B978-0-12-420045-6.00005-5
16. Salmasi V, Olatoye OO, Terkawi AS, et al. Peripheral Nerve Stimulation for Occipital Neuralgia. Pain Med. 2020;21(Suppl 1):S13-S17. doi: 10.1093/ pm/pnaa083
17. Davis G, Curtin CM. Management of Pain in Complex Nerve Injuries. Hand Clin. 2016;32(2):257-62. doi: 10.1016/j.hd.2015.12.011
18. Cobianchi S, Casals-Diaz L, Jaramillo J, Navarro X. Differential effects of activity dependent treatments on axonal regeneration and neuropathic pain after peripheral nerve injury. Exp Neurol. 2013;240:157-167
19. Buwembo J, Munson R, Rizvi SA, et al. Direct Sciatic Nerve Electrical Stimulation for Complex Regional Pain Syndrome Type 1. Neuromodulation. 2021;24(6):1075-1082. doi: 10.1111/ner.13294
20. Мещерягина И.А., Скрипников А.А. Применение комбинированной электростимуляции при изолированных и сочетанных повреждениях периферических нервов верхних и нижних конечностей. Российский медицинский журнал. 2015;21(3):14-19.
21. Bolivar S, Navarro X, Udina E. Schwann Cell Role in Selectivity of Nerve Regeneration. Cells. 2020;9(9):2131. doi: 10.3390/cells9092131
22. Gordon T, Sulaiman O, Boyd JG. Experimental strategies to promote functional recovery after peripheral nerve injuries. J Peripher Nerv Syst. 2003;8(4):236-250. doi: 10.1111/j.1085-9489.2003.03029.x
23. Gordon T. Electrical Stimulation to Enhance Axon Regeneration After Peripheral Nerve Injuries in Animal Models and Humans. Neurotherapeutics. 2016;13(2):295-310. doi: 10.1007/s13311-015-0415-1
24. Alrashdan MS, Sung MA, Kwon YK, et al. Effects of combining electrical stimulation with BDNF gene transfer on the regeneration of crushed rat sciatic nerve. Acta Neurochir (Wien). 2011;153(10):2021-9. doi: 10.1007/s00701-011-1054-x
25. Li X, Zhang T, Li C, et al. Electrical stimulation accelerates Wallerian degeneration and promotes nerve regeneration after sciatic nerve injury. Glia. 2023;71(3):758-774. doi: 10.1002/glia.24309
26. Sunderland S. A classification of peripheral nerve injuries producing loss of function. Brain. 1951;74(4):491-516. doi: 10.1093/brain/74.4.491
27. Huskisson EC. Measurement of pain. Lancet. 1974;2(7889):1127-31. doi: 10.1016/s0140-6736(74)90884-8
28. Compston A. Aids to the investigation of peripheral nerve injuries. Medical Research Council: Nerve Injuries Research Committee. His Majesty's Stationery Office: 1942; pp. 48 (iii) and 74 figures and 7 diagrams; with aids to the examination of the peripheral nervous system. By Michael O'Brien for the Guarantors of Brain. Saunders Elsevier: 2010; pp. [8] 64 and 94 Figures. Brain. 2010;133(10):2838-44.
29. Хамзаев Р.И. Результаты хирургического лечения повреждений седалищного нерва и его ветвей: автореф. дис... канд. мед наук. Санкт- Петербург; 2009:22
30. Черепанов Е.А. Русская версия опросника Освестри: культурная адаптация и валидность. Хирургия позвоночника. 2009;(3):093-098.
31. Толкачев В.С., Бажанов С.П., Коршунова Г.А. и др. Ближайшие клинические результаты хирургического лечения пациентов с повреждениями седалищного нерва после тотального эндопротезирования тазобедренного сустава. Гений ортопедии. 2022;28(6):774-777.
32. Maeder B, Goetti P, Mahlouly J, et al. Entrapment of the Sciatic Nerve Over the Femoral Neck Stem After Closed Reduction of a Dislocated Total Hip Arthroplasty. J Am Acad Orthop Surg Glob Res Rev. 2019;3(2):e081.
33. Мещерягина И.А., Мухтяев С.В., Россик О.С. и др. Нейропатия седалищного нерва у пациентки после эндопротезирования по поводу врожденного вывиха головки бедра (клинический случай из практики).
34. Худяев А.Т., Мартель И.И., Самылов В.В. и др. Малоинвазивные методы лечения повреждений периферических нервов. Гений ортопедии. 2012;(1):85-88.
35. Zuo KJ, Gordon T, Chan KM, Borschel GH. Electrical stimulation to enhance peripheral nerve regeneration: Update in molecular investigations and clinical translation. Exp Neurol. 2020;332:113397. doi: 10.1016/j.expneurol.2020.113397
Сведения об авторах
1. Сергей Петрович Бажанов - доктор медицинских наук, начальник отдела
2. Владимир Сергеевич Толкачев - младший научный сотрудник
3. Шамиль Малачиляевич Айтемиров - врач-нейрохирург;
4. Владимир Владимирович Островский - доктор медицинских наук, директор НИИТОН
Вклад авторов:
Бажанов С.П. - концептуализация, методология, валидация, написание (рецензирование и редактирование), визуализация.
Толкачев В.С. - формальный анализ, исследование, обработка данных, написание (первоначальный вариант), визуализация.
Айтемиров Ш.М. - исследование, обработка данных.
Островский В.В. - контроль, управление проектом.
Теги: седалищный нерв
234567 Начало активности (дата): 11.11.2023 08:45:00
234567 Кем создан (ID): 989
234567 Ключевые слова: седалищный нерв, травма, тотальное эндопротезирование, электростимуляция, хирургическое лечение
12354567899
Похожие статьи
Клиническая эффективность и точность выравнивания механической оси при роботизированном тотальном эндопротезировании коленного суставаАнализ биомеханики проксимального межфалангового сустава после эндопротезирования
Рентген на дому 8 495 22 555 6 8
Выживаемость несвязанных керамических эндопротезов лучезапястного сустава
Экстракорпоральная ударно-волновая терапия тендопериостеопатии связки надколенника



