 06.11.2023
06.11.2023
Анализ биомеханики проксимального межфалангового сустава после эндопротезирования
ВВЕДЕНИЕ
Однако, несмотря на разнообразие ассортимента изделий, все импланты обладают своими достоинствами и недостатками, что сказывается на противоречивости функциональных результатов эндопротезирования ПМФС [6].
В последние годы внимание клиницистов и учёных-медицинских конструкторов привлекла циркониевая керамика. И это неудивительно: износостойкость, биосовместимость и биоинтертность, коррозионная устойчивость - основные качества данного материала, которые превосходно находят своё отражение в ортопедической и дентальной имплантологии. В последнее десятилетие в мировой научной литературе стали появляться первые сообщения об использовании цельнокерамических эндопротезов, и это привлекло внимание, в том числе и кистевых хирургов [7, 8, 9].
Научно-технический прогресс в медицине характеризуется огромным количеством новых изделий медицинского назначения, поступающих на рынок, фармакологических препаратов, методик и технологий лечения. Однако любое новшество, прежде чем поступить в использование широкой сетью лечебных учреждений, проходит тернистый путь доклинических испытаний; применительно к различного рода имплантам это токсикологические исследования на клеточных культурах, технические испытания образцов в лаборатории, обладающей сертификацией в конкретной области, доклиническая апробация на лабораторных животных и кадаверном материале [12].
Многочисленные сообщения о тяжести ревизионных вмешательств при эндопротезировании суставов кисти побудили нас к проведению данного цифрового исследования, для того чтобы оградить пациента от дополнительных физических и психоэмоциональных травм.
Эндопротезирование ПМФС несвязанными имплантами, среди всех прочих, характеризуется следующим рядом наиболее частых осложнений [13, 14]:
- вывих в эндопротезе;
- перелом ножки импланта;
- перипротезный перелом фаланги.
Цель - определить допустимый диапазон нагрузок на проксимальный межфаланговый сустав после эндопротезирования путём анализа его биомеханики для предупреждения развития критических состояний - осложнений.
МАТЕРИАЛЫ И МЕТОДЫ
В период с 2016 по 2021 год проведено обследование 42 пациентов, которые обратились на консультацию травматолога-ортопеда в Клиники Самарского государственного медицинского университета по поводу остеоартрита ПМФС. Среди обратившихся было 25 мужчин (59,5 %) и 17 женщин (40,5 %), средний возраст пациентов составил 44 ± 2,71 года. Все больные предъявляли жалобы на боль, умеренный отёк и выраженное ограничение движений в ПМФС. Болевой синдром у обследованных больных составил 5 ± 1,4 балла по ВАШ, средний объём сгибания в ПМФС составил 48,7 градуса.
Пациенты прошли комплексное обследование, включавшее сбор жалоб и анамнеза, клинический осмотр, рентгенографию кисти в двух проекциях, компьютерную томографию (КТ). С целью биомеханического исследования здоровых и поражённых суставов выполнялась 3D-визуализация КТ-сканов.

Параллельно была выполнена диссекция 25 кадаверных кистей для изучения анатомии капсульно-связочного аппарата ПМФС.
Изделие относится к эндопротезам несвязанного типа и выполнено из цельной циркониевой керамики. Суставные поверхности выполнены анатомично: проксимальный компонент представлен тороидальными мыщелками и бороздой между ними, образует дугу в 210 градусов, дистальный - имеет вогнутую поверхность, эллипсовидную форму и гребень-антагонист борозды посередине. Конструкция посадочных поверхностей суставных частей имеет две плоскости для обеспечения ротационной стабильности при минимальной резекции костной ткани. Ножки эндопротеза имеют коническую форму и округления на верхушках для простоты установки методом press-fit.
Размерная линейка импланта представлена четырьмя позициями и поставляется с набором инструментов для установки. Эндопротез прошёл полный цикл доклинических технических и токсикологических испытаний: технические испытания пройдены на базе АНО «Центр качества, эффективности и безопасности медицинских назначений», г. Москва (акт № 11/022.Р-2021 от 10 ноября 2021 г.). Токсикологические тесты выполнены в физико-химической лаборатории «Дельма», г. Пущино (программа токсикологических исследований медицинского изделия № МИ21-0208/02 от 2 августа 2021 г.).
Медицинская наука, стоящая на службе практического здравоохранения, на сегодняшний день невозможна без коллективной работы специалистов различных специальности: врачей, инженеров-про- ектировщиков, IT-специалистов, графических дизайнеров. Этот эффективный тандем позволяет достичь высоких результатов на доклиническом этапе исследований, что способствует минимизации риска развития осложнений и прочих нежелательных состояний в клинической практике [16].
Для анатомо-биомеханического исследования ПМФС использовали базу сканов КТ-формата DICOM и выполняли SD-моделирование методами полигонального моделирования, SD-скульптинга, а также с использованием систем автоматизированного моделирования, разработанных в Институте инновационного развития СамГМУ. В процессе данного этапа исследования мы работали в программных комплексах ZBrush, Autodesk 3dsMax, в результате чего получали трёхмерные модели суставов для дальнейшего создания эндопротеза нового конструктивного дизайна.
Для воспроизведения критических состояний, приводящих к развитию осложнений, был использован метод конечных элементов (finite element method). Метод конечных элементов (МКЭ) является основным для анализа напряжённо-деформированных состояний конструкций, широко применяемым в авиастроении, промышленности и строительстве. В медицине МКЭ незаменим в разработке имплантов, в частности для ортопедии: с его помощью можно определить действующие нагрузки на эндопротез, винт, пластину, дентальный имплант и пр. и на сегмент опорно-двигательной системы, что позволяет спрогнозировать срок службы изделия при заданных нагрузках и оптимизировать его конструкцию ещё на доклиническом этапе. В данном исследовании МКЭ применяли в программном комплексе Ansys [17, 18]. Из всего многообразия движений кисти мы выбрали основные стереотипы и загрузили в программу в виде SD-моделей.
Мы использовали следующие свойства керамики, представленные в таблице 1.
Таблица 1
Механические свойства керамики
|
Свойства |
Значение |
|
Плотность, г/см3 |
6 |
|
Средний размер частиц, мкм |
< 1 |
|
Прочность на изгиб, МПа |
900 |
|
Модуль Юнга, ГПа |
210 |
|
Твёрдость по Виккерсу, HV 0.1 |
1200 |
Механические свойства кортикальной кости, использованные при разработке цифровой модели:
- модуль Юнга 1,8 * 1010 Па;
- предел прочности 146 МПа;
- удельный вес 1800 кг/м3.
В разработанной цифровой модели эндопротезирования ПМФС для программного комплекса Ansys применялись данные только кортикальной кости, так как моделирование может подразумевать упрощение и абстрагирование от реальной ситуации из-за сложности воспроизведения физиологических и биомеханических процессов в нативной кости.
Твердотельная модель импланта была интегрирована в костную ткань, представляя собой биомеханическую конструкцию, которая подвергалась прочностному анализу.
Целью выполняемых расчетов являлся анализ напряжённого состояния конструкции, выявление наиболее ослабленных зон, как в костной ткани, так и в материале импланта, предотвращение возможного разрушения составляющих биомеханической конструкции.
Для разработки цифровой конечно-элементной модели были взяты основные стереотипы движений, заключающиеся в шаровом захвате предметов с углом сгибания в ПМФС 0, 30, 60 и 90 градусов и сжатием предмета [19, 20].
На основе расчёта напряжённого состояния биомеханической конструкции «имплант - костная ткань» определялись допускаемые рабочие нагрузки для заданных углов сгибания сустава.
Прочностной анализ проводился на основе метода конечных элементов. Модель исследуемой биомеханической конструкции была размечена конечными элементами Solid 45, также к модели были приложены граничные условия: костная ткань проксимальной фаланги жёстко закреплялась по поверхности торца - закрепление «жёсткая заделка», а к дистальному фаланговому элементу кости были приложены усилия в осевом направлении.
Конечно-элементная модель исследуемой биомеханической конструкции показана на рисунках 2-5.
Тип нагружения - шаровой захват с углом сгибания в ПМФС 0, 30, 60, 90 градусов, сжатие предмета. Нагрузки прилагались в диапазоне 1-20 кг. Величина прилагаемой нагрузки выбиралась на основании литературных данных, анализ которых показал предельные нагрузки, при которых возникали критические состояния в реальных клинических условиях [30]. С целью демонстрации на рисунках приведен только один вид прилагаемой нагрузки в качестве примера.
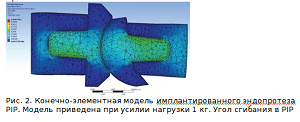

Также, помимо осуществления цифрового моделирования критических состояний методом конечных элементов, мы оценивали клиническую картину и амплитуду движений в оперированном суставе. В наше наблюдение вошло 10 пациентов, которым было выполнено эндопротезирование проксимального межфалангового сустава по поводу посттравматического артрита, максимальный срок наблюдения составил 6 месяцев.
РЕЗУЛЬТАТЫ
ОБСУЖДЕНИЕ
ЗАКЛЮЧЕНИЕ
СПИСОК ИСТОЧНИКОВ
4. Zhu AF, Rahgozar P, Chung KC. Advances in Proximal Interphalangeal Joint Arthroplasty: Biomechanics and Biomaterials. Hand Clin. 2018;34(2):185-194. doi: 10.1016/j.hcl.2017.12.008
5. Николаенко А.Н., Иванов В.В., Згирский Д.О. и др. Эндопротезирование проксимального межфалангового сустава. Обзор литературы.
6. Forster N, Schindele S, Audige L, Marks M. Complications, reoperations and revisions after proximal interphalangeal joint arthroplasty: a systematic review and meta-analysis. J Hand Surg Eur Vol. 2018;43(10):1066-1075.
7. Castagnini F, Cosentino M, Bracci G, et al. Ceramic-on-Ceramic Total Hip Arthroplasty with Large Diameter Heads: A Systematic Review. Med Princ Pract. 2021;30(1):29-36. doi: 10.1159/000508982
8. Lakhdar Y, Tuck C, Binner J. et al. Additive manufacturing of advanced ceramic materials. Progress in Materials Science. 2021;116. doi: 10.1016/j. pmatsci.2020.100736
9. Backes LT, Oldorf P, Peters R, et al. Study of the tribological properties of surface structures using ultrashort laser pulses to reduce wear in endoprosthetics. J Orthop Surg Res. 2020;15(1):205. doi: 10.1186/s13018-020-01719-1
10. Riviere C, Vendittoli PA, editors. Personalized Hip and Knee Joint Replacement [Internet]. Cham (CH): Springer; 2020. doi: 10.1007/978-3-030-24243-5
11. Zhang D, Bauer AS, Blazar P, Earp BE. Three-Dimensional Printing in Hand Surgery. J Hand Surg Am. 2021;46(11):1016-1022. doi: 10.1016/j. jhsa.2021.05.028
12. Shegokar R. Preclinical-testing understanding the basics first. Drug Delivery Aspects. 2020:19-32. doi: 10.1016/b978-0-12-821222-6.00002-6
13. Helder O, Marks M, Schweizer A, et al. Complications after surface replacing and silicone PIP arthroplasty: an analysis of 703 implants. Arch Orthop Trauma Surg. 2021;141(1):173-181. doi: 10.1007/s00402-020-03663-5
14. Wagner ER, Weston JT, Houdek MT, et al. Medium-Term Outcomes With Pyrocarbon Proximal Interphalangeal Arthroplasty: A Study of 170 Consecutive Arthroplasties. J Hand Surg Am. 2018;43(9):797-805. doi: 10.1016/j.jhsa.2018.06.020
15. Колсанов А.В., Николаенко А.Н., Ушаков А.А. и др. Эндопротез проксимального межфалангового сустава кисти. Патент РФ на полезную модель № 202476 U1. 19.02.2021. Бюл. № 5.
16. Chien S, Bashir R, Nerem RM, Pettigrew R. Engineering as a new frontier for translational medicine. Sci Transl Med. 2015;7(281):281fs13. doi: 10.1126/scitranslmed.aaa4325
17. Angeles Maslucan R, Dominguez JA. A Finite Element Stress Analysis of a Concical Triangular Connection in Implants: A New Proposal. Materials (Basel). 2022;15(10):3680. doi: 10.3390/ma15103680
18. Wei Y, Zou Z, Wei G, et al. Subject-Specific Finite Element Modelling of the Human Hand Complex: Muscle-Driven Simulations and Experimental Validation. Ann Biomed Eng. 2020;48(4):1181-1195. doi: 10.1007/s10439-019-02439-2
19. Duruoz MT. Assessment of hand functions. In: Duruoz, M. (eds) Hand Function. Springer, New York, NY. 2014:41-55. doi: 10.1007/978-1-4614- 9449-2_3
20. Pang EQ, Yao J. Anatomy and Biomechanics of the Finger Proximal Interphalangeal Joint. Hand Clin. 2018;34(2):121-126. doi: 10.1016/j.hcl.2017
21. Вороков А.А., Бортулев П.И., Хайдаров В.М. с соавт. Эндопротезирование тазобедренного и коленного суставов: показания к операции. Ортопедия, травматология и восстановительная хирургия детского возраста. 2020;8(3):355-364. doi: 10.17816/PTORS34164
22. Maradit Kremers H, Larson DR, Crowson CS, et al. Prevalence of Total Hip and Knee Replacement in the United States. J Bone Joint Surg Am. 2015;97(17):1386-97. doi: 10.2106/JBJS.N.01141
23. Singh JA, Yu S, Chen L, Cleveland JD. Rates of Total Joint Replacement in the United States: Future Projections to 2020-2040 Using the National Inpatient Sample. J Rheumatol. 2019;46(9):1134-1140. doi: 10.3899/jrheum.170990
24. Vakalopoulos K, Arner M, Denissen G, et al. Current national hand surgery registries worldwide. J Hand Surg Eur Vol. 2021;46(1):103-106. doi: 10.1177/1753193420970155
25. Swann J. The world at your finger tips: how the hand functions. Nursing and Residential Care. 2015;17(8):444-448. doi: 10.12968/nrec.2015.17.8.444
26. Conson M, Di Rosa A, Polito F, et al. "Mind the thumb”: Judging hand laterality is anchored on the thumb position. Acta Psychol (Amst). 2021;219:103388. doi: 10.1016/j.actpsy.2021.103388
27. Young RW. Evolution of the human hand: the role of throwing and clubbing. JAnat. 2003;202(1):165-74. doi: 10.1046/j.1469-7580.2003.00144.x
28. Qiu S., Kermani M.R. Inverse Kinematics of High Dimensional Robotic Arm-Hand Systems for Precision Grasping. J Intell Robot Syst. 2021;101(4). doi: 10.1007/s10846-021-01349-7
29. Leibovic SJ, Bowers WH. Anatomy of the proximal interphalangeal joint. Hand Clin. 1994;10(2):169-78. 1994;10(2):169-178. doi: 10.1016/S0749- 0712(21)01280-4
30. Groenwold RHH, Dekkers OM. Measurement error in clinical research, yes it matters. Eur J Endocrinol. 2020;183(3):E3-E5. doi: 10.1530/EJE- 20-0550
Информация об авторах:
1. Геннадий Петрович Котельников - доктор медицинских наук, профессор, академик РАН, заведующий кафедрой
2. Александр Владимирович Колсанов - доктор медицинских наук, профессор, профессор РАН, ректор
3. Андрей Николаевич Николаенко - доктор медицинских наук, директор НИИ
4. Денис Олегович Згирский - аспирант кафедры
5. Святослав Олегович Дороганов - аспирант кафедры
Вклад авторов:
Котельников Г.П. - концептуализация.
Колсанов А.В. - концептуализация, валидация.
Николаенко А.Н. - контроль, управление проектом.
Згирский Д.О. - исследование, написание (первоначальный вариант, редактирование, визуализация).
Дороганов С.О. - визуализация, написание - редактирование.
Теги: эндопротезирование
234567 Начало активности (дата): 06.11.2023 17:18:00
234567 Кем создан (ID): 989
234567 Ключевые слова: эндопротезирование проксимального межфалангового сустава, метод конечных элементов, эндопротезирование суставов кисти, цифровое моделирование
12354567899
Похожие статьи
Выживаемость несвязанных керамических эндопротезов лучезапястного суставаРентген на дому 8 495 22 555 6 8
Сравнение прочностных характеристик углеродной пары трения эндопротеза тазобедренного сустава, включающей компоненты из монолитного или немонолитного пироуглерода
Сравнительная оценка клинической эффективности и безопасности применения различных хирургических доступов при выполнении эндопротезирования тазобедренного сустава
Мультидисциплинарный подход к лечению пациентов с перипротезной инфекцией тазобедренного сустава, осложненной повреждением магистральных сосудов



