 15.05.2026
15.05.2026
Хирургическое лечение инвазивных микозов легких у онкогематологических больных после химиотерапии и трансплантации гемопоэтических стволовых клеток
Роль хирургического лечения инвазивных микозов (ИМ) легких после трансплантации гемопоэтических стволовых клеток (ТГСК) и противоопухолевой химиотерапии (ПХТ) у больных онкогематологического профиля не определена
Введение.
Пациенты со злокачественными опухолями кроветворной и лимфатической ткани (онкогематологические) относятся к группе повышенного риска развития инфекционных осложнений и, в частности, инвазивных микозов (ИМ) [1]. Трансплантация гемопоэтических стволовых клеток (ТГСК) – метод лечения различных гематологических заболеваний, некоторых солидных опухолей, аутоиммунных заболеваний и иммунодефицитных состояний, является одним из этапов программной терапии онкогематологических заболеваний [2]. Хотя результаты ТГСК, в целом, можно признать удовлетворительными, инфекционные осложнения в той или иной степени имеют место больше чем у половины реципиентов [3, 4]. Наиболее тяжело протекают, сложны для диагностики и лечения ИМ. Основным органом поражения ИМ являются легкие, а основными возбудителями микозов легких являются оппортунистические микромицеты Aspergillus species, реже встречаются мукормицеты (Rhizopus spp. и др.), очень редко – Cryptococcus neoformans, гиалогифомицеты (Fusarium spp. и др.) и феогифомицеты (Cladosporium spp. и др.), а летальность, в зависимости от особенностей пациентов и вида микоза, составляет от 20 до 100 % [4–8].
Международные рекомендации по лечению мукормикоза и инвазивного аспергиллеза содержат противоречивые положения о хирургическом лечении и лишь вероятностные положения [9, 10].
Так, глобальные рекомендации поддерживают необходимость хирургического лечения мукормикоза в дополнение к системной противогрибковой лекарственной терапии, при необходимости резекцию или санацию следует повторить. Резекция легкого может быть показана как с целью предотвращения кровотечения, так и в плановом порядке [11, 12], раннее хирургическое лечение предпочтительнее позднего вмешательства [12–15]. Однако эти положения основаны на изучении опыта хирургического лечения не у онкогематологических пациентов, опубликованы лишь единичные работы о клинических особенностях легочного мукормикоза у реципиентов аллогенной трансплантации гемопоэтических стволовых клеток (алло-ТГСК), почти всегда это описания единичных клинических наблюдений. Хирургическое лечение при инвазивном аспергиллезе считается показанным при резистентности к противогрибковой терапии, в случае развития жизнеугрожающих осложнений, а также при перенесенном аспергиллезе с операбельными очагами до начала периода риска при продолжении противоопухолевой терапии, включая ТГСК [10].
Методы и материалы.
Проведен ретроспективный анализ непосредственных и отдаленных результатов лечения пациентов с онкогематологическими заболеваниями, перенесших противоопухолевую химиотерапию (ПХТ) и/или ТГСК, которым с 2013 г. проведены резекции легких по поводу ИМ, подтвержденного результатами лабораторных исследований до и/или после проведения операции.
Дооперационное обследование включало компьютерную томографию (KT) грудной клетки и брюшной полости, придаточных пазух носа, магнитно-резонансную томографию головного мозга.
Диагностика и лекарственное лечение ИМ легких проводились на основании международных рекомендаций, локальных протоколов и стандартных операционных процедурах [16–20]. Всем пациентам выполнялась диагностическая бронхоскопия с бронхоальвеолярным лаважем (БАЛ) с определением галактоманнанового антигена Aspergillus, микроскопия БАЛ, микробиологическое и микологическое исследование с определением чувствительности к антимикробным препаратам. При необходимости проводилась чрезбронхиальная или трансторакальная биопсия внутрилегочных очагов. Решение об операции принималось на мультидисциплинарном консилиуме. Основными показаниями к операции были отсутствие динамики или прогрессирующие поражения легочной паренхимы и соседних тканей, несмотря на адекватную противогрибковую терапию, наличие кровохарканья. При двустороннем поражении легких возможность хирургического лечения рассматривалась при существенном преобладании микотических изменений паренхимы с одной стороны. Все удаленные препараты подвергались гистологическому, микробиологическому анализу. Проведен анализ состояния пациентов на момент выявления микоза и проведения операции, особенностей операций, объема резекции легких, изучено течение раннего послеоперационного периода, эффективности хирургического вмешательства и отдаленные результаты с точки зрения микотического поражения.
Результаты.
В исследование включено 13 больных, 3 детей и 10 взрослых, 11 мужчин и 2 женщин, медиана возраста составила 25 лет (от 10 до 64 лет). Основными диагнозами были: острый лейкоз – у 4 больных (31 %), хронические миелопролиферативные заболевания – у 4 (31 %), апластическая анемия – у 3 (23 %), лимфома – у 2 пациентов (15 %).
В 11 наблюдениях (85 %) ИМ развился у пациентов после алло-ТГСК, еще в 2 (15 %) – при проведении ПХТ. Медиана времени развития ИМ от алло-ТГСК или начала ПХТ составила 96 суток (20–510 суток), при инвазивном аспергиллезе – 131 сутки (20–510 суток), при мукормикозе – 42 дня (28–329 суток). Иммуносупрессивную терапию в связи с течением хронической или острой реакции «трансплантат против хозяина» на момент развития ИМ получали 4 из 11 реципиентов алло-ТГСК (36 %).
Лихорадка имела место у всех 13 пациентов, кашель – у 5 (39 %), боль в грудной клетке – у 5 больных (39 %), кровохарканье – у 2 (15 %). На момент проведения операции общее состояние 7 (54 %) больных расценено как удовлетворительное, 4 (31 %) – средней тяжести, 2 (15 %) – тяжелое. Кислородозависимыми были 2 (15 %) пациента, не мог самостоятельно передвигаться 1 (7,7 %) больной. Индекс массы тела ниже 18,5 имел место у 10 пациентов из 13 (77 %). На момент решения вопроса об операции у 46 % больных (n=6) наблюдалась нейтропения, а у 4 пациентов (31 %) – нейтропения 4 степени (абсолютное количество нейтрофилов менее 0,5×109/л). Уровень гемоглобина составлял от 50 до 114 г/л, уровень альбумина – 20–34 г/л. Количество тромбоцитов в крови было ниже 50×109/л у 10 пациентов из 13 (77 %).
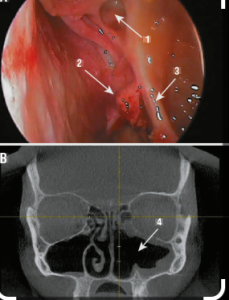
Рентгенологически у 7 пациентов (53,8 %) определялось двустороннее, у 6 пациентов (46,2 %) – одностороннее поражение легких: одиночные очаги/участки консолидации в пределах 1 или 2 долей одного легкого имели место у 4 больных (30,8 %), множественные очаги/участки консолидации с суммарным поражением более 3 долей – у 9 пациентов (69,2 %). Изменения легочной ткани были представлены участками консолидации без симптома «гало» у 5 пациентов (38,5 %), с симптомом «гало» – у 2 пациентов (15 %), симптом «обратного гало» определялся у 4 больных (31 %), симптом «воздушного полумесяца» у 1 пациента (8 %). У 2 пациентов (15 %) отмечалось формирование зоны центрального некроза в участках консолидации легочной ткани, у 4 пациентов (31 %) – формирование полостей. Значимый плевральный выпот имел место у 3 больных (23 %). Инвазия микоза в грудную стенку с деструкцией ребер отмечалась у 2 пациентов (15 %).
Наличие внелегочных очагов поражения имело место у 2 (15 %) больных.
До операции были установлены следующие микологические диагнозы: вероятный инвазивный аспергиллез легких – 39 % (n=5), мукормикоз легких – 46 % (n=6), сочетание инвазивного аспергиллеза с мукормикозом – 7,7 % (n=1), без верифицированного диагноза оперирован 1 пациент. 3 пациентам (23 %) противогрибковая терапия назначена в момент диагностики ИМ, 10 больных (77 %) на момент подтверждения наличия ИМ уже получали противогрибковую терапию.
Все оперативные вмешательства были односторонними, выполнены через боковую торакотомию, повторных операций не было. В предоперационном периоде проводилось интенсивное устранение, а чаще – уменьшение выраженности факторов риска (компенсация сопутствующих состояний, отмена химиотерапии и иммуносупрессии, гемотрансфузии эритроцитарной массы, тромбоцитов). Решение об окончательном объеме вмешательства принималось интраоперационно. Произведено 5 пневмонэктомий, 4 нижние лобэктомии, 2 верхние билобэктомии, 2 атипичные резекции легкого, 1 верхняя лобэктомия. У 2 больных выполнена резекция грудной стенки, резецированы участки от 2 до 4 ребер. Средняя длительность операций составила 150 мин (от 50 до 180 мин).
Средний объем кровопотери – 250 мл, ни в одном наблюдении кровопотеря не превышала 10 % ОЦК. Особенностями операций были: диффузная кровоточивость, выраженный спаечный процесс в плевральной полости, облитерация междолевых щелей, сложность диссекции тканей и их визуальная дифференцировка, необходимость прерывания однолегочной вентиляции. Интраоперационных осложнений не было.
11 из 13 больных экстубированы в операционной, у 2 потребовалась продленная искусственная вентиляция легких. Длительность дренирования плевральной полости после пневмонэктомий составила 2 суток, после лобэктомий – 3,1±0,9 суток, случаев длительной негерметичности оставшейся части легкого не было. Значимых послеоперационных осложнений не зафиксировано, за исключением 1 больного (7,7 %) с двусторонним микотическим поражением легких и ХОБЛ среднетяжелого течения, который умер через 5 суток после правосторонней пнемонэктомии из-за нарастания дыхательной и сердечнососудистой недостаточности.
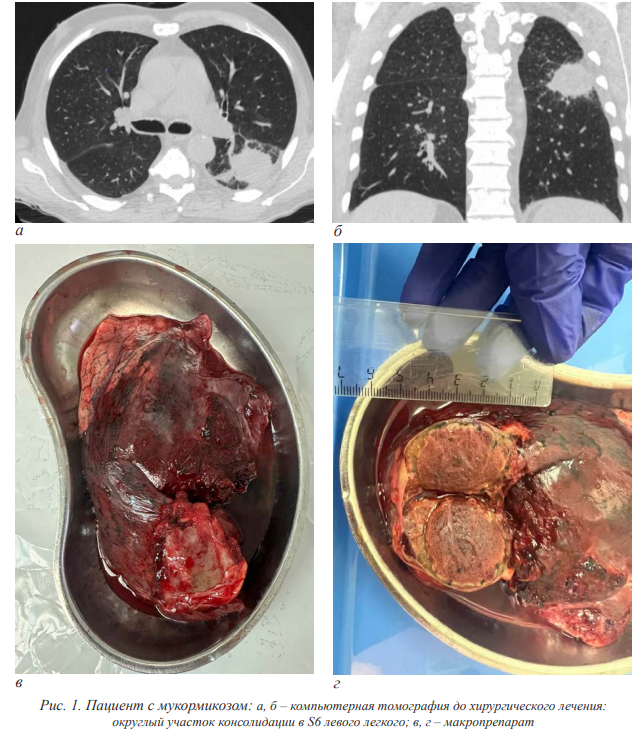
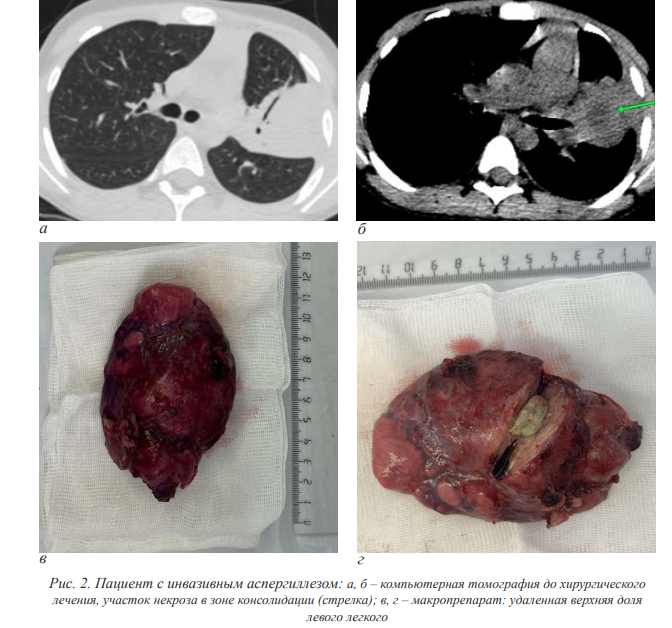
При послеоперационном гистологическом и микологическом исследовании удаленных препаратов ИМ был подтвержден у всех пациентов. Исследование удаленных препаратов позволило увеличить долю пациентов с идентифицированными возбудителями до вида и получить культуру для определения чувствительности к противогрибковым препаратам c 15 % перед операцией (2 из 13) до 46 % (6 из 13). На рис. 1, 2 представлены примеры компьютерной томографии и фотографии удаленных препаратов у больных мукормикозом и инвазивным аспергиллезом легких.
Во всех наблюдениях хирургическое вмешательство привело к излечению в соответствии с критериями оценки ответа на терапию ИМ [20, 21]. 8 больных (61,5 %) излечились от ИМ легких с медианой наблюдения 118 дней (от 42 до 900 суток), трое погибли от прогрессирования основного заболевания.
Обсуждение.
Мукормикоз и аспергиллез — инвазивная грибковая инфекция, включает в себя многочисленные варианты возбудителей, широко распространенные в природе [16]. При вдыхании спор, прямом контакте с открытыми ранами и употреблении зараженной пищи эти условно-патогенные микроорганизмы могут вызывать инфекционный процесс, обычно развивающийся у лиц с резко ослабленным иммунитетом, в первую очередь у онкогематологических больных, получающих ПХТ и/ или ТГСК [16, 17]. Авторами представлены клинические характеристики больных, у которых развился ИМ легких, потребовавший хирургического лечения за последнее десятилетие.
У 85 % больных инвазивный микоз легких развился после алло-ТГСК, которая характеризуется более глубокой иммуносупрессией и многофакторным комплексом реакций организма по сравнению с пациентами после ПХТ, где основным фактором риска является нейтропения. Риск инвазивных микозов после алло-ТГСК существенно повышается в позднюю фазу приживления трансплантата, в нашем исследовании медиана времени от ТГСК/ПХТ до развития ИМ составил 96 суток. Особенностью ИМ является ангиоинвазия с множественными тромбозами и некрозом легочной паренхимы, что приводит к деструкции и/или легочному кровотечению, которое может быть фатальным [20].
Сложным аспектом диагностики ИМ является необходимость точной идентификации возбудителя до вида, вызвавшего поражение легочной паренхимы [21, 22]. Часть наших пациентов оперированы без микологического подтверждения. Результатом хирургического лечения стало не только выздоровление от ИМ, но и увеличение доли пациентов с идентифицированными возбудителями до вида, а также получение культуры гриба для определения чувствительности к противогрибковым препаратам у 46 % больных. При некоторых вариантах ИМ, несмотря на точное знание этиологического фактора и вовремя начатое лечение, только полное хирургическое удаление очага поражения будет способствовать положительному терапевтическому результату. Задержка с проведением операции может быть фатальной в связи с быстрым развитием диссеминации, полиорганной недостаточности, что делает операцию невозможной [23]. В то же время очень непросто определить, в какой момент каждому конкретному больному именно хирургическое лечение принесет максимальную пользу. В литературе встречаются лишь единичные работы, описывающие хирургическое лечение ИМ у онкогематологических больных с различными вариантами проведенных операций, но почти всегда это описания отдельных клинических случаев [24, 25]. В этой работе мы представляем самый большой из известных нам опубликованных работ одноцентрового опыта хирургического лечения ИМ легких (инвазивный аспергиллез и мукормикоз, n=13) у онкогематологических больных после ПХТ и ТГСК. В нашу серию наблюдений включены только односторонние операции вплоть до удаления всего легкого с резекцией вовлеченной в патологический процесс грудной стенки, хотя у части пациентов имел место двусторонний ИМ легких.
Операция со стороны максимального поражения позволяет повысить эффективность лекарственного лечения грибкового патологического процесса и с контралатеральной стороны, что продемонстрировано и у пациентов, включенных в данное исследование. Проведенное хирургическое лечение позволяет достичь полного или частичного ответа на терапию, сократить время до ответа и общую продолжительность противогрибковой терапии, а в случае мукормикоза – является жизнеспасающей операцией [22–25]. Важным результатом, представленным в настоящем анализе, является отсутствие интраоперационных и значимых послеоперационных осложнений, за исключением одного летального исхода у больного с двусторонним микотическим поражением и ХОБЛ среднетяжелого течения. Несмотря на исходную тяжесть состояния пациентов, в том числе низкий уровень иммунного ответа, критическую тромбоцитопению, техническую сложность большинства операций, – большой опыт общей торакальной и онкоторакальной хирургии, высокий уровень анестезиологической и реанимационной помощи, хорошее лекарственное и заместительное обеспечение позволили достичь таких хирургических результатов. Чрезвычайно важной представляется и работа мультидисциплинарной команды, включающей торакального хирурга с момента постановки диагноза ИМ, что позволило провести своевременную диагностику с ранним началом лекарственной терапии и корректным выбором момента для проведения хирургического вмешательства, хотя этот вопрос требует накопления еще большего опыта.
Выводы.
Развитие ИМ легких у онкогематологических больных после ТГСК или ПХТ определяет плохой прогноз течения посттрансплантационного периода и основного заболевания. Хирургическое лечение данной группы пациентов возможно при условии устранения, а чаще – уменьшения выраженности факторов риска (компенсация сопутствующих состояний, отмена ХТ и ГКС, гемотрансфузии эритроцитарной массы, тромбоцитов). При корректном и своевременном отборе гематологических больных с ИМ легких непосредственные результаты хирургического лечения благоприятны. Конфликт интересов Авторы заявили об отсутствии конфликта интересов. Conflict of interest The authors declare no conflict of interest. Соответствие нормам этики Авторы подтверждают, что соблюдены права людей, принимавших участие в исследовании, включая получение информированного согласия в тех случаях, когда оно необходимо, и правила обращения с животными в случаях их использования в работе.
Литература
1. Valentine J. C., Morrissey C. O., Tacey M. A. et al. A population-based analysis of invasive fungal disease in haematology-oncology patients using data linkage of state-wide registries and administrative databases: 2005-2016. BMC Infect Dis. 2019. Vol. 19. P. 274.
2. Zubarovskaya L. S., Moiseev I. S., Vladovskaya M. D. et al. Trends in Outcome of Hematopoietic Stem Cell Transplantation: 5000 Transplantations and 30 Years of Single-Center Experience. Cancers. 2023. Vol. 15. P. 4758.
3. Young J. A. H., Weisdorf D. J. Infections in Recipients of Hematopoietic Stem Cell Transplants. Mandell, Douglas, and Bennett’s Principles and Practice of Infectious Diseases. 2015. Vol. 2. P. 3425–3439.e5. https:// doi.org/10.1016/B978-1-4557-4801-3.00312-X.
4. Popova M., Rogacheva Yu. Epidemiology of invasive fungal diseases in patients with hematological malignancies and haematopoietic cell transplantation recipients: Systematic review and meta-analysis of trends over time. Journal of Infection and Public Health. 2025. Vol. 18, Issue 8. P. 102804.
5. Souza L., Nouér S. A., Morales H. et al. Epidemiology of invasive fungal disease in haematologic patients. Mycoses. 2021. Vol. 64, № 3. P. 252–256.
6. Шадривова О. В., Хостелиди С. Н., Шагдилева Е. В. и др. Мукормикоз и инвазивный аспергиллез у пациентов с онкогематологической патологией в России (результаты многоцентрового исследования). Проблемы медицинской микологии. 2024. Т. 26, № 2. С. 26–37.
7. Климко Н. Н. Глава 1. Микозы легких / Н. Н. Климко. Респираторная медицина: руководство: в 5 томах. Издание третье, дополненное и переработанное. Москва: Общество с ограниченной ответственностью «ПУЛЬМОМЕДИА», 2024. С. 656-679.
8. Interim Report April 2023 Fungiscope.
9. Cornely O. A., Alastruey-Izquierdo A., Arenz D. et al. Mucormycosis ECMM MSG Global Guideline Writing Group. Global guideline for the diagnosis and management of mucormycosis: an initiative of the European Confederation of Medical Mycology in cooperation with the Mycoses Study Group Education and Research Consortium. Lancet Infect Dis. 2019. Vol. 19, № 12. P. e405–e421
10. Ullmann A. J., Aguado J. M., Arikan-Akdagli S. et al. Diagnosis and management of Aspergillus diseases: executive summary of the 2017 27 «Grekov’s Bulletin of Surgery» • 2025 • Vol. 184 • № 6 • P. 21–28 Akopov A. L. et al. ESCMID-ECMM-ERS guideline. Clin Microbiol Infect. 2018. Vol. 24 Suppl 1. P. e1–e38.
11. Etienne K. A., Gillece J., Hilsabeck R. et al. Whole genome sequence typing to investigate the Apophysomyces outbreak following a tornado in Joplin, Missouri, 2011. PLoS One. 2012. Vol. 7, № 11. P. e49989.
12.Sun H. Y., Aguado J. M., Bonatti H. et al. Pulmonary zygomycosis in solid organ transplant recipients in the current era. Am J Transplant. 2009. Vol. 9, № 9. P. 2166–71.
13. Roden M. M., Zaoutis T. E., Buchanan W. L. et al. Epidemiology and outcome of zygomycosis: a review of 929 reported cases. Clin Infect Dis. 2005. Vol. 41, № 5. P. 634–53
14. Skiada A., Pagano L., Groll A. et al. Zygomycosis in Europe: analysis of 230 cases accrued by the registry of the European Confederation of Medical Mycology (ECMM) Working Group on Zygomycosis between 2005 and 2007. Clin Microbiol Infect. 2011. Vol. 17, № 12. P. 1859–67.
15. Almyroudis N. G., Sutton D. A., Linden P. et al. Zygomycosis in solid organ transplant recipients in a tertiary transplant center and review of the literature. Am J Transplant. 2006. Vol. 6, № 10. P. 2365–74.
16. De Pauw B., Walsh T. J., Donnelly J. P. et al. European Organization for Research and Treatment of Cancer/Invasive Fungal Infections Cooperative Group; National Institute of Allergy and Infectious Diseases Mycoses Study Group (EORTC/MSG) Consensus Group. Revised definitions of invasive fungal disease from the European Organization for Research and Treatment of Cancer/Invasive Fungal Infections Cooperative Group and the National Institute of Allergy and Infectious Diseases Mycoses Study Group (EORTC/MSG) Consensus Group. Clin Infect Dis. 2008. Vol. 46, № 12. P. 1813–21.
17. Donnelly J. P., Chen S. C., Kauffman C. A. et al. Revision and Update of the Consensus Definitions of Invasive Fungal Disease From the European Organization for Research and Treatment of Cancer and the Mycoses Study Group Education and Research Consortium Clin Infect Dis. 2020. Vol. 71, № 6. P. 1367–1376.
18. Попова М. О. Диагностика и лечение инвазивных микозов в гематологии и ТГСК у взрослых: алгоритм. Санкт-Петербург: НИИ ДОГиТ им. Р. М. Горбачевой ПСПбГМУ им. акад. И. П. Павлова, 2024. 1 с. EDN NIDYXR.
19. Попова М. О. Диагностика и лечение инвазивных микозов в гематологии и ТГСК у детей: алгоритм. Санкт-Петербург: НИИ ДОГиТ им. Р.М. Горбачевой ПСПбГМУ им. акад. И. П. Павлова, 2024. 1 с. EDN DBXILD.
20. Попова М. О., Рогачева Ю. А., Синяев А. А. и др. Диагностика и лечение инвазивных микозов в гематологии и трансплантации костного мозга: руководство для врачей. Санкт-Петербург: НИИ ДОГиТ им. Р.М. Горбачевой ПСПбГМУ им. акад. И. П. Павлова, 2024. 84 с. EDN PKLMHO.
21. Segal B. H., Herbrecht R., Stevens D. A. et al. Defining responses to therapy and study outcomes in clinical trials of invasive fungal diseases: Mycoses Study Group and European Organization for Research and Treatment of Cancer consensus criteria. Clin Infect Dis. 2008. Vol. 47, № 5. P. 674–83.
22. Roden M. M., Zaoutis T. E., Buchanan W. L. et al. Epidemiology and outcome of zygomycosis: a review of 929 reported cases. Clin Infect Dis. 2005. Vol. 41, № 5. P. 634–53.
23. Skiada A., Pagano L., Groll A. et al. European Confederation of Medical Mycology Working Group on Zygomycosis. Zygomycosis in Europe: analysis of 230 cases accrued by the registry of the European Confederation of Medical Mycology (ECMM) Working Group on Zygomycosis between 2005 and 2007. Clin Microbiol Infect. 2011. Vol. 17, № 12. P. 1859–67.
24. Choi H., Lee H., Jeon K. et al. Factors affecting surgical resection and treatment outcomes in patients with pulmonary mucormycosis. J Thorac Dis. 2019. Vol. 11, № 3. P. 892–900.
25. Shao W., Zhang J., Ma S. et al. Characteristics of pulmonary mucormycosis and the experiences of surgical resection. J Thorac Dis. 2020. Vol. 12, № 3. P. 733–740.
Информация об авторах:
Акопов Андрей Леонидович, доктор медицинских наук, профессор, руководитель отдела торакальной хирургии клиники НИИ хирургии и неотложной медицины, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова (Санкт-Петербург, Россия), ORCID: 0000-0001-8698-7018;
Мишра Радеж Прадипович, кандидат медицинских наук, врач-торакальный хирург онкологического отделения № 4 (торакальной хирургии) клиники НИИ хирургии и неотложной медицины, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова (Санкт-Петербург, Россия), ORCID: 0000-0002-8387-9182;
Швецов Александр Николаевич, зав. операционным блоком, врач – детский хирург клиники НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова (СанктПетербург, Россия), ORCID: 0000-0001-7173-7673;
Попова Марина Олеговна, кандидат медицинских наук, врач-гематолог отделения трансплантации костного мозга для взрослых клиники НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, доцент кафедры гематологии, трансфузиологии и трансплантологии с курсом детской онкологии ФПО им. Б. В. Афанасьева, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова (Санкт-Петербург, Россия), ORCID: 0000-0001-8536-5495;
Рогачева Юлия Александровна, врач-гематолог отделения трансплантации костного мозга для взрослых клиники НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова (Санкт-Петербург, Россия), ORCID: 0000-0001-8270-4535; Николаев Илья Юрьевич, врач-рентгенолог отделения рентгеновской компьютерной томографии № 1 Научно-клинического центра лучевой диагностики и лучевой терапии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова (Санкт-Петербург, Россия), ORCID: 0000-0002-8589-4618;
Заграничнов Валентин Дмитриевич, врач клинической лабораторной диагностики отделения клинической микробиологии, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова (Санкт-Петербург, Россия), ORCID: 0009-0009-6601-7984;
Зубаровская Людмила Степановна, доктор медицинских наук, заместитель директора по трансплантации костного мозга НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой; профессор кафедры гематологии, трансфузиологии и трансплантологии с курсом детской онкологии ФПО им. Б. В. Афанасьева, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова (Санкт-Петербург, Россия), ORCID: 0000-0003-2594-7703;
Кулагин Александр Дмитриевич, доктор медицинских наук, проректор по научной работе, директор НИИ детской онкологии, гематологии и трансплантологии им. Р. М. Горбачевой, зав. кафедрой кафедры гематологии, трансфузиологии и трансплантологии с курсом детской онкологии ФПО им. Б. В. Афанасьева, Первый Санкт-Петербургский государственный медицинский университет им. акад. И. П. Павлова (Санкт-Петербург, Россия),
Теги: микозы легких
234567 Начало активности (дата): 15.05.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: инвазивные микозы легких, мукормикоз, инвазивный аспергиллез, онкогематология, резекции легких, трансплантация гемопоэтических стволовых клеток, противоопухолевая химиотерапия
12354567899
Похожие статьи
Значение показателей ферритина и В2 микроглобулина в процессе лечения больных туберкулезом легкихРентген на дому 8 495 22 555 6 8
Абсцессы легких и абсцедирующие пневмонии
Общая семиотика диффузных заболеваний легких по данным компьютерной томографии высокого разрешения
Грудина



