 23.04.2026
23.04.2026
Сравнительная эффективность хирургических методов коррекции синдрома «висящей стопы» при изолированной нейропатии малоберцового нерва
Современные хирургические подходы включают различные варианты сухожильных транспозиций, среди которых наиболее распространены тенодез длинного разгибателя пальцев и транспозиция задней большеберцовой мышцы через межкостную мембрану
ВВЕДЕНИЕ
Нейропатия малоберцового нерва с развитием синдрома «висящей стопы» представляет актуальную проблему современной ортопедии, существенно ограничивая функциональные возможности пациентов и значительно снижая качество их жизни [1]. Анатомические особенности расположения малоберцового нерва в области головки малоберцовой кости обусловливают его высокую уязвимость к компрессионным воздействиям различной этиологии, что подтверждается данными эпидемиологических исследований о частоте поражения в данной локализации [2].
Современные исследования демонстрируют, что при длительности денервации более 12 месяцев эффективность прямых нейрореконструктивных вмешательств значительно снижается вследствие развития необратимых структурных изменений в мышечной ткани и фиброзных процессов в денер- вированных мышцах [3]. В таких случаях сухожильные транспозиции становятся методом выбора для восстановления функции тыльного сгибания стопы.
Современные хирургические подходы включают различные варианты сухожильных транспозиций, среди которых наиболее распространены тенодез длинного разгибателя пальцев и транспозиция задней большеберцовой мышцы через межкостную мембрану [4]. Однако опубликованные исследования демонстрируют противоречивые данные относительно сравнительной эффективности этих методик, что обусловлено преимущественно ретроспективным характером работ, небольшими размерами выборок и отсутствием стандартизированных критериев оценки функциональных результатов [5]. Недостаток прямых сравнительных исследований с использованием объективных методов функциональной оценки затрудняет формирование доказательных клинических рекомендаций.
Цель работы — определение оптимальной хирургической тактики восстановления функции тыльного сгибания стопы при изолированном поражении малоберцового нерва путем сравнительного анализа результатов тенодеза длинного разгибателя пальцев и транспозиции задней большеберцовой мышцы.
Проведения настоящего исследования обусловлено потребностью в получении объективных данных о сравнительной эффективности двух наиболее распространенных методик сухожильной коррекции синдрома «висящей стопы». Комплексная оценка функциональных результатов с использованием ва- лидированных шкал, инструментальных методов измерения силы и амплитуды движений, а также современных стабилометрических технологий позволяет получить многостороннюю характеристику эффективности хирургического лечения. Анализ не только непосредственных результатов операций, но и отдаленных исходов на протяжении двухлетнего периода наблюдения обеспечивает оценку стабильности достигнутого улучшения и выявление потенциальных отсроченных осложнений.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводили на базе отделения реконструктивной хирургии в период с января 2018 г. по декабрь 2023 г.
Критерии включения: возраст от 18 до 65 лет; длительность нейропатии более 12 месяцев; изолированная нейропатия малоберцового нерва, подтвержденная методом электронейромиографии; отсутствие эффекта от консервативной терапии в течение минимум шести месяцев, информированное согласие на участие в исследовании.
Критерии невключения: множественные повреждения нервов нижней конечности; сопутствующие ортопедические заболевания стопы и голеностопного сустава; системные нейромышечные заболевания; тяжелая соматическая патология в стадии декомпенсации; психические расстройства, препятствующие участию в исследовании; отказ от участия или нарушение протокола наблюдения.
Способ формирования выборки осуществляли методом сплошного отбора среди пациентов, соответствующих критериям включения. Дизайн исследования представлял собой проспективное сравнительное когортное исследование с параллельными группами.
В исследование включено 84 пациента, средний возраст — (41,3 ± 7,8) года, соотношение мужчин и женщин — 1,4:1. Первую группу составили 42 пациента, которым выполняли тенодез сухожилия длинного разгибателя пальцев к переднему краю большеберцовой кости по модифицированной методике Ламбринуди. Во вторую группу включены 42 пациента, перенесших транспозицию задней большеберцовой мышцы через межкостную мембрану с фиксацией к латеральной клиновидной кости по технике Bridle.
Функциональная оценка проведена с использованием шкалы AOFAS для голеностопного сустава и заднего отдела стопы, которая оценивает болевой синдром, функциональные возможности и выравнивание стопы по 100-балльной шкале. Измерения амплитуды тыльного сгибания проводили стандартным гониометром в положении пациента лежа на спине с фиксированной голенью, при этом измеряли максимальный угол между продольной осью стопы и передней поверхностью голени.
Динамометрию силы тыльных сгибателей выполняли на аппарате MicroFET2 (Hoggan Health Industries) с измерением силы в кг при максимальном изометрическом сокращении в положении сидя с согнутой под прямым углом голенью, результаты выражали в % от силы контралатеральной конечности.
Стабилометрическое исследование проводили на платформе Стабилан-01-2 (ОКБ «Ритм») в статическом режиме с регистрацией колебаний центра давления при стоянии с открытыми глазами в течение 30 сек. Анализировали длину траектории центра давления в мм, площадь статокинезиограммы в мм2, средние квадратические отклонения во фронтальной и сагиттальной плоскостях, коэффициент Ромберга. Контрольные точки наблюдения установлены через три, шесть, 12 и 24 месяца после операции.
Статистическую обработку данных производили с помощью пакета анализа данных IBM SPSS Statistics версии 26.0. Проверку нормальности распределения осуществляли с использованием критерия Шапиро - Уилка при объеме выборки менее 50 наблюдений и критерия Колмогорова - Смирнова при большем объеме выборки. При нормальном распределении данных применяли параметрический t-критерий Стьюдента для независимых выборок, при отклонении от нормального распределения использовали непараметрический критерий Манна - Уитни. Количественные характеристики показателей в выборочных совокупностях представляли в виде среднего арифметического и стандартного отклонения при нормальном распределении или медианы и интерквартильного размаха при распределении, отличном от нормального. Для оценки однородности групп рассчитывали коэффициент вариации как отношение стандартного отклонения к среднему арифметическому, выраженное в процентах. Уровень статистической значимости принят за p < 0,05.
РЕЗУЛЬТАТЫ
Дооперационные показатели в группах статистически не различались, что обеспечивало корректность последующего сравнительного анализа. Средний балл AOFAS составлял (52,4 ± 6,1) в первой группе и (51,8 ± 5,9) во второй группе при p = 0,614. Амплитуда активного тыльного сгибания находилась в пределах минус (12,3 ± 3,4)° и минус (11,9 ± 3,7)° соответственно (табл. 1).

Через 12 месяцев в группе тенодеза отмечено увеличение балла AOFAS до (78,6 ± 8,2), что на 26,2 балла превысило исходный уровень при p < 0,001. Амплитуда тыльного сгибания достигла (8,4 ± 4,1)°, демонстрируя прирост 20,7°. Во второй группе функциональный результат оказался более выраженным: балл AOFAS составил (86,3 ± 6,7) с приростом 34,5 балла при p < 0,001, а амплитуда движений увеличилась до (14,8 ± 3,9)° с общим улучшением на 26,7°.
Межгрупповое сравнение выявило статистически значимое преимущество транспозиции задней большеберцовой мышцы как по шкале AOFAS при p = 0,003, так и по амплитуде движений при p = 0,001. Динамометрия показала восстановление силы тыльного сгибания до (62,4 ± 11,3) % от контралатеральной конечности в первой группе и до (78,9 ± 9,6) % во второй группе при p < 0,001 (табл. 2).
При стабилометрическом исследовании зарегистрировано статистически значимое улучшение показателей контроля баланса в обеих группах. Длина траектории центра давления сократилась на 34,8 % при тенодезе и на 51,6 % при транспозиции относительно дооперационных значений. Площадь статокинезиограммы уменьшилась на 28,3 % в первой группе и на 42,7 % во второй группе. Средние квадратические отклонения во фронтальной плоскости снизились с (4,8 ± 1,2) мм до (3,2 ± 0,9) мм в группе тенодеза и с (4,9 ± 1,3) мм до (2,6 ± 0,8) мм в группе транспозиции.

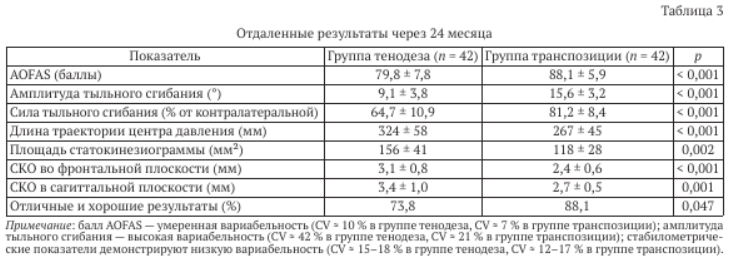
Через 24 месяца наблюдения результаты в обеих группах стабилизировались с незначительным дополнительным улучшением. В группе транспозиции балл AOFAS достиг (88,1 ± 5,9), амплитуда тыльного сгибания составила (15,6 ± 3,2)°. В группе тенодеза соответствующие показатели составили (79,8 ± 7,8) балла и (9,1 ± 3,8)°. Отличные и хорошие результаты по критериям AOFAS получены у 73,8 % пациентов первой группы и у 88,1 % второй группы при p = 0,047.
Стабилометрические показатели через 24 месяца подтвердили превосходство активной мышечной транспозиции. Длина траектории центра давления в группе транспозиции составила (267 ± 45) мм против (324 ± 58) мм в группе тенодеза при p < 0,001. Площадь статокинезиограммы равнялась (118 ± 28) мм2 против (156 ± 41) мм2 соответственно при p
= 0,002 (табл. 3).
Осложнения развились у шести пациентов после тенодеза, что составило 14,3 %, включая три случая недостаточной коррекции, потребовавших ревизионного вмешательства, два случая формирования болезненных рубцов и один случай инфицирования раны. В группе транспозиции зарегистрировано четыре осложнения, составивших 9,5 %: два случая транзиторной слабости подошвенного сгибания, один случай туннельного синдрома переднего отдела голени и один случай гипертрофического рубца. Различия по частоте осложнений статистически незначимы при p = 0,386.
ОБСУЖДЕНИЕ
Полученные результаты убедительно демонстрируют преимущество транспозиции задней большеберцовой мышцы над тенодезом длинного разгибателя пальцев при коррекции синдрома висящей стопы, обусловленного изолированной нейропатией малоберцового нерва. Разница в функциональном восстановлении между двумя методиками объясняется фундаментальным различием в механизме их действия, — транспозиция создает активную мышечную тягу, тогда как тенодез обеспечивает лишь пассивную стабилизацию стопы. Эти данные согласуются с наблюдениями, продемонстрировавшими значительное улучшение дорсифлексии и походки после применения процедуры Bridle при травматическом повреждении малоберцового нерва, причем все пациенты достигли функционального восстановления без использования дополнительных ортопедических приспособлений [1, 6].
Достигнутое в нашем исследовании восстановление силы тыльного сгибания до 78,9 % от контралатеральной конечности в группе транспозиции коррелирует с международными данными, представленными различными исследовательскими группами. N. Eisenstein et al. подчеркивали важность тщательного планирования и соблюдения показаний к сухожильным транспозициям, что находит подтверждение в наших результатах [2]. А.М. Мацакян с соавт. при использовании миниинвазивного метода транспозиции сухожилия задней большеберцовой мышцы получили хороший результат у 12 из 16 пациентов, что демонстрирует воспроизводимость данной техники в различных клинических условиях [3]. Важно отметить, что модификация A. Medina процедуры пересадки сухожилия для коррекции обширного некроза мышц передней группы голени открывает возможности индивидуализации хирургических подходов в зависимости от степени поражения мышечных структур [4].
Меньшее восстановление силы при тенодезе, составившее 62,4 % от контралатеральной конечности, объясняется отсутствием активного мышечного компонента и зависимостью эффекта от натяжения фиксированного сухожилия. Это наблюдение согласуется с выводами L. Wareham et al. о важности комплексного подхода к лечению пациентов с нейродегенеративными процессами, однако наш анализ выявил существенные различия в долгосрочных функциональных исходах между различными методиками сухожильных транспозиций [5]. K.L. McCormick подчеркивал важность определения этиологии паралича малоберцового нерва для выбора оптимальной хирургической тактики, учитывая вариабельность спектра деформаций и слабости в голеностопном суставе, что находит отражение в различной эффективности применяемых нами методик [7].
Стабилометрические показатели продемонстрировали объективное улучшение контроля баланса и качества походки, причем сокращение длины траектории центра давления составило 51,6 % при транспозиции против 34,8 % при тенодезе относительно дооперационных значений. Эти данные коррелируют с выводами Ю.Б. Голубевой с соавт., установившими при ретроспективном анализе данных 375 пациентов, что при синдроме висящей стопы отмечается нарушение опорности, устойчивости, симметричности и ритмичности ходьбы, что значительно ухудшает качество жизни [8]. G. Chen продемонстрировал, что функциональное электростимулирование способно восстанавливать физиологический паттерн активации мышц дорсифлексоров и улучшать биомеханические показатели походки у пациентов с имплантированными нейростимуляторами, что открывает перспективы комбинированного лечения [9].
Достигнутая разница в 7,7 балла по шкале AOFAS и 6,5 ° амплитуды движений через 24 месяца имеет не только статистическое, но и клиническое значение для повседневной активности пациентов. I. Wiszomirska подтвердила важность комплексного подхода к коррекции биомеханических нарушений, что согласуется с нашими наблюдениями о многофакторности функционального восстановления [10]. Е.И. Аксенова установила высокую эффективность комплексных реабилитационных программ с биологической обратной связью в послеоперационном восстановлении функции стопы, что подчеркивает необходимость интеграции хирургического лечения с современными реабилитационными технологиями [11].
Частота осложнений в наших группах оказалась сопоставимой и составила 14,3 % после тенодеза против 9,5 % после транспозиции, что согласуется с данными М.Г. Башлячева с соавт., наблюдавшими 80 пациентов с компрессионной невропатией общего малоберцового нерва и выполнивших 84 операции декомпрессии [12]. Характер осложнений существенно различался между группами: недостаточная коррекция при тенодезе связана с техническими аспектами определения оптимального натяжения сухожилия, что требует значительного хирургического опыта. М.М. Сомова и В.Л. Доманский разработали технологию интраоперационного визуального нейромониторинга для операций реконструктивной нейропластики, создав специальный электростимулятор ЭСВМ-1, который может потенциально снизить частоту подобных осложнений за счет объективизации контроля натяжения [13].
Транзиторная слабость подошвенного сгибания после транспозиции является ожидаемым явлением и регрессирует в процессе нейромышечной адаптации в течение трех-четырех месяцев. Это согласуется с наблюдениями А.В. Новикова и В.А. Антоновой, проанализировавшими результаты лечения 254 пациентов после эндопротезирования коленного сустава и установившими, что комплексное интенсивное восстановительное лечение, проводимое с перерывами на протяжении не менее шести месяцев, в 75 % случаев позволило восстановить функцию пораженного нерва [14]. F.M. Leclere в исследованиях по невротизированному переносу мышц подчеркивал значимость медикаментозной поддержки процессов реиннервации, что корреспондирует с необходимостью комплексного подхода к профилактике и лечению послеоперационных осложнений [15].
Временной фактор играет критическую роль в определении показаний к различным хирургическим методикам. Z. Pang et al. в ретроспективном исследовании 45 пациентов с повреждениями общего малоберцового нерва установили, что оптимальный временной интервал для достижения восстановления тыльного сгибания стопы до уровня М3 составляет 9,5 месяцев с площадью под ROC-кривой 0,871, а для восстановления до уровня М4 оптимальный срок составил 5,5 месяцев [16]. Наш критерий включения пациентов с длительностью нейропатии более 12 месяцев обосновывает выбор сухожильных транспозиций при неэффективности нервной реконструкции. B. Bao et al. продемонстрировали появление новых электрических потенциалов в передней большеберцовой мышце и длинных разгибателях у семи из восьми пациентов через 10-15 месяцев после прямой пересадки мышечной ветви камбаловидной мышцы большеберцового нерва к глубокому малоберцовому нерву, что подчеркивает важность ранних нейрореконструктивных вмешательств [17].
Критический анализ электрофизиологических показателей как предикторов успешности хирургического лечения представляет важный аспект нашего подхода. В отличие от работы С.С. Никитина с соавт., сосредоточенной на феноменологии блока проведения, наше исследование установило, что при длительности денервации более 12 месяцев целесообразность прямой нервной реконструкции существенно снижается [18]. А.А. Фоминых с соавт. исследовали эффективность невролиза при компрессионной нейропатии малоберцового нерва в фибулярном канале у 29 пациентов и получили отличные результаты лечения в 89,7 % случаев, что подтверждает эффективность декомпрессивных вмешательств в ранние сроки заболевания [19].
А.П. Власов с соавт. отметили, что закрытые повреждения малоберцового нерва самопроизвольно восстанавливаются примерно у трети пациентов, но у оставшихся двух третей может потребоваться хирургическое вмешательство, причем отдаленные результаты хирургического лечения по восстановлению нерва или невролиза малоберцового нерва не всегда удовлетворительные [20]. Это наблюдение обосновывает необходимость разработки альтернативных хирургических стратегий для пациентов с длительной денервацией. Z. Liu et al. в ретроспективном когортном исследовании 387 пациентов, перенесших хирургическую ревизию поврежденного общего малоберцового нерва, установили, что высокая предоперационная мышечная сила снижает риск неблагоприятного исхода с относительным риском 0,18, что подчеркивает важность раннего хирургического вмешательства до развития выраженной мышечной атрофии [21].
Анатомические исследования B. Lezak предоставили фундаментальную основу для понимания особенностей малоберцового нерва и его ветвей, подчеркивая важность точной локализации зоны компрессии для определения объема невролиза и прогнозирования функциональных результатов операции [22]. M. Bojovic разработал систематический подход к диагностике туннельных синдромов, включающий детальную клиническую оценку, дифференциальную диагностику и интеграцию результатов дополнительных методов исследования, что находит отражение в нашем комплексном предоперационном обследовании [23]. M. Fakih продемонстрировал важность тщательного клинического интервьюирования и фокусированного физикального обследования для локализации нейропатии, что особенно актуально при атипичных причинах компрессии [24].
Специфические клинические ситуации требуют особого диагностического подхода с учетом патофизиологических механизмов. U. Yadav et al. представили детальный анализ ятрогенного синдрома висящей стопы после реконструкции передней крестообразной связки, при хирургической ревизии которого была обнаружена интраневральная гематома с контузией нервного ствола, потребовавшая проведения нейролиза с последующим восстановлением функции через три месяца [25]. A. Lale исследовал частоту и причины развития синдрома висящей стопы после бариатрических вмешательств, установив связь между потерей жировой прослойки вокруг головки малоберцовой кости и развитием компрессионной нейропатии, что расширяет понимание разнообразия этиологических факторов [26].
M. Jimenez описала случай 13-тилетнего пациента с прогрессирующим парезом малоберцового нерва, вызванным интраневральной ганглиозной кистой атипичной удлиненной формы, что затруднило своевременную диагностику и лечение [27]. B.R. Peters установил существование четырех клинических подтипов нейропатии общего малоберцового нерва, включая случаи с нормальными электродиагностическими показателями, что расширяет диагностический спектр заболевания и подчеркивает необходимость хирургической декомпрессии даже при отсутствии конвенциональных симптомов [28]. C. Strother проанализировала демографические характеристики и исходы хирургического лечения травматических повреждений малоберцового нерва, подчеркнув важность правильного консультирования пациентов относительно сложности лечения и вариабельности результатов [29].
Патофизиологические механизмы развития синдрома висящей стопы представляют собой сложный каскад структурных и функциональных нарушений нервной проводимости. C. Oosterbos продемонстрировал в рандомизированном контролируемом исследовании FOOTDROP эффективность хирургической декомпрессии малоберцового нерва по сравнению с консервативной терапией при длительном наблюдении пациентов в течение восемнадцати месяцев [30]. П.К. Мирошникова установила перспективность применения мезенхимальных стволовых клеток для стимуляции регенеративных процессов в поврежденных нервных волокнах при экспериментальном моделировании нейропатии, что открывает перспективы медикаментозной поддержки хирургического лечения [31].
Мультидисциплинарный подход с участием невролога, нейрохирурга и специалиста по реабилитации обеспечивает комплексную оценку и разработку индивидуального плана лечения. Интраоперационная оценка жизнеспособности нервных волокон с использованием электростимуляции позволяет уточнить показания к невролизу во время операции, что представляет важное техническое нововведение. R. Mens и B. Haviv показали важность профилактических мероприятий при ятрогенных повреждениях нерва, что дополняет понимание этиологической структуры синдрома висящей стопы [32].
Необходимость комплексного подхода к послеоперационной реабилитации, включающего современные технологии биологической обратной связи и стабилометрического контроля, подтверждается различиями в восстановлении не только локальной функции голеностопного сустава, но и общих биомеханических показателей походки. Интеграция хирургического лечения с персонализированными реабилитационными программами представляет перспективное направление дальнейшего совершенствования результатов лечения пациентов с синдромом «висящей стопы». Дальнейшие исследования должны быть направлены на изучение возможностей минимально инвазивных техник сухожильной транспозиции и применения биологических факторов, стимулирующих процессы нейромышечной адаптации в послеоперационном периоде.
ЗАКЛЮЧЕНИЕ
Транспозиция задней большеберцовой мышцы демонстрирует статистически значимое и клинически существенное преимущество над тенодезом длинного разгибателя пальцев в восстановлении функции тыльного сгибания стопы при изолированной нейропатии малоберцового нерва длительностью более 12 месяцев. Фундаментальное различие в механизме действия, создание активной мышечной тяги при транспозиции против пассивной стабилизации при тенодезе обеспечивает более физиологичное восстановление двигательной функции.
Достижение силы тыльного сгибания до 78,9 % от контралатеральной конечности при транспозиции против 62,4 % при тенодезе подтверждает функциональное превосходство метода. Сопоставимая частота осложнений при значительном преимуществе в восстановлении двигательной функции обосновывает применение транспозиции задней большеберцовой мышцы в качестве метода выбора при данной патологии.
Сопоставимая частота осложнений между группами при лучших функциональных результатах транспозиции обосновывает ее применение в качестве метода выбора при изолированной нейропатии малоберцового нерва с длительной денервацией. Транзиторная слабость подошвенного сгибания после транспозиции, регрессирующая в процессе нейромышечной адаптации, не должна рассматриваться как препятствие к выполнению операции, учитывая значительное превосходство метода в восстановлении тыльного сгибания. Напротив, недостаточная коррекция при тенодезе представляет более серьезную проблему, требующую ревизионных вмешательств и связанную с техническими сложностями определения оптимального натяжения сухожилия.
Полученные данные позволяют рекомендовать транспозицию задней большеберцовой мышцы в качестве предпочтительной хирургической методики для пациентов с изолированной нейропатией малоберцового нерва при длительности денервации более двенадцати месяцев и отсутствии эффекта от консервативной терапии или нейрореконструктивных вмешательств. Тенодез длинного разгибателя пальцев может рассматриваться как альтернативная методика при наличии противопоказаний к транспозиции или технических ограничений, однако пациенты должны быть информированы о меньшей эффективности этого метода в восстановлении силы и амплитуды тыльного сгибания.
СПИСОК ИСТОЧНИКОВ
Febriana A, Subawa IW, Aryana IGNW, Sanjaya E. Revolutionizing Recovery: Tendon Transfer (Bridle Procedure) for Foot Drop in Traumatic Peroneal Nerve Injuries - A Case Series. IJRR. 2025;12(5):62-68. doi: 10.52403/ijrr.20250508.
Eisenstein N, Fischer B, Nayagam S. Tibialis Posterior Tendon Transfer for the Management of Foot Drop. Strategies Trauma Limb Reconstr. 2023;18(1):56-62. doi: 10.5005/jp-journals-10080-1583.
Мацакян А.М., Ширмазанян А.Г., Горохводацкий А.В. Операции на сухожилии задней большеберцовой мышцы при лечении статической плоско-вальгусной деформации. Вестник Смоленской государственной медицинской академии. 2017;16(4):168-177.
Medina A. Modified bridle tendon transfer procedure following a complete musculature loss of the anterior leg compartment: Case report and literature review. Trauma Case Rep. 2019;24:100262. doi: 10.1016/j.tcr.2019.100262.
Wareham LK, Liddelow SA, Temple S, et al. Solving neurodegeneration: common mechanisms and strategies for new treatments. MolNeurodegener. 2022;17(1):23. doi: 10.1186/s13024-022-00524-0.
Григорян А.А., Макинян Л.Г., Маннанов А.М. и др. Эффективность метода Bridle при хирургическом лечении пациентов с синдромом «висящей стопы», вызванным нейропатией малоберцового нерва. Гений ортопедии. 2025;31(6):737-743. doi: 10.18019/1028-4427-2025-31-6-737-743.
McCormick KL, Patel D, Chien BY, et al. Surgical Management of Foot Drop. Orthop Rev (Pavia). 2024;16:120047. doi: 10.52965/001c.120047.
Голубева Ю.Б., Андриевская А.О., Горелова И.К. и др. Ортопедическое обеспечение как инструмент медицинской реабилитации пациентов с синдромом отвисающей стопы. Журнал неврологии и психиатрии им. С.С. Корсакова. 2020;120(10):91-99. doi: 10.17116/jnevro202012010191.
Chen G, Ma L, Song R, et al. Speed-adaptive control of functional electrical stimulation for dropfoot correction. J Neuroeng Rehabil. 2018;15(1):98. doi: 10.1186/s12984-018-0448-x.
Wiszomirska I, BJazkiewicz M, Kaczmarczyk K, et al. Effect of Drop Foot on Spatiotemporal, Kinematic, and Kinetic Parameters during Gait. ApplBionicsBiomech. 2017;2017:3595461. doi: 10.1155/2017/3595461.
Аксенова Е.И., Горбатов С.Ю., Маклакова Ю.А. Экспертный обзор: Индустрия реабилитационных технологий в России и мире. М.: ГБУ «НИООЗММ ДЗМ»; 2020:64.
Башлачев М.Г. Клиника, диагностика и хирургическое лечение компрессионной невропатии общего малоберцового нерва на уровне головки малоберцовой кости: дис.... канд. мед. наук. М.; 2022:126.
Сомова М.М., Доманский В.Л. Технология интраоперационного нейромониторинга методом полипрограммной электростимуляции при операциях реконструктивной нейропластики. Клиническая практика. 2019;10(4):46-52.
Новиков А.В., Антонова В.А. Невропатия малоберцового нерва как осложнение после тотального эндопротезирования коленного сустава: особенности реабилитации. Вестник травматологии и ортопедии им. Н.Н. Приорова. 2020;27(4):41-45. doi: 10.17816/vto57137.
Leclere FM, Badur N, Mathys L, Vogelin E. Neurotized lateral gastrocnemius muscle transfer for persistent traumatic peroneal nerve palsy: Surgical technique. Neurochirurgie. 2015;61(4):292-297. doi: 10.1016/j.neuchi.2014.08.001.
Pang Z, Zhu S, Shen YD, et al. Functional outcomes of different surgical treatments for common peroneal nerve injuries: a retrospective comparative study. BMCSurg. 2024;24(1):64. doi: 10.1186/s12893-024-02354-x.
Bao B, Wei H, Zhu H, Zheng X. Transfer of Soleus Muscular Branch of Tibial Nerve to Deep Fibular Nerve to Repair Foot Drop After Common Peroneal Nerve Injury: A Retrospective Study. Front Neurol. 2022;13:745746.
Никитин С.С., Муртазина А.Ф., Дружинин Д.С. Блок проведения возбуждения по периферическому нерву как электрофизиологический феномен: обзор литературы. Нервно-мышечные болезни. 2019;9(1):12-23. doi: 10.17650/2222-8721-2019-9-1-12-23.
Фоминых А.А., Котов Н.Б., Бессарабова А.О. и др. Компрессионная нейропатия малоберцового нерва в фибулярном канале. Вопросы реконструктивной и пластической хирургии. 2022;25(4):44-52. doi: 10.52581/1814-1471/83/05.
Власов А.П., Лазарев М.П., Кисель Д.А. и др. Наш опыт сухожильно-мышечных транспозиций при лечении застарелых повреждений малоберцового нерва. Инновации в травматологии, ортопедии и реабилитологии: сборник научных трудов Международной научно-практической конференции. Чита: РИЦ ЧгМА; 2024:31-33.
Liu Z, Yushan M, Liu Y, Yusufu A. Prognostic factors in patients who underwent surgery for common peroneal nerve injury: a nest case-control study. BMC Surg. 2021;21(1):11. doi: 10.1186/s12893-020-01033-x.
Lezak B, Massel DH, Varacallo MA. Peroneal Nerve Injury. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025.
Bojovic M, Dimitrijevic S, Olory BCR, et al. Overview of nerve entrapment syndromes in the foot and ankle. Int Orthop. 2025;49(4):853- 862. doi: 10.1007/s00264-025-06469-5.
Fakih M, Alhojailan K, Volesky M. Knee intra-articular loose body causing a compression common peroneal nerve neuropathy with foot drop. BMJ Case Rep. 2025;18(1):e262880. doi: 10.1136/bcr-2024-262880.
Yadav U, Nemani M, Devgun A, et al. Iatrogenic Foot Drop After Anterior Cruciate Ligament Reconstruction With Peroneus Longus Tendon Autograft: Report of a Rare Case. Cureus. 2022;14(6):e26476. doi: 10.7759/cureus.26476.
Lale A, Kirkil C, Ozturk S, et al. The results of surgical decompression in the treatment of foot drop due to peroneal nerve entrapment after bariatric surgery. SurgObesRelatDis. 2020;16(11):1684-1691. doi: 10.1016/j.soard.2020.06.054.
Jimenez Siebert M, Kaiser N, Ziebarth K. Complete foot drop due to atypical peroneal ganglion in a 13 year old boy. Neurochirurgie. 2025;71(1):101606. doi: 10.1016/j.neuchi.2024.101606.
Peters BR, Pripotnev S, Chi D, Mackinnon SE. Complete Foot Drop With Normal Electrodiagnostic Studies: Sunderland "Zero" Ischemic Conduction Block of the Common Peroneal Nerve. Ann Plast Surg. 2022;88(4):425-428. doi: 10.1097/SAP.0000000000003053.
Carlson Strother C, Dittman LE, Spinner RJ, et al. Surgical management of peroneal nerve injuries. Acta Neurochir (Wien). 2023;165(9):2573-2580. doi: 10.1007/s00701-023-05727-y.
Oosterbos C, Rummens S, Bogaerts K, et al. Conservative versus surgical treatment of foot drop in peroneal nerve entrapment: rationale and design of a prospective, multi-centre, randomized parallel-group controlled trial. Trials. 2022;23(1):1065. doi: 10.1186/ s13063-022-07009-x.
Мирошникова П.К., Лындуп А.В., Бацаленко Н.П. и др. Перспективные нервные кондуиты для стимуляции регенерации поврежденных периферических нервов. Вестник РАМН. 2018;73(6):388-400. doi: 10.15690/vramn1063.
Mens R, van Houten A, Brokelman RBG, Hoogeslag R. Iatrogenic common peroneal nerve injury during harvesting of semitendinosus tendon for anterior cruciate ligament reconstruction. BMJ Case Rep. 2021;14(4):e240736. doi: 10.1136/bcr-2020-240736.
Информация об авторах:
Арцрун Андраникович Григорян — аспирант
Вессам Мусса Абу Заалан — аспирант, врач — травматолог-ортопед
Левон Гагикович Макинян — кандидат медицинских наук, доцент кафедры, заведующий отделением
Альберт Маратович Маннанов — кандидат медицинских наук, врач — травматолог-ортопед
Чынгис Молдамырзаев — аспирант
Михаил Александрович Иманкулов — аспирант
Теги: синдром висящей стопы
234567 Начало активности (дата): 23.04.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: синдром висящей стопы, нейропатия малоберцового нерва, транспозиция задней большеберцовой мышцы, тенодез длинного разгибателя пальцев
12354567899
Похожие статьи
Эффективность метода Bridle при хирургическом лечении пациентов с синдромом «висящей стопы», вызванным нейропатией малоберцового нерваРентген на дому 8 495 22 555 6 8
Гистопатология тканей кистевого сустава и некоторые клинико-морфологические корреляции у больных с последствиями переломов ладьевидной кости
Перелом голеностопного сустава (голеностопа)
«Гонорейная» стопа



