 04.04.2026
04.04.2026
Особенности лучевой диагностики COVID-ассоциированного мукормикоза околоносовых пазух: проспективное исследование
Мукормикоз — тяжело протекающая инфекция, преимущественно развивающаяся у иммунокомпрометированных пациентов.
Введение.
Мукормикоз является тяжелым инфекционным заболеванием, вызванным грибами семейства Mucorales. Эти микромицеты широко распространены в природе. Они встречаются в почве, на различных поверхностях, в том числе на продуктах питания. Возбудителями мукормикоза преимущественно являются представители Rhizopus spp. (46%), Rhizomucor spp. (18%), Lichtheimia spp. (14%) и Mucor spp. (12%) [1–6]. Развивается мукормикоз преимущественно у иммунокомпрометированных пациентов. Основными фоновыми заболеваниями и состояниями для развития мукормикоза являются: аллогенная трансплантация гемопоэтических клеток и реакция «трансплантат против хозяина»; длительное применение глюкокортикостероидов (ГКС) или других иммуносупрессивных препаратов; агранулоцитоз 10 дней и более, лимфоцитопения 14 дней и более, первичные иммунодефициты и декомпенсированный сахарный диабет. Пациенты с COVID-19 тоже вошли в эту группу риска, не только в результате воздействия вируса на человека, но и активного применения ГКС, создавая ятрогенную иммуносупрессию, помимо имеющейся вирусной нагрузки [1–3]. Эти пациенты стали основной группой риска развития рино-орбитоцеребрального мукормикоза.Высокую распространенность мукормикоза околоносовых пазух (ОНП) во время пандемии COVID19 наблюдали в Индии , Иране, Египте, Турции , а также значительное увеличение количества случаев произошло в странах Европы, например, в Германии [9] и Нидерландах [10].
В России количество COVID-ассоциированного рино-орбито-церебрального мукормикоза у пациентов только за 2021 г. увеличилось на 29% [3]. В период с января 2021 по декабрь 2021 г. в регистр с тяжелыми грибковыми инфекциями, вызванными редкими возбудителями, на базе кафедры клинической микологии, аллергологии и иммунологии ФГБОУ ВО СЗГМУ им. И. И. Мечникова Минздрава России проспективно включили 60 взрослых пациентов с COVID-M [3, 4]. Заболевание наблюдали во многих регионах страны, в том числе в Воронежской, Липецкой, Пензенской [11] в Пермском [12, 13] и Красно - дарском краях [14, 15].
Ведущим лучевым методом диагностики является мультиспиральная компьютерная томография.
Согласно международным данным, наиболее патогномоничным симптомом является остеодеструкция. Более ранние признаки микотической инфекции включают гиперплазию тканей разной степени .
Особенности диагностики мукормикоза ОНП у пациентов с COVID-М в Российской Федерации изучены недостаточно. В связи с этим целью нашего исследования было выявить наиболее патогномоничные КТ-симптомы для ранней диагностики заболевания. Цель. Проанализировать результаты МСКТ околоносовых пазух и МРТ головного мозга у пациентов с COVID-ассоциированным рино-орбитоцеребральным мукормикозом для повышения эффективности ранней диагностики заболевания, уменьшения летальности и инвалидизации пациентов. Представить рентгенологические признаки рино-орбито-церебрального мукормикоза.
Для достижения цели были поставлены следующие задачи:
1) сформировать регистр пациентов с COVIDассоциированным рино-орбито-церебральным мукормикозом;
2) проанализировать данные МСКТ околоносовых пазух на разных этапах микотического поражения;
3) оценить результаты лечения мукормикоза ОНП с помощью компьютерно-томографического мониторинга.
Материалы и методы.
Исследование одобрено Локальным этическим комитетом ФГБОУ ВО СЗГМУ им. И. И. Мечникова Минздрава России, протокол от 03.11.2021 г. № 10, 01.03.2023 № 3. Информированное согласие получено от каждого пациента. На базе кафедры клинической микологии, аллергологии и иммунологии ФГБОУ ВО СЗГМУ им. И. И. Мечникова Минздрава России создан регистр пациентов с мукормикозом, в который включены более 100 пациентов с COVID-M1.
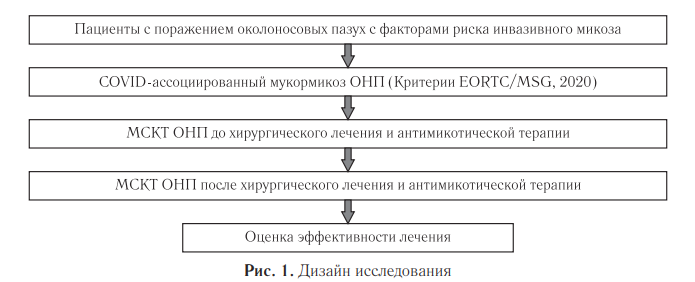
Для постановки диагноза инвазивного микоза использовали критерии Европейской организации по исследованию и лечению рака (EORTС) и группы, исследующей микозы MSGERC (США), 2020 [2]. Основным методом лучевой диагностики для постановки диагноза являлась мультиспиральная компьютерная томография. МСКТ околоносовых пазух проводили всем пациентам, применяли томографы GE Revolution HD, Philips Ingenuity Core 64, CTGE Bright Speed 16, Aquilion PRIME 1. Для просмотра КТ-изображений использовали программу Weasis v 4.5.0. В процессе изучения применен метод научного исследования путем разложения предмета исследования (КТ-семиотика) риноорбито-церебрального мукормикоза. Оценивали изменения слизистых оболочек, костных стенок ОНП, костей черепа, поражения структур лицевой области, орбиты и головного мозга. Статистический анализ данных выполняли с использованием пакета программ Microsoft Office Excel 2019. Анализ выживаемости проводили методом Каплана–Майера.
Авторы провели анализ публикаций, посвященных проблеме мукормикоза ОНП у пациентов, перенесших COVID-19. Использовали поисковые базы PubMed (на декабрь 2024), ScienceDirect (на декабрь 2024) и е-library (на декабрь 2024). При поиске информации использовали следующие ключевые слова: мукормикоз, околоносовые пазухи, мультиспиральная компьютерная томография, COVID-19. В статье также представлен клинический случай распространенного микотического риносинусита с вовлечением тканей орбиты.
Результаты.
В исследование включили 41 пациента с рино-орбито-церебральным мукормикозом. Все пациенты были взрослыми в возрасте от 22 до 83 лет, медиана возраста составила 61±2,34 года. Из них мужчин — 56%, женщин — 44%. Основными фоноПоражение стенок верхнечелюстных пазух выявлено у 100% пациентов, стенок и ячеек решетчатой кости — 93%, стенок лобной пазухи — 37%, стенок основной пазухи и клиновидной кости — 83%, стенок орбит — 95%, верхней челюсти — 85%, нижней челюсти — 5% (табл. 2), отек, утолщение мягких тканей лица, орбиты и ЦНС — 93%, эмфизема мягких тканей лица, орбиты и головного мозга — 73% (см. табл. 1), поражение зрительного нерва — 66%, поражение лобной доли — 32%, поражение височной доли — 15%, поражение затылочной доли — 2%, тромбоз кавернозного синуса — 46%, внутренней сонной артерии — 5% (табл. 3).

Объективно изменения параорбитальной области наблюдали у 71% пациентов (экзофтальм, офтальмоплегии, птоз верхнего века, хемоз и др.), в том числе снижения зрения — 46%, вплоть до полной слепоты — 20%.
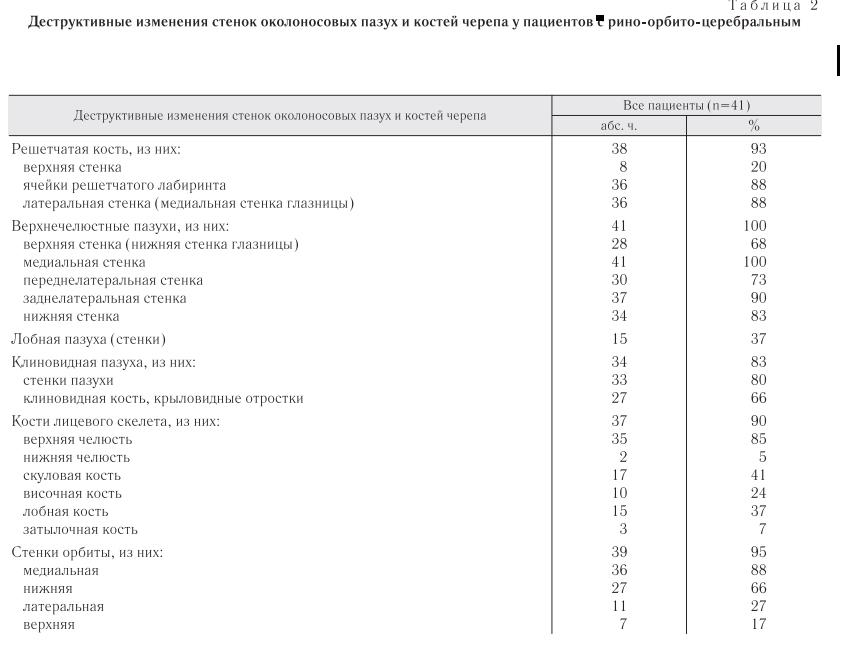
Поражение околоносовых пазух чаще было одностороннее — у 54%, двустороннее — 46%. В основном выявляли поражение верхнечелюстных пазух (100%) и решетчатой кости (93%) с распространением в орбиту — 95%, верхнюю челюсть — 85% (см. табл. 2), с изменениями воспалительного характера мягких тканей — 93%, реже головного мозга — 37%. Неврологическая симптоматика связана была с поражением лобных долей — 32%, височных долей — 15%, тромбозами кавернозного синуса — 46% (см. табл. 3).

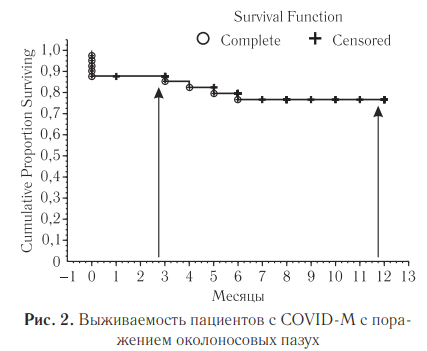
Антимикотическую терапию получали 95% всех пациентов. Проведенный анализ показал, что чаще всего для лечения мукормикоза околоносовых пазух использовали липосомальный амфотерицин B (46%), позаконазол (33%) и изавуконазол (22%). Комбинированную терапию применяли в 46% случаев. Средняя продолжительность антимикотической терапии была 55,1 дня. Хирургическое лечение с удалением очагов остеомиелита и пораженных участков мягких тканей проводилось у 98% пациентов. Общая выживаемость пациентов с COVID-M после проведения хирургического лечения и антимикотической терапии в течение 3 месяцев составила 88% и в течение 1 года — 78% (рис. 2).
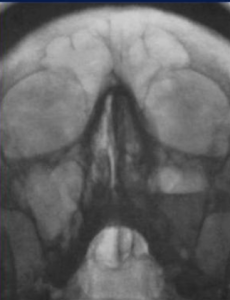
Пациент У., 1949 г.р., госпитализирован 09.2021 с жалобами на онемение левой половины лица, отек левого глаза, затруднение глотания твердой пищи, асимметрию лица. Из анамнеза известно, что заболевание началось 08.2021 с повышения температуры тела более 38°С, появились боль в горле, кашель, головокружение, отсутствие аппетита, снизилось обоняние. Пациент самостоятельно принимал парацетамол без улучшения состояния. 29.08.2021 потерял сознание, госпитализирован в областную больницу. Выполнено МСКТ головного мозга — данных, свидетельствующих об остром нарушении мозгового кровообращения (ОНМК), не получено. На МСКТ органов грудной клетки выявлена двусторонняя полисегментарная пневмония, выраженность изменений соответствует КТ-2. Диагностирована новая коронавирусная инфекция COVID-19, подтвержденная ПЦР. Проводили противовирусную терапию, вводили ГКС, антибиотики, антикоагулянты. Состояние ухудшилось через неделю, когда пациент стал отмечать онемение левой половины лица, отек в области левого глаза, асимметрию лица, затруднение приема пищи. Переведен в районную клиническую больницу, где на МСКТ головного мозга ОНМК вновь не подтвердилось, выявили двусторонний гайморит, флегмону левой орбиты и остеомиелит верхней челюсти слева. При осмотре оториноларингологом периостит верхней челюсти слева, при осмотре офтальмологом флегмона левой орбиты. Провели дренирование ретробульбарного пространства слева, конъюнктивотомию на 10-е сутки госпитализации. В анализах крови: нейтро- и лимфоцитопении не выявляли, повышение уровня глюкозы до 7,8 ммоль/л. Диагностирован сахарный диабет 2-го типа. На контрольной МСКТ ОНП выявили деструкцию и истончение медиальной стенки левой орбиты, ячеек решетчатого лабиринта, деструкцию боковой стенки клиновидной пазухи и клиновидной кости слева, утолщение и отек мягких тканей левой орбиты с пузырьками воздуха (рис. 3).
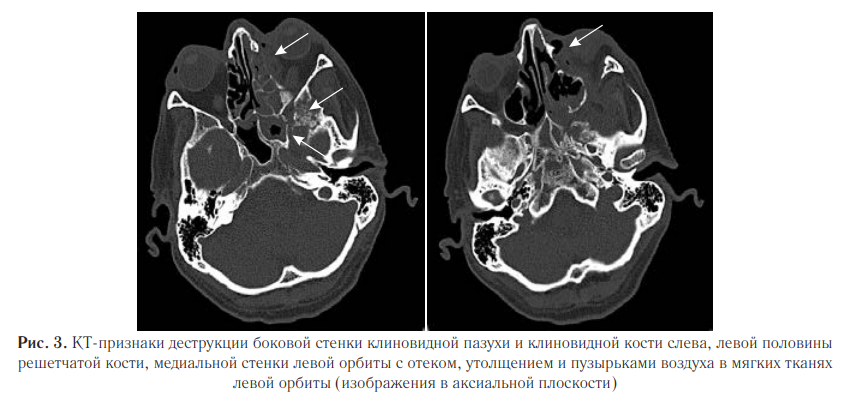
В левой верхнечелюстной пазухе наблюдали деструкцию и истончение переднелатеральной стенки, а также отек и утолщение мягких тканей лицевой области слева с пузырьками воздуха (рис. 4).
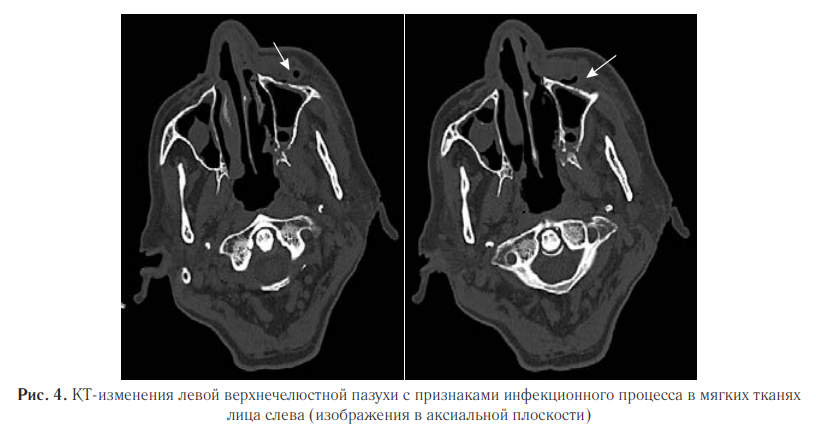
Деструктивные изменения были обнаружены и в левой скуловой кости (рис. 5).
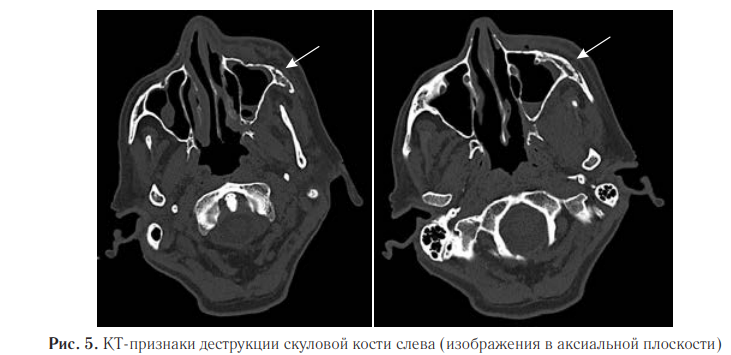
На реконструкции КТ-изображений в коронарной и сагиттальной плоскостях выявили деструкцию и истончение медиальной, нижней стенок левой орбиты, задней стенки левой верхнечелюстной пазухи, боковой и нижней стенки основной пазухи слева (рис. 6).
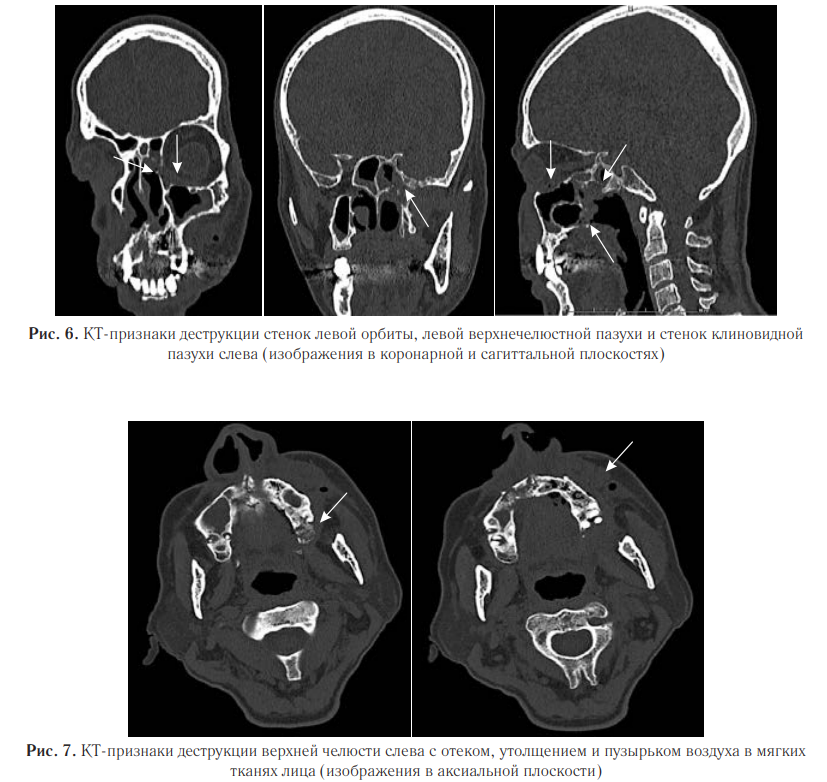
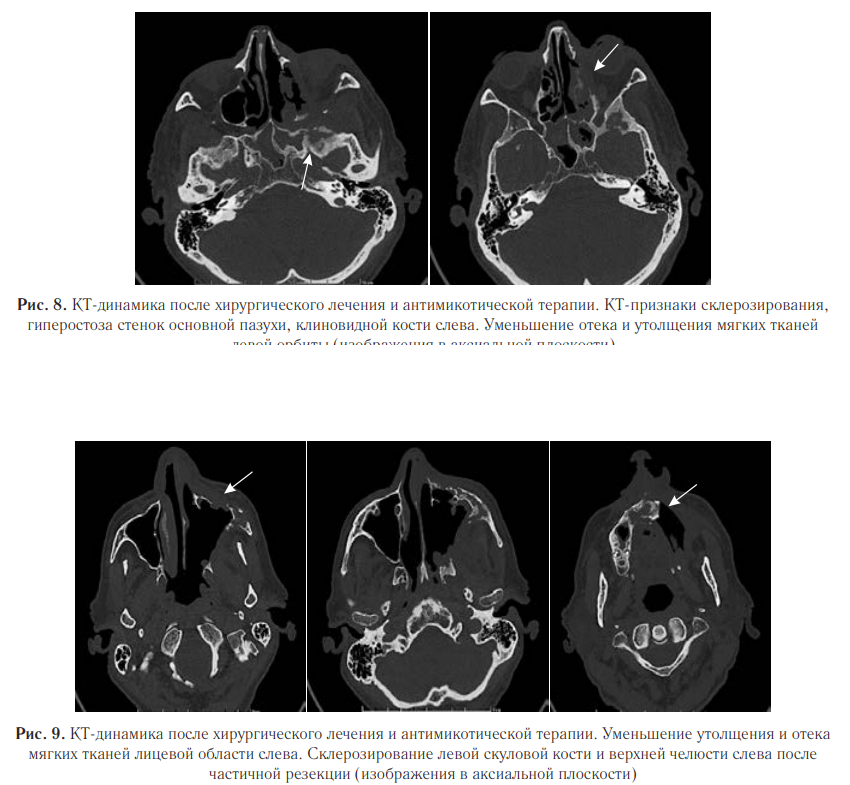
Также были выявлены деструктивные изменения верхней челюсти с утолщением и эмфиземой мягких тканей лицевой области слева (рис. 7). Пациент был переведен в специализированное отделение. Проведена секвестрэктомия верхней челюсти, удаление зубов слева. В гистологических препаратах послеоперационного материала выявлены нити мицелия. При пересмотре гистологического материала в НИИ Медицинской микологии им. П. Н. Кашкина, был обнаружен широкий несептированный мицелий, характерный для мукоромицетов. На основании клинической картины, данных КТ и микологического обследования был диагностирован COVID-ассоциированный мукормикоз околоносовых пазух и структур орбиты. Назначили антимикотическую терапию: введение липосомального амфотерицина В 10 мг/кг в сутки, после стабилизации состояния переход на пероральную терапию. По месту ведения пациента была начата антимикотическая терапия липидным амфотерицином В 14 дней, далее амфотерицином В дезоксихолатом, который был отменен ввиду нефротоксичности. В последующем лечение продолжили изавуконазолом в стандартной дозе. Согласно международным рекомендациям, проводился контроль уровня глюкозы крови и произведена отмена ГКС. Общая продолжительность лечения составила 105 дней. Ежедневно в первую неделю, затем по мере необходимости проводили осмотр области оперативного вмешательства с местной обработкой слизистых оболочек препаратами амфотерицина В. После проведенной антимикотической терапии на контрольных МСКТ ОНП выявили признаки стабилизации мукормикоза в виде отсутствия прогрессирования процесса; склерозирования, утолщения и гиперостоза костей; уменьшения отека и утолщения мягких тканей с их фиброзированием (рис. 8, 9).
Обсуждение.
Мукормикоз — тяжелое заболевание с высокой летальностью. Инфицирование человека происходит в основном путем вдыхания спор грибов семейства Mucorales и колонизации слизистой оболочки полости носа. В норме у иммунокомпетентных людей развитие заболевания не происходит [16]. Основными фоновыми заболеваниями при мукормикозе на сегодня остаются COVID-19 (46%) и онкогематологическая патология (37%) [1–3, 17]. При анализе факторов риска развития рино-орбитоцеребрального мукормикоза основное значение имеет наличие сопутствующего сахарного диабета (88%), а также длительный прием ГКС в высоких дозах (90%) [3], что сходно с аналогичными зарубежными данными [5, 6, 18]. Так, M. I. Metwally отмечали сахарный диабет у 81% и прием в анамнезе ГКС у 83% пациентов с COVID-M [18]. Считают, что у этих пациентов в основе инфекционного процесса лежит инвазия грибов в костную ткань, а также некротизирующий васкулит и тромбозы сосудов [17, 19]. В дальнейшем распространение инфекции на близлежащие ткани происходит предположительно по периваскулярным каналам [18, 19]. Согласно полученным нами данным, деструктивные процессы проявляются в течение 8–16 дней от момента первых клинических проявлений мукормикоза. Опубликованные исследования зарубежных авторов свидетельствуют, что задержка в лечении на неделю повышает смертность с 35% до 66% [18, 20]. Таким образом, при несвоевременной постановке диагноза COVID-M у пациентов происходит быстрое поражение жизненно важных структур (не только разрушение костных стенок ОНП) орбиты и головного мозга. В нашем исследовании показано, что основными клиническими симптомами у пациентов с COVID-M были локальный болевой синдром, отек мягких тканей лица и глаза, парестезии, онемение лица, нарушение зрения [7, 18]. В полости носа во всех случаях наблюдалась гипертрофия слизистых оболочек, во многих случаях с образованием некротических масс и «черных корок». Согласно международным данным, патогномоничным признаком COVID-M было образование «черного струпа» 48–81% [7, 18]. Характерными КТ-признаками рино-орбито-церебрального мукормикоза по полученным нами данным, помимо деструктивных процессов, являются обнаруженные на компьютерных томограммах отек, утолщение мягких тканей лица, орбиты и ЦНС (93%).
Очень важным диагностическим КТ- и МРТ-признаком риноорбито-церебрального мукормикоза является наличие эмфиземы мягких тканей лица, орбиты и/или головного мозга (73%). Одним из маркеров лучевых методов исследования COVID-M можно считать тромбоз кавернозного синуса, внутренней сонной артерии и других сосудов (56%). По данным иностранных авторов, основными лучевыми признаками были гипертрофии слизистых оболочек околоносовых пазух, отек и утолщение мягких тканей лица, деструктивные изменения костей черепа, поражение структур орбиты и головного мозга [2, 7, 18, 21].
Авторы G. Slonimsky, J. D. McGinn, N. Goyal показали, что мукормикоз ОНП протекает агрессивнее, чем другие инвазивные микотические синуситы [17, 22]. В их исследовании обнаружилось, что рино-орбито-церебральный мукормикоз имеет чаще двустороннее поражение, а также более частое распространение на мягкие ткани лица и параорбитальную клетчатку в сравнении с синуситами, вызванными грибами семейства Aspergillus.
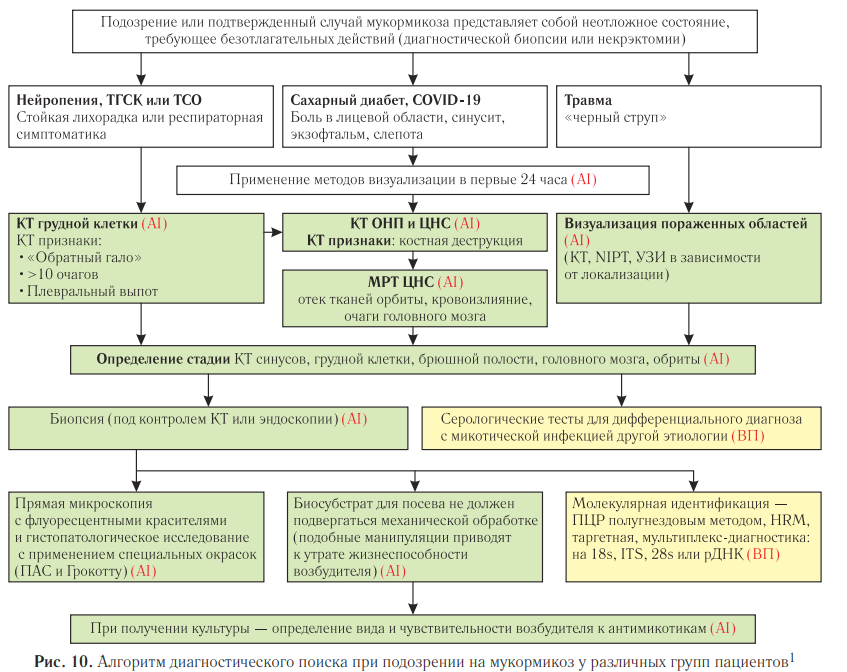
Современные клинические рекомендации предлагают обязательное исследование с помощью МСКТ зоны поражения инфекцией для постановки диагноза и оценки степени распространенности микотического процесса [2, 22]. На рис. 10 представлен алгоритм лучевого обследования у различных групп пациентов с подозрением на мукормикоз.
Заключение.
Лучевые исследования являются ведущими методами визуализации при рино-орбитоцеребральном мукормикозе. Протокол исследования обязательно должен включать МСКТ околоносовых пазух и МРТ головного мозга.
В лучевой диагностике мукормикоза околоносовых пазух важна оценка объема поражения различных структур. МСКТ околоносовых пазух необходима для оценки степени распространенности в первую очередь деструктивных изменений костей черепа, МРТ головного мозга — для более точной оценки распространенности поражения мягких тканей лица, интраорбитальных и интракраниальных изменений, выявлении тромбозов кавернозного синуса и др. сосудов головного мозга. Проведение ранней лучевой диагностики у больных с рино-орбито-церебральным мукормикозом позволяет сохранить жизнь пациентов. Выводы. 1. Для COVID-M характерна ранняя деструкция (медиана 12±4,26 дня) стенок околоносовых пазух, быстрое распространение деструктивного процесса в течение 7–12 дней. 2. Наиболее часто визуализируют деструкцию стенок верхнечелюстных пазух (100%), стенок орбиты (95%), решетчатой кости (93%), стенок основной пазухи (83%). 3. Поражение мягких тканей лица, орбиты наблюдают у 93%, ЦНС — у 37%, тромбоз кавернозного синуса — у 46%, эмфизему мягких тканей лица, орбиты — у 73% пациентов. Перспективы дальнейшей разработки темы. В настоящее время исследование продолжается, необходимо проанализировать результаты лучевых методов исследования групп сравнения: пациентов с классическим синуситом и пациентов с аспергиллезными синуситами.
Сведения об авторах:
Вагин Александр Викторович — врач-рентгенолог рентгенкабинета микологической клиники при рентгеновском отделении федерального государственного бюджетного образовательного учреждения высшего образования «Северо-Западный государственный медицинский университет имени И. И. Мечникова» Министерства здравоохранения Российской Федерации; 194291, Санкт-Петербург, ул. Сантьяго-де-Куба, д. 1/28 (НИИ медицинской микологии им. П. Н. Кашкина)
Хостелиди Софья Николаевна — доктор медицинских наук, профессор, доцент кафедры клинической микологии, аллергологии и иммунологии федерального государственного бюджетного образовательного учреждения высшего образования «Северо-Западный государственный медицинский университет имени И. И. Мечникова» Министерства здравоохранения Российской Федерации; 194291, Санкт-Петербург, ул. Сантьяго-де-Куба, д. 1/28 (НИИ медицинской микологии им. П. Н. Кашкина)
Топольскова Наталья Викторовна — кандидат медицинских наук, главный врач Медицинского центра «Приоритет диагностика» КТ и МРТ; 197350, СанктПетербург, ул. Шаврова, д. 26, стр. 1
Чарушин Артем Олегович — кандидат медицинских наук, доцент кафедры оториноларингологии, врач-оториноларинголог федерального государственного бюджетного образовательного учреждения высшего образования «Пермский государственный медицинский университет имени академика Е. А. Вагнера» Министерства здравоохранения Российской Федерации; государственное бюджетное учреждение здравоохранения Пермского края «Пермская краевая клиническая больница»; 614000, г. Пермь, Петропавловская ул., д. 26
Вартанян Сейран Ашотович — заведующий отделением челюстно-лицевой хирургии государственного бюджетного учреждения здравоохранения «Краевая клиническая больница скорой медицинской помощи» Министерства здравоохранения Краснодарского края; 350042, г. Краснодар, ул. 40 Лет Победы, д. 14
Васильева Наталья Всеволодовна — доктор биологических наук, профессор, заведующий кафедрой медицинской микробиологии федерального государственного бюджетного образовательного учреждения высшего образования «Северо-Западный государственный медицинский университет имени И. И. Мечникова» Министерства здравоохранения Российской Федерации; директор НИИ медицинской микологии имени П. Н. Кашкина; 194291, Санкт-Петербург, ул. Сантьягоде-Куба, д. 1/28
ЛИТЕРАТУРА
1. Хостелиди С.Н. Мукормикоз у взрослых на фоне COVID-19 (результаты проспективного исследования) // Журнал инфектологии. 2023. Т. 15, № 1 S1. С. 179–180 [Khostelidi S.N. Mucormycosis in adults with COVID-19 (results of a prospective study). J. Infectol., 2023, Vol. 15, No. 1 S1, pp. 179–180 (In Russ.)].
2. Cornely O.A., Alastruey-Izquierdo A., Arenz D. et al. Global guideline for the diagnosis and management of mucormycosis: an initiative of the European Confederation of Medical Mycology in cooperation with the Mycoses Study Group Education and Research Consortium. Mucormycosis ECMM MSG Global Guideline Writing Group // Lancet Infect. Dis. 2019. Vol. 19, No. 12. P. 405–421
3. Хостелиди С.Н., Зайцев В.А., Вартанян С.А. и др. Мукормикоз у больных COVID-19 в России: результаты проспективного многоцентрового исследования // Журнал инфектологии. 2022. Т. 14, № 2. С. 116–127 [Khostelidi S.N., Zaitsev V.A., Vartanyan S.A. et al. Mucoromycosis in patients with COVID-19 in Russia: results of a prospective multi-center study. Journal of Infectology, 2022, Vol. 14, No. 2, рр. 116–127 (In Russ.)]. http://doi.org/10.22625/2072-6732-2022-14-2-116-127.
4. Voruz F., Neofytos D., Van Delden C., Lobrinus J., De Vito C., Macario S., Daskalou D., Hsieh J.W., Becker M., Landis B.N. The Importance of MRI in the Early Diagnosis of Acute Invasive Fungal Rhinosinusitis // Diagnostics (Basel). 2025. Jan 28; Vol. 15, No. 3. Р. 311. doi: 10.3390/diagnostics15030311.
5. Jeong W., Keighley C., Wolfe R. et al. The epidemiology and clinical manifestations of mucormycosis: a systematic review and meta-analysis of case reports // Clin. Microbiol. Infect. 2019. Vol. 25, No. 1. P. 26–34.
6. Laşin Öz., Umur T., Mehtap M. et al. COVID-19-associated mucormycosis: a systematic review and meta-analysis of 958 cases // Clin. Microbiol. Infection. 2023. Vol. 29, No. 6. P. 722–731.
7. Chakravarty S., Nagarkar N.M., Mehta R. et al. Skull Base Involvement in Covid Associated Rhino-Orbital-Cerebral Mucormycosis: A Comprehensive Analysis // Ind. J. Otolaryngol. Head Neck Surg. 2023. Vol. 75, No. 3. P. 1–13.
8. Prakash H., Chakrabarti A. Global Epidemiology of Mucormycosis // J. Fungi (Basel). 2019. Vol. 5, No. 1. P. 6.
9. Seidel D., Sprute R., Cornely O.A. et al. Results from a national survey on COVID-19-associated mucormycosis in Germany: 13 patients from six tertiary hospitals // Mycoses. 2022. Vol. 65, No. 1. P. 103–109.
10. Buil J.B., G. Melchers W.J., Verweij P.E. et al. Case series of four secondary mucormycosis infections in COVID-19 patients, the Netherlands, December 2020 to May 2021 // Eurosurveillance. 2021. Vol. 26, No. 23. P. 1–4.
11. Неровный А.И., Панченко И.Г., Моренко М.В. и др. Мукормикоз у пациентов с COVID-19 // Российская оториноларингология. 2023. Т. 22, № 3 (124). С. 8–14 [Nerovny A.I., Panchenko I.G., Morenko M.V. et al. Mucormycosis in patients with COVID-19. Russian otorhinolaryngology, 2023, Vol. 22, No. 3 (124), pp. 8–14 (In Russ.)]
12. Чарушин А.О., Хостелиди С.Н., Боровинский Р.И. и др. Первое описание клинического случая мукормикоза околоносовых пазух в Пермском крае // Проблемы медицинской микологии. 2022. Т. 24, № 1. С. 19–24 [Charushin A.O., Khostelidi S.N., Borovinsky R.I. et al. The first clinical case of invasive mucormicosis of the paranasal sins in the Perm region. Problems of medical mycology, 2022, Vol. 24, No. 1, pp. 19–24 (In Russ.)]
13. Чарушин А.О., Хостелиди С.Н., Боровинский Р.И. и др. Случай успешного лечения риноорбитального мукормикоза у больной COVID-19 в Пермском крае // Проблемы медицинской микологии. 2022. Т. 24, № 3. С. 13–19 [Charushin A.O., Khostelidi S.N., Borovinsky R.I. et al. The case of successful treatment of rhinoorbital mucormycosis in a COVID-19 patient in the Perm Region. Problems of medical mycology, 2022, Vol. 24, No. 3, pp. 13–19 (In Russ.)].
14. Элизбарян И.С., Лазарева Л.А., Семенов Ф.В. и др. Мукормикоз риноорбитальной локализации у пациентов с постковидным синдромом. Клинико-морфологические особенности // Российская ринология. 2023. Т. 31, № 1. С. 66–75 [Elizbaryan I.S., Lazareva L.A., Semenov F.V. et al. Rhinoorbital mucormycosis in patients with the post-COVID syndrome. Clinical and morphological features. Russian rhinology, 2023, Vol. 31, No. 1, pp. 66–75 (In Russ.)].
15. Савосин Ю.В., Шафранова С.К., гайворонская Т.В. и др. Риноцеребральная форма инвазивных микозов у пациентов, перенесших новую коронавирусную инфекцию COVID-19: клиника, диагностика, опыт лечения. Проспективное неконтролируемое одномоментное исследование // Kубанский научный медицинский вестник. 2022. T. 29, № 5. C. 63–79 [Savosin Yu.V., Shafranova S.K., Gaivoronskaya T.V. et al. Rhinocerebral form of invasive mycosis in covid-19 patients: clinical course, diagnosis, treatment experience. prospective uncontrolled cross-sectional trial. Kuban Scientific Medical Bulletin, 2022, Vol. 29, No. 5, pp. 63–79 (In Russ.)].
16. Honavar S.G. Code Mucor: Guidelines for the Diagnosis, Staging and Management of Rhino-Orbito-Cerebral Mucormycosis in the Setting of COVID-19 // Indian J. Ophthalmol. 2021. Vol. 69, No. 6. P. 1361–13655.
17. Slonimsky G., McGinn J.D., Goyal N. et al. A model for classification of invasive fungal rhinosinusitis by computed tomography // Sci. Rep. 2020. Vol. 10, No. 1. P. 12591.
18. Климко Н.Н. Инвазивный аспергиллез у гематологических и онкогематологических больных // Онкогематология. 2006. № 1–2. С. 97–107 [Klimko N.N. Invasive aspergillosis in hematological and oncohematological patients. Oncogematology, 2006, No. 1–2, pp. 97–107 (In Russ.)].
19. Glöckner A., Vehreschild J.J., Cornely O.A. Zygomycosis-current epidemiological aspects // Mycoses. 2007. Vol. 51, No. 2. P. 179.
20. Metwally M.I., Mobashir M., Sweed A.H. et al. Post COVID-19 Head and Neck Mucormycosis: MR Imaging Spectrum and Staging // Acad. Radiol. 2022. Vol. 29, No. 5. P. 674–684.
21. Маляревская М.В., Лукина О.В., Зубарева А.А. и др. Лучевая диагностика инвазивного мукормикоза полости носа, околоносовых пазух, костей черепа у пациентов, перенесших новую коронавирусную инфекцию (COVID-19): проспективное исследование // Лучевая диагностика и терапия. 2022. Т. 3, № 13. С. 28– 42 [Malyarevskaya M.V., Lukina O.V., Zubareva A.A. et al. Invasive mucormycosis of nasal cavity, paranasal sinuses, bones of the skull post COVID-19 patients: prospective study. Diagnostic radiology and radiotherapy, 2022, Vol. 3, No. 13, pp. 28–42 (In Russ.)]
22. Werthman-Ehrenreich A. Mucormycosis with orbital compartment syndrome in a patient with COVID-19 // Am. J. Emerg. Med. 2021. Vol. 42. P. 264.e5–264.e8.
Теги: околоносовые пазухи
234567 Начало активности (дата): 04.04.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: мукормикоз, околоносовые пазухи, мультиспиральная компьютерная томография, COVID-19, антимикотическая терапия, изавуконазол, позаконазол
12354567899
Похожие статьи
ОКОЛОНОСОВЫЕ ПАЗУХИРентген на дому 8 495 22 555 6 8
Клиновидные пазухи
Верхнечелюстные пазухи



