 10.10.2025
10.10.2025
Ревизионное эндопротезирование тазобедренного сустава - что нас ждет?
Интенсивное увеличение числа ревизионных операций с нарастанием числа случаев сложных ревизий, требующих использования сложных и дорогостоящих имплантатов, а также чрезвычайно быстрое увеличение числа случаев инфекционных ревизий свидетельствует о том, что проблемы ревизионного эндопротезирования очень скоро могут коснуться всех хирургов, выполняющих первичную замену ТБС, сначала через необходимость лечить инфекционные осложнения, а затем за счет постепенного накопления пула пациентов, нуждающихся в других вариантах ревизий, в том числе повторных
ВВЕДЕНИЕ
В современной ортопедической литературе публикации, основанные на данных регистров ар- тропластики, дают наиболее полное представление о трендах в использовании различных имплантатов и периоперационных технологий, а также их ближайшей и долгосрочной эффективности в разных группах пациентов [1, 2, 3, 4, 5, 6, 7]. Огромные накопленные массивы записей регистров позволяют оценивать выживаемость различных конструкций в зависимости от нескольких групп факторов одновременно, например тип фиксации компонентов эндопротеза, используемая пара трения и возраст пациентов1 или выживаемость конкретной модели бедренного компонента в сочетании с определенной моделью вертлужного компонента2. Анализ данных из базы регистра позволяет также планировать расходы системы здравоохранения на многие годы вперед и принимать организационные решения по маршрутизации пациентов и характеру специализированной помощи [8, 9].
Несмотря на многочисленные усилия по созданию национального регистра артропластики тазобедренного сустава (ТБС) в Российской Федерации как со стороны отдельных организаций, так и со стороны органов управления здравоохранением, в настоящий момент база регистрации всех случаев замены ТБС по-прежнему отсутствует. Имеются только локальные базы данных, которые не отражают в полной мере процессы, происходящие в регионах, учреждениях различной ведомственной принадлежности, и не позволяют даже оценить общее число выполняемых вмешательств, не говоря уже о причинах, потребовавших замены сустава, уровне осложнений и структуре ревизионных операций и их результатах [10, 11].
Основываясь на отдельных исследованиях [12] и учитывая общую тенденцию к увеличению числа операций, можно предполагать, что в настоящее время в стране выполняется не менее 100 тыс. операций по установке искусственного ТБС. При этом доля ревизионного эндопротезирования (ЭП) в целом составляет около 6% [12]. С одной стороны, это не более, чем в других странах, с другой стороны, это несколько тысяч операций в год, результаты которых будут существенно хуже, чем при первичном ЭП, и большая часть этих пациентов снова будет нуждаться в специализированной помощи [13, 14]. Ревизионная операция даже может быть угрозой для жизни — согласно статистике, умирает 1 из 145 пациентов, подвергшихся ревизии [15].
Кроме того, ревизионная нагрузка на различные центры ЭП существенно варьирует, что, вероятно, требует коррекции финансового обеспечения этих операций, поскольку международный опыт показывает необходимость периодического пересмотра тарифов. Иначе медицинские организации начинают «подстраиваться» под имеющиеся тарифы, используя неэффективные технологии, что увеличивает последующую нагрузку на систему здравоохранения [16].
В последние годы в области ЭП ТБС произошло множество организационных изменений — из разряда высокотехнологичных это вмешательство перешло в разряд массовых и погрузилось в систему ОМС, что предполагает возможность выполнения этих операций во всех медицинских организациях Российской Федерации, оказывающих специализированную травматолого-ортопедическую помощь. Разумеется, этот процесс имеет серьезное положительное влияние на повышение доступности специализированной помощи для граждан Российской Федерации. С другой стороны, широкое распространение первичного ЭП ТБС ведет к тому, что масса пациентов, которым требуется выполнение ревизионных вмешательств, будет нарастать, поскольку операции ревизионной ар- тропластики пока производятся не во всех медицинских организациях, и очередь на такие операции имеет тенденцию к увеличению. В то же время необходимость выполнения ревизионной операции во многих случаях носит значительно более яркий характер, чем при первичном ЭП, поскольку пациенты с такими проблемами, как инфекция, рецидивирующий вывих или перипротезный перелом, нуждаются в неотложной помощи, но вынуждены длительно ожидать госпитализации ввиду большого листа ожидания.
Отсутствие национального регистра ЭП ТБС в Российской Федерации затрудняет получение полноценной информации о распространенности операций по замене ТБС, их структуре и реальной эффективности как первичного, так и ревизионного ЭП, выполняемого в отечественных учреждениях здравоохранения. Соответственно, только отдельные публикации, основанные на значительном числе наблюдений, в том числе из локальных баз данных, позволяют получить приблизительную информацию о популяционных характеристиках отечественных пациентов и актуальных направлениях развития данного направления травматологии и ортопедии [10, 17, 18]. Последний анализ структуры ревизионных операций, сведения
МАТЕРИАЛ И МЕТОДЫ
Всего в очищенной базе локального регистра ЭП ТБС содержится информация о 90 427 случаях замены ТБС в период с 2007 по 2024 г., из которых 11 201 (12,4%) приходится на различные ревизионные вмешательства (рис. 1).
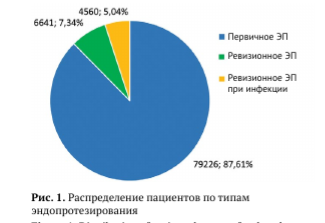
Выделялись следующие категории операций.
1. «Первичное ЭП ТБС» рассматривается в работе только в общем контексте.
2. «Ревизионное ЭП ТБС» включает несколько асептических причин для выполнения повторной операции:
- «асептическое расшатывание компонентов эндопротеза» — потеря фиксации одного или обоих компонентов;
- «вывихи» — рецидивирующие и невправи- мые вывихи, требующие хирургического вмешательства на искусственном суставе;
- «перипротезные переломы (ППП)» — переломы в области эндопротеза, требующие хирургического лечения;
- «износ полиэтиленового вкладыша/цемент- ной чашки и сопутствующий остеолиз»;
- «другие причины» включали в себя болевой синдром, мальпозицию компонентов, механическое повреждение компонентов эндопротеза, мышечную недостаточность и гетеротопические оссификаты.
3. «Ревизионное ЭП при инфекции» включает в себя несколько вариантов ревизионных вмешательств у пациентов, которым на различных этапах был установлен диагноз перипротезной инфекции (ППИ) в соответствии с критериями Согласительной конфереции по скелетно-мышечной инфекции (2018) [19]:
- «санирующие операции с сохранением эндопротеза (DAIR3)»;
- «одноэтапное ЭП» — удаление компонентов эндопротеза, санирующая операция и установка нового эндопротеза в ходе одной хирургической процедуры;
- «двухэтапное ЭП» (каждый этап рассматривался как отдельный случай):
• удаление эндопротеза и санирующая операция — 1-й этап;
• удаление временного эндопротеза (спей- сера) и установка нового эндопротеза — 2-й этап;
- удаление эндопротеза с различными вариантами мышечной пластики или резекционной артропластики;
- установка нового эндопротеза после мышечной или резекционной пластики;
- «другое» — использование аппаратов внешней фиксации для восстановления опороспособности конечности без эндопротеза или формирование постоянного свища для снижения бактериальной нагрузки.
Рассматриваемыми категориями являлись динамические изменения в структуре ревизионных вмешательств, причины ревизии, объем выполненных ревизионных операций, характеристика пациентов. В ряде случаев, при наличии информации о предшествующем вмешательстве (связанные записи), оценивались возможные риски ревизии или повторной ревизии.
Статистический анализ
Расчеты производились в программах Microsoft Excel for Mac (Office 365) и SPSS (version 24.0). Использовались методы описательной статистики, представление абсолютных значений и долевые соотношения. Для количественных переменных указывались средние значения, 95% доверительный интервал [95% ДИ] и медиана. При сравнении средних использовался непараметрический критерий Манна - Уитни. Сравнение долей осуществлялось с помощью х2, а также в ряде случаев выполнялся расчет отношения шансов.
РЕЗУЛЬТАТЫ
Доля ревизий в общей структуре ЭП ТБС
Всего с 2007 по 2024 г. ревизии составили 12,4% от всех операций ЭП ТБС, при этом в разные годы отмечается колебание доли ревизионных вмешательств по отношению к общему числу выполненных операций по замене сустава от 8,4 до 20,8%, при этом прослеживается отчетливая тенденция к увеличению в структуре ревизий инфекционных причин, доля которых колеблется от 24,1 до 50,6% (рис. 2).
Значительные колебания в долевом соотношении первичных и ревизионных операций ЭП ТБС обусловлены не изменяющейся потребностью в этом виде помощи, а выделенными объемами по направлениям финансирования специализированной помощи (ВМП, ВМП ОМС) и возможностями медицинских учреждений, информация о работе которых фиксируется в базе регистра. К сожалению, мы не имеем реального представления о потребности в этом виде помощи, но анализ листа ожидания нашего центра и структуры телемедицинских консультаций показывает, что для многих пациентов, нуждающихся в ревизии, срок от момента возникновения проблемы до попадания в специализированное учреждение может составлять от нескольких месяцев до трех лет. В то же время на операцию первичного ЭП пациенты могут попасть практически сразу после консультации в одном из центров, выполняющих эти операции.
Гендерно-возрастная характеристика и география пациентов
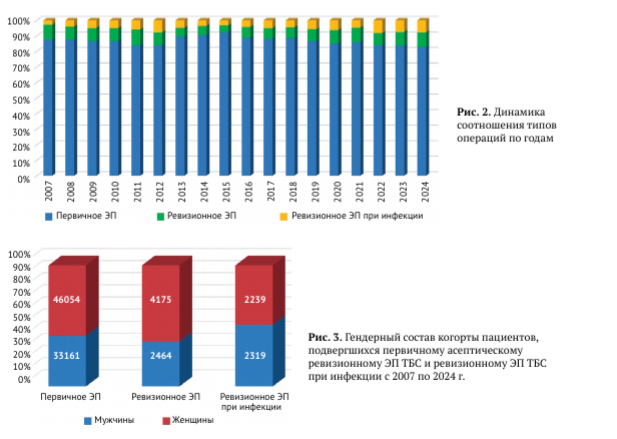
Гендерный состав при первичном и асептическом ревизионном ЭП ТБС (рис. 3) статистически значимо различался (р<0,001). При этом отношение шансов для асептической ревизии было выше для женщин (ОШ = 1,242; 95% ДИ 1,179-1,308), а для мужчин имелся более высокий риск инфекционной ревизии (ОШ = 1,284; 95% ДИ 1,211-1,361).
Средний возраст на момент операции при асептическом ревизионном ЭП ТБС составил 60,7 года (95% ДИ 60,4-61,0; Ме 62 года), что несколько больше, чем при первичном ЭП — 58,0 года (95% ДИ
58,0-59,1; Ме 60 лет), и чем при ревизии по поводу инфекции — 58,5 года (95% ДИ 58,1-58,8; Ме 60 лет).
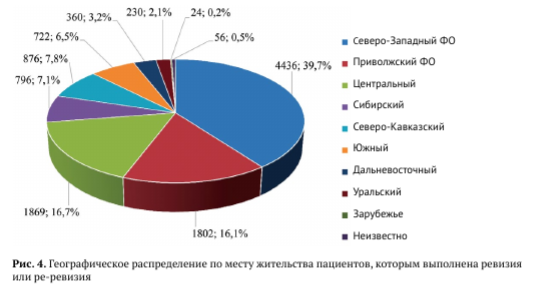
К сожалению, информация о конкретных медицинских организациях, в которых выполнялось первичное ЭП ТБС, очень ограничена и не подлежит анализу. Существенных гендерных различий между группами пациентов, оперированных в различных регионах, в нашем исследовании не наблюдалось.
Центрального федерального округа и с небольшой разницей — Приволжского федерального округа. Жители других регионов представлены в меньших объемах (рис. 4).
■ северо-западный Фо
■ приволжский Фо
■ Центральный
■ сибирский
■ северо-Кавказский
■ Южный
■ Дальневосточный
■ уральский
■ зарубежье
■ неизвестно
Сроки выполнения ревизий и их причины
К сожалению, не во всех случаях известна дата предшествующей операции, и в данной работе было доступно лишь 5 962 наблюдения. Как показали два ранее выполненных анализа, наибольшее число ревизий выполняется в первые годы после предшествующей операции [11, 17]. Структура графика на рисунке 5 остается практически неизменной и демонстрирует, что уже во второй год отмечается более чем двукратное сокращение числа ревизий и дальнейшее их постепенное уменьшение с незначительным всплеском на сроке 9-10 лет, который объясняется накоплением отсроченных проблем.
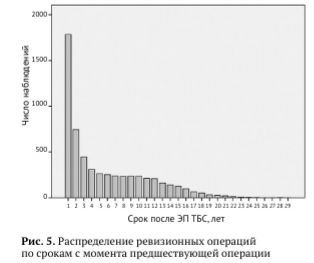
Однако если рассматривать отдельно асептические ревизии и операции, выполненные по поводу инфекционных осложнений, характер графиков значительно изменяется, но во всех случаях наибольшее число ревизий приходится на первые три года (рис. 6).
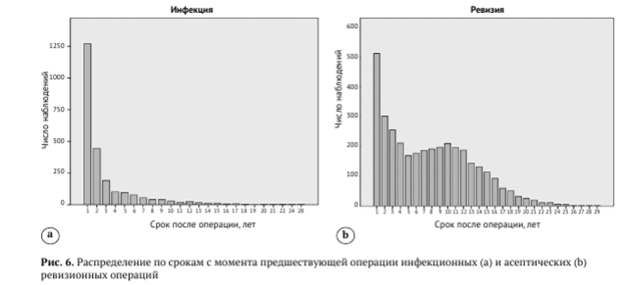
Основными причинами всех ревизий являлись инфекция (40,7%) и асептическое расшатывание компонентов эндопротеза (40,2%), на третьем месте были вывихи эндопротеза (7,7%), а на следующей позиции — износ полиэтилена и остеолиз (7,0%), на ППП и другие причины пришлось 2,8% и 1,6% соответственно (рис. 7).
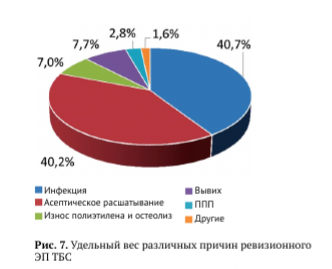
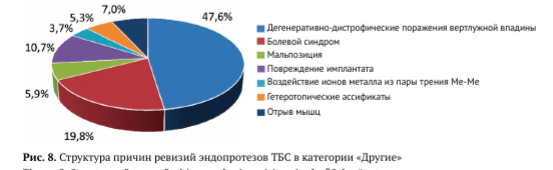
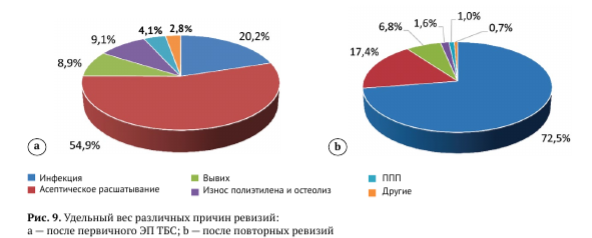
Сто восемьдесят семь случаев асептической ревизии, отнесенных к категории «Другие», включали 89 (47,6%) случаев дегенеративно-дистрофических поражений вертлужной впадины при однополюсном или биполярном ЭП, 37 (19,8%) — болевого синдрома различной этиологии, 11 (5,9%) — мальпозиции компонентов, 20 (10,7%) — переломов ножек эндопротеза или модульных шеек (повреждение имплантата), 7 (3,7%) — повреждений, обусловленных воздействием ионов металла из металло-металлических пар трения, 10 (5,3%) — гетеротопических оссификатов, потребовавших удаления, и 13 (7,0%) случаев повреждений отводящего аппарата бедра (рис. 8).
Так же как и в более раннем анализе, существенно различались структуры первой ревизии и последующих ре-ревизий. В случае если предшествующей операцией было первичное ЭП ТБС, доля инфекционных ревизий была существенно меньше, чем в общей массе ревизионных операций (20,2%), а основной причиной ревизии было асептическое расшатывание (54,9%), далее в порядке убывания следовали износ и остеолиз (9,1%), вывихи (8,9%), ППП (4,1%) и другие причины ревизии (2,8%) (рис. 9 a). В случае ре-ревизий основной причиной являлись различные вмешательства у пациентов, которым на разных этапах был установлен диагноз ортопедической инфекции (72,5%), асептическое расшатывание компонентов составило 17,4%, вывихи встречались в 6,8%, ППП и другие причины были отмечены в 1% и 0,7% соответственно (рис. 9 b). Соотношение ревизий и ре-ревизий в различные годы не имеет четкой закономерности, но, как было сказано выше, прослеживается тенденция к увеличению общего количества операций.
■ Дегенеративно-дистрофические поражения вертлужной впадины
■ Болевой синдром Мальпозиция
■ Повреждение имплантата
Воздействие ионов металла из пары трения Ме-Ме Гетеротопические ассификаты
■ Отрыв мышц
■ Инфекция
■ Вывих
■ Асептическое расшатывание щ Износ полиэтилена и остеолиз
■ ппп
■ Другие
Внутри группы асептических ревизий прослеживается тенденция к уменьшению доли асептического расшатывания компонентов c 86,4% в 2007 г. до 57,6% в 2024 г. и к увеличению доли износа полиэтилена с 0,6% в 2007 г. до 19,6% в 2023 г. с последующим незначительным смещением до 18,3% (рис. 10). Доля вывихов в структуре причин асептической ревизии увеличилась с 8,4 до 16,4%, доля ППП колебалась в разные годы от 1,9 до 8,4%. Колебания других причин ревизии весьма незначительны.
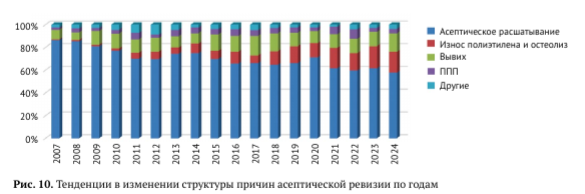
Что весьма интересно, доля асептического расшатывания не просто уменьшается, имеется стойкий тренд к уменьшению доли асептического расшатывания обоих компонентов (рис. 11). В первые годы работы регистра расшатывание обоих компонентов фиксировалось в 47,7-52,1% случаев, а в последние годы отмечается 14,7-16,2% всех случаев асептического расшатывания компонентов. Сложно сказать, имеют ли здесь какое-то значение особенности постановки диагноза или раньше действительно существенно чаще наблюдалось расшатывание обоих компонентов. В свою очередь, частота изолированного расшатывания бедренного компонента увеличилась с 7,5-12,7% до 31,2-33,5%. Доля изолированного расшатывания вертлужного компонента в разные годы составляла от 33,3% до 55,4%.
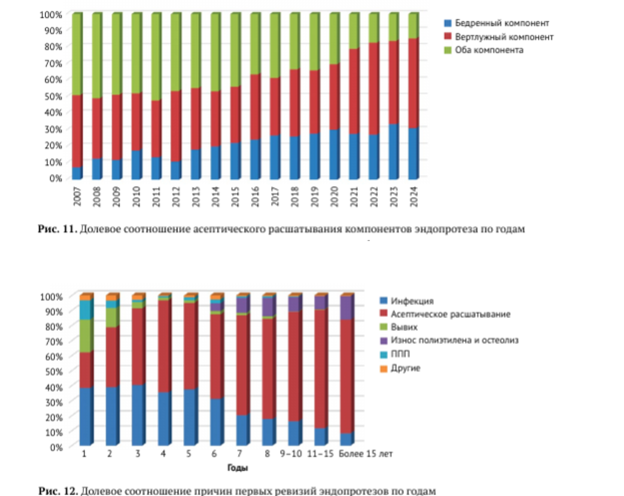
Большой интерес представляет не только удельный вес различных причин в структуре ревизионного ЭП ТБС, но и их распределение по времени выполнения вмешательства с момента предшествующей операции, атакже в зависимости от того, первая ли это ревизия или ре-ревизия. Как видно на рисунке 12, в первый год после первичного ЭП основной причиной ревизии является инфекция, что составляет 38,2% от всех первых ревизий. На второй и третьей позициях находятся асептическое расшатывание компонентов (24,0%) и рецидивирующие вывихи (22,0%), 12,8% приходится на ППП и 3,3% — на другие причины ревизии. Со второго года ситуация меняется: на первую позицию выходит асептическое расшатывание (38,8%) и остается основной причиной на всех дальнейших сроках наблюдения, колеблясь с 51,0% на третий год до 78,9% после 15 лет наблюдения. Доля инфекции постепенно снижается, но остается заметной во все периоды наблюдения. Доля вывихов и ППП в ревизиях заметно уменьшается со второго года (12,8% и 4,8% соответственно), становясь практически незаметной уже с четвертого года после первичного ЭП. С шестого года постепенно увеличивается доля износа и связанного с ним остеолиза в структуре ревизии и колеблется от 5,2% до 12,3%.
■ Асептическое расшатывание
■ Износ полиэтилена и остеолиз Вывих
■ ППП Другие
■ Бедренный компонент
■ Вертлужный компонент Оба компонента
■ Инфекция■ Асептическое расшатывание Вывих
■ Износ полиэтилена и остеолиз ... ППП
Средний срок выполнения ревизии по поводу инфекции составляет 2,4 года (95% ДИ 2,2-2,5 года; Ме 1 год), но колеблется от 2 нед. до 28 лет, когда инфекция, вероятнее всего, развивается, присоединяясь к воспалению на фоне асептического расшатывания имплантатов. Для асептического расшатывания средний срок ревизии составляет 7,9 года, но несколько различается внутри группы. Так, для расшатывания обоих компонентов средний срок составляет 8,3 года (95% ДИ 8,0-8,8;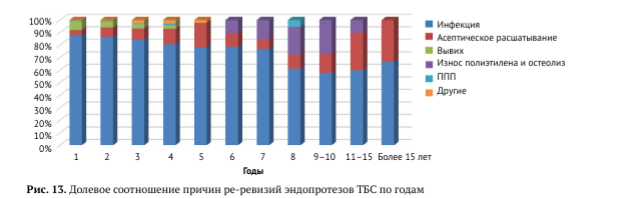
Ме 8 лет, от 1 мес. до 29 лет), для вертлужного компонента средний срок практически такой же — 8,5 года (95% ДИ 8,1-8,8; Ме 8 лет, от 1 мес. до 27,5 года). Для изолированной замены бедренного компонента средний срок был статистически значимо меньше — 6,1 года (95% ДИ 5,8-6,6; Ме 5 лет, от 1 мес. до 21 года) (р<0,001). Средний срок ревизии по поводу рецидивирующего вывиха составляет 2,7 года (95% ДИ 2,4-3,0; Ме 1 год, от 1 нед. до 18 лет).
Значительно более поздний средний срок ревизии наблюдался при износе полиэтилена и остеолизе — 10,6 года (95% ДИ 10,1-11,1; Ме 11 лет, от 6 лет до 28 лет), а ППП, требующие ревизии, наблюдались преимущественно в первые годы после первичного протезирования, средний срок составил 3,1 года (95% ДИ 2,6-3,6; Ме 1,5 года, от 1 мес. до 18 лет). Для других причин ревизии средний срок составил 5,2 года (95% ДИ 3,9-6,4; Ме 3,5 года, от полугода до 14,5 года).
В структуре первой ревизии 13,6% случаев приходятся на первый год после первичного ЭП, 9,1% — на второй, 8,2% — на третий, 6,1% — на четвертый, 5,3% — на пятый и 57,7% всех ревизий выполняются в более поздние сроки. В структуре ре-ревизий на первый год приходится 56,8% всех случаев повторных ревизий, на второй год — 18,1%, на третий — 6,3%, на четвертый — 3,8%, на пятый — 3,0%; на все остальные сроки — 12,4% случаев.
Среди причин ре-ревизий абсолютным лидером является инфекция, составляя 85,6% всех причин, при этом 86,0% всех инфекционных ре-ревизий приходится на первые два года, затем их роль несколько уменьшается, но остается ведущей причиной на всех сроках наблюдения с момента предшествующей операции (рис. 13). Доля асептического расшатывания компонентов среди причин повторных ревизий нарастает постепенно с 4,5%, достигая в отдаленном периоде 33,3%. Рецидивирующие вывихи и ППП значительно более равномерно распределены по срокам ре-ревизии, чем в группе ревизий после первичного ЭП ТБС, но встречаются преимущественно в первые пять лет после предшествующего вмешательства. Износ, так же как и в случае первых ревизий, встречается в основном после первых пяти лет, достигая максимума среди причин ревизии в период 9-10 лет.
Из 2272 повторных ревизий в 1521 случае (66,9%) это была первая ре-ревизия, в 560 (24,6%) — вторая, в 102 (4,5%) — третья-четвертая, в остальных 89 (3,9%) случаях пациенты подверглись от пятой до девятой ревизии.Средний срок до ревизии после первичного ЭП ТБС составил 7,0 года (95% ДИ 6,8-7,1; Ме 6 лет), до первой ре-ревизии — 3,3 года (95% ДИ 3,1-3,5; Ме 1 год), до второй ре-ревизии — 2,9 года (95% ДИ 2,5-3,2; Ме 1 год), и в дальнейшем средний срок не превышал 2 лет между очередными ре-ревизиями, хотя в отдельных случаях от ревизии до ревизии срок составлял до 20 лет. При этом средний возраст пациентов на момент ревизии после первичного ЭП ТБС составлял 60,0 года (95% ДИ 59,5-60,4; Ме 61 год), а средний возраст пациентов при первой ре-ревизии был меньше — 58,1 года (95% ДИ 57,6-58,7; Ме 59 лет), т.е. молодые пациенты являются группой риска более ранней ревизии и последующих ре-ревизий.
Объем ревизий после первичного ЭП ТБС в зависимости от причин и сроков их выполнения
Асептические ревизии
У 546 (8,2%) пациентов с асептическими ревизиями не указан или не понятен объем выполненной ревизии, и они не учитывались при анализе объема ревизионных операций. Как представлено на рисунке 14, в целом наиболее часто осуществлялась изолированная замена вертлужного компонента, затем — тотальная замена всего искусственного сустава, еще реже — изолированная замена бедренного компонента и замена модульных компонентов эндопротеза, и совсем редко выполнялись различные варианты остеосинтеза и другие варианты ревизионных вмешательств.
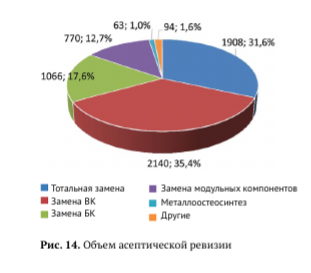
Самой частой причиной асептических ревизий было асептическое расшатывание одного или обоих компонентов эндопротеза — 4491 случай (67,7% от всех случаев асептической ревизии), при этом изолированная замена только вертлужного компонента выполнена в 39,5% наблюдений асептического расшатывания компонентов, изолированная замена бедренного компонента выполнена в 19,5% случаев и в 40,9% наблюдений выполнена тотальная замена эндопротеза (рис. 15).
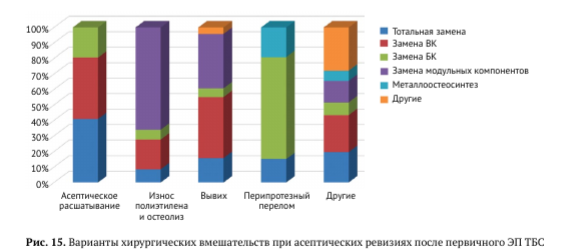
При ревизии по поводу износа полиэтилена и остеолиза наиболее часто — 488 (65,9%) наблюдений — объем ревизии заключался в замене одного или обоих модульных компонентов, в 141 (19,0%) случае выполнялась замена чашки, замена обоих компонентов и только бедренного компонента производились в 63 (8,5%) и 47 (6,3%) случаях соответственно. Статистической разницы в сроках выполнения различных вариантов ревизии по поводу износа отмечено не было.
■ Тотальная замена
■ Замена модульных компонентов
■ Замена
ВК
■ Металлоостеосинтез
У пациентов с рецидивирующими вывихами чаще всего — 293 (38,8%) наблюдения — производилась замена вертлужного компонента, включая установку цементируемой чашки двойной мобильности в старый ацетабулярный компонент. С несколько меньшей частотой осуществлялась замена модульных элементов эндопротеза — вкладыша, головки или вкладыша и головки — 262 (34,7%) случая. Тотальная замена эндопротеза выполнена у 118 (15,6%) пациентов, а в 42 (5,6%) случаях переустанавливался бедренный компонент. У 31 (4,1%) пациента борьба с рецидивирующим вывихом осуществлялась другими методами, главным образом путем различных вариантов мышечной пластики.
ППП, требующие ревизии, отмечались только в области бедренного компонента, вероятно, переломы в области вертлужного компонента всегда сопровождались потерей его фиксации и трактовались как асептическое расшатывание. Соответственно, самым частым вмешательством в этих случаях была изолированная замена бедренного компонента — 178 (65,9%) наблюдений. В 52 (19,3%) случаях имелась возможность выполнить остеосинтез переломов без замены компонентов эндопротеза, и в 41 (15,2%) случае потребовалась замена обоих компонентов эндопротеза.
Объем ревизии у пациентов, вошедших в категорию «Другие», заключался в изолированной ацетабулярной ревизии (11,8% наблюдений), тотальной ревизии сустава (9,8% случаев), изолированной замене бедренного компонента (4,1% случаев), замене модульных компонентов (6,9% наблюдений), металлоостеосинтезе (3,2% случаев), и у 13,9% пациентов были выполнены различные вмешательства на мягких тканях.
■ Тотальная замена■ Замена ВК Замена БК
■ Замена модульных компонентов ... Металлоостеосинтез
Инфекционные ревизии
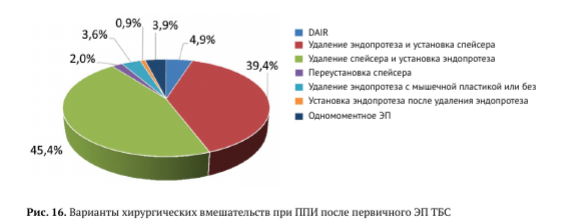
При ревизиях эндопротезов ТБС по поводу инфекции долевое соотношение типов хирургических вмешательств было следующим: ревизия раны с сохранением эндопротеза и заменой полиэтиленового вкладыша (DAIR) — 4,9%, удаление компонентов эндопротеза с установкой спейсе- ра — 39,4%, одномоментное удаление компонентов эндопротеза и установка нового эндопротеза (одномоментное эндопротезирование) — 3,9%, удаление компонентов эндопротеза и мышечная пластика или резекционная артропластика — 3,6%. Самой частым вмешательством был второй этап инфекционной ревизии — установка нового эндопротеза после удаления спейсера (45,4%), а самым редким вариантом — установка нового эндопротеза после предшествующего удаления эндопротеза в сочетании с мышечной пластикой, резекционной артропластикой или их сочетанием — 0,9% (рис. 16). Сроки выполнения 1-го этапа лечения ППИ (установки спейсера) сильно варьировали — от 2 нед. до 28 лет и в среднем составили 3,6 года (95% ДИ 3,3-3,8; Ме 2 года). Это существенно меньше, чем при предыдущем анализе (5,4 года; Ме 4 года), но все равно включает большую долю случаев хронической ППИ. Учитывая длительные сроки листа ожидания, остается непонятным, какое число случаев могло бы быть пролечено другими методами при своевременном выявлении инфекции и госпитализации пациентов. В подавляющем большинстве случаев (74,8%) применялись артикулирующие спейсеры, в других случаях — блоковидные спейсеры.
При острой ППИ (до 30 сут. с момента первичного ЭП ТБС) в 72,4% случаев применялась процедура DAIR, в остальных случаях — двухэтапная методика ревизии с установкой спейсера.
При одноэтапном ЭП средний срок выполнения вмешательства был таким же, как и при первом этапе двухэтапного ревизионного ЭП — в среднем 3,6 года (95% ДИ 3,0-4,4; Ме 2 года), отличались лишь условия для выполнения той или иной операции. Второй этап двухэтапной замены выполнялся в среднем через 1,2 года после установки спейсера (95% ДИ 1,1 — 1,3; Ме 7 мес.), что объясняется длительным листом ожидания на ревизионные вмешательства.
Полное удаление эндопротеза традиционно выполняется только при самом неблагоприятном прогнозе лечения инфекции с мышечной пластикой при особенно негативном прогнозе или без нее и, как правило, при нескольких неудавшихся ранее вмешательствах (81,2% наблюдений). Средний срок выполнения этого вмешательства с момента предыдущего достаточно небольшой — 2,3 года (95% ДИ 1,4-3,1; Ме 6 мес.). Однако при предшествующем первичном ЭП средний срок был значительно больше — 7,2 года (95% ДИ 6,8-7,6; Ме 6 лет). Вероятно, выбор такого вмешательства объяснялся длительным сроком наличия хронической инфекции.
Технологии, используемые в ревизионном ЭП ТБС
В основе ревизионной замены ацетабулярного компонента лежит использование бесцементных полусферических чашек, широко используемых в первичном ЭП, но, как правило (в 78,0% случаев), с множественными отверстиями под винты. До 2015 г. включительно наиболее используемыми для ревизии компонентами были чашки с пористым покрытием или шероховатой поверхностью, такие как Trilogy (Zimmer), Duraloc (DePuy), Plasmarnp (Aesculap) и некоторые другие (рис. 17).
■ DAIR
■ Удаление эндопротеза и установка спейсера Удаление спейсера и установка эндопротеза
■ Переустановка спейсера
Удаление эндопротеза с мышечной пластикой или без Установка эндопротеза после удаления эндопротеза
■ Одномоментное ЭП
Рис. 16. Варианты хирургических вмешательств при ППИ после первичного ЭП ТБС Figure 16. Surgical options for PJI-related revisions after primary THA
■ Полусферическая чашка
■ Ревизионная чашка Цементная чашка
■ Антипротрузионный кейдж С двойной мобильностью Индивидуальные
■ Logeeks
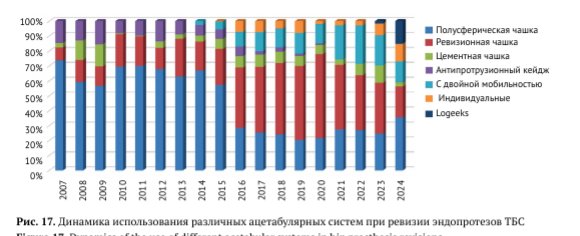
С 2012 по 2020 г. постепенно происходит замена модельного ряда — в основном используются Trilogy IT (Zimmer-Biomet), Plasmafit (Aesculap), Pinnacle (DePuy), R3 (Smith & Nephew), Continuum (Zimmer-Biomet). В разные годы доля вертлужных компонентов этого типа колебалась от 20,4% до 73,7%. В 8,2% случаев использование полусферических компонентов сочеталось с установкой металлических аугментов.
С 2016 г. отмечается более широкое использование специальных ревизионных полусферических чашек, таких как TM Modular (Zimmer- Biomet), TM Revision (Zimmer-Biomet), Pinnacle Revision (DePuy) и некоторых других, в том числе в сочетании с металлическими аугментами в 42,2% наблюдений. Их доля в структуре ревизий постепенно нарастала с 8,8% в 2007 г. до 56,5% в 2020 г., но затем уменьшилась до 20,6% в 2024 г., постепенно замещаясь индивидуальными (кастомизированными) компонентами и полностью пористыми титановыми чашками Tuberlock Multi-hole (Logeeks, Новосибирск), изготовленными методом 3D-печати. Доля индивидуальных имплантатов в общей структуре колебалась от 1,9% до 11,9%. Новые отечественные чашки Tuberlock Multi-hole
(Logeeks, Новосибирск) в 34 из 79 случаев (43,6%) сочетались с пористыми металлическими аугментами и использовались как части сложных ревизионных систем, включающих цементные чашки с двойной мобильностью. Вообще, применение имплантатов с двойной мобильностью имеет явный тренд к увеличению доли в структуре ревизий, но проследить все случаи их использования затруднительно ввиду их сочетания с другими вертлужными компонентами. Также сложно определить долю случаев, когда цементируемые чашки с двойной мобильностью устанавливались без удаления хорошо фиксированного старого вертлужного компонента.
В 2007 г. совокупная доля бедренных компонентов типов Wagner и Zweymuller в ревизионном ЭП ТБС составляла 25,8%. Наиболее используемым на тот момент являлись полнопокрытые пористые бедренные компоненты типа AML (DePuy), Solution (DePuy) и Malory-Head (Biomet) (рис. 18). Затем интенсивно выросла доля компонентов типа Zweymuller, представленных моделями Alloclassic (Zimmer), SL-Plus (Smith & Nephew), а позже добавились модели CBH (Mathys), TRJ (Aesculap), Sl-Plus MIA (Smith&Nephew) и ЯР-ТЭЗ (Рыбинск, Россия).
■ Типа Wagner
■ Полнопокрытые пористые Типа Corail
■ Цементные с гладкой поверхностью
Онкологический эндопротез Типа Zweymuller
■ Ревизионная ножка
с дистальным блокированием
■ Другие бесцементые
■ Другие цементные
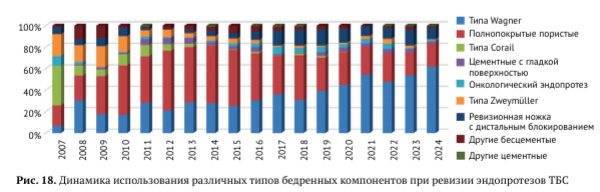
Компоненты типа Alloclassic (Zimmer) и SL-Plus (Smith & Nephew) чаще (69,5%) использовались в ревизионных вариантах Alloclassic SLL и SLR-Plus. Вплоть до 2018 г. этот тип ножек оставался самым часто применяемым вариантом бедренной ревизии. С 2019 г. подавляющее большинство (от 39,4% до 61,7%) ревизий выполняются с использованием ножек типа Wagner, представленных компонентами Wagner SL Revision (Zimmer-Biomet), Redapt (Smith & Nephew) и Wagner Cone (Zimmer-Biomet).
ОБСУЖДЕНИЕ
В результате интенсивного роста числа первичных операций и постепенного накопления пула пациентов, имеющих всевозможные осложнения после установки искусственного ТБС, в нашей стране ревизионное ЭП становится все более массовым хирургическим вмешательством [20, 21, 22, 23, 24, 25]. Этот анализ базы локального регистра не дает полного представления о структуре ревизионного ЭП в Российской Федерации в целом, но за счет значительного числа наблюдений позволяет представить основные тренды в ревизионной замене сустава, тем более что основная масса пациентов изначально была прооперирована в самых разных регионах нашей страны.
Первое, что следует отметить, — это значительное число ранних ревизий — 42,2% первых ревизий и 87,6% последующих ре-ревизий выполняются в первые пять лет после предшествующего вмешательства. Срок в пять лет для определения ранней ревизии взят по аналогии с другими исследованиями [17, 26, 27], но, вероятно, более правильно считать ранними ревизиями вмешательства, выполненные в первые два или три года после предшествующей операции. В первые два года выполняется 22,6% первых ревизий и 74,5% повторных ревизий, а в первые три года эти показатели меняются на 30,1% и 80,1% соответственно. Возможно, правильно считать ранними для первой ревизии выполненные в первые пять лет, а для ре-ревизий — два года.
Следующий важный тренд — это весьма интенсивный рост в структуре ревизий абсолютного числа и доли инфекционных ревизий [28]. В последние годы немногим меньше половины всех случаев ревизии эндопротезов ТБС выполняется у пациентов, имеющих в анамнезе диагностированную ППИ. Эти данные перекликаются с данными новозеландского регистра4, где не только доля, но и абсолютное число случаев ППИ утроилось с 2011-2012 гг., и инфекция вышла на первое место среди причин ревизии. Такая же ситуация наблюдается в Австралии, где, согласно данным национального регистра артропластики5, в 2022 г. инфекция тоже стала причиной номер один для ревизии эндопротезов ТБС и остается таковой в 2023 г.
Финские коллеги отмечают, что частота ранних случаев инфицирования возросла с 0,11 на 100 первичных обращений за медицинской помощью в 2008 г. до 1,09 в 2021 г. [29]. При наблюдении в течение года 26,6% (95% ДИ 22,2-31,2) пациентов перенесли повторную операцию, а 7,9% (95% ДИ 5,4-10,9) умерли. Риск повторной операции был самым высоким после DAIR (36,6%, 95% ДИ 28,544,7) и самым низким после одномоментной ревизии (20,2%, 95% ДИ 13,4-28,0) [30]. Общий показатель успеха DAIR в отношении сохранения компонентов и излечения от инфекции через два года составил 68% [31]. Определение истинной частоты ППИ остается чрезвычайно важной задачей, поскольку многочисленные публикации свидетельствуют о быстром росте числа случаев инфекции как из-за общего увеличения числа операций ЭП суставов, так и числа трудно распознаваемых инфекционных процессов. На основе эпидемиологического исследования тайваньские коллеги ожидают рост частоты инфекционных перипротезных осложнений в 4,79 раза к 2035 г. при росте затрат на их лечение в 4,86 раза, что может стать серьезным экономическим бременем для системы здравоохранения [32]. Когортное исследование с использованием данных немецкого регистра ЭП суставов (EPRD) показало, что совокупная смертность в течение первого года после септической ревизии ТБС составила 14%, а в течение семи лет — 40%. В случае нескольких предыдущих ревизий частота повторных ревизий при септической ревизии превышает 40%. Критический период для вероятности повторной ревизии при септической ревизии определен как первые 6 мес. [33]. Данные нашего регистра о крайне высокой частоте инфекции в случае множественных ревизий полностью согласуются с этими данными, и вопрос будущих исследований — определение уровня смертности в результате этих вмешательств.
Другой значимой проблемой является чрезвычайно молодой средний возраст пациентов, подвергающихся ревизиям, что было продемонстрировано ранее [11], и особенно при ре-ревизиях, как показывает настоящий анализ.
Коллеги из Нидерландов на основании данных национального регистра отметили, что результаты ревизий у пациентов моложе 55 лет значительно хуже, чем в общей популяции пациентов. Частота всех неудач, требующих повторных ревизионных операций, за 5 лет составила 22% (95% ДИ 19-25), а за 10 лет — 28% (95% ДИ 24-33). Суммарная частота инфекционных осложнений после ревизионных вмешательств за 10 лет составила 7,8% (95% ДИ 6,1-9,7), асептического расшатывания вертлужной впадины — 7,0% (95% ДИ 4,1-11,0), вывиха — 3,8% (95% ДИ 2,6-5,2) и расшатывания бедренного компонента — 2,7% (95% ДИ 1,6-4,1). При этом, если ревизия выполнялась по поводу инфекции, частота последующих ревизий в течение 10 лет составила 45% (95% ДИ 37-55) [34].
В нашей стране данная проблема усугубляется особенностями общей популяции пациентов, подвергающихся первичному ЭП ТБС [10]. Пациентов младше 50 лет в нашей базе регистра при первичном ЭП ТБС 22,7%, т.е. практически вдвое больше, чем в популяции Австралии или Соединенного Королевства6. Большое популяционное исследование, опубликованное в журнале Lancet, продемонстрировало, что у мужчин младше 50 лет вероятность ревизии в течение жизни составляет 35% [35]. А учитывая избыточно широкое использование традиционного полиэтилена сверхвысокой молекулярной массы вплоть до недавнего времени [18] и сегодняшние тенденции по росту числа ревизий, связанных с износом узла трения эндопротеза и прогрессирующим остеолизом, в ближайшие годы нам придется столкнуться со значительным ростом ревизий такого типа. Эта проблема характерна и для других стран. В частности в США подчеркивается предстоящий рост числа ревизий, связанных с молодым возрастом пациентов, а также с инфекционными осложнениями [36]. С учетом особенностей нашей популяции пациентов особое значение приобретает корректный выбор имплантатов [37].
Но здесь имеется еще одна проблема — резкое изменение спектра используемых имплантатов. В нашем исследовании полная замена всех компонентов эндопротеза выполнена в 31,6% всех асептических ревизий при наличии отчетливого тренда к уменьшению ее доли в последние годы. Сохранение одного из компонентов, согласно данным литературы, является безопасной процедурой с низкой частотой ре-ревизии [38], и, вероятно, выполнение парциальной ревизии — это общая тенденция. В частности в Германии замена только одного из компонентов осуществляется в 75% случаев, но отсутствует статистика изменения доли изолированных ревизий одного из компонентов по годам [39]. Возможно, значительно более высокая потребность в тотальной замене всех компонентов в прошлые годы была связана с проблемой остеолиза, частота которого значительно сокращается на фоне практически полного перехода на полиэтилен с поперечными связями [40, 41]. Однако у нас в стране происходит значительное замещение хорошо себя зарекомендовавших моделей эндопротезов ведущих мировых производителей на модели, выпущенные в КНР, Индии, Турции и других странах, а также постепенный переход на эндопротезы отечественного производства. Информации по этим моделям недостаточно в национальных регистрах других стран, что делает особенно важным формирование нашего собственного регистра для своевременного выявления потенциально опасных моделей искусственных суставов. Локальный регистр сможет отследить потенциально неблагоприятную ситуацию не ранее чем через 10-12 лет, в то время как национальный регистр способен выявить проблемные имплантаты через 7-8 лет, соответственно, сотни тысяч пациентов могут быть избавлены от слишком ранних ревизий, связанных с недостаточной устойчивостью имплантатов к изнашиванию.
Интересен тренд к увеличению числа и доли ревизионных вертлужных компонентов из трабекулярного металла, достигший максимума в 2020 г., и достаточно заметное последующее снижение. Ревизионные системы из трабекулярного металла обладают хорошо доказанной эффективностью как в отношении снижения риска асептического расшатывания, так и уменьшения частоты инфекционных осложнений [25, 42, 43, 44]. Но, с другой стороны, они существенно дороже, чем стандартные полусферические многодырчатые чашки с пористым покрытием. Всегда непросто оценить обоснованность применения более дорогостоящих конструкций в условиях значительного разнообразия имплантатов и неменьшего плюрализма мнений относительно возможной их эффективности [45, 46, 47]. В частности данные недавнего метаанализа китайских коллег демонстрируют отсутствие статистически значимой разницы между использованием вертлужных компонентов из трабекулярного металла и другими ацетабулярными системами [48]. Однако в любом обобщающем исследовании невозможно определить степень сложности входящих в него клинических наблюдений и обоснованность выбора того или иного имплантата для решения проблемы. Кроме того, по мнению других исследователей, данный метаанализ был выполнен с определенными методологическими погрешностями, ограничивающими его ценность [49]. Что касается нашего анализа, существенное увеличение доли конструкций из трабекулярного металла в 2019-2020 гг., вероятнее всего, объясняется нарастанием доли ревизий, требующих для достижения адекватной фиксации использования аугментов и расширенной дополнительной фиксации винтами. То есть появление значительного числа случаев, когда возможность формирования дополнительных отверстий под винты в необходимых местах, заложенная конструктивными особенностями имплантата, является фактором, перевешивающим даже более высокую стоимость таких конструкций. В свою очередь, снижение интереса к использованию таких имплантатов в дальнейшем можно объяснить повышением доступности других ревизионных систем, подходящих для применения в условиях тяжелых костных дефектов, а именно индивидуальных трехфланцевых чашек, индивидуальных аугментов, и появлением отечественных серийных вертлужных компонентов, изготовленных методом SD-печати, тренд на увеличение доли которых ярко выражен в 2023-2024 гг. В настоящий момент такие титановые вертлужные компоненты, изготовленные методом SD-печати, в сочетании с фиксацией на костный цемент полиэтиленового вкладыша или системы двойной мобильности являются эффективным [43, 50, 51] и относительно недорогим вариантом ревизионного ЭП при значительных костных дефектах, тем более что выбор имплантатов на предоперационнном этапе с учетом современных возможностей визуализации становится стандартом ревизионной хирургии [20, 52, 53]. Следует тем не менее отметить, что планирование, изготовление и установка индивидуальных эндопротезов — чрезвычайно непростой путь в ревизионной хирургии, и вероятность всевозможных ошибок при использовании таких имплантатов остается весьма значительной [50, 54, 55, 56], поэтому данные конструкции должны применяться по строгим показаниям. Отдельно необходимо указать на тренд к более широкому применению вертлужных компонентов с двойной мобильностью, которые все шире применяются при рецидивирующих вывихах и при других ревизиях на фоне мышечной недостаточности как конструкции, обладающие наивысшей устойчивостью к вывихам [57, 58, 59].
Тренд к использованию бедренных компонентов типа Wagner в ревизионной хирургии объясняется высокой эффективностью этих конструкций в условиях даже протяженных дефектов бедренной кости, высокой надежностью фиксации и относительной простотой хирургической техники, а также возможностью их использования с техникой расширенной вертельной остеотомии [60]. Как показывают механические исследования, имплантаты сохраняют стабильность при циклической нагрузке, превышающей 200% веса тела, а разрушение кости происходит при нагрузке, превышающей 400% [61]. Не случайно большинство производителей ортопедических изделий имеют в своей линейке имплантатов такие ревизионные ножки. Однако в случае крайне тяжелых дефектов даже длинные бедренные компоненты типа Wagner не позволяют добиться надежной фиксации, и тогда остается место для использования конструкций с дистальным блокированием и индивидуальных имплантатов, изготовленных методом 3D-печати, число которых, хоть и невелико, но также находит свое отражение в базе регистра [62].
ЗАКЛЮЧЕНИЕ
Несмотря на отсутствие всеобъемлющей информации о структуре первичного и ревизионного эндопротезирования в Российской Федерации, данный анализ продемонстрировал несколько важных трендов: интенсивное увеличение числа ревизионных операций с нарастанием числа случаев сложных ревизий, требующих использования сложных и дорогостоящих имплантатов, а также чрезвычайно быстрое увеличение числа случаев инфекционных ревизий. Поэтому совершенно ясно, что проблемы ревизионного эндопротезирования очень скоро могут коснуться всех хирургов, выполняющих первичную замену тазобедренного сустава, сначала через необходимость лечить инфекционные осложнения, а затем за счет постепенного накопления пула пациентов, нуждающихся в других вариантах ревизий, в том числе повторных.
ЛИТЕРАТУРА
1. Bruggemann H., Dalen I., Bache-Mathiesen L.K., Fenstad A.M., Hallan G., Fosse L. Incidence and risk factors of intraoperative periprosthetic femoral fractures during primary total hip arthroplasty: 218,423 cases reported to the Norwegian Arthroplasty Register between 1987 and 2020. Acta Orthop. 2022;93:405-412. doi: 10.2340/17453674.2022.2431.
2. Dale H., B0rsheim S., Kristensen T.B., Fenstad A.M., Gjertsen J.E., Hallan G. et al. Perioperative, short-, and long-term mortality related to fixation in primary total hip arthroplasty: a study on 79,557 patients in the Norwegian Arthroplasty Register. Acta Orthop. 2020;91(2): 152-158. doi: 10.1080/17453674.2019.1701312.
3. Groot L., Latijnhouwers D.A.J.M., Reijman M., Verdegaal S.H.M., Vliet Vlieland T.P.M., Gademan M.G.J. et al. Recovery and the use of postoperative physical therapy after total hip or knee replacement. BMCMusculoskeletDisord. 2022;23(1):666. doi: 10.1186/s12891-022-05429-z.
4. Kuijpers M.F., Hannink G., van Steenbergen L.N., Schreurs B.W. A significant change towards cemented fixation in revision total hip arthroplasty in patients younger than 55 years in the Netherlands: results of an observational cohort study in the Dutch Arthroplasty Register in 28,516 primary hip replacements and 1285 revision procedures. Hip Int. 2023;33(2):288-297. doi: 10.1177/11207000211020002.
5. Lutro O., Tj0rhom M.B., Leta T.H., Gjertsen J.E., Hallan G., Bruun T. et al. How many doses and what type of antibiotic should be used as systemic antibiotic prophylaxis in primary hip and knee arthroplasty? A register-based study on 301,204 primary total and hemi- hip and total knee arthroplasties in Norway 2005-2023. Acta Orthop. 2025;96:217-225. doi: 10.2340/17453674.2025.43003.
6. Mikkelsen R.T., Overgaard S., Pedersen A.B., Karrholm J., Rolfson O., Fenstad A.M. et al. Does choice of bearings influence the survival of cementless total hip arthroplasty in patients aged 20-55 years? Comparison of 21,594 patients reported to the Nordic Arthroplasty Register Association dataset 2005-2017. Acta Orthop. 2023;94:266-273. doi: 10.2340/17453674.2023.13384.
7. Springer B.D., Mullen K.P., Donnelly P.C., Tucker K., Caton E., Huddleston J.I. Is American Joint Replacement Registry Data Consistent With International Survivorship in Hip and Knee Arthroplasty? A Comparative Analysis. J Arthroplasty. 2024;39(9S1):S46-S50. doi: 10.1016/j.arth.2024.02.055.
8. Rasmussen M.B., El-Galaly A., Daugberg L., Nielsen P.T., Jakobsen T. Projection of primary and revision hip arthroplasty surgery in Denmark from 2020 to 2050. Acta Orthop. 2022;93:849-853. doi: 10.2340/17453674.2022.5255.
9. Premkumar A., Kolin D.A., Farley K.X., Wilson J.M., McLawhorn A.S., Cross M.B. et al. Projected Economic Burden of Periprosthetic Joint Infection of the Hip and Knee in the United States. J Arthroplasty. 2021;36(5): 1484-1489.e3.
10. Шубняков И.И., Тихилов Р.М., Николаев Н.С., Григоричева Л.Г., Овсянкин А.В., Черный А.Ж. и др. Эпидемиология первичного эндопротезирования тазобедренного сустава на основании данных регистра артропластики РНИИТО им. Р.Р. Вредена. Травматология и ортопедия России. 2017;23(2): 81-101. doi: 10.21823/2311-2905-2017-23-2-81-101. Shubnyakov I.I., Tikhilov R.M., Nikolaev N.S., Grigoricheva L.G., Ovsyankin A.V., Cherny A.Z. et al. Epidemiology of Primary Hip Arthroplasty: Report from Register of Vreden russian research institute of traumatology and orthopedics. Traumatology and Orthopedics of Russia. 2017;23(2):81-101. (In Russian). doi: 10.21823/2311-2905-2017-23-2-81-101.
11. Шубняков И.И., Тихилов Р.М., Денисов А.О., Ахмедилов М.А., Черный А.Ж., Тотоев З.А. и др. Что изменилось в структуре ревизионного эндопротезирования тазобедренного сустава в последние годы? Травматология и ортопедия России. 2019;25(4): 9-27. doi: 10.21823/2311-2905-2019-25-4-9-27. Shubnyakov I.I., Tikhilov R.M., Denisov A.O., Akhmedilov M.A., Cherny A.Z., Totoev Z.A. et al. What Has Changed in the Structure of Revision Hip Arthroplasty? Traumatology and Orthopedics of Russia. 2019;25(4):9-27. (In Russian). doi: 10.21823/2311-2905-2019-25-4-9-27.
12. Середа А.П., Кочиш А.А., Черный А.А., Антипов А.П., Алиев А.Г., Вебер Е.В. и др. Эпидемиология эндопротезирования тазобедренного и коленного суставов и перипротезной инфекции в Российской Федерации. Травматология и ортопедия России. 2021; 27(3):84-93. doi: 10.21823/2311-2905-2021-27-3-84-93. Sereda A.P., Kochish A.A., Cherny A.A., Antipov A.P., Aliev A.G., Veber E.V. et al. Epidemiology of Hip And Knee Arthroplasty and Periprosthetic Joint Infection in Russian Federation. Traumatology and Orthopedics of Russia. 2021;27(3):84-93. (In Russian). doi: 10.21823/2311-2905-2021-27-3-84-93.
13. Yenigul A.E., Dikici A.E., Eken G., Bilgen M.S. Comparison of patients undergoing revision total hip arthroplasty and patients undergoing re-revision. Eur Rev Med Pharmacol Sci. 2023;27(11):5053-5058. doi: 10.26355/eurrev_202306_32622.
14. Brown T.S., McLaughlin R.J., Berry D.J., Lewallen D.G., Trousdale R.T., Sierra R.J. What Is the Survivorship of Revision Surgery Performed for the Chronically Dislocated THA? Clin Orthop Relat Res. 2019;477(2): 374-379. doi: 10.1097/CORR.0000000000000392.
15. Rullan P.J., Orr M.N., Emara A.K., Klika A.K., Molloy R.M., Piuzzi N.S. Understanding the 30-day mortality burden after revision total hip arthroplasty. Hip Int. 2023;33(4):727-735. doi: 10.1177/11207000221094543.
16. Ashkenazi I., Christensen T., Oakley
C., Bosco J., Lajam C., Slover J. et al. Trends in Revision Total Hip
Arthroplasty Cost, Revenue, and Contribution Margin 2011 to 2021. J
Arthroplasty. 2023;38(7S):S34-S38.
17. Тихилов Р.М., Шубняков И.И., Коваленко А.Н., Тотоев З.А., Лю Б., Билык С.С. Структура ранних ревизий эндопротезирования тазобедренного сустава. Травматология и ортопедия России. 2014;20(2):5-13
18. Шубняков И.И., Риахи А., Денисов А.О., Корыткин А.А., Алиев А.Г., Вебер Е.В. и др. Основные тренды в эндопротезировании тазобедренного сустава на основании данных регистра артропла- стики НМИЦ ТО им. Р.Р. Вредена с 2007 по 2020 г. Травматология и ортопедия России. 2021;27(3): 119-142.
19. Материалы Второй международной согласительной конференции по скелетно-мышечной инфекции. Пер. с англ.; под общ. ред. Р.М. Тихилова, С.А. Божковой, И.И. Шубнякова. Спб.: РНИИТО им. Р.Р. Вредена, 2019. 314 с.
20. Базлов В.А., Мамуладзе Т.З., Голенков О.И., Ефименко М.В., Пронских А.А., Харитонов К.Н. и др. Выбор хирургической тактики при первичном и ревизионном эндопротезировании тазобедренного сустава с использованием инструментов объемной визуализации. Травматология и ортопедия России. 2020;26(2):60-70. doi: 10.21823/2311-2905-2020-26-2-60-70.
Bazlov V.A., Mamuladze T.Z., Golenkov O.I., Efimenko M.V., Pronskikh A.A., Kharitonov K.N. et al. Effects of 3D Imaging on Surgical Tactics in Primary and Revision Hip Arthroplasty. Traumatology and Orthopedics of Russia. 2020;26(2):60-70. (In Russian). doi: 10.21823/2311-2905-2020-26-2-60-70.
21. Гольник В.Н., Федорова Н.В., Ларичкин А.Ю., Бойко С.В., Панченко А.А., Косинов А.М. и др. Замещение дефектов вертлужной впадины методом импакционной костной пластики при ревизионном эндопротезировании тазобедренного сустава: биомеханические аспекты. Травматология и ортопедия России. 2024;30(4):101-113. doi: 10.17816/2311-2905-17564.
Golnik V.N., Fedorova N.V., Larichkin A.Yu., Boyko S.V., Panchenko A.A., Kosinov A.M. et al. Impaction Bone Grafting for Acetabular Bone Defects Replacement in Revision Hip Arthroplasty: Biomechanical Aspects. Traumatology and Orthopedics of Russia. 2024;30(4): 101-113. (In Russian). doi: 10.17816/2311-2905-17564.
22. Рыков А.Г., Щебеньков Б.В., Кожевникова С.Ю., Воловик В.Е., Коршняк В.Ю., Пальшин Г.А. Опыт ревизионного эндопротезирования тазобедренных суставов с использованием модульных систем. Здравоохранение Дальнего Востока. 2020;3(85):59-63. doi: 10.33454/1728-1261-2020-3-59-63.
Rykov A.G., Schebenkov B.V., Kozhevnikova S.Yu., Volovik V.E., Korshnyak V.Yu., Palshin G.A. Experience in revision hip arthroplasty using modular systems. Public Health of the Far East. 2020;3(85):59-63. (In Russian). doi: 10.33454/1728-1261-2020-3-59-63.
23. Цед А.Н., Муштин Н.Е., Дулаев А.К. Причины ревизионного эндопротезирования тазобедренного сустава после гемиартропластики по поводу перелома шейки бедренной кости. Травматология и ортопедия России. 2024;30(4):25-37. doi: 10.17816/2311-2905-17545.
Tsed A.N., Mushtin N.E., Dulaev A.K. Causes of Revision Hip Arthroplasty After Hemiarthroplasty for Femoral Neck Fracture. Traumatology and Orthopedics of Russia. 2024;30(4):25-37. (In Russian). doi: 10.17816/2311-2905-17545.
24. Каминский А.В., Матвеева Е.Л., Гасанова А.Г., Лунева С.Н., Спиркина Е.С., Ермаков А.М. Анализ биохимических показателей сыворотки крови у больных с ревизионным эндопротезированием тазобедренного сустава и нарушением углеводного обмена. Наука молодых (Eruditio Juvenium). 2023;11(1):5-14. doi: 10.23888/HMJ20231115-14. Kaminskiy A.V., Matveyeva E.L., Gasanova A.G., Luneva S.N., Spirkina E.S., Ermakov A.M. Analysis of Biochemical Parameters of Blood Serum in Patients with Revision Hip Arthroplasty and Disorder of Carbohydrate Metabolism. Science of the Young (Eruditio Juvenium). 2023;11(1):5-14. (In Russian). doi: 10.23888/HMJ20231115-14.
25. Корыткин А.А., Новикова Я.С., Ковалдов К.А., Королёв С.Б., Зыкин А.А., Герасимов С.А. и др. Среднесрочные результаты ревизионного эндопротезирования тазобедренного сустава с использованием ацетабулярных аугментов у пациентов с дефектами вертлужной впадины. Травматология и ортопедия России. 2019;25(1):9-18. doi: 10.21823/231129052019251918.
Korytkin A.A., Novikova Ya.S., Kovaldov K.A., Korolev S.B., Zykin A.A., Gerasimov S.A. et al. Mid-Term Outcomes of Revision Hip Arthroplasty with Acetabular Augments. Traumatology and Orthopedics of Russia. 2019;25(1):9-18. (In Russian). doi: 10.21823/2311-2905-2019-25-1-9-18.
26. Melvin J.S., Karthikeyan T., Cope R., Fehring T.K. Early failures in total hip arthroplasty - a changing paradigm. J Arthroplasty. 2014;29(6):1285-1288. doi: 10.1016/j.arth.2013.12.024.
27. Jafari S.M., Coyle C., Mortazavi S.M., Sharkey P.F., Parvizi J. Revision hip arthroplasty: infection is the most common cause of failure. Clin Orthop Relat Res. 2010;468(8):2046-2051.
28. Мурылев В.Ю., Парвизи Д., Руднев А.И., Куковенко Г.А., Елизаров П.М., Музыченков А.В. и др. Влияние расширенного предоперационного обследования на выбор тактики лечения перед вторым этапом ревизионного эндопротезирования тазобедренного сустава. Травматология и ортопедия России. 2024;30(2):29-39. doi: 10.17816/2311-2905-17510. Murylev V.Yu., Parvizi J., Rudnev A.I., Kukovenko G.A., Elizarov P.M., Muzychenkov A.V. et al. The Impact of Extended Preoperative Examination on the Treatment Tactics Choice Before the Second Stage of Revision Hip Arthroplasty. Traumatology and Orthopedics of Russia. 2024;30(2):29-39. (In Russian). doi: 10.17816/2311-2905-17510.
29. Liukkonen R.J., Honkanen M., Reito A.P., Skytta E.T., Karppelin M., Eskelinen A.P. Trends in Revision Hip Arthroplasty for Prosthetic Joint Infection: A SingleCenter Study of 423 Hips at a High-Volume Center Between 2008 and 2021. J Arthroplasty. 2023;38(6): 1151-1159. doi: 10.1016/j.arth.2023.02.061.
30. Liukkonen R., Honkanen M., Skytta E., Eskelinen A., Karppelin M., Reito A. Clinical Outcomes After Revision Hip Arthroplasty due to Prosthetic Joint Infection — A Single-Center Study of 369 Hips at a High- Volume Center With a Minimum of One Year Follow-Up. J Arthroplasty. 2024;39(3):806-812.e3. doi: 10.1016/j.arth.2023.08.078.
31. Veerman K., Raessens J., Telgt D., Smulders K., Goosen J.H.M. Debridement, antibiotics, and implant retention after revision arthroplasty: antibiotic mismatch, timing, and repeated DAIR associated with poor outcome. Bone Joint J. 2022;104-B(4):464-471. doi: 10.1302/0301-620X.104B4.BJJ-2021-1264.R1.
32. Chang C.H., Lee S.H., Lin Y.C., Wang Y.C., Chang C.J., Hsieh P.H. Increased periprosthetic hip and knee infection projected from 2014 to 2035 in Taiwan. J Infect Public Health. 2020;13(11):1768-1773. doi: 10.1016/j.jiph.2020.04.014.
33. Resl M., Becker L., Steinbruck A., Wu Y., Perka C. Re-revision and mortality rate following revision total hip arthroplasty for infection. Bone Joint J. 2024;106-B(6):565-572. doi: 10.1302/0301-620X.106B6.BJJ-2023-1181.R1.
34. Kuijpers M.F.L., Hannink G., van Steenbergen L.N., Schreurs B.W. Outcome of revision hip arthroplasty in patients younger than 55 years: an analysis of 1,037 revisions in the Dutch Arthroplasty Register. Acta Orthop. 2020;91(2):165-170. doi: 10.1080/17453674.2019.1708655.
35. Bayliss L.E., Culliford D., Monk A.P., Glyn-Jones S., Prieto-Alhambra D., Judge A. et al. The effect of patient age at intervention on risk of implant revision after total replacement of the hip or knee: a population- based cohort study. Lancet. 2017;389(10077):1424-1430. doi: 10.1016/S0140-6736(17)30059-4.
36. Schwartz A.M., Farley K.X., Guild G.N., Bradbury T.L.Jr. Projections and Epidemiology of Revision Hip and Knee Arthroplasty in the United States to 2030. J Arthroplasty. 2020;35(6S):S79-S85. doi: 10.1016/j.arth.2020.02.030.
37. Smith L.K., Dures E., Beswick A.D. Systematic review of the clinical effectiveness for long-term follow-up of total hip arthroplasty. Orthop Res Rev. 2019;11:69-78. doi: 10.2147/ORR.S199183.
38. Poursalehian M., Zafarmandi S., Razzaghof M., Mortazavi S.M.J. The impact of retaining the femoral stem in revision total hip arthroplasty: a systematic review, meta-analysis, and meta-regression. Arch Orthop Trauma Surg. 2024;144(2):947-966. doi: 10.1007/s00402-023-05087-3.
39. Freitag T., Reichel H. Contemporary indications for aseptic revision total hip arthroplasty. Orthopadie (Heidelb). 2022;51(8):609-618. (In German).
40. Bildik C., Kahraman H.£., Saygi B. Vitamin E-added Highly Cross-Linked Polyethylene Decreases the Risk of Osteolysis in an in vivo Arthroplasty Model. Cureus. 2023;15(2):e34955. doi: 10.7759/cureus.34955.
41. Prock-Gibbs H., Pumilia C.A., Meckmongkol T., Lovejoy J., Mumith A., Coathup M. Incidence of Osteolysis and Aseptic Loosening Following Metal-on- Highly Cross-Linked Polyethylene Hip Arthroplasty: A Systematic Review of Studies with Up to 15-Year Follow-up. J Bone Joint Surg Am. 2021;103(8):728-740. doi: 10.2106/JBJS.20.01086.
42. Matharu G.S., Judge A., Murray D.W., Pandit H.G. Trabecular Metal Versus Non-Trabecular Metal Acetabular Components and the Risk of ReRevision Following Revision Total Hip Arthroplasty: A Propensity Score-Matched Study from the National Joint Registry for England and Wales. J Bone Joint Surg Am. 2018;100(13):1132-1140. doi: 10.2106/JBJS.17.00718.
43. Hitz O., Le Baron M., Jacquet C., Argenson J.N., Parratte S., Ollivier M. et al. Use of dual mobility cup cemented into a tantalum acetabular shell for hip revision with large bone loss can decrease dislocation risk without increasing the risk of mechanical failure. Orthop Traumatol Surg Res. 2024;110(2):103739. doi: 10.1016/j.otsr.2023.103739.
44. Mirghaderi P., Eshraghi N., Sheikhbahaei E., Razzaghof M., Roustai-Geraylow K., Pouramini A. et al. Does Using Highly Porous Tantalum in Revision Total Hip Arthroplasty Reduce the Rate of Periprosthetic Joint Infection? A Systematic Review and Meta-Analysis. Arthroplast Today. 2024;25:101293. doi: 10.1016/j.artd.2023.101293.
45. Волошин В.П., Шавырин Д.А., Ошкуков С.А., Галкин А.Г. Варианты замещения дефектов вертлужной впадины при ревизионном эндопротезировании тазобедренного сустава. Здравоохранение Дальнего Востока. 2022;2(92):66-67.
46. Тихилов Р.М., Джавадов А.А., Коваленко А.Н., Денисов А.О., Демин А.С., Ваграмян А.Г. и др. Какие особенности дефекта вертлужной впадины влияют на выбор ацетабулярного компонента при ревизионном эндопротезировании тазобедренного сустава? Травматология и ортопедия России. 2020;26(2): 31-49. doi: 10.21823/2311-2905-2020-26-2-31-49. Tikhilov R.M., Dzhavadov A.A., Kovalenko A.N., Denisov A.O., Demin A.S., Vahramyan A.G. et al. What Characteristics of the Acetabular Defect Influence the Choice of the Acetabular Component During Revision Hip Arthroplasty? Traumatology and Orthopedics of Russia. 2020;26(2):31-49. (In Russian). doi: 10.21823/2311-2905-2020-26-2-31-49.
47. Коваленко А.Н., Шубняков И.И., Тихилов Р.М., Чёрный А.Ж. Обеспечивают ли новые и более дорогие имплантаты лучший результат эндопротезирования тазобедренного сустава? Травматология и ортопедия России. 2015;21(1):5-20. doi: 10.21823/2311-2905-2015-0-1-30-36.
48. Shen X., Oin Y., Li Y., Tang X., Xiao
J. Trabecular metal versus non-trabecular metal acetabular components for
acetabular revision surgery: A systematic review and meta-analysis. Int J Surg.
2022;100:106597.
49. Su Q., Wan X., Wang D., Zhou Z. A commentary on “Trabecular metal versus non-trabecular metal acetabular components for acetabular revision surgery: A systematic review and meta-analysis” (Int J Surg. 2022;100:106597). Int J Surg. 2022;103:106660. doi: 10.1016/j.ijsu.2022.106660.
50. Гольник В.Н., Джухаев Д.А., Красовский И.Б., Павлов В.В., Пелеганчук В.А. Хирургические аспекты позиционирования индивидуальных трехфланцевых имплантатов при замещении дефектов тазовой кости в ревизионном эндопротезировании тазобедренного сустава. Кафедра травматологии и ортопедии. 2022;4(50):15-26.
51. Shichman I., Somerville L., Lutes W.B., Jones S.A., McCalden R., Schwarzkopf R. Outcomes of novel 3D-printed fully porous titanium cup and a cemented highly cross-linked polyethylene liner in complex and revision total hip arthroplasty. Arthroplasty. 2022;4(1):51. doi: 10.1186/s42836-022-00152-5.
52. Садовой М.А., Павлов В.В., Базлов В.А., Мамуладзе Т.З., Ефименко М.В., Аронов А.М. и др. Возможности 3D-визуализации дефектов вертлужной впадины на этапе предоперационного планирования первичного и ревизионного эндопротезирования тазобедренного сустава. Вестник травматологии и ортопедии им. Н.Н. Приорова. 2017;24(3):37-42. doi: 10.17816/vto201724337-42. Sadovoy M.A., Pavlov V.V., Bazlov V.A., Mamuladze T.Z., Efimenko M.V., Aronov A.M. et al. Potentialities of 3D-Visualization in Preoperative Planning of Primary and Revision Total Hip Arthroplasty. N.N. Priorov Journal of Traumatology and Orthopedics. 2017;24(3):37-42. (In Russian). doi: 10.17816/vto201724337-42.
53. Коваленко А.Н., Шубняков И.И., Джавадов А.А., Билык C.C., Черкасов М.А., Амбросенков А.В. и др. Роль трехмерной визуализации при ревизионном эндопротезировании тазобедренного сустава. Гений ортопедии. 2020;26(3):364-369. doi: 10.18019/1028-4427-2020-26-3-364-369. Kovalenko A.N., Shubniakov I.I., Dzhavadov A.A., Bilyk S.S., Cherkasov M.A., Ambrosenkov A.V. et al. The role of three-dimensional visualization in revision hip arthroplasty. Genij Ortopedii. 2020;26(3):364-369. (In Russian). doi: 10.18019/1028- 4427-2020-26-3-364-369.
54. Коваленко А.Н., Тихилов Р.М., Билык С.С., Шубняков И.И., Черкасов М.А., Денисов А.О. Позиционирование индивидуальных вертлужных компонентов при ревизиях тазобедренного сустава: действительно ли они подходят как «ключ к замку»? Вестник травматологии и ортопедии им. Н.Н. Приорова. 2017;24(4):31-37.
55. Romagnoli M., Zaffagnini M., Carillo E., Raggi F., Casali M., Leardini A. et al. Custom-made implants for massive acetabular bone loss: accuracy with CT assessment. J Orthop Surg Res. 2023;18(1):742. doi: 10.1186/s13018-023-04230-5.
56. Weber M., Witzmann L., Wieding J., Grifka J., Renkawitz T., Craiovan B. Customized implants for acetabular Paprosky III defects may be positioned with high accuracy in revision hip arthroplasty. Int Orthop. 2019;43(10):2235-2243. doi: 10.1007/s00264-018-4193-3.
57. Unter Ecker N., Kocaoglu H., Zahar A., Haasper C., Gehrke T., Citak M. What Is the Dislocation and Revision Rate of Dual-mobility Cups Used in Complex Revision THAs? Clin Orthop Relat Res. 2021;479(2):280-285. doi: 10.1097/CORR.0000000000001467.
58. Donovan R.L., Johnson H., Fernando S., Foxall-Smith M., Whitehouse M.R. et al. A Meta-Analysis of the Incidence and Temporal Trends of Postoperative Dislocation in Revision Total Hip Arthroplasty Utilizing Constrained Acetabular Components or Dual Mobility Implants. J Arthroplasty. 2023;38(5):957-969.e1. doi: 10.1016/j.arth.2022.11.007.
59. Scholz J., Perka C., Hipfl C. Dual-mobility bearings reduce instability but may not be the only answer in revision total hip arthroplasty for recurrent dislocation. Bone Joint J. 2024;106-B(5 Supple B):89-97. doi: 10.1302/0301-620X.106B5.BJJ-2023-0828.R2.
60. Тихилов Р.М., Джавадов А.А., Копцов А.В., Филонов П.В., Курбанова С.М., Шубняков И.И. Какие факторы могут привести к проседанию немодульного конического бедренного компонента после ревизионного эндопротезирования тазобедренного сустава? Травматология и ортопедия России. 2024;30(1):42-51.doi: 10.17816/2311-2905-17417. Tikhilov R.M., Dzhavadov A.A., Koptsov A.V.,
Filonov P.V., Kurbanova S.M., Shubnyakov I.I. Which Factors Can Lead to Subsidence of a Non-Modular Tapered Stem after Revision Hip Arthroplasty? Traumatology and Orthopedics of Russia. 2024;30(1): 42-51. (In Russian). doi: 10.17816/2311-2905-17417.
61. Boettcher J.M., Sellenschloh K., Huber G., Ondruschka B., Morlock M.M. A Modified Wagner Stem Design Increases the Primary Stability in Cementless Revision Hip Arthroplasty. Arthroplast Today. 2025;32:101622. doi: 10.1016/j.artd.2025.101622.
62. Ковалдов К.А., Морозова Е.А., Герасимов Е.А., Герасимов С.А. Применение индивидуального импланта при ревизионном эндопротезировании тазобедренного сустава с костным дефектом типа IV по Paprosky. Гений ортопедии. 2023;29(5):546-551. doi: 10.18019/1028-4427-2023-29-5-546-551.
Kovaldov K.A., Morozova E.A., Gerasimov E.A., Gerasimov S.A. Revision total hip arthroplasty with custom-made hip implant for Paprosky type IV femoral bone loss. Genij Ortopedii. 2023;29(5):546-551. (In Russian). doi: 10.18019/1028-4427-2023-29-5-546-551.
Сведения об авторах
Н Шубняков Игорь Иванович — д-р мед. наук Адрес: Россия, 195427, г. Санкт-Петербург, ул. Академика Байкова, д. 8
Корыткин Андрей Александрович — канд. мед. наук, доцент
Денисов Алексей Олегович — д-р мед. наук
Джавадов АлисагибАббасович - канд. мед. наук
Pиахи
Аймен - канд. мед. наук
Гуацаев Максим Сосланович
Чилилов Абдула Магомедович — канд. экон. наук, доцент
Тихилов Рашид Муртузалиевич — д-р мед. наук, профессор, чл.-кор. РАН
Теги: эндопротезирование тазобедренного сустава
234567 Начало активности (дата): 10.10.2025
234567 Кем создан (ID): 989
234567 Ключевые слова: ревизионное эндопротезирование тазобедренного сустава, регистры эндопротезирования
12354567899
Похожие статьи
Модульная ревизия эндопротезов тазобедренного сустава у пациентов с износом полиэтиленовых вкладышей и перипротезным остеолизом: обзор литературыРентген на дому 8 495 22 555 6 8
Диагностика, лечение и профилактика венозных тромбоэмболических осложнений
Кто чаще всего страдает от артроза тазобедренного сустава
Интраоперационные перипротезные переломы бедренной кости при эндопротезировании тазобедренного сустава, обзор классификаций и метод лечения



