 13.08.2025
13.08.2025
Клинико-рентгено-морфологическая диагностика гиперчувствительного пневмонита
Диагностика ГП сложна и должна быть основана на мультидисциплинарном подходе с участием клиницистов (пульмонологов), рентгенологов, специалистов по функциональной диагностике и патологоанатомов
ВВЕДЕНИЕ
Гиперчувствительный пневмонит (экзогенный аллергический альвеолит, ГП) относится к иммунологически обусловленным заболеваниям легочной ткани, терминальных и респираторных бронхиол, развивающимся в ответ на ингаляцию антигенов [1].
Наиболее известными вариантами ГП являются болезнь любителей птиц [2], болезнь фермеров, болезнь, связанная с холодным воздухом в помещениях с системами кондиционирования, болезнь легких у рабочих, занятых в химическом производстве, ба- гассоз, индуцированный лекарственными препаратами [3]. По данным Fernandez E. Perez и соавт. [4], распространенность ГП колеблется от 0,3 до 0,9 на 100 тыс. населения. По данным F. Morell и соавт. [5], частота ГП составляет 6,2 на 100 тыс. у лиц, спящих на перьевых подушках, и 54,6 на 100 тыс. у птицеводов. По данным S. Dhooria и соавт. [6], из 803 больных интерстициальными заболеваниями легких в период с 2015 по 2017 г. ГП был выявлен в 10,7% наблюдений.
Основные патогенетические механизмы развития заболевания до сих пор неясны, однако показано развитие реакций гиперчувствительности III и IV типа. Ключевую роль играет процесс сенсибилизации к антигену и появление клинических симптомов после повторного воздействия антигена [7].
Исторически ГП был разделен на три варианта течения: острый, подострый и хронический. В дальнейшем стали выделять острый (воспалительный, клеточный) и хронический варианты ГП, которые отражали клиническое течение заболевания и различались по исходам, выживаемости, терапевтическому подходу [8, 9]. В 2020 г. появился первый международный консенсус по ГП, который предлагает выделять нефиброзный (НФГП) и фиброзный фенотипы (ФГП) гиперчувствительного пневмонита [1].
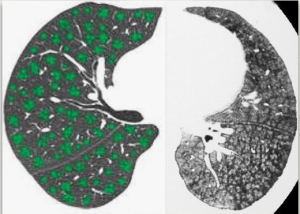
Симптомами НФГП (воспалительного) являются одышка, кашель, озноб, высокая температура, возникающие через 4-8 ч (при болезни фермеров через 12-18 ч) после воздействия антигена, которые могут нарастать в течение нескольких часов или дней [9, 10]. При ФГП у пациентов появляются одышка, незначительно усиливающаяся со временем, сухой кашель, недомогание, усталость, потеря аппетита [9, 10]. Для НФГП при компьютерной томографии высокого разрешения (КТВР) легких характерны мультифокальные, диффузные и центрилобулярные участки уплотнения по типу матового стекла (МС), воздушные ловушки (ВЛ) во время фазы выдоха, участки мозаичной плотности [11, 12]. Последние чаще встречаются при НФГП среди всех интерстициальных заболеваний легких (ИЗЛ), что делает этот признак диагностически значимым и может навести на верную постановку диагноза [13]. Основными признаками ФГП являются нарушение архитектоники, ретикулярные изменения (РИ), появление участков мозаичной плотности, признака head cheese (сочетание участков уплотнения по типу матового стекла и участков повышенной воздушности), тракционных бронхоэктазов, сотового легкого [12, 14].
Золотым стандартом для забора материала является хирургическая биопсия легкого. Трансбронхиальные биопсии малоинформативны из-за небольшого объема ткани легкого. Считается, что более перспективным для диагностики ГП могут быть трасбронхиальные криобиопсии [15, 16].
При НФГП при гистологическом исследовании обнаруживают бронхиолоцентрическую клеточную интерстициальную пневмонию (ИП), клеточный хронический бронхиолит, гранулематозное воспаление. Причем гранулемы обычно небольшие и рыхлые, плохо ограниченные, состоят из эпителиоидных и гигантских многоядерных клеток (ГМК), которые, как правило, расположены перибронхиолярно. Кроме того, встречаются разрозненные ГМК, содержащие в цитоплазме астероидные тельца, игольчатые кристаллы холестерина, кальцификаты (тельца Шаумана).
Цель исследования - изучить взаимосвязь клинико-рентгено-морфологических признаков при нефиброзном и фиброзном вариантах гиперчувствительного пневмонита при ретроспективном анализе.
При ФГП преобладают рыхлый коллагеновый фиброз, микросоты, облитерирующий бронхиолит (ОБ), ГМК в просветах альвеол, межальвеолярных перегородках и просветах микросот, легочная артериальная гипертензия (ЛАГ).
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включены 175 пациентов, у которых изучены клинические симптомы, функция внешнего дыхания, выполнена КТВР легких, получены открытые (видеоторакоскопические, при малой торакотомии) и трансбронхиальные биопсии. Клинически изучены одышка по шкале mMRC, кашель, отделение мокроты, наличие или отсутствие слабости.
При анализе КТВР обращали внимание на локализацию изменений ткани легкого, наличие симптома МС, РИ, наличие ВЛ, признака head cheese, тракционных бронхоэктазов (БЭ), очаговой диссеминации (ОД).
При изучении функции внешнего дыхания учитывали уровень форсированной жизненной емкости (ФЖЕЛ), объем форсированного выдоха за 1 с (ОФВ1), отношение объема форсированного выдоха за 1 с к форсированной жизненной емкости (ОФВ17 ФЖЕЛ), общую емкость легких (ОЕЛ), остаточный объем легких (ООЛ), диффузионную способность легких (DC).
Были изучены гистологические изменения в легких, которые были сопоставлены с направительными клиническими диагнозами и заключениями патологоанатомов.
При гистологическом исследовании срезов, окрашенных гематоксилином и эозином, пикрофуксином и фукселином для выявления коллагена и эластических волокон, были изучены следующие изменения: ОБ, перибронхиолярный фиброз с лимфоидной инфильтрацией, организующаяся пневмония (ОП), умеренно выраженный фиброз, метаплазия гладких мышц в фиброзе и межальвеолярных перегородках, неспецифическая интерстициальная пневмония (НСИП), ненекротические рыхлые гранулемы, микросоты, гигантские многоядерные клетки в про
светах альвеол, в межальвеолярных перегородках и микросотах, фибробластические фокусы (ФФ) и их локализация, бронхиолоэктазы, тельца Шаумана, гистологические признаки вторичной ЛАГ.
Статистический анализ осуществляли при помощи программы Statistica 10.0 в среде Windows 10. С помощью Ж-критерия Шапиро - Уилка определяли характер выборки, с помощью ^-критерия Манна - Уитни - достоверность различий выборок с распределением, отличным от нормального, которые считали статистически значимыми при p < 0,05. Корреляционные отношения оценивали с помощью коэффициента Спирмена, для оценки силы связи коэффициентов корреляции использовали шкалу Чеддока.
РЕЗУЛЬТАТЫ
Среди направительных клинических диагнозов ГП был диагностирован лишь в 15,5% наблюдений, т.е. уровень ошибок клиницистов составил 84,5%. Весь спектр диагнозов приведен на рис. 1.
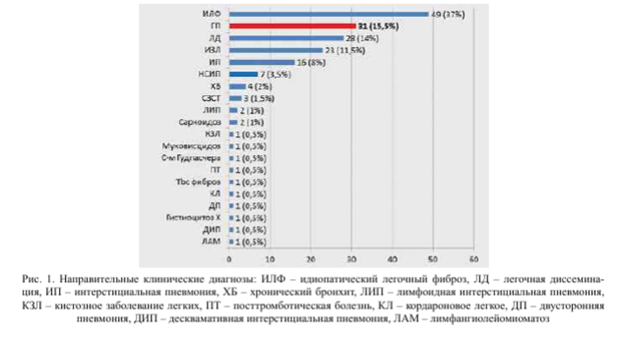
Гистологические диагнозы представлены на рис. 2. Только в 8% наблюдений был диагностирован ГП. Чаще всего больным ставился диагноз фибрози- рующего заболевания (идиопатического легочного фиброза). Другими словами, уровень ошибок при гистологическом исследовании достигал 92%. Следует заметить, что в 49,5% гистологическое заключение не предоставлено.
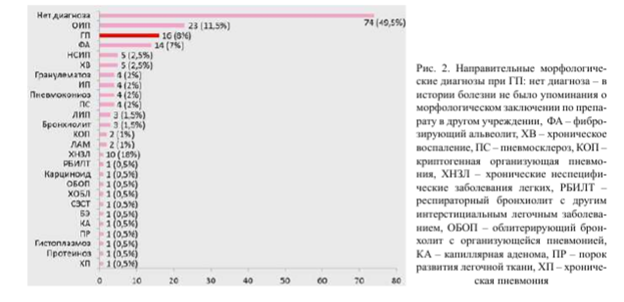
Частота вышеперечисленных клинических симптомов при НФГП и ФГП показана на рис. 3. При ФГП преобладали одышка, кашель, продукция мокроты. Однако показатель одышки по шкале mMRC не носил достоверного характера.
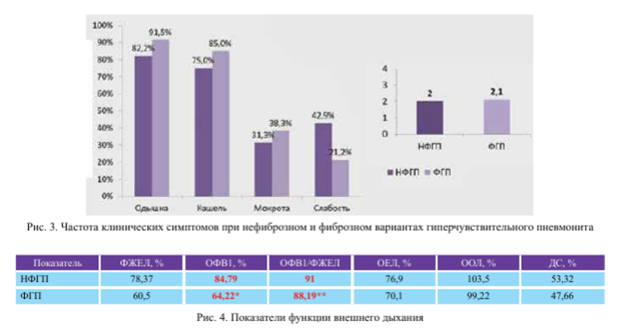
Показатели функции внешнего дыхания представлены на рис. 4. При НФГП преобладали показатели, указывающие на обструкцию бронхиального дерева, в то же время показатели диффузионной способности легких недостоверно отличались при двух вариантах ГП.
Данные по признакам КТВР представлены на рис. 5. При КТВР при ФГП достоверно больше было РИ и чаще встречались БЭ. Соты наблюдали только при ФГП. Остальные показатели отличались при НФГП и ФГП недостоверно.
Показано, что при двух вариантах ГП изменения в 42% наблюдений носили диффузный характер, но преобладали поражения нижних долей (47%) в обоих легких. В то же время поражение верхних долей было обнаружено в 11%, чего практически не встречается при обычной интерстициальной пневмонии (ОИП).
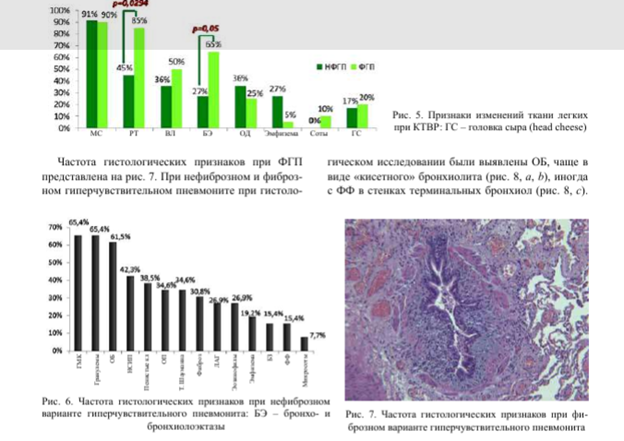
Гистологические изменения ткани легкого при НФГП представлены на рис. 6. Как видно на рис. 6, при этом варианте ГП наиболее часто встречались ОБ, гранулемы и гигантские многоядерные клетки в меньшей степени.
Неспецифическая клеточная интерстициальная пневмония и ОП, облитерирующий бронхиолит с ОП были обнаружены в 96,1% наблюдений.
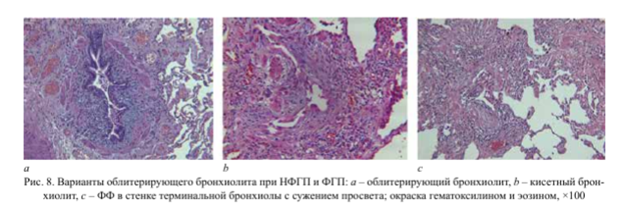
При НФГП наблюдали гигантские многоядерные клетки в просветах альвеол, полостей и в интерстиции (рис. 9, а), ненекротические рыхлые гранулемы (рис. 9, с), НСИП (рис. 10).
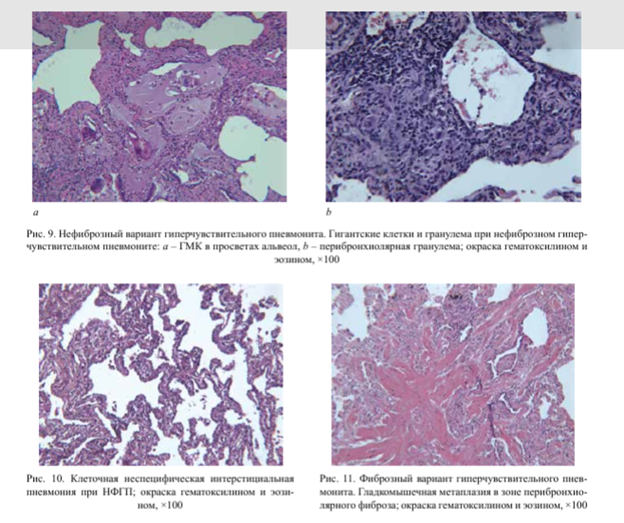
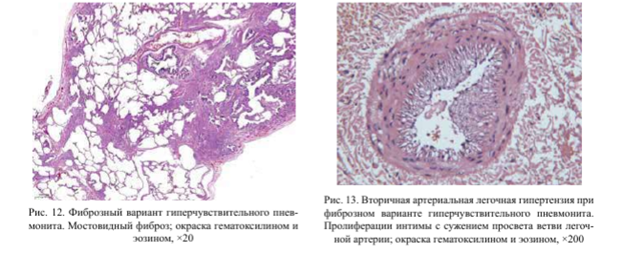
При ФГП также могут встречаться гигантские многоядерные клетки, умеренно выраженный перибронхиолярный интерстициальный фиброз с метаплазией гладких мышц (рис. 11), участки мостовидного фиброза (рис. 12), перибронхиолярный фиброз с лимфоидной инфильтрацией, ОП, микросоты, тельца Шаумана, бронхиолоэктазы, гистологические признаки вторичной ЛАГ (рис. 13)
Исходя из проведенного гистологического анализа в сопоставлении с данными компьютерной томографии легких в 16% наблюдений был установлен НФГП, в 62% - ФГП, в 22% - вероятный ГП. Эмфизема легких была обнаружена только у 16 (9%) больных, в одном наблюдении имело место сочетание ФГП с легочным альвеолярным протеинозом. Описанная ранее классическая триада морфологических признаков ГП (гранулемы и (или) ГМК, ОБ, НСИП) при НФГП встречалась в 19,2% наблюдений, при ФГП - в 5,6%.
При проведении корреляционного анализа выявлены достоверные корреляционные связи умеренной силы между: частотой НСИП при гистологическом исследовании и наличием сотового легкого при КТВР (г = -0,34), НСИП и симптомом head cheese при КТВР (r = 0,40), наличием гранулем и РИ (r = -0,34), гранулем и тракционными БЭ (г = -0,31), микросот и тракционными БЭ (r = 0,42), микросот и ОД (г = -0,32
ОБСУЖДЕНИЕ
Клинические проявления ГП неспецифичны. Наличие одышки при обоих вариантах ГП по шкале mMRC носила недостоверный характер. Как и в исследованиях G. Raghu и соавт., M. Vasakova и со- авт., M. Selman и соавт. [1, 9, 10], одышка, кашель и наличие мокроты встречались чаще при ФГП на 9,3 и 10,7% соответственно, но носили недостоверный характер. В то же время слабость в 2 раза чаще наблюдали при НФГП. При КТВР изменения в легких при двух вариантах ГП наблюдали в верхних, средних и нижних отделах легких в отличие от обычной интерстициальной пневмонии и изменений легких при системных заболеваниях соединительной ткани.
При НФГП чаще наблюдали диссеминацию и эмфизему легких, что согласуется с данным G. Raghu и соавт., B.J. Chong и соавт., S.J. Kligerman и соавт. [1, 11, 13], однако эти изменения не носили достоверного характера. Не отличается от данных G. Raghu и соавт., L.J. Wang и соавт., O.M. Dias и соавт. [1, 12, 14] и то, что наличие ретикулярных изменений, воздушных ловушек, бронхоэктазов достоверно чаще наблюдали при ФГП.
При гистологическом исследовании легких для НФГП были обнаружены бронхиолоцентрическая клеточная интерстициальная пневмония, клеточный хронический бронхиолит, гранулематозное воспаление. Причем гранулемы - обычно небольшие и рыхлые, в виде плохо ограниченных скоплений эпителиоидных и ГМК, которые, как правило, расположены перибронхиолярно. Кроме того, встречались разрозненные ГМК в просветах альвеол, терминальных и респираторных бронхиол, в просветах микросот, в интерстиции. Эти клетки часто содержали неспецифические цитоплазматические включения, такие как астероидные тельца и (или) кристаллы холестерина, тельца Шаумана. Согласуется с данными G. Raghu и соавт., M. Kitaichi и соавт. [1, 17] и то, что при вероятном НФГП наблюдали описанные выше гистологические признаки при отсутствии гранулем.
При ФГП характерно сочетание нарушения архитектоники легкого за счет центриацинарного и мостового фиброза, фиброзной интерстициальной пневмонии, появления ФФ, как правило, в стенках терминальных бронхиол, перибронхиолярной метаплазии, реже - наличие гранулем. Согласуется с данными G. Raghu и соавт., M. Kitaichi и соавт., S. Chiba и соавт. [1, 17, 18] и то, что при этом фиброз охватывает как субплевральные, так и центроацинарные области. Однако при прогрессировании фиброза при ГП крайне трудно отличить изменения в легких от ОИП.
Согласуется с данными G. Raghu и соавт. [1] и то, что при вероятном ФГП наблюдают те же гистологические признаки, что и при достоверном ФГП, но могут отсутствовать соты, в меньшей степени выражена перибронхиолярная метаплазия, отсутствуют гранулемы, встречаются единичные ГМК.
По нашему мнению, имеющиеся гистологические признаки в консенсусе 2020 г. следует дополнить такими признаками, как рыхлый мозаичный перибронхиолярный фиброз при ФГП, гладкомышечная метаплазия в зонах фиброза, наличие фибробластических фокусов в стенках терминальных бронхиол, в отличие от таких же фокусов в стенках сот при ОИП. При проведенном корреляционном анализе обнаружены достоверные корреляции умеренной силы между показателями КТВР и гистологическими изменениями легких, однако, по нашему мнению, это не позволяет с уверенностью диагностировать ГП. Диагноз ГП преимущественно основан на идентификации воздействия внешнего фактора, КТ-картине легких и гистопатологических признаках. Главная проблема заключается в том, что ни один индивидуальный признак не является достаточным в отдельности и не является обязательным. Это приводит к возможности множественных комбинаций признаков, которые способствуют правильной диагностике ГП, предложенной в консенсусе 2020 г. [1].
Следует учитывать возраст пациентов с интерстициальными заболеваниями легких. Для разных вариантов ГП возраст пациентов, как правило, менее 60 лет, возраст больных с ОИП - старше 60 лет.
ВЫВОДЫ
Уровень ошибок в клинической практике при гиперчувствительном пневмоните составляет 84,5%, среди патологоанатомов он достигает 92%.
Среди всех вариантов гиперчувствительного пневмонита наиболее часто встречался фиброзный.
Ненекротические гранулемы, гигантские клетки в просветах альвеол, микросот и в межальвеолярных перегородках более характерны для нефиброзного гиперчувствительного пневмонита.
При фиброзном гиперчувствительном пневмоните мозаичный перибронхиолярный фиброз, гладкомышечная метаплазия в зонах фиброза, наличие фибробластических фокусов в стенках терминальных бронхиол являются отличительными признаками от обычной интерстициальной пневмонии.
Классическую триаду наблюдали лишь в 19,2% при нефиброзном и 5,6% при фиброзном гиперчувствительном пневмоните.
Диагностика гиперчувствительного пневмо- нита сложна и должна быть основана на мультидисциплинарном подходе с участием клиницистов (пульмонологов), рентгенологов, специалистов по функциональной диагностике и патологоанатомов. При этом следует обязательно учитывать возраст пациентов и выявлять факторы, вызывающие развитие заболевания.
ЛИТЕРАТУРА
Raghu G., Remy-Jardin M., Ryerson C.J., Myers J.L., Kreu- ter M., Vasakova M. et al. Diagnosis of hypersensitivity pneumonitis in adults. An official ATS/JRS/ALAT Clinical Practice Guideline. Am. J. Respir. Crit. Care Med. 2020; 202 (3): e36- e69. DOI: 10.1164/rccm.202005-2032ST.
Mikumo H., Yanagihara T., Hamada N., Hashisako M., Ijichi K., Suzuki K. et al. An autopsy case of bird-related chronic hypersensitivity pneumonitis presenting with repeated acute exacerbation. Respir. Med. Case Rep. 2018; 24: 92-94. DOI: 10.1016/j.rmcr.2018.04.016.
Roden A.C., Camus P. Iatrogenic pulmonary lesions. Semin. Diagn. Pathol. 2018; 35 (4): 260-271. DOI: 10.1053/j.sem- dp.2018.03.002.
Fernandez Perez E.R., Kong A.M., Raimundo K., Koelsch T.L., Kulkarni R., Cole A.L. Epidemiology of Hypersensitivity Pneumonitis among an Insured Population in the United States: A Claims-based Cohort Analysis. Ann. Am. Tho- rac. Soc. 2018; 15 (4): 460-469. DOI: 10.1513/Annal- sATS.201704-288OC.
Morell F., Villar A., Ojanguren I., Munoz X., Cruz M.J., San- sano I. et al. Hypersensitivity pneumonitis and (idiopathic) pulmonary fibrosis due to feather duvets and pillows. Arch.
Bronconeumol. 2021; 57 (2): 87-93. DOI: 10.1016/j.ar- bres.2019.12.003.
Dhooria S., Agarwal R., Sehgal I.S., Prasad K.T., Garg M., Bal A. et al. Spectrum of interstitial lung diseases at a tertiary center in a developing country: A study of 803 subjects. PLoS One. 2018; 13 (2): e0191938. DOI: 10.1371/journal.pone.0191938.
Johansson E., Boivin G.P., Yadav J.S. Early immunopatholog- ical events in acute model of mycobacterial hypersensitivity pneumonitis in mice. J. Immunotoxicol. 2017; 14 (1): 77-88. DOI: 10.1080/1547691X.2016.1273284.
Salisbury M.L., Myers J.L., Belloli E.A., Kazerooni E.A., Martinez F.J., Flaherty K.R. Diagnosis and treatment of fibrotic hypersensitivity pneumonia. Where we stand and where we need to go. Am. J. Respir. Crit. Care Med. 2017; 196 (6): 690-699. DOI: 10.1164/rccm.201608-1675PP.
Vasakova M., Morell F., Walsh S., Leslie K., Raghu G. Hypersensitivity pneumonitis: perspectives in diagnosis and management. Am. J. Respir. Crit. Care Med. 2017; 196 (6): 680-689. DOI: 10.1164/rccm.201611-2201PP.
Selman M., Pardo A., King T.E. Jr. Hypersensitivity pneumonitis: insights in diagnosis and pathobiology. Am. J. Respir. Crit. Care Med. 2012; 186 (4): 314-324. DOI: 10.1164/rc- cm.201203-0513CI.
Chong B.J., Kanne J.P., Chung J.H. Headcheese sign. J. Thorac. Imaging. 2014; 29 (1): W13. DOI: 10.1097/ RTI.0000000000000067.
Wang L.J., Cai H.R., Xiao Y.L., Wang Y., Cao M.S. Clinical characteristics and outcomes of hypersensitivity pneumonitis: a population-based study in China. Chin. Med. J. (Engl.). 2019; 132 (11): 1283-1292. DOI: 10.1097/ CM9.0000000000000256.
Kligerman S.J., Henry T., Lin C.T., Franks T.J., Galvin J.R. Mosaic attenuation: etiology, methods of differentiation, and pitfalls. Radiographics. 2015; 35 (5): 1360-1380. DOI: 10.1148/rg.2015140308.
Dias O.M., Baldi B.G., Pennati F., Aliverti A., Chate R.C., Sawamura M.V.Y. et al. Computed tomography in hypersensitivity pneumonitis: main findings, differential diagnosis and pitfalls. Expert. Rev. Respir. Med. 2018; 12 (1): 5-13. DOI: 10.1080/17476348.2018.1395282.
Myers J.L. Hypersensitivity pneumonia: the role of lung biopsy in diagnosis and management. Mod. Pathol. 2012; 25 (1): S58-67. DOI: 10.1038/modpathol.2011.152.
Mooney J.J., Koth L.L. Surgical lung biopsy over broncho- alveolar lavage in chronic hypersensitivity pneumonitis. Am. J. Respir. Crit. Care Med. 2014; 189 (3): 371-372. DOI: 10.1164/rccm.201309-1736LE.
Kitaichi M., Shimizu S., Tamaya M., Takaki M., Inoue Y. Pathology of hypersensitivity pneumonitis. In: Sharma O.P., (ed.). Clinical focus series, hypersensitivity pneumonitis. New Delhi, India: Jaypee Brothers Medical Publishers, 2013: 2232. DOI: 10.5005/jp/books/12031_3.
Chiba S., Tsuchiya K., Akashi T, Ishizuka M., Okamoto T., Furusawa H. et alChronic hypersensitivity pneumonitis with a usual interstitial pneumonia-like pattern: correlation between histopathologic and clinical findings. Chest. 2016; 149 (6): 1473-1481. DOI: 10.1016/j.chest.2015.12.030.
Сведения об авторах
Черняев Андрей Львович, д-р мед. наук, профессор, зав. отделом фундаментальной пульмонологии, НИИ институт пульмонологии; вед. науч. сотрудник, НИИМЧ им. А.П. Авцына, г. Москва.
Кусраева Элина Валерьевна, ординатор, кафедра патологической анатомии и клинической патологической анатомии педиатрического факультета, РНИМУ им. Н.И. Пирогова, г. Москва.
Самсонова Мария Викторовна, д-р мед. наук, зав. лабораторией патологической анатомии, НИИ пульмонологии; ст. науч. сотрудник, Московский клинический научно-практический центр им. А.С. Логинова Департамента здравоохранения города Москвы, г. Москва.
Авдеев Сергей Николаевич, д-р мед. наук, профессор, чл.-корр. РАН, зав. клиническим отделом, НИИ пульмонологии, г. Москва.
Трушенко Наталья Владимировна, канд. мед. наук, ассистент, кафедра пульмонологии, Сеченовский университет; научный сотрудник НИИ пульмонологии, г. Москва.
Туманова Елена Леонидовна, д-р мед. наук, профессор, зав. кафедрой патологической анатомии и клинической патологической анатомии педиатрического факультета, РНИМУ им. Н.И. Пирогова, г. Москва.
Теги: пневмонит
234567 Начало активности (дата): 13.08.2025 08:37:00
234567 Кем создан (ID): 989
234567 Ключевые слова: нефиброзный и фиброзный гиперчувствительный пневмонит, мультидисциплинарная диагностика, гистологические признаки
12354567899
Похожие статьи
12.08.2025 14:22:53Рентген на дому 8 495 22 555 6 8
Разработка информационно-рекомендательной системы для анализа рентгеновских снимков с использованием ИИ
Автоматическое распознавание патологий на рентгеновских, КТ и МРТ снимках
Врожденная пневмония



