 13.06.2025
13.06.2025
Использование шарнирного эндопротеза коленного сустава
Тотальное эндопротезирование коленного сустава (ТЭКС) включает замену всех отделов коленного сустава для восстановления работоспособности и функции.
На сегодняшний день применяются как готовые спейсе- ры фабричного производства, так и цементные метил- метакрилатные интраоперационного изготовления [6]. После этапного применения спейсера, проводимого консервативного лечения и купирования воспалительного процесса, но не ранее чем через 3-6 месяцев, проводится второй этап лечения — имплантация ревизионного эндопротеза коленного сустава [7].
Основные сложности РТЭКС после использования различных спейсеров заключаются в развитии артрофиброза коленного сустава, с большим или меньшим разрастанием соединительной ткани, потере костной ткани, утрате анатомических ориентиров, потере связочного аппарата, сложности с восстановлением исходной суставной линии, мягкотканным балансом
При этом, к сожалению, отмечается недостаточная врачебная преемственность, так как первичный эндопротез коленного сустава устанавливается в одном учреждении, лечение инфекционных осложнений и установка спейсера происходят в другом учреждении, а последующее ревизионное протезирование — в третьем [9].
При планировании ревизионного вмешательства, тотального эндопротезирования коленного сустава (ТЭКС), мы использовали классификацию костных дефектов AORI (Anderson Orthopaedic Research Institute, 2006) и варианты восстановления суставной линии для правильного подбора компонентов ревизионного эндопротеза [10-12].
КЛАССИФИКАЦИЯ КОСТНЫХ ДЕФЕКТОВ AORI (2006)
Современная классификация костных дефектов AORI (табл. 1) была предложена Ортопедическим Научно-исследовательским институтом Андерсона в 2006 году. В данной классификации учитываются костные дефекты бедренной и большеберцовой костей после проведённого первичного эндопротезирования коленного сустава, которые разделены в зависимости от типа, глубины и локализации дефекта.
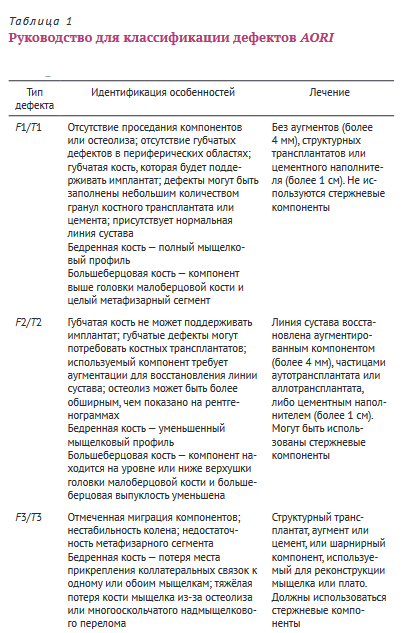
Следует отметить, что в классификации AORI учитываются только те дефекты, которые возникли после удаления компонентов протеза. Дефекты оцениваются по предоперационным рентгенограммам и, в последующем, классификация может быть изменена интраоперационно. Бедренные надмыщелки, задние бедренные мыщелки и положение надколенника относительно суставной линии могут использоваться в качестве ориентиров, чтобы дифференцировать сложные бедренные дефекты. Головка малоберцовой кости и большеберцовая бугристость также должны использоваться в качестве ориентиров для тех большеберцовых дефектов, которые трудно оценить.
Основами этой классификации являются следующие определения типа дефектов:
Тип 1. Дефект (интактная метафизарная кость): лёгкие костные дефекты, не ставящие под угрозу стабильность компонента.
Тип 2. Дефект (повреждённая метафизарная кость): потеря губчатой кости, требующая заполнения цементом, аугментом или костным трансплантатом, чтобы восстановить обоснованный уровень суставной линии. Костные дефекты типа 2 могут появиться в одном бедренном мыщелке или большеберцовом плато (2 А), или в обеих мыщелках или плато (2 B).
Тип 3. Дефект (недостаточный метафизарный сегмент): потеря костной массы, ставящая под угрозу большую часть мыщелка или плато. Эти дефекты обычно связаны с недостаточностью коллатеральных или пателлярных связок и обычно требуют костных трансплантатов или кастомных имплантатов.
Как всегда, в любой классификации некоторые случаи являются пограничными. Для их классификации необходимо оценивать как послеоперационные рентгенограммы, так и проведенное хирургическое лечение.
Костные дефекты также возможны и в надколеннике, но эти случаи были исключены из классификации костных дефектов AORI, потому что они не влияют на выбор методов в ревизионной хирургии, не используется костная пластика и специальные ревизионные компоненты для их лечения — за редкими исключениями.
Бедренный костный дефект F1
Предоперационные рентгенограммы бедренной кости Типа 1 демонстрируют правильно выровненный компонент без доказательств бедренного остеолиза.
Они также не показывают значительной составляющей миграции, должен был хороший уровень суставной линии. Незначительные поверхностные дефекты от остатков цементных пробок излечены частичным костным трансплантатом или цементом. Табл. 1 суммирует особенности и методики лечения дефекта F1.
Послеоперационные рентгенограммы бедренной кости Типа 1 показывают относительно нормальный уровень суставной линии с надколенником на 1 см проксимальнее относительно большеберцового плато. Бедренные мыщелки кажутся целыми на переднего перелома
Без аугментов (более 4 мм), структурных трансплантатов или цементного наполнителя (более 1 см). Не используются стержневые компоненты
Линия сустава восстановлена аугментиро- ванным компонентом (более 4 мм), частицами аутотрансплантата или аллотрансплантата, либо цементным наполнителем (более 1 см). Могут быть использованы стержневые компоненты
Структурный трансплантат, аугмент или цемент, или шарнирный компонент, используемый для реконструкции мыщелка или плато. Должны использоваться стержневые компоненты задней рентгенограмме; задний мыщелковый офсет сохранён на боковой рентгенограмме. Проксимальный кончик заднего мыщелка компонента должен соответствовать проксимальному концу заднего мыщелка бедра пациента. Дальнейшая потеря костной массы может также произойти после удаления импланта.
Бедренный костный дефект F2
Бедренный костный дефект F2 характеризуется остеолизом или значительной проксимальной миграцией бедренного компонента. Рентгенограммы могут показать проседание имплантата с круговой рентгенопрозрачностью. Кроме того, потеря расстояния от надмыщелков до края имплантата будет очевидна на переднезадней рентгенограмме. Бедренный остеолиз не должен распространяться дальше надмыщелков.
В некоторых дефектах F2 могут быть изменены нормальные соотношения бедренного компонента и диафиза бедренной кости (6-градусное вальгусное отклонение). Имплантат проседает с угловой миграцией в неправильную варусную или вальгусную позицию относительно анатомической оси бедра.
Дефекты F2A: один мыщелок
Дефект бедра Типа 2A может вовлекать любой мыщелок. Губчатая кость вовлечённого мыщелка, возможно, была повреждена остеолизом или ятрогенно, если была сделана неправильная дистальная угловая резекция кости бедра во время первичной артропластики. Кость противоположного бедренного мыщелка относительно интактна при нормальном уровне суставной линии.
Рентгенографический критерий бедренной кости Типа 2A определяется наличием одностороннего возвышения суставной линии на фоне сохранения для фиксации имплантата кости в противоположном мыщелке. Наличие небольших костных дефектов в противоположном мыщелке не изменяет классификацию дефекта Типа 2A, пока противоположный мыщелок поддерживает относительно нормальный уровень суставной линии.
Реконструкция дефекта F2A с использованием первичного имплантата производится редко. В большинстве случаев используется модульный аугмент, чтобы восстановить нормальную суставную линию. При некоторых обстоятельствах методика лечения дефекта F2A должна включать частичное восстановление суставной линии. Это может быть необходимо, чтобы исправить большую дооперационную сгибательную контрактуру. Дефект F2A преобразовывается в дефект F2B, когда противоположный мыщелок резецирован на более проксимальном уровне. Когда суставная линия повышена, необходим меньший размер бедренного компонента, чтобы восстановить сгибательно-разги- бательный баланс. Послеоперационные рентгенограммы правильно восстановленного дефекта F2A должны показывать мыщелок с аугментом или восстановленный мыщелок.
Переднезадняя рентгенограмма может продемонстрировать более проксимальный уровень резекции мыщелка. Однако аугментирование не всегда видно на боковой рентгенограмме, если имеется картер-бокс заднестабилизированного или связанного импланта.
Дефект F2B: оба мыщелка
Дефект в бедренной кости Типа 2B идентичен дефекту 2А, но включает оба бедренных мыщелка. Повреждённая метафизарная кость требует восстановления при помощи цемента, аугментов, костных графтов для достижения приемлемого уровня суставной линии. На переднезадней рентгенограмме просевшего бедренного компонента типа 2B расстояние от дистального края компонента относительно надмыщелков уменьшается.
Если надмыщелки уплощены за счёт миграции компонентов, то дефект приобретает уровень типа F3. Остеолиз может быть отмечен на переднезадней рентгенограмме между компонентом и метафизарным краем. Кроме того, на боковой рентгенограмме может присутствовать пателла baja. В связи с проксимальной миграцией суставной линии задний мыщелок компонента протеза, возможно, переместился выше оставшегося заднего мыщелка бедра пациента. Использование большого количества цемента проксимальнее бедренного компонента обычно приводит к классификации F2B. Часто необходима аугментация обеих бедренных мыщелков дистально и сзади с помощью модульных аугментов для восстановления нормального уровня линии сустава. Цементная мантия иногда усиливается губчатыми костными винтами. Дефект F2B всегда следует восстанавливать ревизионным компонентом со стержнем. Для некоторых дефектов F2B требуется поднятие суставной линии для восстановления адекватного движения в коленном суставе. Это справедливо для тугого колена при сгибательной контрактуре более 20 градусов.
Послеоперационные рентгенограммы дефекта F2B демонстрируют как подъём суставной линии без устранения больших дефектов кости, так и нормальную линию сустава, которая была восстановлена аугментами, костным трансплантатом или толстой цементной мантией под компонентом. Метафизарный сегмент бедра будет казаться укороченным или замененным на бедренный компонент увеличенной толщины.
Костные трансплантаты будет трудно различить, если трансплантат плотно примыкает к кости пациента. Надколенник может находиться на уровне или ниже верхней части большеберцового компонента, тем самым указывая на подъём суставной линии.
Дефект F3
Бедренные дефекты Типа 3 имеют обширную структурную потерю костной ткани, включая большую часть одного или обеих бедренных мыщелков. См. табл. 1 для идентификации особенностей дефектов F3.
Предоперационные рентгенограммы дефектов F3 демонстрируют остеолиз и выраженную миграцию к уровню надмыщелков. Когда бедренная кость мигрирует, надмыщелки находятся вблизи компонента. Хотя тяжесть остеолиза не всегда очевидна на рентгенограммах, хирург должен предполагать, что остеолиз может быть намного более тяжёлым, чем ожидается. Остеолиз обычно проявляется как дефект в губчатой кости, прилегающей к имплантату.
Остеолиз часто проявляется на краях бедренного компонента и сопровождается склеротической или зубчатой границей. Часто литические повреждения остеолиза видны в областях, где бедренный компонент не скреплён с костью пациента. Самые агрессивные литические повреждения остеолиза могут не иметь рентгенографической склеротической границы. Расшатывание шарнирного, кастомного, ревизионного компонента часто приводит к дефекту F3. Эти конструкции компонентов часто имеют стержень, мигрирующий в канале бедра. Существенное количество кости было удалено при установке таких компонентов. В этих случаях укорачивается метафизарный сегмент бедренной кости.
Хирургическая реконструкция дефекта типа F3 является процедурой «спасения», требующей восстановления метафизарной кости массивным структурным аллотрансплантатом или кастомным бедренным компонентом.
Обширная потеря костной массы может включать один или оба мыщелка. Может потребоваться варусно-вальгусный связанный имплантат, или сохранение и повторное присоединение одной или обеих коллатеральных связок. В этом случае требуется ножка, заполняющая канал бедра. Достижение ротационной стабильности бедренного компонента может потребовать полного цементирования бедренного канала или использования аллотрансплантата.
Послеоперационные рентгенограммы дефекта бедра типа 3 демонстрируют восстановление дистального метафиза бедра и, в некоторых случаях, диафиза. Все конструкции с хинчами или шарнирами относятся по умолчанию к типу F3, потому что они заменяют метафизарный сегмент и связывают соседние компоненты и компартменты. Из-за отличающейся плотности кости установление границ аллотрансплантата от прилегающей кости пациента очевидно несложно. Идеальная реконструкция дефекта F3 включает восстановление нормальной суставной линии на фоне полиэтиленового вкладыша минимальной толщины.
Большеберцовый костный дефект T1
Те же принципы, используемые в классификации бедренных дефектов, относятся к большеберцовым дефицитам кости. В большеберцовых отделах расшатывание имплантата более распространено. Часто большеберцовый компонент проседает в варусном положении, создавая костный дефект в медиальном отделе плато. Большеберцовая кость Типа 1 имеет те же особенности идентификации, что и бедренный дефект F1 (см. табл. 1).
Предоперационные рентгенограммы показывают правильно выровненный большеберцовый компонент без значительного проседания имплантата или большеберцового остеолиза. Проксимальный отдел большеберцовой кости находится выше головки малоберцовой кости. Для дефектов 71 рекомендуется стандартный большеберцовый компонент, потому что сохранена соответствующая губчатая кость пациента.
Послеоперационные рентгенограммы тоже подтверждают, что кости и контуры большеберцового метафиза были сохранены выше головки малоберцовой кости. Обычно используются стандартные компоненты с толщиной всего компонента (металл+полиэтилен) менее чем 20 мм.
Большеберцовый костный дефект T2
Дефект 7 2 часто бывает вызван расшатыванием большеберцового компонента и вторичным проседанием большеберцовой кости, обычно в варусном положении. Круговая рентгенопрозрачная линия формируется между цементом и костью, когда компонент проседает. Уменьшается расстояние между головкой малоберцовой кости и компонентом. Для измерения этого расстояния будет полезна боковая рентгенограмма. Рентгенологическая картина остеолиза проявляется просветлениями различной формы ниже компонента (см. табл. 1 для большеберцовых дефектов).
Дефект T2A: одно плато
Дефект типа 2A обычно является результатом расшатывания большеберцового компонента и его проседания в варусной позиции. Тибиальный компонент редко проседает в вальгусное положение, даже в валь- гусных коленях.
На предоперационных рентгенограммах часто отмечаются просветления различной формы ниже большеберцового компонента. В противоположном большеберцовом плато костная ткань присутствует на относительно нормальном уровне суставной линии. Дефекты типа T2A могут также присутствовать при асептическом расшатывании одномыщелкового большеберцового компонента.
Хирургическое лечение дефекта T2A включает использование модульного компонентата со стержнем одновременно с небольшим аутотрансплантатом, аллотрансплантатом или аугментом. Важно избегать превращения дефекта T2A в дефект T2B путём большей резекции кости большеберцового плато на более дистальном уровне. В этом случае, когда создаётся ятрогенный дефект T2B, будет требоваться более толстый большеберцовый компонент.
Дефект T2B: оба плато
Дефект Типа 2B включает всё тибиальное плато. Рентгенологическая картина дефектов T2B демонстрирует повреждение метафизарного сегмента большеберцовой кости путём проседания компонента, остеолиза или обеими способами. Повреждение может распространиться на уровень головки малоберцовой кости, но не должно включать обширную деструкцию кости ниже этого уровня.
Проксимальный метафиз большеберцовой кости должен быть уменьшен, но всё ещё присутствовать. Остеолитические поражения должны иметь чёткие границы с некоторым количеством губчатой кости для возможности связывания цемента во время реконструкции. Хирургическое лечение дефектов T2B обычно включает использование модульного большеберцового компонента с длинным стержнем и реконструкцию тибиального плато костным трансплантатом, аугментами или утолщённым большеберцовым компонентом. Аугмент, имеющий форму клина, будет адекватен для лечения дефекта T2B, если потеря костной массы преимущественно с одной стороны плато.
Если использовался структурный костный трансплантат, то необходимы заполняющие канал стержни.
Для реконструкций дефекта T2B часто используется заполнение дефекта цементом. Укрепление губчатыми винтами может обеспечить более прочную конструкцию, чем один только цемент. Самый сложный метод реконструкции дефектов большеберцовой кости типа 2 и типа 3 достигается правильным использованием цемента и аллотрансплантата. Преимущество использования аллотрансплантата заключается в воссоздании ложа губчатой кости для цементного соединения с костью пациента. Фактически структурные аллотрансплантаты в ревизионных операциях на коленном суставе показали долговременную эффективность.
Рентгенологическая картина после восстановления дефектов типа T2B показывает восстановленный уровень суставной линии путём использования тиби- альных аугментов, цемента или аллотранспланта. Аугмент может быть в виде утолщённого ревизионного компонента, ступенчатого или углового аугмента под модульным компонентом. В дополнение к аугменту может использоваться костный трансплантат. Если уровень суставной линии не был восстановлен, то плато большеберцового компонента будет находится на одном уровне или ниже уровня головки малоберцовой кости.
Большеберцовый костный дефект T3
Большеберцовый дефект Типа 3 обычно является следствием тяжёлой большеберцовой нестабильности, вызванной асептическим расшатыванием и миграцией импланта. Развитию дефекта типа T3 может способствовать остеолиз или перипротезный перелом. При дефекте типа T3 имеется расширенное повреждение губчатой кости проксимальной тибии. Головка малоберцовой кости может быть сохранена и находиться выше, чем проксимальная большеберцовая кость. Для стабильности модульного компонента необходимо использовать заполняющие канал ножки. В тяжёлых случаях метафизарный отдел большеберцовой кости полностью отсутствует. Поэтому для восстановления проксимальной тибии, фиксации компонентов и нормальной суставной линии необходимо использование больших структурных аллотрансплантатов.
Рентгенологическая предоперационная картина дефекта T3 показывает тяжёлую миграцию, нестабильность и деструкцию проксимального метафиза тибии. Часто поражаются как места прикрепления собственной связки надколенника, так и точки прикрепления коллатеральных связок вследствие большой потери костной массы. Могут присутствовать patella alta и поражение разгибательного механизма.
Для восстановления прокимального тибиального дефекта типа T3 показаны массивные структурные аллотрансплантаты или индивидуальные кастомные большеберцовые компоненты. Ротационной стабильности будут способствовать цементные заполняющие канал ножки. При восстановлении прокимального тибиального дефекта типа T3 могут использоваться варусно-вальгусно ограниченные имплантаты, реплантация коллатеральных связок и реконструкция раз- гибательного механизма.
Рентгенологическая послеоперационная картина дефекта типа T3 демонстрирует восстановленный метафизарный сегмент проксимальной большеберцовой кости.
Если классификация костных дефектов применяется правильно, то метод используемой реконструкции должен быть адекватен каждой категории дефекта.
При планировании РТЭКС мы также использовали классификацию вариантов восстановления суставной линии по M. Innocenti (2013) для правильного подбора и установки компонентов ревизионного эндопротеза [13, 14] (табл. 2).
При РТЭКС поднятие суставной линии — частое явление, связанное с более низким клиническим и функциональным результатом [15-17]. Основа этого доказательства кроется в сложности проведения баланса сгибательно-разгибательного промежутка, что в большинстве случаев приводит к проксимизации дистального отдела бедренной кости, для компенсации увеличенного пространства сгибания. Одно из решений, чтобы избежать подъёма линии сустава — это использование бедренного компонента большего размера; однако более крупный компонент имеет более широкий медиолатеральный диаметр, что может приводить к образованию эффекта соударения мягких тканей о протез [18].
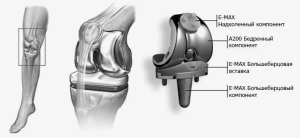
Для РТЭКС мы использовали связанную систему эндопротезов с вращающимся шарниром (RH- TKA) [19].

Система RH-TKA с вращающимся шарниром была разработана, чтобы предоставить хирургу-ортопеду дополнительные возможности, связанные с ревизионным эндопротезированием коленного сустава. RH- TKA — это коленный протез с ограниченным вращением. Протез спроектирован таким образом, чтобы обеспечить внутреннюю/внешнюю ротацию приблизительно на уровне в 10° в каждом направлении. Ротация блокируется большеберцовым вкладышем при полном разгибании. Благодаря штифтовой конструкции протез имеет способность к удлинению, то есть к дистракции между бедренным и большеберцовым компонентами до 30 мм. В крайне согнутом положении бедренный компонент может отодвигаться от большеберцового вкладыша, что компенсирует сагиттальные рычажные усилия, воздействующие на ножку протеза в этих ситуациях.
Имплантаты доступны в пяти размерах (2, 4, 6, 8 и 10). Помимо размера 2, размеры можно комбинировать со следующим размером, на один размер больше или меньше. Система RH-TKA позволяет использовать металлические аугменты, цементные и бесцементные, прямые или офсетные стержни, метафизарные конусы. Совместимость модульного RH-TKA с монолитным RH-TKA позволяет (при необходимости) во время операции комбинировать компоненты протезов.
Клинический пример
Пациентка Ю., 56 лет, находилась на лечении в ортопедическом отделении с диагнозом «Контрактура левого коленного сустава. Гнойный гонит левого коленного сустава. Состояние после установки спейсера левого коленного сустава».
При поступлении предъявляла жалобы на боль, отёчность, гиперемию в области левого коленного сустава, субфебрильное повышение температуры до 37,5°С, деформацию и нарушение опороспособности левой нижней конечности.
Из анамнеза пациентки известно, что была неоднократно госпитализирована в районную клиническую больницу, где была проведена, со слов больной, 5-кратная артроскопия левой нижней конечности в период с 2016 по 2018 год. При артроскопии от 06.2018 был поставлен дренаж, проводилась антибиотикотерапия. После последней госпитализации вышеуказанные жалобы продолжали проявляться с периодической интенсивностью.
В 2019 году был поставлен диагноз «Гонит левого коленного сустава» и выполнена резекция коленного сустава с установкой антибактериального спейсера.

При осмотре: функция ходьбы нарушена. Передвигается, разгружая нижнюю конечность. Контуры левого коленного сустава деформированы. Пальпация области коленного сустава безболезненная. Отмечается ограничение активных и пассивных движений в суставе, за счёт излишнего натяжения коллатеральных связок.
Объём движений: разгибание - 5°, сгибание - 85°. Функциональная оценка левого коленного сустава по шкале WOMAC (Western Ontario and McMaster University Osteoarthritis Index) - 47 56. Отмечается гипотрофия мышц левой нижней конечности. Признаков сосудистой и неврологической патологии не выявлено.
Инфекция была исключена по данным лабораторных биохимических, иммунологических и микробиологических исследований. После многократных отрицательных посевов из коленного сустава, отрицательных биохимических и иммунологических анализов крови на С-реактивный белок и интерлейкин-6 было рекомендовано ревизионное протезирование коленного сустава.
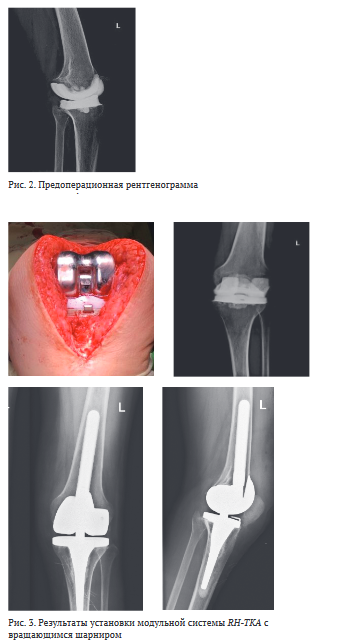
При предоперационом планировании измеряли угол вальгусного отклонения, проводили проверку состояния связочного аппарата. Костный дефект по классификации AORI был оценен как F3/T3 по результатам рентгенографического и, в последующем, интраоперационных исследований (рис. 2).
Восстановление суставной линии планировалось как вариант 1 по M. Innocenti - использование феморального компонента большего размера.
Показаниями к назначению эндопротеза RH-TKA с вращающимся шарниром являлось наличие костных дефектов F3/T3, связочной нестабильности, выраженного дисбаланса сгибательного и разгибательного промежутков.
26.02.2020 было проведено ревизионное эндопротезирование с извлечением спейсера и установкой ревизионного модульного эндопротеза коленного сустава типа RH- TKA (рис. 3). Модульная система RH-TKA с вращающимся шарниром. Использовались модульные компоненты, бедренные аугменты и заполняющие канал ножки. Операция была произведена с использованием стандартного костного цемента с антибиотиком. Выбор модели эндопротеза осуществлялся также с учётом выраженной метафизарной потери костной ткани F3/T3 (двусторонняя потеря костной ткани, включая большую часть одного или обеих бедренных мыщелков и повреждение метафиза тибии ниже головки малоберцовой кости) по классификации AORI.
Рентгенологическая послеоперационная картина демонстрирует восстановление дистального метафиза бедра и метафизарного сегмента проксимальной большеберцовой кости и суставной линии.
Послеоперационное наблюдение через 3 года. Опороспособность конечности была восстановлена.
Функциональная оценка коленного сустава по шкале WOMAC - 81. При контрольном осмотре: пациентка передвигается самостоятельно без дополнительной опоры. Рецидива воспаления за весь период наблюдения с момента ревизионной операции до настоящего времени не было отмечено.
ЗАКЛЮЧЕНИЕ
Мы считаем, что с увеличением числа пациентов с тяжёлыми деформациями и дефектами костей, вращающиеся шарнирные протезы коленного сустава будут играть всё более важную роль. Однако для этого типа коленного имплантата имеются недостаточные и разнородные данные относительно показаний к использованию и последующему клиническому результату. Некоторые авторы рассматривают их исключительно как ревизионные протезы и, в меньшей степени, как протезы для первичной имплантации, из-за повышенного риска расшатывания по сравнению с несвязанными протезами. Тем не менее существует согласие относительно показаний для вращающихся шарнирных протезов коленного сустава для решения таких проблем, как крупная потеря костной ткани, дисбаланс сгибательно-разгибательного промежутка, грубой связочной нестабильности коленного сустава, а также больших варусных и вальгусных деформаций. При предоперационном планировании ревизионного эндопротезирования коленного сустава возможно использование классификации костных дефектов AORI (2006) или вариантов восстановления суставной линии Innocenti (2013).
Хоммель и соавт. сообщают о многообещающих клинических результатах применения шарнирных протезов коленного сустава. Исследование проводилось у 62 пациентов (62 колена), со средним периодом наблюдения 6,8±2,2 года (диапазон, 2,8-11,7 лет), 15 мужчин и 47 женщин. Средний возраст на момент наблюдения составил 74,1±9,9 лет, средний индекс массы тела составил 30,2±5,2 кг/м2. Совокупный коэффициент выживаемости для системы шарнирных протезов коленного сустава с ревизией по любой причине составил 99,2% (95% доверительный интервал (ДИ), 94,5-99,9) через 5 лет и 89,4% (95% ДИ, 68,8-96,7) через 10 лет. Все обследованные пациенты заявили, что они удовлетворены имплантированным коленным протезом, со средним баллом боли 1,7±2,0 по визуальной аналоговой шкале для боли. Никаких рентгенологических признаков расшатывания или миграции имплантата не было обнаружено [20].
Таким образом, если стабильность колена не может быть достигнута с помощью стандартного первичного эндопротеза, то оправданно использование вращающегося шарнирного коленного протеза. Тщательный отбор пациентов и щадящая техника имплантации являются предпосылками для достижения хорошего послеоперационного результата и высокой степени удовлетворённости пациентов. Для уточнения долгосрочных клинических результатов необходимы дальнейшие перспективные исследования, сравнивающие используемые конструкции вращающихся шарнирных протезов коленного сустава различной степени связанности.
СПИСОК ИСТОЧНИКОВ
Загородний Н.В., Степанян Р.В., Захарян Н.Г., Ауде Ф.С., Алиев Р.Н., Безверхий С.В. и др. Эндопротезирование коленного сустава при нестабильности капсульно-связочного аппарата. Современная наука: актуальные проблемы теории и практики. Серия: Естественные и Технические Науки. 2018;(4): 135-141.
Корнилов Н.Н., Куляба Т.А. Артропластика коленного сустава. РНИИТО, 2012.
Загородний Н.В., Джалилов Ш.О., Скипенко Т.О., Ворошилов А.С. Проблема осложнений после эндопротезирования коленного сустава. Современная наука: актуальные проблемы теории и практики. Серия: Естественные и Технические Науки. 2019;(1):88-91.
Иржанский А.А., Куляба Т.А., Корнилов Н.Н. Валидация и культурная адаптация шкал оценки исходов заболеваний, повреждений и результатов лечения коленного сустава womac, kss и fjs-12. Травматология и ортопедия России. 2018;24(2):70-79.
Корнилов Н.Н., Куляба Т.А., Новоселов К.А. Эндопротезирование коленного сустава. Санкт-Петербург: Гиппократ; 2006.
Баитов В.С., Ганчуков Е.Б. Инфекционные осложнения при тотальном эндопротезировании коленного сустава. Современные проблемы науки и образования. 2017;(5).
Кавалерский Г., Сметанин С., Лычагин А. Классификация дефектов костной ткани при эндопротезировании коленного сустава. Врач. 2017;(4):70-71.
Тихилов Р.М., Корнилов Н.Н., Куляба Т.А., Филь А.С., Дроздова П.В. Принципы создания и функционирования регистров артроплас- тики коленного сустава. Вестник Российской военно-медицинской академии. 2014;1(45):220-226.
Шпиняк С.П., Барабаш А.П., Гиркало М.В. Двухэтапное ревизионное эндопротезирование при перипротезной инфекции коленного сустава. Кафедра травматологии и ортопедии. 2016;(3):58-61.
Engh GA. Classification of Bone Defects Femur and Tibia. In: Scuderi GR, Tria AJ. (eds) Knee Arthroplasty Handbook. New York, NY: Springer; 2006. p. 116-132.
Engh G, Parks N. The management of bone defects in revision total knee Arthroplasty. Instr Course Lect. 1997;46:227-236. PMID: 9143967Engh G, Ammeen D. Bone loss with revision total knee arthroplasty: defect classification and alternatives for reconstruction. Instr Course Lect. 1999;48:167-175. PMID: 10098042
Innocenti M, Matassi F, Carulli C, Soderi S, Villano M, Civinini R. Joint line position in revision total knee arthroplasty: the role of posterior femoral off-set stems. Knee. 2013;20(6):447-450. PMID: 2379067
Partington PF, Sawhney J, Rorabeck CH, Barrack RL, Moore J. Joint line restoration after revision total knee arthroplasty. Clin Orthop RelatRes. 1999; (367):165-171. PMID: 10546611
Hofmann AA, Kurtin SM, Lyons S, Tanner AM, Bolognesi MP. Clinical and radiographic analysis of accurate restoration of the joint line in revision total knee arthroplasty. J Arthroplasty. 2006; 21(8):1154-1162. PMID: 17162175
Porteous AJ, Hassaballa MA, Newman JH. Does the joint line matter in revision total knee replacement? J Bone Joint Surg Br. 2008;90(7):879- 884. PMID: 18591596
Laskin RS. Joint line position restoration during revision total knee replacement. Clin Orthop Relat Res. 2002;(404):169-171. PMID: 12439257
Bellemans J. Restoring the joint line in revision TKA: does it matter? Knee. 2004;11(1):3-5. PMID: 14967319
Lee J, Wang S, Kim K. Is there a difference in joint line restoration in revision Total knee arthroplasty according to prosthesis type? BMC Musculoskelet Disord. 2018;19(1):382. PMID: 30342515
Wilke K, Peggy D, Hommel P, Hommel H. Rotating Hinge Total Knee Arthroplasty RT-PLUS Solution: A Clinical and Radiographic FollowUp. J Orthopedics Rheumatol. 2016;3(1):4.
ИНФОРМАЦИЯ ОБ АВТОРАХ
Логвинов Николай Леонидович - кандидат медицинских наук, заведующий отделением травматологии ООО «Клиника научной медицины»;
Хорошков Сергей Николаевич - доцент, доктор медицинских наук, профессор кафедры травматологии, ортопедии и медицины катастроф ФГБОУ ВО «Российский университет медицины» МЗ РФ;
Ярыгин Николай Владимирович- член-корреспондент РАН, профессор, доктор медицинских наук, заведующий кафедрой травматологии, ортопедии и медицины катастроф ФГБОУ ВО «Российский университет медицины» МЗ РФ;
Голев Станислав Николаевич - врач травматолог-ортопед отделения травматологии и ортопедии № 1 ГБУЗ «ГКБ им. В.П. Демихова ДЗМ»;
Давидян Тигран Тевосович - врач травматолог-ортопед отделения травматологии и ортопедии №1 ГБУЗ «ГКБ им. В.П. Демихова ДЗМ»;
Теги: костные дефекты
234567 Начало активности (дата): 13.06.2025
234567 Кем создан (ID): 989
234567 Ключевые слова: костные дефекты, метафизарная потеря костной массы, ревизионное эндопротезирование коленного сустава, костный цемент
12354567899
Похожие статьи
Исторические аспекты становления и развития методов лучевой диагностики в перинатологииВосстановление функции пальцев кисти при дефектах суставов
Рентген на дому 8 495 22 555 6 8
Травмы рук, полученные при контакте с работающими электрическими мясорубками (обзор литературы, иллюстрированный собственными клиническими наблюдениями)
Первичное и ревизионное эндопротезирование тазобедренного сустава с восполнением дефектов вертлужной впадины



