 03.03.2025
03.03.2025
Первичное и ревизионное эндопротезирование тазобедренного сустава с восполнением дефектов вертлужной впадины
Эндопротезирование тазобедренного сустава при дефектах вертлужной впадины относится к сложному виду хирургических вмешательств, а поиск оптимальных конструкций и остеозамещающих материалов для воссоздания целостности вертлужной области является актуальной проблемой современной травматологии и ортопедии
ВВЕДЕНИЕ
Эндопротезирование тазобедренного сустава при дефектах вертлужной впадины относится к сложному виду хирургических вмешательств, а поиск оптимальных конструкций и остеозамещающих материалов для восстановления целостности вертлужной области на сегодняшний день является одной из актуальных проблем современной травматологии и ортопедии. Образование дефектов в области вертлужной впадины свойственно врожденной дисплазии, системным заболеваниям соединительной ткани, переломам тазовых костей. Костные дефекты формируются при развитии нестабильности имплантов, после резекции костных опухолей, а также вследствие выполненных ранее периацетабуляр- ных остеотомий [1].
Выбор методов восполнения дефектов вертлужной впадины определяется в зависимости от количества и качества оставшейся костной ткани, целостности ацетабулярных колонн и стабильности тазового кольца. Небольшие дефекты при первичном эндопротезировании заполняют неструктурными аутотрансплантатами из резецированной головки бедра или чипсами из аллокости. Более обширные дефекты требуют применения массивных опорных трансплантатов, для которых подходит структурная аллокость, ксенокость или искусственные остеозамещающие материалы (кальций-фосфатная керамика, металлические и титановые аугменты) [2, 3]. В ряде случаев для заполнения дефектов используется костный цемент; однако большинство исследователей в своих работах описывают негативное влияние цемента на костную ткань, приводят данные о большом числе поздних осложнений и неудовлетворительных результатах эндопротезирования [4].
Основной задачей восполнения обширного дефекта вертлужной впадины является восстановление целостности костной структуры впадины, ее полусферической формы и центра ротации тазобедренного сустава для обеспечения первично стабильной имплантации вертлужного компонента [5].
С конца прошлого века для замещения дефектов вертлужной области как при первичном, так и при ревизионном эндопротезировании стали применять укрепляющие и антипротрузионные кольца с опорой на наружные края впадины (кольца Мюллера (Muller), Окснера, Ганса, Бурх - Шнейдера (Burch - Schneider), Безноско и др.). Наиболее известно укрепляющее опорное кольцо, которое было разработано М. Мюллером в 1977 г. Как правило, размеры колец соизмеримы с впадиной, изготовлены из листового металла, имеют отогнутые края для опоры и множество отверстий под винты для крепления к тазовой кости. Для повышения остеоинтегративных качеств ацетабулярная часть кольца может иметь пористое покрытие. Опорное кольцо Бурх - Шнейдера предназначено для дефектов, которые не перекрываются кольцом Мюллера. Применение опорных колец Мюллера и Бурх - Шнейдера подразумевает первоначальное заполнение дефекта аутокостью или аллокостью, сверху костного трансплантата press-fit устанавливается опорная конструкция. В опорное кольцо на цемент крепится стандартная цементная чашка [6].
По данным J. Schatzker et al., за период наблюдения от одного до трех лет после двадцати пяти операций эндопротезирования тазобедренного сустава (20 — опорное кольцо Мюллера, 5 — Бурх - Шнейдера) получены удовлетворительные результаты, что подтверждает логичность их применения при лечении пациентов с дефектами вертлужной впадины [7]. В настоящее время все чаще используются аугменты из трабекулярного металла, а также индивидуальные трехфланцевые опорные конструкции, которые изготавливают при помощи компьютерного моделирования в случаях обширного дефекта и прерывистости впадины [8]. Результаты, полученные А.Н. Коваленко с соавт., показывают, что реконструкция вертлужной впадины с использованием вышеописанных методик требует учитывать индивидуальные анатомические особенности пациента, предусмотреть хирургический доступ и технологию имплантации, иначе имплантат невозможно будет установить. Кроме того, первый опыт индивидуального протезирования не всегда был удачным, и процент неудовлетворительных результатов оставался высоким [9].
Цель работы — анализ результатов первичного и ревизионного эндопротезирования тазобедренного сустава с восполнением дефектов вертлужной впадины.
МАТЕРИАЛЫ И МЕТОДЫ
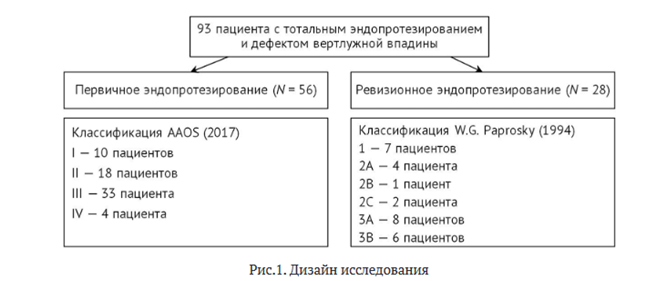
Работа выполнена в рамках госзадания 124020700095-4 ФГБОУ ВО УГМУ МЗ РФ на 2024-2026 гг. Исследование проведено с соблюдением этических принципов Хельсинской декларации и одобрено локальным этическим комитетом ФГБОУ ВО УГМУ (протокол от 22.10.21 № 9). Все пациенты дали информированное добровольное согласие на участие в исследовании. Дизайн исследования представлен на рисунке 1.
Материал исследования составили данные 93 пациентов с выполненным первичным и ревизионным тотальным эндопротезированием тазобедренного сустава при наличии костных дефектов вертлужной впадины различной степени выраженности.
93 пациента с тотальным эндопротезированием и дефектом вертлужной впадины
Первичное эндопротезирование выполнено 65 пациентам (мужчин — 21, женщин — 44), из них 26 пациентов прооперированы в ГАУЗ СО СОКБ № 1, Екатеринбург (СОКБ № 1); 39 — в НМИЦ ТО имени академика Г.А. Илизарова, Курган (Центр Илизарова). Средний возраст пациентов при первичном протезировании составил (56 ± 1,4) года.
Бесцементное эндопротезирование выполнено 49 пациентам, протезы цементной фиксации установлены 16 пациентам. Имплантированы следующие системы протезов: Aesculap (n = 19), Smith&Nephew (n = 13), De Puy (n = 21), Zimmer (n = 12).
Ревизионное эндопротезирование выполнено 28 пациентам (мужчин — 2, женщин — 26), из них 19 пациентов прооперированы в СОКБ № 1; 9 — в Центре Илизарова. Средний возраст пациентов составил (61,0 ± 2,4) года.
Бесцементное ревизионное протезирование выполнено 12 пациентам, цементное — 16 пациентам. Были установлены следующие системы протезов: Aesculap (n = 6), Smith&Nephew (n = 5), De Puy (n = 11), Zimmer (n = 6).
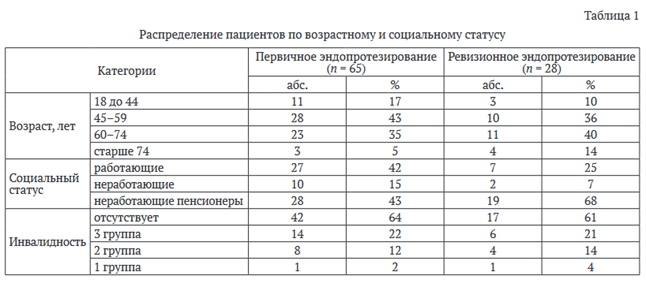
Распределение по возрасту, социальному статусу и инвалидности представлено в таблице 1.
Первичное эндопротезирование в группе больных с ревизионным протезированием ранее выполнено в СОКБ № 1 в четырех случаях; в Центре Илизарова — в одном случае. Остальные 23 пациента первично прооперированы в травматологических стационарах Свердловской и Курганской областей.
Для систематизации первичных дефектов использовали классификацию Американской ассоциации травматологов ортопедов (AAOS, 2017) [10] ввиду ее простоты и возможности предоперационного планирования вариантов костной пластики. По классификации AAOS (2017) выделяют четыре типа дефектов вертлужной впадины: тип I представляет собой сегментарный дефект кости в верхнем, переднем или заднем отделе впадины; тип II — кавитарный дефект (костная полость) в верхнем, переднем или заднем отделе впадины; тип III — комбинированный сегментарно-кавитарный дефект; тип IV — явный или скрытый разрыв тазового кольца [10].
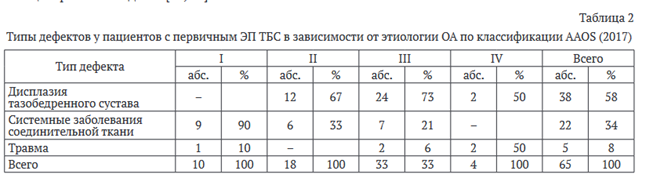
Типы дефектов у пациентов с первичным ЭП ТБС в зависимости от этиологии остеоартроза (ОА) по классификации AAOS (2017) представлены в таблице 2. Ведущей причиной формирования дефектов вертлужной впадины в случаях первичного протезирования явилась дисплазия тазобедренного сустава. У 36 пациентов дисплазия соответствовала II-III типу Crow, в двух случаях — IV типу [11, 12, 13]. Формирующийся неоартроз на уровне верхнего края вертлужной впадины и краниальное смещение головки бедра при дисплазии по Crow II-III [11] приводили к формированию дефектов в области крыши впадины, соответствующих типам II и III по классификации AAOS (2017).
При системных заболеваниях соединительной ткани (РА, системная красная волчанка) на фоне порозной костной ткани формировалась протрузионная деформация впадины со смещением центра ротации сустава медиально, что приводило к формированию дефекта костной ткани впадины в ее центральных отделах [14, 15].
Посттравматические деформации впадины формируются вследствие травм — переломо-вывихов тазобедренного сустава. Р.М. Тихилов с соавт. подразделяют посттравматические деформации вертлужной впадины на три группы: первая — пациенты с переломами дна вертлужной впадины с небольшим смещением отломков или после остеосинтеза задних отделов; вторая — после перелома задних отделов вертлужной впадины с дефектом в области задней стенки и/или крыши вертлужной впадины различной протяженности; третья — с полным нарушением анатомии вертлужной впадины в результате дефекта задней стенки, крыши, а также в результате неправильного сращения костных фрагментов [16]. И если в первой группе возможно проведение первичной стандартной имплантации бесцементной чашки, то во второй и третьей группах для имплантации тазового компонента обязательно требуется применение костной пластики, аугментов и ревизионных опорных колец. Наиболее часто встречаются посттравматические дефекты вертлужной впадины в заднее-верхнем отделе, которые сочетаются с подвывихом бедра и стойкой сгибательно-приводящей контрактурой. Впадина при этом овальновытянутой формы, задняя стенка разрушена, головка бедренной кости смещена кзади и кверху.
Для систематизации ревизионных дефектов использовали классификацию W.G. Paprosky [17]. Данная классификация подробно отражает анатомическую локализацию дефекта, позволяет во время предоперационного планирования выбрать оптимальный способ восполнения дефицита костной ткани с учетом возможных технических трудностей по ходу вмешательства. По классификации W.G. Paprosky выделяют 3 типа дефектов вертлужной впадины. Дефект 1 типа предполагает наличие единичной или множественных костных кист, общий объем которых не превышает 10 мм3. Подтип 2А представляет собой верхне-медиальный кавитарный дефект; 2В дефекты — сегментарные верхнелатеральные дефекты, когда потеря кости не превышает 1/3 окружности впадины; 2С — дефект медиальной стенки впадины; 3А дефект — это верхне-латеральная миграция впадины или «up and out», интактная медиальная опора (латеральнее линии Келера) и наблюдается лизис в области седалищной кости; 3В дефект — это верхне-медиальная миграция или «up and in», нет медиальной и верхней опоры (разрыв линии Келера), выраженный лизис седалищной кости (менее 15 мм выше от верхнезапирательной линии), полное разрушение «фигуры слезы»; 4 тип дефекта — явный или скрытый разрыв тазового кольца.
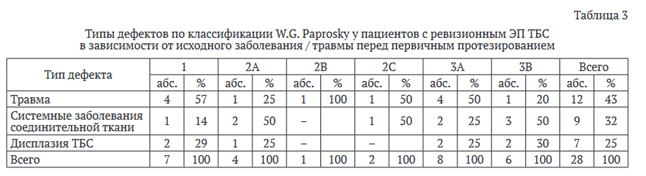
Типы дефектов по классификации W.G. Paprosky у пациентов с ревизионным ЭП ТБС в зависимости от исходного заболевания/травмы перед первичным протезированием представлены в таблице 3.
У пациентов с ревизионным эндопротезированием ведущим поводом выполнения первичного эндопротезирования была предшествующая травма. Из 28 случаев ревизионного протезирования ранняя нестабильность (до 5 лет после первичного эндопротезирования) развилась у 15 пациентов (54 %), поздняя нестабильность (более 5 лет) — у 13 (46 %).
Методы исследования
Клинический. Оценены среднесрочные показатели функции тазобедренного сустава по шкале W.H. Harris [16]: 90 и более баллов оценивали как отличный результат; 80-89 баллов — хороший результат; 70-79 баллов — удовлетворительный результат; 69 баллов и менее — неудовлетворительный результат.
Рентгенологический. Оценку обзорной рентгенограммы таза проводили в прямой проекции, пораженного тазобедренного сустава с бедром — в прямой и боковой проекциях.
Метод компьютерной томографии применяли для уточнения степени костного дефекта вертлужной впадины по классификации AAOS для первичного эндопротезирования, W.G. Paprosky — для ревизионного эндопротезирования.
Статистический метод. В работе использовали пакет анализа Statistica 8.0. Данные описательной статистики представлены в виде M ± SD; Ме, где M — среднее значение признака, SD — среднеквадратичное отклонение.
РЕЗУЛЬТАТЫ
Сведения о способах костной пластики пациентов и среднесрочных результатах приведены в таблице 4.
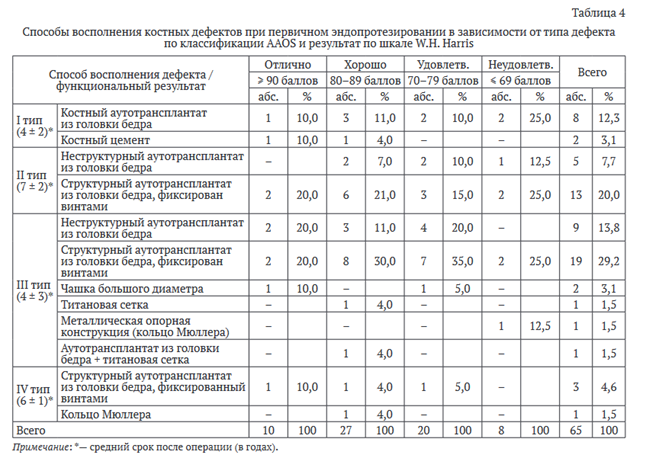
Исходя из анализа таблицы 4, можно отметить, что при первичном эндопротезировании дефекты I типа в двух случаях были заполнены костным цементом, что вполне допустимо при цементном протезировании, которое было выполнено в данных двух случаях, в восьми случаях (три бесцементных протеза и пять цементных) дефекты заполняли костной крошкой/костными чипсами из резецированной головки бедра.
При II типе использовали структурные и неструктурные аутотрансплантаты, что давало хорошие функциональные результаты. Из них три протеза цементной фиксации и 15 бесцементных. При этом типе дефекта отмечено всего три неудовлетворительных результата, связанных с преждевременным лизисом трансплантата; в одном из этих случаев использовалась бесцементная техника и два протеза были цементной фиксации.
Наибольшее разнообразие методик возмещения дефектов применялось при III типе. При данном типе дефекта имплантированы пять протезов цементной фиксации: два в комбинации со структурным аутотрансплантатом, фиксированным на винты, с хорошим и удовлетворительным результатом; один — с применением титановой сетки в качестве опорной структуры с аутопластикой дефекта, один цементный протез установлен с пластикой дефекта крошкой из аутокости с удовлетворительным результатом; неудовлетворительный результат получен при установке цементного протеза с опорным кольцом Мюллера. В остальных 28 случаях при III типе дефекта устанавливались бесцементные протезы. Наилучшие результаты были отмечены при применении структурных аутотрансплантатов, фиксированных дополнительно винтами.
Дефекты IV степени при первичном эндопротезировании встретились в трех случаях и были восполнены массивными структурными аутотрансплантатами, фиксированными на несколько винтов к тазовой кости, что позволило получить хорошие результаты, все три протеза бесцементной фиксации. Цементный протез устанавливался в одном случае вместе с кольцом Мюллера, получен удовлетворительный результат.
Способы восполнения костных дефектов при ревизионном эндопротезировании и оценка функции тазобедренного сустава по шкале W.H. Harris представлены в таблице 5.
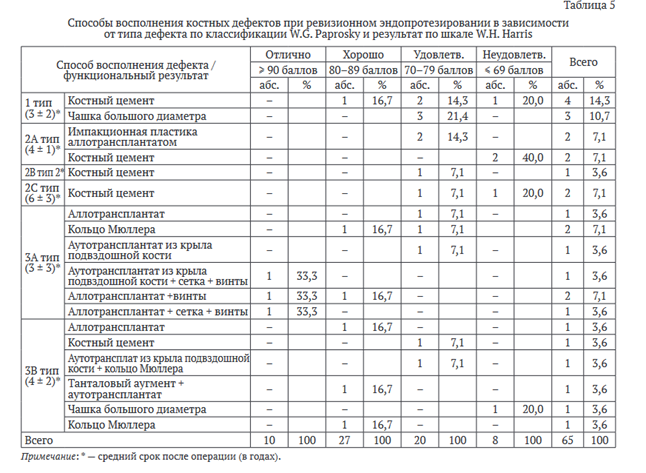
Согласно данным, представленным в таблице 5, при ревизионных операциях для восполнения дефектов 1 типа (всего семь пациентов) в четырех (57 %) случаях при выполнении цементного протезирования дефекты заполнялись костным цементом. При применении чашек большего диаметра использовалась бесцементная фиксация.
У четырех пациентов с типом дефекта 2А в двух случаях применена цементная техника, дефекты заполнены цементом. В двух случаях использована импакционная костная пластика с последующей бесцементной фиксацией чашки. При 2В (один пациент) и 2С (два пациента) дефектах во всех случаях применяли цементную фиксацию чашки. Других остеозамещающих материалов, кроме цемента, не применяли. В случае 2С дефекта получен неудовлетворительный результат.
При 3А дефектах (восемь пациентов) бесцементная техника использовалась вместе с ауто- и аллотрансплантатами, фиксированными press-fit, а также с ауто- и аллотрансплантатами, фиксированными винтами. В остальных случаях использовали цементную технику.
Бесцементное протезирование при дефектах 3В типа (всего шесть пациентов) применяли у трех пациентов: вместе с аутокостью, фиксированной press-fit, чашкой большого диаметра и металлической опорной конструкцией. У 3 пациентов использовалась цементная фиксация: с кольцом Мюллера, с опорной конструкцией из тантала и в одном случае дефект был заполнен исключительно цементом с удовлетворительным результатом.
В зависимости от типа дефекта впадины по классификации W.G. Paprosky (для ревизионного ЭП) и AAOS (для первичного ЭП) нами разработан алгоритм выбора способа замещения костного дефекта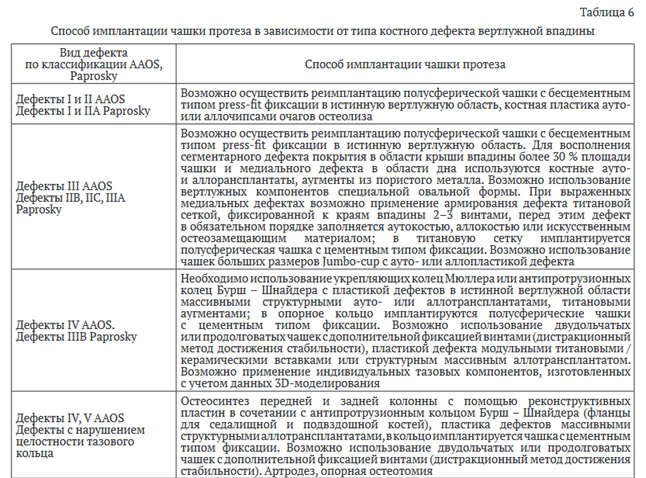
В качестве клинического примера выполнения трех последовательных ревизионных замен тазового компонента в течение пяти лет после первичного протезирования приводим следующее наблюдение.
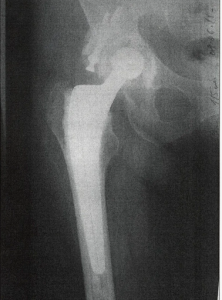
Пациентка А. с диагнозом «Двусторонний диспластический коксартроз III стадии, подвывихи бедер по Crow IV» обратилась в клинику в возрасте 55 лет с жалобами на постоянные боли в тазобедренных суставах (больше слева), ограничение движений, хромоту (рис. 2).
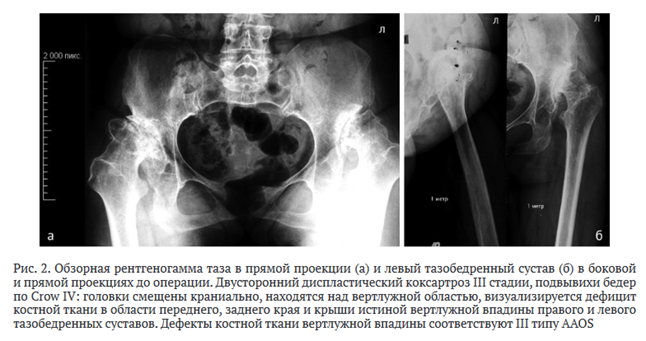
Из анамнеза: в возрасте 3,5 лет выявлен врожденный двусторонний вывих бедер, по поводу которого лечилась консервативно методом вытяжения и этапными гипсовыми повязками, однако вправление вывихов не было достигнуто. С возраста 30 лет отмечала постоянные боли в тазобедренных суставах. После обращения в клинику и комплексного обследования было показано эндопротезирование тазобедренных суставов (рис. 2).
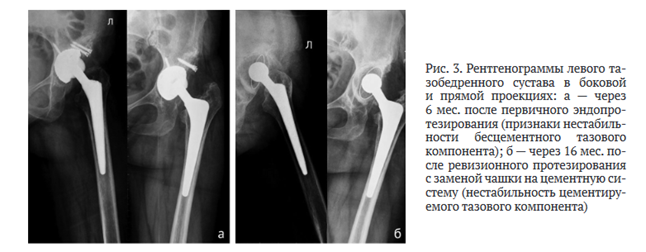
В ноябре 2009 г. выполнено эндопротезирование левого тазобедренного сустава бесцементным протезом Smith&Nephew с пластикой крыши вертлужной впадины аутотрансплантатом из резецированной головки бедра. Дефект костной ткани вертлужной впадины III AAOS адекватно восполнен. Ранний послеоперационный период протекал без осложнений. Однако через четыре месяца вновь появились боли в области оперированного сустава, на рентгенограммах выявлены вероятностные признаки нестабильности тазового компонента: выраженные участки просветления (лизиса) костной ткани на границе чашки протеза и тазовой кости во II и III ацетабулярных зонах De Lee и Charnley (рис. 3, а). Через шесть месяцев после первичной имплантации (05.05.20l0) выполнено ревизионное эндопротезирование левого тазобедренного сустава по поводу ранней нестабильности бесцементной чашки.
Установлена чашка цементной фиксации, признаки нестабильности которой появились через 16 мес. после повтороной ревизии: визуализировалась увеличенная в размерах впадина овальной формы с серповидным просветлением в нижних ее отделах, тазовый компонент располагался в краниальном ее отделе, дефект ЗА Paprosky (рис. 3, б).
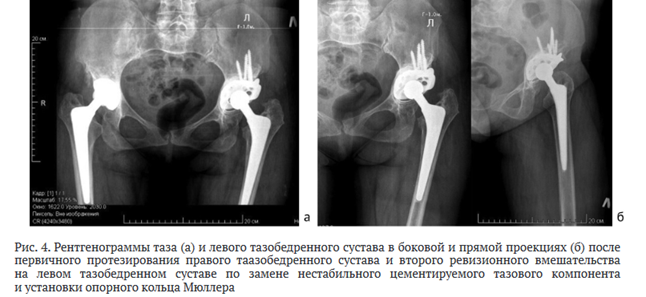
Между повторными ревизиями на левом тазобедренном суставе (до развития повторной нестабильности уже цементируемого тазового компонента) 19.05.2010 г. выполнено первичное бесцементное эндопротезирование правого тазобедренного сустава системой Smith&Nephew с импакционной пластикой костной крошкой из резецированной головки бедра (рис. 4, а).
В сентябре 2011 г. выполнено второе ревизионное вмешательство по замене нестабильного цементируемого тазового компонента: выполнена костная пластика аллочипсами и установлено опорное кольцо Мюллера с имплантацией в него тазового компонента на цемент; бедренный компонент оставался стабильным (рис. 4).
Через три года после второй ревизии пациентка вновь отметила появление болей в левом тазобедренном суставе, паху, с иррадиацией в бедро и коленный сустав. В феврале 2015 г. выполнена третья ревизия левого тазобедренного сустава. Интраоперационно выявлена нестабильность опорной конструкции Мюллера, которая удалена вместе с остатками цемента. Некоторые технические трудности возникли при освобождении пазов головок винтов для отвертки от костного цемента. Выявлен дефект передней стенки и значительный дефект свода вертлужной впадины (3В Paprosky).
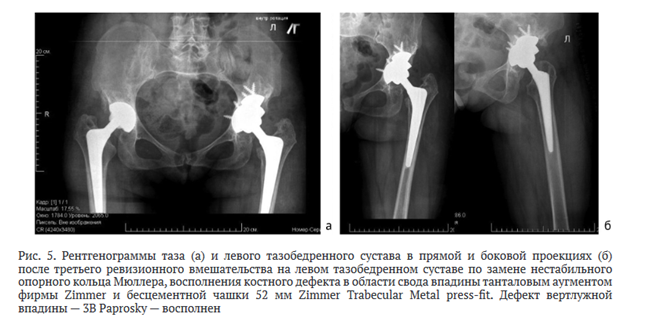
Впадина поочередно обработана фрезами от 40 до 50 мм и костными ложками до кровоточивости. В область дефекта свода вертлужной впадины установлен танталовый аугмент фирмы Zimmer 50 мм высотой 15 мм, фиксирован двумя винтами 6,5 х 35 мм и 6,5 * 30 мм. После этого впадина доработана фрезами 51 и 52 мм с центрацией в истинную вертлужную область, выполнена пластика истонченного дна впадины костной крошкой (с фрез после обработки). Установлена стабильно чашка 52 мм Zimmer Trabecular Metal press-fit. Фиксация чашки дополнена тремя спонгиозными винтами 6,5 * 35 мм (1) и 6,5 * 20 мм (2). Ножка оставалась стабильной. Установлена металлическая головка + 4 мм (L) Smith&Nephew. После вправления сустав стабильный, длина ног одинаковая. На рентгенограммах положение всех компонентов эндопротеза биомеханически правильное (рис. 5).
На момент исследования (2024 г.) прошло 9 лет после третьей ревизионной операции по замене тазового компонента. Пациентка передвигается с тростью, жалоб нет, хромоты нет, пользуется общественным транспортом.
Потребность в обезболивающих препаратах возникает эпизодически, после длительной физической нагрузки. Конечность находится в правильном положении. Объем движений в тазобедренных суставах восстановлен.
Функциональный результат по шкале W.H. Harris оценен как хороший (85 баллов).
ОБСУЖДЕНИЕ
Анализируя представленный выше клинический случай, как череду неудач ревизионных вмешательств, следует отметить, что исходно у больной имелась сложная двусторонняя патология тазобедренных суставов с формированием неоартрозов обеих надацетабулярных областей и высоких подвывихов бедер по Crow III—IV степени на фоне выраженных дегенеративных изменений суставов и окружающих мышц. Несмотря на то, что при первичном эндопротезировании левого тазобедренного сустава был правильно выбран способ возмещения костного дефекта в области свода аутотрансплантатом из резецированной головки бедра, и чашка протеза установлена биомеханически правильно, в истинную вертлужную область, через шесть месяцев развилась ее ранняя нестабильность.
Очевидно, в развитии ранней нестабильности тазового компонента основную роль сыграла перегрузка оперированного сустава в связи с тем, что пациенты практически сразу неосознанно начинают нагружать оперированный сустав, который уже не болит, по сравнению с неоперированным. Даже такой короткий временной промежуток повышенной нагрузки на эндопротез в раннем послеоперационном периоде привел к появлению болевого синдрома и нестабильности тазового компонента: вторичная стабилизация компонента за счет остеоинтеграции вследствие повышенной нагрузки не произошла. В случаях двусторонней тяжелой патологии суставов желательно оба сустава оперировать в одну операционную сессию или с временным промежутком не более 2-4 недель [19, 20].
При первой ревизии бесцементная чашка была заменена на цементируемую. Однако впадина уже была изменена (дефект типа III AAOS), увеличена в продольном размере, и не произошло адекватного замещения расширенной впадины тазовым компонентом. Чашка была установлена в верхние отделы впадины выше истиной вертлужной области, и нижний сектор имплантационного ложа остался незаполненным ни самим компонентом, ни костью, ни цементом. Поэтому развилась нестабильность тазового компонента уже через 16 мес. после ревизии. Потребовалось второе ревизионное вмешательство с установкой опорного кольца Мюллера и костной пластикой аллочипсами. Кольцо Мюллера также было установлено в верхние отделы впадины, выше истинной вертлужной области. Данный факт привел к ассиметричной нагрузке на тазовые кости (перегрузке левого тазобедренного сустава) и развитию нестабильности опорной конструкции. Как при первой, так и при второй ревизии, когда костный дефицит еще был умеренным (3А Paprosky), можно было применить тазовый компонент большого диаметра — Jumbo-cup. Применение чашки большого размера обеспечивает латерализацию и небольшое каудальное смещение ротационного центра тазобедренного сустава. Биомеханика сустава, тем самым, приближается к нормальной, при этом площадь контакта чашки Jumbo-cup с костным ложем достаточно велика, что позволяет надеяться на успешную вторичную стабилизацию за счет остеоинтеграции и на хороший исход.
Удаление нестабильного опорного кольца Мюллера, фиксирующих его винтов, костного цемента при третьей ревизии еще более увеличило костный дефицит в области вертлужной впадины до формирования обширного дефекта свода вертлужной впадины и ее переднего края (дефект типа 3В Paprosky).
При третьей ревизии костный дефект типа 3В Paprosky в области свода впадины был восполнен танталовым аугментом фирмы Zimmer, бесцементной чашкой 52 мм Zimmer Trabecular Metal, имплантированной press-fit в истинную вертлужную область. Адекватное возмещение дефекта, правильный выбор размера аугмента и чашки, биомеханически правильное ее позиционирование в истинной вертлужной области позволило достигнуть ее стабильного положения и хорошего отдаленного результата. Таким образом, следует отметить важность полноценного восполнения дефектов впадины для обеспечения стабильности протеза и возможности имплантировать чашку в истинную вертлужную область для восстановления правильных анатомических взаимоотношений в суставе.
В настоящее время существуют различные варианты имплантации тазового компонента при дефиците костной ткани вертлужной впадины: установка стандартной полнопрофильной чашки бесцементной фиксации в истинную вертлужную область с костной пластикой дефекта; установка чашки в истинную вертлужную область с частичным ее недопокрытием и пластикой костными чипсами; установка чашки в более вертикальном положении; установка чашки со смещением центра ротации выше истинной вертлужной области в сохранившуюся кость в области свода; установка чашки цементной фиксации в опорные и антипротрузионные конструкции. При всех этих вариантах возможно использование в качестве остеозамещающего материала структурной аутокости из резецированной головки бедра, массивных структурных аллотрансплантатов, костных ауто- и аллочипсов, искусственного остеозамещающего материала из титана и керамики, а также их комбинации.
Их анализа данных отечественных и зарубежных исследователей следует, что наиболее широко применяемым методом восполнения дефектов при первичном эндопротезировании остается пластика костной крошкой / чипсами из аутологичной головки бедренной кости. Такая пластика хорошо воссоздает сферичность впадины и при успешной остеоинтеграции обеспечивает механическую поддержку чашки на всем ее протяжении и долгосрочное функционирование протеза. Однако объем остеозамещающего материала при этом очень ограничен и не позволяет восполнить обширный дефект. При неудачной реваскуляризации аутокость со временем может лизироваться, что приводит к потере стабильности [21]. Измельченные костные аллотрансплантаты также широко используют для пластики небольших дефектов, дополняя любую методику. Иногда их используют и как самостоятельный метод аугментации, — импакционная костная пластика. Обычно при этом используется бесцементная чашка press-fit, реже цементируемая чашка. Поверхность тазового компонента в этом случае имеет незначительный контакт с костью пациента, а контакт с донорской аллокостью может приближаться к 100 % [2].
При значительных дефектах костной ткани (тип 2В, 3A, 3B по Paprosky) одним из вариантов пластики является использование структурных ауто- или аллотрансплантатов, применение которых позволяет восстановить центр ротации и сформировать костную опору для возможных будущих ревизий. Неудовлетворительные результаты при этом способе обусловлены лизисом аллокости, если с течением времени не произошла её реваскуляризация [20]. Длительная жизнеспособность аллокости с сохранением ее опорных характеристик остается спорной [22, 23].
Цементную чашку широко использовали при первых операциях эндопротезирования тазобедренного сустава, особенно при ревизионных вмешательствах. Однако результаты ее применения на средних и длительных сроках оказались неудовлетворительными. Поэтому в настоящее время при первичном протезировании предпочтение отдается тазовым компонентам бесцементной фиксации. В случае необходимости цементной фиксации толщина цементной мантии должна быть минимальной. Дефицит толщины медиальной стенки под цементной мантией следует восполнить импакционной костной пластикой [4, 24, 25].
При выполнении ревизионных вмешательств на тазобедренном суставе следует учитывать выраженный остеопороз, рубцовые изменения капсулы, слабость окружающих мышц.
Удаление протеза требует дополнительных физических усилий и сопряжено с риском перипротезных переломов, а также с увеличением протяженности и глубины дефектов костной ткани в области имплантационного ложа [26].
Одним из вариантов ревизионной замены тазового компонента при умеренной потере костной ткани является использование чашек больших размеров Jumbo-cup. Однако при несостоятельности краев вертлужной впадины данный метод неприемлем. Отрицательным моментом имплантации Jumbo-cup является то, что большой компонент, являясь в то же время и опорной конструкцией, перекрывающей дефект, ограничивает возможности регенерации тазовой кости [15].
При наличии больших дефектов 2B, 2С, 3А, 3В Paprosky выполняют пластику дефекта измельченной или структурной аллокостью, устанавливают антипротрузионное кольцо или чашки из трабекулярного металла с фиксацией press-fit и на винты. Затем в металлическую чашку или кольцо на цемент устанавливают пластмассовую чашку, при нестабильности тазового кольца требуется остеосинтез задней колонны. По исследованиям Р.М. Тихилова с соавт., применение антипротрузионного опорного кольца позволяет создать опору для тазового компонента, перенося нагрузку на оставшиеся участки подвздошной и седалищной кости. Имплантацию опорного кольца дополняют костной аллопластикой структурным или измельченным трансплантатом, имплантацией чашки из трабекулярного металла, остеосинтезом задней колонны [27, 28].
В последние годы все большее распространение получили компоненты из высокопористых материалов, в частности трабекулярного металла, которые могут быть использованы как для простых ревизий, так и для более сложных случаев, включающих остеопороз, тяжелые костные дефекты и разрыв тазового кольца [29]. Высокая пористость и сцепление с костью, близкий к костной ткани модуль упругости у конструкций из трабекулярного металла обеспечивают условия для оптимальной первичной и вторичной фиксации компонента, при этом дополнительные отверстия могут быть выполнены высокоскоростной дрелью в любом участке такого компонента для фиксации винтами к тазовой кости.
Для достижения приемлемой первичной стабильности возможно покрытие конструкции костью менее 50 % [30, 31].
Достижение положительного результата лечения и долгосрочного функционирования протеза возможно только при комплексном подходе к пластике дефекта. Дефекты I и II AAOS и 1 и 2а Paprosky позволяют использовать импакционную костную пластику резорбируемыми неструктурными трансплантатами. Дефекты III и IV AAOS и 2B, 2С, 3А, 3В Paprosky требуют применения структурных трансплантатов с дополнительной фиксацией. Предпочтительнее использовать комбинированную костную пластику, включающую нерезорбируемые и резорбируемые материалы.
Перспективными как для первичного, так и для ревизионного эндопротезирования, безусловно, являются тазовые компоненты бесцементной фиксации, которые демонстрируют хорошую выживаемость спустя многие годы функционирования протеза [32].
ЗАКЛЮЧЕНИЕ
Эндопротезирование тазобедренного сустава (первичное или ревизионное) при наличии костного дефекта вертлужной впадины является сложным хирургическим вмешательством, технические аспекты которого окончательно не решены. Дефекты вертлужной впадины в своих анатомических проявлениях многообразны, что создает определенные трудности при выборе тазовых компонентов, аугментов, способов их фиксации к тазовой кости. Длительное и безболезненное функционирование эндопротеза тазобедренного сустава при дефектах вертлужной впадины обеспечивается восстановлением сферичной формы acetabulum и центра ротации сустава в истинной вертлужной области, адекватным восполнением дефицита костной ткани, надежной первичной фиксацией чашки протеза с обеспечением условий для вторичной стабилизации компонента за счет остеоинтеграции.
Разработанный алгоритм выбора способа замещения костного дефекта вертлужной впадины и имплантации чашки протеза позволяет практическому врачу адекватно оценить свой опыт, хирургические навыки и возможности клиники в обеспечении сложных реконструктивных операций на тазобедренном суставе.
Существенные сложности хирургического лечения больных с дефектами вертлужной впадины обусловлены недостаточным развитием законодательной базы в области применения индивидуальных конструкций, новых материалов и техник восполнения костного дефицита.
Конфликт интересов отсутствует.
Источник финансирования. Не заявлен.
СПИСОК ИСТОЧНИКОВ
Пронских А.А., Романова С.В., Лукинов В.Л. и др. Эндопротезирование тазобедренного сустава у пациентов с посттравматическими дефектами и деформациями вертлужной впадины. Травматология и ортопедия России. 2022;28(4):66-78. doi: 10.17816/2311-2905-2001
Гольник В.Н., Пелеганчук В.А., Джухаев Д.А. и др. Импакционная костная пластика как метод выбора в замещении дефектов вертлужной впадины при ревизионном эндопротезировании тазобедренного сустава: серия клинических случаев. Гений ортопедии. 2024;30(2):245-254. doi: 10.18019/1028-4427- 2024-30-2-245-254. EDN: LCXHIZ.
Назаров В.А., Закревский К.В., Согомонян Л.В. Комбинация известных способов костной аутопластики при эндопротезировании диспластического тазобедренного сустава II степени по Hartofilakidis у пациента с тяжелой сопутствующей патологией. Уральский медицинский журнал. 2023;22(4):85-91. doi: 10.52420/2071-5943-2023-22-4-85-91
Clement ND, van der Linden M, Keating JF. Higher rate of complications with uncemented compared to cemented total hip arthroplasty for displaced intracapsular hip fractures: A randomised controlled trial of 50 patients. Eur J Orthop SurgTraumatol. 2021;31(3):587-594. doi: 10.1007/s00590-020-02808-x
Коваленко А.Н., Тихилов Р.М., Шубняков И.И. и др. Дизайн индивидуальных вертлужных компонентов: влияние типа дефекта на вид конструкции. Российский журнал биомеханики. 2021;25(2):159-172. doi: 10.15593/ RZhBiomeh/2021.2.04
Ковалдов К.А., Морозова Е.А., Герасимов Е.А. и др. Результаты лечения пациентов с массивными костными дефектами вертлужной впадины. Политравма. 2024;(1):27-35. doi: 10.24412/1819-1495-2024-1-27-35
Schatzker J, Glynn MK, Ritter D. A preliminary review of the Muller acetabular and Burch-Schneider antiprotrusio support rings. Arch Orthop Trauma Surg(1978). 1984;103(1):5-12. doi: 10.1007/BF00451312
Загородний Н.В., Алексанян О.А., Чрягян Г.А. и др. Реконструкция вертлужной впадины с использованием компонентов из трабекулярного металла. Вестник травматологии и ортопедии им. Н.Н. Приорова. 2019;(1):5-10. doi: 10.17116/vto20190115
Коваленко А.Н., Тихилов Р.М., Шубняков И.И. и др. Ревизии вертлужных компонентов индивидуальными конструкциями с минимальным сроком наблюдения 12 месяцев: функциональные результаты, качество жизни и удовлетворенность пациентов. Травматология и ортопедия России. 2019;25(1):21-31. doi: 10.21823/2311-2905- 2019-25-1-21-31
DAntonio JA, Capello WN, Borden LS, et al. Classification and management of acetabular abnormalities in total hip arthroplasty. Clin OrthopRelatRes. 1989;(243):126-137.
Crowe JF, Mani VJ, Ranawat CS. Total hip replacement in congenital dislocation and dysplasia of the hip. J Bone Joint Surg Am. 1979;61(1):15-23.
Волокитина Е.А., Колотыгин Д.А. Особенности первичной и ревизионной имплантации бесцементного тазового компонента при диспластическом коксартрозе. Травматология и ортопедия России. 2009;(3):119-121. doi: 10.17816/2311-2905-1913
Волокитина Е.А., Колотыгин Д.А. Эндопротезирование тазобедренного сустава при деформациях тазовой кости: особенности предоперационного проектирования и хирургической техники. Вестник травматологии и ортопедии Урала. 2013;1(2):42-48.
Ершов А.С., Волокитина Е.А. Эндопротезирование тазобедренного сустава у больных ревматоидным артритом. Уральский медицинский журнал. 2022;21(2):26-37. doi: 10.52420/2071-5943-2022-21-2-26-37
Удинцева М.Ю., Кутепов С.М. Причины ревизий эндопротезов тазобедренного сустава у больных ревматоидным артритом. Уральский медицинский журнал. 2022;21(2):63-66. doi: 10.52420/2071-5943- 2022-21-2-63-66
Тихилов Р.М., Шубняков И.И., Чиладзе И.Т. и др. Тотальное эндопротезирование тазобедренного сустава с использованием аугментов из трабекулярного металла при последствиях переломов вертлужной впадины. Травматология и ортопедия России. 2011;17(1):76-81. doi: 10.21823/2311-2905-2011-0-1-76-81
Paprosky WG, Perona PG, Lawrence JM. Acetabular defect classification and surgical reconstruction in revision arthroplasty. A 6-year follow-up evaluation. J Arthroplasty. 1994;9(1):33-44. doi: 10.1016/0883-5403(94)90135-x
Волокитина Е.А., Удинцева М.Ю., Ершов А. С., Кутепов С.М. Восполнение дефектов вертлужной впадины при первичном и ревизионном эндопротезировании. Учебное пособие. Екатеринбург: «ИИЦ «Знак качества»; 2022:32.
Бабушкин В.Н. Билатеральное эндопротезирование в лечении дегенеративно-дистрофических заболеваний тазобедренных суставов: автореф. дис.... канд. мед. наук. Курган; 2007:25. Доступно по: https://medical-diss.com/ docreader/240392/a#?page=1. Ссылка активна на 04.10.2024.
Волокитина Е.А., Колотыгин Д.А. Особенности первичной и ревизионной имплантации бесцементного тазового компонента при диспластическом коксартрозе. Травматология и ортопедия России. 2009;(3):119-121. doi: 10.17816/2311-2905-1913
Malahias MA, Mancino F, Gu A, et al. Acetabular impaction grafting with mesh for acetabular bone defects: a systematic review. Hip Int. 2022;32(2):185-196. doi: 10.1177/1120700020971851
Dawson J, Fitzpatrick R, Carr A, Murray D. Questionnaire on the perceptions of patients about total hip replacement. JBone Joint SurgBr. 1996;78-B(2):185-190. doi:10.1302/0301-620X.78B2.0780185
Morlock MM, Hube R, Wassilew G, et al. Taper corrosion: a complication of total hip arthroplasty. EFORT Open Rev. 2020;5(11):776-784. doi: 10.1302/2058-5241.5.200013
Петров А.Б., Рузанов В.И., Машуков Т.С. Отдаленные результаты хирургического лечения пациентов с переломами вертлужной впадины. Гений ортопедии. 2020;26(3): 300-305. doi: 10.18019/1028-4427-2020-26-3-300-305
Hao Y, Luo D, Wu J, et al. A novel revision system for complex pelvic defects utilizing 3D-printed custom prosthesis. J Orthop Translat. 2021;31:102-109. doi: 10.1016/j.jot.2021.09.006
Цыбин А.В., Любчак В.В., Фалькович А.С. и дп. Определение конгруэнтности стандартного полусферического вертлужного компонента и посттравматически деформированной вертлужной впадины при первичном эндопротезировании тазобедренного сустава. Экспериментальное исследование. Гений ортопедии. 2022;28(5):698- 703. doi: 10.18019/1028-4427-2022-28-5-698-703
Ершов А. С., Волокитина Е. А., Меньшикова И. А., Удинцева М. Ю. Особенности морфологии вертлужной впадины, определяющие технологию имплантации тазового компонента протеза. Уральский медицинский журнал. 2022;21(2):6-12. doi: 10.52420/2071-5943-2022-21-2-6-12
Тихилов Р.М., Джавадов А.А., Денисов А.О. и др. Анализ экономической эффективности использования индивидуальных и серийных вертлужных конструкций при ревизионном эндопротезировании тазобедренного сустава. Гений ортопедии. 2022;28(2):234-240. doi: 10.18019/1028-4427-2022-28-2-234-240
Рукин Я.А., Лычагин А.В., Мурылев В.Ю. и др. Ранние результаты эндопротезирования тазобедренного сустава с применением индивидуальных аугментов при диспластическом коксартрозе. Травматология и ортопедия России. 2020;26(2):50-59. doi: 10.21823/2311-2905-2020-26-2-50-59
Николаев Н.С., Малюченко Л.И., Преображенская Е.В. и др. Применение индивидуальных вертлужных компонентов в эндопротезировании тазобедренного сустава при посттравматическом коксартрозе. Гений ортопедии. 2019;25(2):207-213. doi: 10.18019/1028-4427-2019-25-2-207-213
Алексанян О.А., Чрагян Г.А., Каграманов С.В., Загородний Н.В. Лечение обширного дефекта вертлужной впадины у пациентки с асептической нестабильностью тотального эндопротеза тазобедренного сустава. Вестник травматологии и ортопедии им. Н.Н. Приорова. 2020;27(3):60-66. doi: 10.17816/vto202027360-66
Lychagin AV, Rosenberg N, Gritsyuk AA. Evaluation of the potential complications of surgical wound drainage in primary total hip arthroplasty: a prospective controlled double-blind study. Hip Int. 2021;31(5):589-592.
Мария Юрьевна Удинцева — аспирант, травматолог-ортопед
Елена Александровна Волокитина — доктор медицинских наук, профессор, заведующая кафедрой, ведущий научный сотрудник
Денис Анатольевич Колотыгин — кандидат медицинских наук, врач травматолог-ортопед, kolotigin@inbox.ru; Сергей Михайлович Кутепов — доктор медицинских наук, профессор, член-корр. РАН, руководитель института
Вклад авторов:
Удинцева М.Ю. — поиск и анализ публикаций по теме, интерпретация полученных данных, подготовка и написание текста статьи, редактирование текста статьи.
Волокитина Е.А. — идея и разработка концепции статьи, интерпретация полученного материала, окончательное редактирование текста статьи,
Колотыгин Денис Анатольевич — поиск и анализ публикаций по теме, подготовка и написание текста статьи. Кутепов Сергей Михайлович — поиск и анализ публикаций по темеТеги: эндопротезирование тазобедренного сустава
234567 Начало активности (дата): 03.03.2025
234567 Кем создан (ID): 989
234567 Ключевые слова: эндопротезирование тазобедренного сустава, дефект вертлужной впадины, остеозамещающий материал, костная пластика
12354567899
Похожие статьи
Переломы лодыжекРентген на дому 8 495 22 555 6 8
Повреждение мениска коленного сустава
Переломы дистального отдела костей голени
Повреждения хряща коленного сустава



