 25.05.2025
25.05.2025
Клиническое наблюдение редкого осложнения тупой травмы груди: псевдоаневризма створки аортального клапана
Повреждения клапанного аппарата сердца являются крайне редким осложнением тупой травмы груди.
Введение.
Закрытая травма груди представляет собой все повреждения в данной анатомической области без нарушения целости кожных покровов, включая тупую травму сердца с повреждением его стенок, папиллярных мышц и клапанов. Ушибы, рваные раны и разрывы являются наиболее частыми повреждениями клапанного аппарата в раннем посттравматическом периоде. Предсказать клиническую картину и патологические изменения различных структур клапанов сердца крайне сложно из-за вариабельности механизмов и тяжести травмы [1, 2]. По данным D. de Castro и соавт., именно аортальный клапан наиболее подвержен травматическим изменениям [3]. Одним из часто встречающихся проявлений травматического повреждения аортального клапана при тупой травме сердца служит аортальная регургитация, в то время как повреждения его створок крайне редки [1, 4].
Клинический случай. Пациент К., 45 лет, был направлен Военно-медицинскую академию им. С. М. Кирова Минобороны РФ в связи с неконтролируемой артериальной гипертензией, дислипиде- мией, дискомфортом в области сердца при физической нагрузке, периодическими перебоями в работе сердца. Ранее за медицинской помощью к кардиологу не обращался.
Из анамнеза известно, что в возрасте 18 лет был установлен диагноз «врожденный порок сердца, двустворчатый аортальный клапан». Клапан был визуализирован достаточно четко, дополнительные структуры выявлены не были. При ретроспективной оценке данных эхокардиографии (ЭхоКГ) была выявлена аортальная недостаточность, при этом отмечено ее нарастание с 1 до 2 ст. в динамике за 3 года.
При обследовании пациента в клинике, по данным лабораторных анализов, повышены показатели липопротеинов низкой и очень низкой плотности. Маркеры повреждения миокарда находятся в норме. Уровень артериального давления 190/110 мм рт.ст. На стандартной ЭКГ была установлена пароксизмальная форма фибрилляции предсердий.
По данным ЭхоКГ подтверждена аортальная недостаточность 2 ст. Остальные показатели находятся в пределах возрастной нормы: локальная и глобальная сократимость левого желудочка (ЛЖ) и правого желудочка (ПЖ) не нарушены. КДР/КСО — 4,7,
КСР/КСО — 3,1, индекс массы миокарда ЛЖ 100 г/м2. Фракция выброса ЛЖ=62%. При оценке аортального клапана снят диагноз двустворчатого аортального клапана. Определялось частичное сращение правой и левой коронарных створок, левая коронарная створка была уменьшена в размерах, при этом выявлялась дополнительная структура, располагающаяся ниже зоны коаптации створок аортального клапана, вызывающая второй уровень их смыкания, что было отнесено, вероятнее, к врожденному пороку аортального клапана (рис. 1).
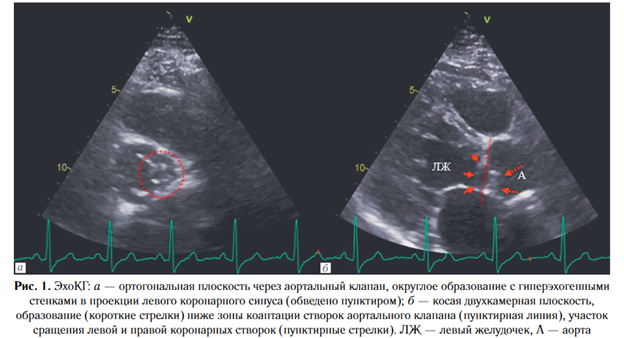
При 24-часовом мониторировании ЭКГ были выявлены эпизоды типичного трепетания и фибрилляции предсердий. С учетом всех полученных данных принято решение выполнить компьютернотомографическую коронарографию (КТ-КГ) для исключения атеросклеротического поражения коронарных артерий и определения анатомических особенностей аортального клапана.
На момент выполнения КТ-КГ у пациента был нерегулярный сердечный ритм, а частота сердечных сокращений (ЧСС) в покое достигала 110 уд/мин. В связи с этим решено было выполнить исследование на КТ с шириной детектора 160 мм, который относится к томографам последнего поколения и позволяет получить изображение сердца за одно сердечное сокращение. Это позволяет получить качественные изображения всех структур сердца вне зависимости от ритма. Были выбраны следующие параметры сканирования: сила тока на рубке — 380 мА, напряжение — 120 кВ, что позволило получить поглощенную дозу 312 мГрхсм, или эффективную дозу 3,7 мЗв.
По данным КТ-КГ атеросклеротические изменения коронарных артерий выявлены не были, при этом обнаружен кинкинг огибающей артерии с септальным стенозом 50% (рис. 2).
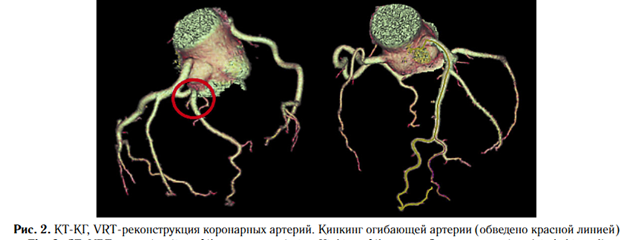
Размеры камер сердца остаются в пределах нормальных показателей: переднезадний размер левого предсердия — 40 мм, поперечный размер левого желудочка — 54 мм, правого предсердия — 44 мм, правого желудочка — 33 мм.
При оценке аортального клапана между некоронарной и левой коронарной створками было обнаружено аневризматическое выпячивание размерами 11x14 мм, исходившее из стенки левой коронарной створки (рис. 3, а, б). Левый коронарный синус уменьшен в размерах с наличием частичного сращения и утолщения створки на границе с правым коронарным синусом (рис. 3, в).
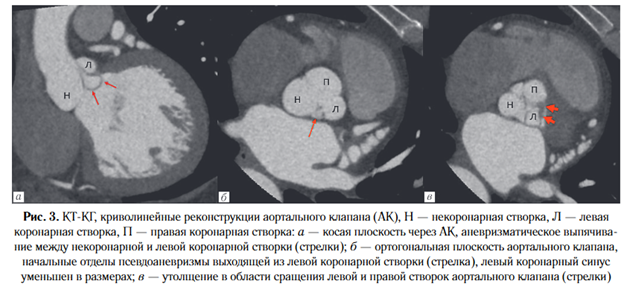
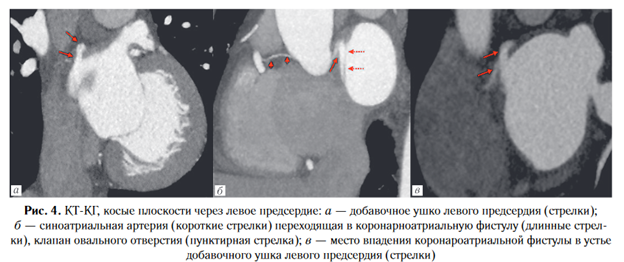
При оценке левого предсердия по передне-верхней стенке выявлено добавочное ушко размерами 5x6 мм, в основание которого впадала синоатриальная артерия с формированием коронароатриальной фистулы, которая располагалась на фоне участка жировой ткани (рис. 4). При этом липоматозная гипертрофия межпредсердной перегородки у пациента выявлена не была. Из дополнительных находок был обнаружен карман межпредсердной перегородки в области овального отверстия без видимого сброса контрастного препарата через него.
При построении дополнительных реконструкций для оценки легочных вен в рамках подготовки к возможной катетерной аблации был выявлен типичный паттерн их ветвления и оценен объем левого предсердия, который составил 76 мл. Таким образом, по результатам проведенных исследований у пациента была установлена псевдоаневризма левой коронарной створки аортального клапана, утолщение и частичное сращение правой и левой коронарных створок, аортальная недостаточность 2 ст. Из случайных находок обнаружены: коронароатриальная фистула, карман межпредсердной перегородки, дополнительные хорды левого желудочка и кинкинг огибающей артерии с наличием септального стеноза 50%. Подтвержден диагноз дислипидемии и гипертонической болезни 2 ст. Данные КТ-КГ позволили исключить атеросклеротический генез нарушения ритма сердца, после чего пациент был направлен к хирургу-аритмологу для решения вопроса о восстановлении ритма сердца и необходимости выполнения катетерной аблации устьев легочных вен.
Обсуждение.
При анализе полученных данных мы исключили основные причины развития диссекции створки аортального клапана, включая инфекционный эндокардит, ревматизм и системные заболевания соединительной ткани.
При более подробном сборе анамнеза было установлено, что 6 лет назад при выполнении своих профессиональных
обязанностей вследствие минно-взрывной травмы пациент получил тупую травму груди, в связи с чем находился в медсанчасти с подозрением на нестабильную стенокардию, после исключения которой выписан в часть с улучшением. Однако после этого случая пациент начал впервые отмечать эпизодические загрудинные боли, что склонило нас к установлению в качестве наиболее вероятной причины развития аневризмы именно травматический генез. Вариант врожденного развития четырехстворчатого клапана был нами исключен ввиду отсутствия четырех створок на предыдущих УЗИ.
Представленный клинический случай демонстрирует редкое осложнение тупой травмы груди в виде развития псевдоаневризмы вследствие разрыва структур аортального клапана. Механизмом повреждения аортального клапана считается внезапное повышение внутрисердечного давления во время наиболее уязвимой фазы сердечного цикла, а именно ранней диастолы, когда трансаортальный градиент максимален, а давление в пустом левом желудочке низкое [5]. Именно аортальный клапан является наиболее часто травмируемым клапаном [2]. Псевдоаневризмы синуса Вальсальвы возникают в результате скопления крови в ложном просвете после разрыва интимы корня аорты, и даже самые маленькие из этих псевдоаневризм могут иметь коварное течение. Очень немногие из них остаются стабильными с течением времени, в то время как увеличение их в размерах и последующий разрыв считаются обычным явлением [3]. Результатом течения таких псевдоаневризм может быть заполнение их тромботическими массами, вплоть до сдавления близлежащих структур, а также формирование различных фистул [6].
Хирургическое вмешательство после постановки диагноза является стандартным лечебным решением в остром периоде развития псевдоаневризмы, поскольку промедление может привести к смерти, кардиогенному шоку или, реже, к симптомам подострой сердечной недостаточности [3]. В приведенном нами клиническом случае верификация псевдоаневризмы была в отдаленном периоде при стабильной клинической картине, что предполагает именно динамическое наблюдение пациента.
Травматическая аортальная регургитация также является осложнением тупой травмы грудной клетки. Хотя клиническое течение травматической аортальной регургитации обычно характеризуется быстрым прогрессированием, у некоторых пациентов может наблюдаться отсроченное ее начало, даже после 7-летнего бессимптомного периода от момента получения [7]. Такие пациенты должны находиться под постоянным диспансерным наблюдением с выполнением ЭхоКГ в динамике. В нашем наблюдении у пациента имеется нарастание аортальной недостаточности с 1 до 2 ст. в динамике за 3 года, что не исключает ее травматический генез.
Интересной находкой оказалась коронароатри- альная фистула между синоатриальной артерией и основанием добавочного ушка левого предсердия. Данная фистула располагалась в передне-верхних отделах межпредсердной борозды. В этом месте проходит пучок Бахмана, по которому импульс возбуждения передается из правого предсердия в левое. Он представляет собой мышечный тяж и питается из ветвей синоатриальной артерии. Наличие в области его расположения жировой ткани свидетельствует о дегенеративных изменениях, связанных с нарушением питания, что может приводить к удлинению межпредсердного проведения и быть предиктором развития наджелудочковых аритмий, включая фибрилляцию предсердий [8].
Таким образом, представленный нами клинический случай показывает важность использования мульти - модальной диагностики для выявления такого редкого осложнения тупой травмы груди, как развитие псевдоаневризмы створки аортального клапана и травматической аортальной регургитации, что крайне важно для дальнейшего наблюдения за данной группой пациентов. Использование компьютерных томографов последнего поколения позволяет получить качественные изображения всех структур сердца за одно сердечное сокращение вне зависимости от ритма и ответить на большинство поставленных задач, связанных с определением анатомических особенностей сердца.
Сведения об авторах:
Меньков Игорь Анатольевич — кандидат медицинских наук, заведующий отделением — врач-рентгенолог отделения лучевой диагностики (стационарных пациентов) клиники рентгенорадиологии федерального государственного бюджетного образовательного учреждения высшего образования «Военно-медицинская академия имени С. М. Кирова» Минобороны Российской Федерации; 194044, Санкт-Петербург, ул. Академика Лебедева, д. 6;
Железняк Игорь Сергеевич — доктор медицинских наук, профессор, заведующий кафедрой рентгенологии и радиологии (с курсом ультразвуковой диагностики) федерального государственного бюджетного образовательного учреждения высшего образования «Военно-медицинская академия имени С. М.Кирова» Минобороны Российской Федерации; 194044, Санкт-Петербург, ул. Академика Лебедева, д. 6; ORCID 0000-0001-7383-512X;
Беликова Мария Яковлевна — доктор медицинских наук, профессор кафедры лучевой диагностики и ядерной медицины медицинского факультета Санкт- Петербургского государственного университета, заведующая отделением лучевой диагностики ООО «Мой медицинский центр Высокие технологии», Ленинградская область, Всеволожский район, с.п. Юкковское, тер. «Клиника Белоостров», зд. 1, к. 1; ORCID 0000-0002-6768-7711;
Барсуков Антон Владимирович — доктор медицинских наук, профессор, доцент кафедры госпитальной терапии федерального государственного бюджетного образовательного учреждения высшего образования «Военно-медицинская академия имени С.М.Кирова» Минобороны Российской Федерации; 194044, Санкт-Петербург, ул. Академика Лебедева, д. 6; заместитель главного врача акционерного общества «КардиоКлиника»; 196105, Санкт-Петербург, ул. Кузнецовская, д. 25; ORCID 0000-0002-1943-9545;
Шуленин Константин Сергеевич — доктор медицинских наук, доцент, заместитель начальника кафедры военно-морской терапии федерального государственного бюджетного военного образовательного учреждения высшего образования «Военно-медицинская академия имени С.М.Кирова» Министерства обороны Российской Федерации; 194044, Санкт-Петербург, ул. Академика Лебедева, д. 6; ORCID 0000-0002-3141-7111;
Калюжный Денис Станиславович — аспирант кафедры рентгенологии и радиологии (с курсом ультразвуковой диагностики) федерального государственного бюджетного образовательного учреждения высшего образования «Военно-медицинская академия имени С. М.Кирова» Минобороны Российской Федерации; 194044, Санкт-Петербург, ул. Академика Лебедева, д. 6; ORCID 0009-0006-6663-9597;
Свеклина Татьяна Сергеевна — кандидат медицинских наук, доцент кафедры пропедевтики внутренних болезней, федерального государственного бюджетного образовательного учреждения высшего образования «Военно-медицинская академия имени С.М.Кирова» Минобороны Российской Федерации; 194044, Санкт-Петербург, ул. Академика Лебедева, д. 6; ORCID 0000-0001-9546-7049.
ЛИТЕРАТУРА / REFERENCES
Игнатенко ГА., Ватутин Н.Т., Тарадин ГГ и др. Аортальная регургитация: эпидемиологические, этиологические и патофизиологические особенности // Клиницист. 2021. Т. 14, № 3-4. С. 57-68. [Ignatenko G.A., Vatutin N.T., Taradin G.G. еt al. Aortic regurgitation: epidemiological, etiological and pathophysiological features. Clinician, 2021, Vol. 14, No. 3-4, pp. 57-68 (In Russ.)]. doi: 10.17650/1818-8338-2020-14-3-4-K639.
Qamar S.R., Wu Y., Nicolaou S., Murray N. State of the Art Imaging Review of Blunt and Penetrating Cardiac Trauma // Canadian Association of Radiologists Journal = Journal l’Association Canadienne DesRadiologistes. 2020. Vol. 71, No. 3. Р, 301-312. doi: 10.1177/0846537119899200.
De Castro D., Rasines-Rodrfguez A., Usano A., Mingo S. Acute Post-Traumatic Aortic Regurgitation // JACC: Case Reports. 2022. Vol. 4, No. 21. H. 1432-1434. doi: 10.1016/j.jaccas.2022.07.018.
Карпова Н.Ю., Рашид М.А., Казакова Т.В., Шостак Н.А. Аортальная регургитация // РМЖ. 2014. № 12. С. 883. [Karpova N.Yu., Rashid M.A., Kazakova T.V., Shostak N.A. Aortic regurgitation. Russian Medical Journal, 2014, No. 12, pp. 883 (In Russ.)].
Eghbalzadeh K., Sabashnikov A., Zeriouh M., Choi Y.-H. et al. Wahlers T. Blunt chest trauma: a clinical chameleon // Heart (British Cardiac Society). 2018. Vol. 104, No. 9. Р 719-724. doi: 10.1136/heartjnl-2017-312111.
Pretre R., Chilcott M. Blunt trauma to the heart and great vessels // The New England Journal of Medicine. 1997. Vol. 336, No. 9. Р 626-632. doi: 10.1056/NEJM199702273360906
Tateishi K., Asselin C.Y., Elmann E.M., De Gregorio J. Delayed Aortic Valve Perforation Caused by Blunt Trauma // Diagnostics (Basel, Switzerland). 2023. Vol. 13, No. 3. Р 549. doi: 10.3390/diagnostics13030549.
Saremi F., Channual S., Krishnan S., Gurudevan S.V. et al. Bachmann Bundle and its arterial supply: imaging with multidetector CT-implications for interatrial conduction abnormalities and arrhythmias // Radiology. 2008. Vol. 248, No. 2. Р 447-457. doi: 10.1148/radiol.2482071908.
Теги: тупая травма груди
234567 Начало активности (дата): 25.05.2025
234567 Кем создан (ID): 989
234567 Ключевые слова: : псевдоаневризма створки аортального клапана, тупая травма груди, КТ-коронарография, аортальный клапан, аортальная регургитация
12354567899
Похожие статьи
Клиническое наблюдение редкого осложнения тупой травмы груди: псевдоаневризма створки аортального клапанаРентген на дому 8 495 22 555 6 8
Вывих шейного позванка
Тяжелая кранифациальная травма



