 17.03.2025
17.03.2025
Замещение тотального дефекта таранной кости с использованием индивидуального SD-имплантата из пористого титана при нейроостеоартропатии Шарко у пациентки с нейросифилисом
Предлагаемый способ оперативного лечения при тотальном разрушении таранной кости и образующемся вследствие этого дефект-диастазе позволяет произвести реконструктивное вмешательство с одномоментной компенсацией укорочения, вне зависимости от формы и величины дефекта, избежать вторичного укорочения конечности с сохранением ее опороспособности, тем самым, предупреждая возникновение вторичных перегрузочных изменений в смежных суставах
ВВЕДЕНИЕ
Нейропатическая артропатия, или артропатия Шарко, характеризуется быстро прогрессирующей деструкцией костей на фоне тяжелого нарушения ноцицептивной и проприоцептивной иннервации пораженной конечности. Jean-Martin Charcot в 1868 г. выявил взаимосвязь между поражением спинного мозга (tabes dorsalis), формой третичного нейросифилиса, которая может развиваться от месяцев до десятилетий после первоначального заражения пациента, и специфической деформацией стопы, в основе которой лежит асептическая деструкция ее костно-суставного аппарата и/или голеностопного сустава [1]. В настоящее время наиболее часто артропатия Шарко встречается у больных сахарным диабетом [2]. Известны случаи развития артропатии Шарко и при других поражениях периферической и центральной нервной системы, при этом на современном этапе развития общества и здравоохранения сифилитическая этиология артропатии встречается достаточно редко [3].
Нейроостеоартропатия Шарко может приводить к некрозу и патологическому разрушению костной ткани голеностопного сустава, в том числе таранной кости, в связи с чем эндопротезирование голеностопного сустава в данном случае недопустимо [4]. Также наличие движений и нагрузки в пораженной области является триггером, обостряющим патологический процесс. Поэтому одним из основных компонентов лечения является исключение нагрузки на пораженный сегмент и иммобилизация, достигаемые при консервативном лечении с помощью полимерных индивидуальных разгрузочных повязок ТСС (англ.: Total Contact Cast) или различных ортезов, при оперативном лечении — с использованием различных вариантов артродезирования суставов [5, 6].
Вопрос замещения тотальных дефектов таранной кости при проведении реконструктивных оперативных вмешательств всегда стоял остро. Поиск материалов для замещения обширных дефектов приводил к пластике последних имплантатами из пористого титана или никелид-титана [7-10], применяли имплантаты разных форм, как с полостями для интеграции гетеротопического аутотрансплантата, так и без них.
Цель работы — продемонстрировать и проанализировать результаты выполнения резекционного пяточно-большеберцового артродеза с пластикой дефекта индивидуальным 3И-имплантатом из пористого титана у пациентки с манифестацией артропатии Шарко как осложнения третичного сифилиса.
С 2015 г. с развитием SD-моделирования и SD-печати из пористого титана начали появляться публикации о внедрении данной технологии в области хирургии стопы. Применение индивидуальных имплантов додекаэдрической формы ознаменовало новое направление в замещении дефектов заднего отдела стопы [11, 12]. Однако, несмотря на рост числа публикаций на эту тему, в литературе нами найдено всего два описания клинических случаев о применении SD-имплантатов из пористого титана у пациентов с артропатией Шарко [13, 14]. Поиск в электронном ресурсе PubMed (ключевые слова — neuropathic arthropathy; syphilis) показал, что за последние 15 лет опубликовано лишь 10 наблюдений о развитии артропатии Шарко различных суставов как осложнения третичного сифилиса. Тем не менее, исходя из анализа опубликованных клинических случаев и обзоров литературы, можно предположить, наиболее частой локализацией артропатии при третичном сифилисе является коленный сустав [3, 15].
МАТЕРИАЛЫ И МЕТОДЫ
Женщина 50 лет, без сахарного диабета, ИМТ — 22 кг/м2; в анамнезе — впервые диагностированный сифилис в 1997 г., лечилась курсом пенициллина, повторный курс антибиотикотерапии — в 2008 г., после этого специфическую терапию не получала. В анализах от 31.03.03.2016: РМП 4+, РПГА 4+, ИФА + 10,9; от 11.08.2016: РМП 2+, РПГА 4+, ИФА 10.9; от 23.03.2020: РМП +1, РПГА 4+, ИФА 13,3. Состоит на учете в кожно-венерологическом диспансере по месту жительства. Контрольный анализ от 21.09.2023: Syphilis RPR (+) в титре 1:2.
За 2 мес. до обращения выполнено тотальное эндопротезирование левого коленного сустава по поводу артроза 3 степени. Во время реабилитации после увеличения продолжительности ходьбы с помощью костылей и нагрузки на левую нижнюю конечность отметила появление отека, незначительную локальную гипертермию и гиперемию в области левого голеностопного сустава и стопы. Болевая чувствительность при пассивных и активных движениях отсутствовала. Травмы отрицала. Амбулаторно выполнено КТ-исследование левого голеностопного сустава, выявлен патологический перелом и деструкция таранной кости с ее фрагментацией и смещением фрагментов.
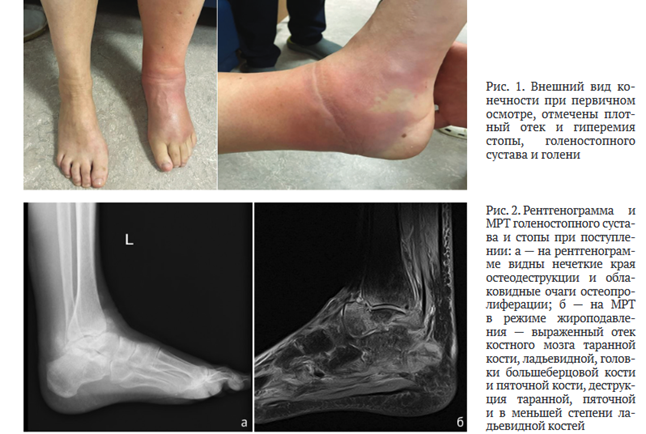
По результатам исследования пациентка консультирована в Центре хирургии стопы и диабетической стопы ГКБ им. С.С. Юдина, госпитализирована. При первичном осмотре: стопа и голень отечны, умеренная гиперемия в области левого голеностопного сустава (рис. 1). По данным лабораторных исследований отмечено увеличение скорости оседания эритроцитов (СОЭ по Панченкову) — 42 мм/ч; количество лейкоцитов в общем анализе крови — 7,6 х 109/л; уровень С-реактивного белка — 6,52 мг/л.
При рентгенографии выявлено разрушение подтаранного сустава, соответствующее 2 стадии по классификации Eichenholtz [16-18]. При магнитно-резонансной томографии подтверждены масштабы поражения, а также выявлен отек костного мозга ладьевидной и большеберцовой костей и явления сино- виита сопряженных суставов (рис. 2).
После осмотра выполнено наложение задней гипсовой иммобилизирующей повязки от пальцев стопы до верхней трети голени, разрешена ходьба без нагрузки на левую ногу с помощью костылей. В дальнейшем осуществлялось амбулаторное наблюдение пациентки в ГКБ им. С.С. Юдина.
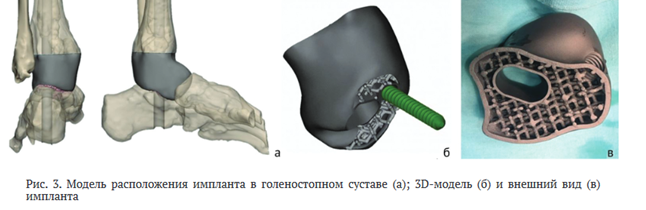
Через 2,5 мес. после иммобилизации конечности с помощью гипсовой повязки и разгрузки посредством дополнительных средств опоры пациентка госпитализирована в ГКБ им. С.С. Юдина. По результатам КТ-исследования левого голеностопного сустава выполнено SD-моделирование индивидуального имплантата с учетом необходимости замещения костного дефекта. По SD-модели изготовлен индивидуальный SD-имплантат из пористого титана (рис. 3).
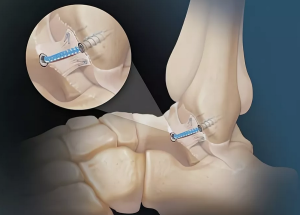
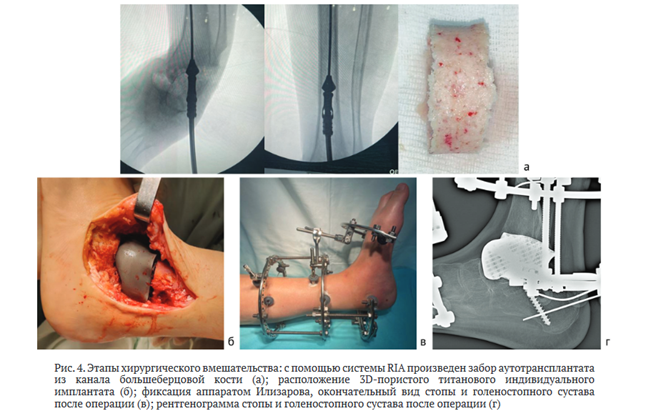
Интраоперационно выявлена деструкция таранной кости левой стопы, произведено удаление ее фрагментов, суставных поверхностей пяточной и большеберцовой костей. Далее системой RIA (англ.: Reamer Irrigator Aspirator) произведен забор аутотрансплантата из канала большеберцовой кости ретроградным доступом (рис. 4). После выведения стопы в нормокоррекцию произведена пластика дефекта, образованного после удаления таранной кости, индивидуальным SD-имплантатом из пористого титана с предварительной интеграцией костного аутотрансплантата в межбалочное пространство и фиксация аппаратом Илизарова [7, 19].
После выписки на 12-е сут. пациентка наблюдалась амбулаторно; швы сняты через 6 нед. Этапную поддерживающую компрессию в аппарате проводили ежемесячно по 1 мм.
Через 5 мес. после операции по результатам контрольных рентгенограмм и компьютерной томографии определены перестройка костного трансплантата в межбалочном пространстве имплантата, отсутствие явлений лизиса и нестабильности импланта. В плановом порядке выполнен демонтаж аппарата Илизарова (рис. 5).
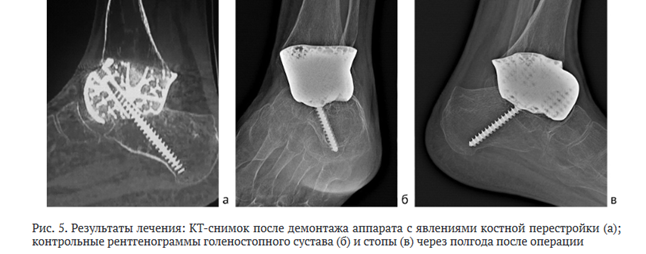
В дальнейшем в течение 6 мес. разгрузку левого голеностопного сустава осуществляли с помощью индивидуальной полимерной разгрузочной повязки. Пациентку активизировали с помощью дополнительных средств опоры с дозированной нагрузкой на оперированную нижнюю конечность до 20 % от веса с последующим постепенным ее увеличением до полной нагрузки.
РЕЗУЛЬТАТЫ
На контрольном осмотре через 10 мес. клинически и рентгенологически ранней нестабильности компонентов эндопротеза и ^-пористого титанового имплантата не наблюдали (рис. 6). Пациентка ходит без использования средств дополнительной опоры в ортопедической диабетической обуви с индивидуальными ортопедическими стельками.
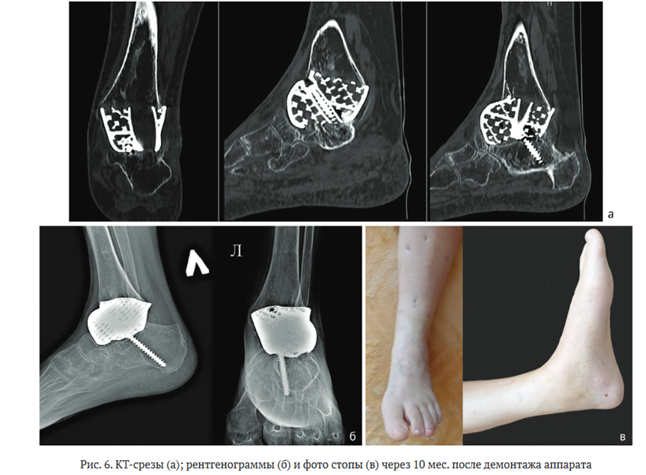
ОБСУЖДЕНИЕ
Данный клинический случай демонстрирует необходимость тщательного сбора анамнеза и предоперационного обследования для верификации сопутствующих заболеваний и связанных с ними возможных осложнений.
Консервативные методы до сих пор являются преобладающими в лечении диабетической нейроостеоартропатии, но не могут быть применимы для пациентов с полным или частичным нарушением опорной функции стопы, что, в свою очередь, существенно увеличивает актуальность ортопедической реконструкции [20].
Данный способ оперативного лечения используют при тотальном разрушении таранной кости и образующемся вследствие этого дефект-диастазе в процессе выполнения резекционного пяточно-большеберцового артродеза. Способ позволяет произвести реконструктивное вмешательство с одномоментной и точной компенсацией укорочения, вне зависимости от формы и величины дефекта, избежать вторичного укорочения конечности с сохранением ее опороспособности, тем самым профилактируя возникновение вторичных перегрузочных изменений в смежных суставах. Вместе с тем, одной из ключевых задач ортопедического лечения пациентов с нейроостеоартропатией
Шарко является снижение риска высокой ампутации и сохранение двигательной активности пациента. Проведение стабилизации стопы аппаратом внешней фиксации является фактором, способствующим стиханию процесса и, как следствие, положительно влияет на состоятельность выполняемого артродеза. Следует также отметить, что результат проводимого лечения во многом зависит от комплаентности и приверженности к лечению пациента, а также соблюдению им назначений и рекомендаций [21].
Для уточнения показаний к данному методу лечения и критериев отбора пациентов требуется увеличение группы пациентов и проведение дополнительных исследований.
ЗАКЛЮЧЕНИЕ
Результаты выполнения резекционного пяточно-большеберцового артродеза с пластикой дефекта SD-пористым титановым индивидуальным имплантатом, продемонстрированные у пациентки с манифестацией артропатии Шарко как осложнения третичного сифилиса, являются обнадеживающими. Учитывая персонализированный подход, данный метод представляется перспективной концепцией лечения, позволяющей восстановить опороспособность нижней конечности без ее укорочения.
СПИСОК ИСТОЧНИКОВ
Charcot JM. On some arthropathies which seem to depend on a lesion of the brain or spinal cord. Arch Physiol Norm Pathol. 1868;1:161- 178. (in French).
Rogers LC, Frykberg RG, Armstrong DG, et al. The Charcot foot in diabetes. Diabetes Care. 2011;34(9):2123-2129. doi: 10.2337/dc11-0844.
Wang M, Huang R, Wang L, et al. Syphilis with Charcot arthropathy: A case report. Dermatol Ther. 2019;32(3):e12862. doi: 10.1111/ dth.12862.
Bonasia DE, Dettoni F, Femino JE, et al. Total ankle replacement: why, when and how? Iowa Orthop J. 2010;30:119-130.
Klaue K, Zwipp H, Mittlmeier T, Espinosa N. Internal circular arc osteosynthesis of tibiotalocalcaneal arthrodesis. Unfallchirurg. 2016;119(10):885-9. (In German). doi: 10.1007/s00113-016-0210-4.
Belczyk RJ, Rogers LC, Andros G, et al. External fixation techniques for plastic and reconstructive surgery of the diabetic foot. Clin Podiatr Med Surg. 2011;28(4):649-660. doi: 10.1016/j.cpm.2011.07.001.
Kreulen C, Lian E, Giza E. Technique for Use of Trabecular Metal Spacers in Tibiotalocalcaneal Arthrodesis With Large Bony Defects. Foot Ankle Int. 2017;38(1):96-106. doi: 10.1177/1071100716681743.
Henricson A, Rydholm U. Use of a trabecular metal implant in ankle arthrodesis after failed total ankle replacement. Acta Orthop. 2010;81(6):745-747. doi: 10.3109/17453674.2010.533936.
Long WJ, Scuderi GR. Porous tantalum cones for large metaphyseal tibial defects in revision total knee arthroplasty: a minimum 2-year follow-up. J Arthroplasty. 2009;24(7):1086-1092. doi: 10.1016/j.arth.2008.08.011.
Frigg A, Dougall H, Boyd S, Nigg B. Can porous tantalum be used to achieve ankle and subtalar arthrodesis?: a pilot study. Clin Orthop RelatRes. 2010;468(1):209-216. doi: 10.1007/s11999-009-0948-x.
Dekker TJ, Steele JR, Federer AE, et al. Use of Patient-Specific 3D-Printed Titanium Implants for Complex Foot and Ankle Limb Salvage, Deformity Correction, and Arthrodesis Procedures. Foot Ankle Int. 2018;39(8):916-921. doi: 10.1177/1071100718770133.
Bejarano-Pineda L, Sharma A, Adams SB, Parekh SG. Three-Dimensional Printed Cage in Patients With Tibiotalocalcaneal Arthrodesis Using a Retrograde Intramedullary Nail: Early Outcomes. Foot Ankle Spec. 2021;14(5):401-409. doi: 10.1177/1938640020920947.
Hsu AR, Ellington JK. Patient-Specific 3-Dimensional Printed Titanium Truss Cage With Tibiotalocalcaneal Arthrodesis for Salvage of Persistent Distal Tibia Nonunion. Foot Ankle Spec. 2015;8(6):483-489. doi: 10.1177/1938640015593079.
Wang G, Lin J, Zhang H, et al. Three-dimension correction of Charcot ankle deformity with a titanium implant. Comput Assist Surg (Abingdon). 2021;26(1):15-21. doi: 10.1080/24699322.2021.1887356.
Lu V, Zhang J, Thahir A, et al. Charcot knee - presentation, diagnosis, management - a scoping review. Clin Rheumatol. 2021;40(11):4445- 4456. doi: 10.1007/s10067-021-05775-8.
Eichenholtz SN. Charcot Joints. Springfield, IL, USA: Charles C. Thomas; 1966.
Shibata T, Tada K, Hashizume C. The results of arthrodesis of the ankle for leprotic neuroarthropathy. J Bone Joint Surg Am. 1990;72(5):749-756.
Chantelau EA, Richter A. The acute diabetic Charcot foot managed on the basis of magnetic resonance imaging--a review of 71 cases. Swiss Med Wkly. 2013;143:w13831. doi: 10.4414/smw.2013.13831.
Оснач С.А., Оболенский В.Н., Процко В.Г. и др. Метод двухэтапного лечения пациентов с тотальными и субтотальными дефектами стопы при нейроостеоартропатии Шарко. Гений ортопедии. 2022;28(4):523-531. doi: 10.18019/1028-4427-2022-28-4-523-531.
Wukich DK, Schaper NC, Gooday C, et al. Guidelines on the diagnosis and treatment of active Charcot neuro-osteoarthropathy in persons with diabetes mellitus (IWGDF 2023). Diabetes Metab Res Rev. 2024;40(3):e3646. doi: 10.1002/dmrr.3646.
Демина А.Г., Бреговский В.Б., Карпова И.А. Ближайшие результаты лечения активной стадии стопы Шарко в амбулаторных условиях. Сахарный диабет. 2020;23(4):316-323. doi: 10.14341/DM10363.
Статья поступила 21.10.2024; одобрена после рецензирования 30.10.2024; принята к публикации 10.12.2024.
The article was submitted 21.10.2024; approved after reviewing 30.10.2024; accepted for publication 10.12.2024.
Информация об авторах:
Станислав Александрович Оснач — врач — травматолог-ортопед
Владимир Николаевич Оболенский — кандидат медицинских наук, врач-хирург, врач — травматолог-ортопед, заведующий Центром гнойной хирургии
Вадим Борисович Бреговский — доктор медицинских наук, врач-эндокринолог
Василий Викторович Кузнецов — кандидат медицинских наук, врач — травматолог-ортопед
Алексей Витальевич Мазалов — врач — травматолог-ортопед
Саргон Константинович Тамоев — кандидат медицинских наук, врач — травматолог-ортопед, заведующий отделением
Виктор Геннадьевич Процко — доктор медицинских наук, врач — травматолог-ортопед, руководитель Центра хирургии стопы и диабетической стопы
Теги: отальный дефект таранной кости
234567 Начало активности (дата): 17.03.2025
234567 Кем создан (ID): 989
234567 Ключевые слова: артропатия Шарко, тотальный дефект таранной кости, индивидуальный 30-пористый титановый имплантат, резекционный пяточно-большеберцовый артродез
12354567899
Похожие статьи
Переломы лодыжекРентген на дому 8 495 22 555 6 8
Перелом нижней челюсти
Множественные переломы мозгового и лицевого отделов черепа
Эндопротезирование головки таранной кости при лечении болезни Мюллера - Вейса: три клинических случая



