 05.09.2024
05.09.2024
КТ-навигация как залог успеха бронхобиопсии при периферических образованиях в легких
Определение характера очаговых изменений в легких по-прежнему остается актуальной проблемой онкологии, пульмонологии и рентгенологии.
Введение
Солидные очаги встречаются чаще, субсолидные потенциально более злокачественны. Риск злокачественности прямо пропорционален размерам очагов [4]. При обнаружении очага в легком в первую очередь перед врачом-рентгенологом встает вопрос о вероятности злокачественности новообразования.
Компьютерная томография (КТ) является приоритетным методом в диагностике заболеваний органов дыхания. Возможности метода существенно расширяются с применением болюсного контрастирования, позволяющего на основании динамики накопления препарата проводить дифференциальную диагностику выявленных изменений в легочной ткани [5, 6].
Появление и совершенствование новых методик, в частности перфузионного сканирования, позволяют с большей долей вероятности судить о характере очаговых изменений в легких на основании качественных и количественных параметров кровотока в зоне интереса [7].
С помощью высокоразрешающей КТ с толщиной среза 1 мм и менее можно повысить точность 30 характеристик очагов и образований, а также выполнять мультипланарные реформации (multiplanar reformation, МРR) в аксиальной, сагиттальной, ко- рональной, произвольной плоскостях. Программы проекций максимальной интенсивности (maximum intensity projection, MIP) применяются для обнаружения очагов и очаговых диссеминаций, а также для характеристики сосудов при артериовенозной мальформации, внутридолевой секвестрации, аномалии легочных вен, аневризматических расширениях и т.д. [5]. Виртуальная бронхоскопия позволяет получить информацию о внутренней поверхности трахеи и бронхов, выявить сужение или дилатацию просвета бронхов диаметром 2 мм и более, определиться с уровнем и степенью выраженности изменений, оценить состояние бронха дистальнее уровня стеноза [8, 9]. Недостатком виртуальной бронхоскопии является отсутствие возможности оценки состояния слизистой оболочки и подслизистого слоя трахеобронхиального дерева, получить материал для последующего исследования [10]. Данные ресурсы постпроцессинговой обработки, несомненно, оказывают значимую помощь при работе с диагностическими изображениями.
Тем не менее зачастую судить о характере очагов в легких на основании только рентгенологической картины не представляется возможным ввиду схожей семиотики доброкачественных и злокачественных изменений. В большинстве случаев окончательный диагноз устанавливается на основании изучения морфологического материала, полученного в ходе бронхобиопсии, трансоракальной биопсии или хирургического лечения [11, 12].
Вероятность получения неинформативного материала при трансторакальной биопсии увеличивается при наличии очагов в легких небольшого размера или неудобного для пункции их расположения (вблизи крупных сосудистых структур, в наддиафрагмальных, задних кортикальных отделах легких на уровне лопаток и т.д.). Манипуляция сопряжена с риском возникновения осложнений в виде пневмоторакса, кровотечения, степень выраженности которых варьируется от незначительной до массивной [13].
Бронхобиопсия является первым этапом миниинвазивной диагностики на пути к морфологической верификации диагноза [14]. Однако ее роль в диагностике очаговых образований легких небольшого размера ограниченна [15]. По данным литературы, результативность (т.е. возможность получения ткани опухоли для последующего гистологического или цитологического исследования) для центральных и периферических образований вместе составляет от 20% до 86%. Для образований размером 2 см и менее этот показатель не выше 34% [16]. Трудность получения диагностически информативного материала при бронхобиопсии из очагов периферической локализации в легких заключается непосредственно в строении бронхиального дерева. Задача специалистов дополнительно усложняется при наличии особенностей развития бронхолегочной системы. Наиболее частыми анатомическими вариациями являются наличие справа (чаще) или слева трахеального бронха, кардиального бронха слева, аге- незия В7 справа, самостоятельное отхождение В1 и В2 от верхнедолевого бронха слева. Нередко присутствует дополнительная междолевая щель (особенность чаще наблюдается в левом легком) либо вовсе отсутствует какая-нибудь из основных междолевых щелей. После 40 лет происходят атрофические изменения слизистой оболочки и подслизистого слоя, обызвествление хрящевых полуколец, что также оказывает влияние на возможность получения материала. Следует отметить и высокий риск угрозы кровотечения ввиду близкого расположения крупных сосудистых структур при работе с пораженными лимфоузлами, очагами, локализующимися в парамедиастинальных отделах или вблизи корней легких [17].
Морфологические данные позволяют определиться с дальнейшей тактикой в конкретной клинической ситуации. Более того, с учетом последних достижений в области таргетной терапии становится все более необходимым получать опухолевую ткань для анализа молекулярных данных с целью персонализации лечения [18-20].
Как показал наш опыт, предварительный анализ КТ-изображений, в частности применение программ постпроцессинговой обработки с целью определения оптимальной траектории до очага, в большинстве случаев дает возможность получить цитологический материал во время бронхобиопсии в сравнении с эндоскопическими исследованиями, проводившимися только на основании описательной картины. Знания о соотношении анатомических структур и очага, в частности с сосудами, позволяют снизить риск осложнений инвазивной процедуры. С помощью КТ с толщиной среза 2 мм и менее можно с точностью указать, на каком уровне деления бронхиального дерева локализуется очаг, выявить наличие либо отсутствие связи с бронхом, при положительном симптоме «подходящего» бронха определить оптимальную трассу до объекта изучения. Применение лучевых методов исследования позволяет предположить ожидаемую эндоскопическую картину путем изучения взаимосвязи очага и бронха, в частности компрессию извне, деформацию стенки бронха, что является маркером достижения области интереса, или инвазию опухолевых масс в просвет бронха.
Представляем серию клинических наблюдений, демонстрирующих применение технологии КТ-навигации при выполнении бронхобиопсии у пациентов с очаговыми образованиями в легких.
Описания случаев
Случай 1
Пациенту Н., 53 года, с подозрением на пневмонию выполнена КТ органов грудной клетки. По данным КТ в периферических отделах С3 левого легкого выявлен мелкий очаг, предположен поствоспалительный характер изменений.
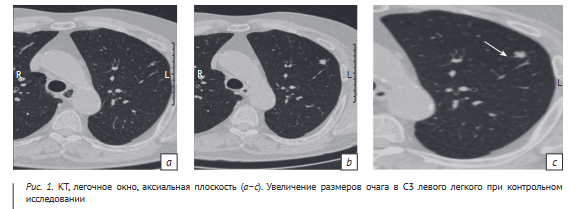
Через 1 год проведено повторное КТ-исследо- вание легких в связи с жалобами на сухой кашель. При сравнении исследований отмечено увеличение размеров солидного очага в С3 левого легкого. Очаг приобрел бугристые контуры, имел связь с бронхом, изменений в окружающей паренхиме не выявлено (рис. 1). С учетом отрицательной динамики размеров заподозрен злокачественный характер изменений.
На основании данных КТ выполнена бронхобиопсия. При осмотре трахея не изменена, карина острая, бронхи правого и левого легких имеют обычное анатомическое строение, шпоры острые, устья не деформированы.
Слизистая бронхов гладкая, блестящая, без признаков опухолевой инфильтрации. Проведена браш-биопсия из С3 верхней доли левого легкого. Материал направлен на цитологическое исследование. По результатам
цитологического исследования: аденокарцинома С3 левого легкого.
При бронхоскопическом исследовании инструмент возможно провести до 4-5-го уровня деления бронхиального дерева, оценить состояние дистальнее расположенных ветвей ввиду мелкого диаметра бронхов не представляется возможным. Материал берется «вслепую», направление биопсийных инструментов осуществляется с учетом ранее определенной на КТ-изображениях траектории.
Несмотря на маленькие размеры и периферическую локализацию очага, у этого пациента удалось верифицировать диагноз посредством изучения материала, полученного в ходе брохобиопсии. Больной направлен на консультацию к торакальному хирургу. Выполнено хирургическое лечение в объеме верхней лобэктомии слева с медиастинальной лимфодиссекцией.
Случай 2
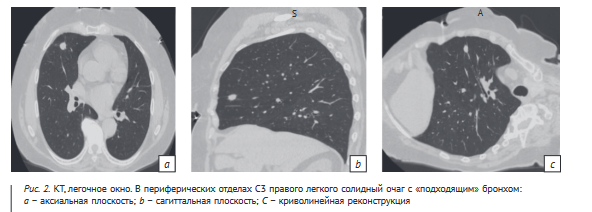
Пациенту К., 68 лет, по месту жительства проведена КТ органов грудной клетки. Согласно представленному протоколу в С5 правого легкого выявлен очаг. Выполнен пересмотр КТ-исследования. Очаг определен в С3 правого легкого, выявлена связь очага с бронхом (рис. 2). Проводилась дифференциальная диагностика между периферическим раком и хондрогамартомой.
На основании данных КТ выполнена бронхобиопсия. Проведена браш-биопсия из С3 верхней доли правого легкого. Материал направлен на цитологическое исследование. По результатам цитологического исследования: нейроэндокринная опухоль легкого Grade 1 (типичный карциноид).
Правильное определение топики изменений позволило получить материал при бронхоскопии для последующего морфологического исследования. Пациент направлен на консультацию к торакальному хирургу. Выполнено хирургическое лечение в объеме верхней лобэктомии справа с медиастинальной лимфодиссекцией.
Случай 3
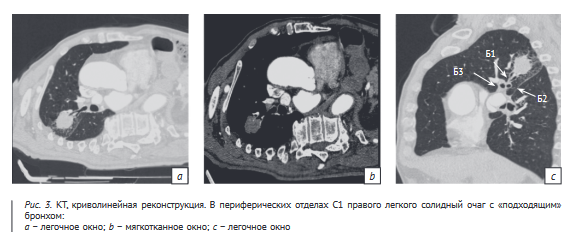
Пациенту Х., 59 лет, по месту жительства выполнена КТ органов грудной клетки. Согласно представленному протоколу в С2 правого легкого выявлен очаг. Выполнен пересмотр исследования. Очаг определен в С1 правого легкого, присутствует связь очага с бронхом (рис. 3).
На основании данных КТ выполнена бронхобиопсия. При осмотре субсегментарный бронх Б-1б полностью обтурирован бугристым опухолевым образованием. Слизистая оболочка по периферии образования с наличием патологической сосудистой сети ярко гиперемирована. Проведена брашбиопсия из С1 верхней доли правого легкого. Материал направлен на цитологическое исследование. По результатам цитологического исследования: немелкоклеточный рак типа плоскоклеточного.
Пациент направлен на консультацию к торакальному хирургу. Выполнено хирургическое лечение в объеме верхней лобэктомии справа с медиастинальной лимфодиссекцией.
Случай 4
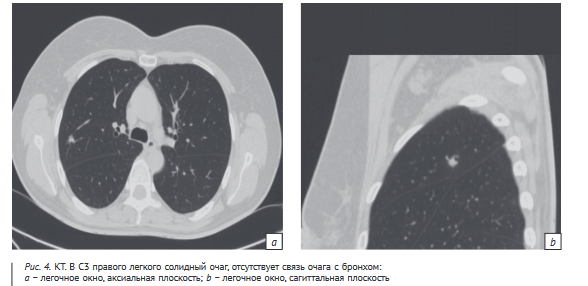
Пациентке Ф., 49 лет, выполнена КТ органов грудной клетки. В С3 правого легкого выявлен солидный очаг размерами до 8 мм, отсутствует связь очага с бронхом (рис. 4).
На основании данных КТ выполнена бронхобиопсия. При осмотре патологии в бронхах, доступных осмотру, не выявлено. По результатам цитологического исследования элементов злокачественной опухоли в пределах материала не обнаружено. Проведена трансторакальная биопсия. Гистологическое заключение: узел атипической аденоматозной гиперплазии легкого.
Пациентка направлена на консультацию к торакальному хирургу. Выполнено хирургическое лечение в объеме верхней лобэктомии справа с медиастинальной лимфодиссекцией.
Случай 5
Пациентке Р, 67 лет, с раком мочевого пузыря в анамнезе ^1N0M0) в плане динамического контроля выполнена КТ органов грудной клетки. По результатам КТ-исследования в С8 правого легкого выявлен очаг по типу матового стекла, предположен поствоспалительный характер изменений.
Повторная КТ через 1 год 2 мес показала увеличение размеров очага в С8 правого легкого, нарастание денситометрических характеристик в зоне интереса, отсутствует связь очага с бронхом
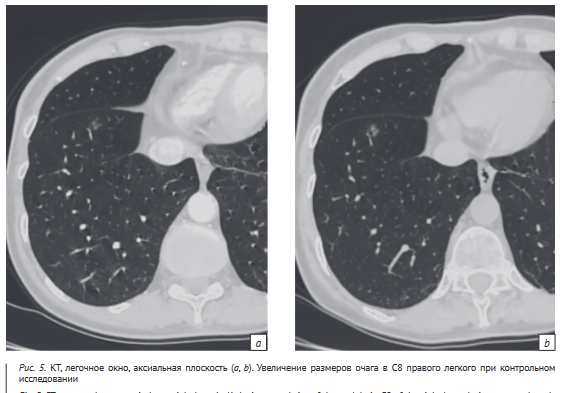
На основании данных КТ выполнена бронхобиопсия. При осмотре патологии в бронхах, доступных осмотру, не выявлено. По результатам цитологического исследования элементов злокачественной опухоли в пределах материала не обнаружено. Выполнена трансторакальная биопсия. Гистологическое заключение: верифицированная минимально инвазивная аденокарцинома легкого.
Выполнена видеоторакоскопическая резекция нижней доли правого легкого.
Обсуждение
Наиболее часто это локализация патологического очага в периферической зоне С1, С2 верхней доли и С6 нижней доли левого легкого, а также в случаях, когда бронхи проксимальных отделов сдавлены бронхопульмональными лимфоузлами, что сопровождается невозможностью достичь патологического очага.
Таким образом, получение материала бронхобиопсии, достаточного для морфологического подтверждения диагноза, зависит, в первую очередь, от анатомической локализации и наличия связи с бронхом. Проведение предварительной КТ-на- вигации, точное представление врачом-эндоско- пистом трассы, ведущей к образованию, - залог успеха в получении диагностического материала.
Заключение
Применение новых технологий, включая сочетание КТ-навигации и бронхоскопических методов при очаговых образованиях, позволяет повысить возможности малоинвазивных методов диагностики, способствует установлению диагноза в более сжатые сроки, что, в свою очередь, имеет значение для результатов лечения.
Литература
MacMahon H, Naidich DP, Goo JM. Guidelines for management of incidental pulmonary nodules detected on CT images: from the Fleischner Society 2017. Radiology. 2017; 284(1): 228-43.
Gould MK, Donington J, Lynch WR, et al. Evaluation of individuals with pulmonary nodules: when is it lung cancer? Diagnosis and management of lung cancer, 3rd ed: American College of Chest Physicians evidence-based clinical practice guidelines. Chest. 2013; 143(5 Suppl): e93S-120S.
Тюрин И.Е. Дифференциальная диагностика одиночных очагов в легких. Поликлиника. 2014; 3-1: 28-32.
Weinberger SE, McDermott S. Diagnostic evaluation of the incidental pulmonary nodule.
Котляров П.М. Постпроцессинговая обработка данных мультиспиральной компьютерной томографии в уточненной диагностике патологических изменений при диффузных заболеваниях легких. Пульмонология. 2017; 27(4): 472-7.
Лагкуева И.Д., Сергеев Н.И., Котляров П.М. и др. Перфузионная компьютерная томография в уточнении природы очаговой патологии легких. Лучевая диагностика и терапия. 2019; 1: 62-8.
Adachi T, Machida H, Nishikawa M, et al. Improved delineation of CT virtual bronchoscopy by ultrahigh-resolution CT: comparison among different reconstruction parameters. J Radiol. 2020; 38(9): 884-9.
Hiddinga BI, Slebos DD, David Koster T, et al. Added diagnostic value of virtual bronchoscopic navigation in patients with pulmonary nodules - the NAVIGATOR study. Lung Cancer. 2023; 177: 37-43.
Kato A, Yasuo M, Tokoro Y, et al. Virtual bronchoscopic navigation as an aid to CT-guided transbronchial biopsy improves the diagnostic yield for small peripheral pulmonary lesions. Respirology. 2018; 23(11): 1049-54.
Hou WS, Wu HW, Yin Y, et al. Differentiation of lung cancers from inflammatory masses with dual-energy spectral CT imaging. Acad Radiol. 2015; 22(3): 337-44
Nanavaty P, Alvarez MS, Alberts WM. Lung cancer screening: advantages, controversies, and applications. Cancer Control. 2014; 21(1): 9-14.
.
Azour L, Liu S, Washer SL, Moore WH. Percutaneous transthoracic lung biopsy: optimizing yield and mitigating risk. J Comput Assist Tomogr. 2021; 45(5): 765-75.
Shen YC, Chen CH, Tu CY. Advances in diagnostic bronchoscopy. Diagnostics (Basel). 2021; 11(11): 1984.
Miyoshi S, Isobe K, Shimizu H, et al. The utility of virtual bronchoscopy using a computed tomography workstation for conducting conventional bronchoscopy: a retrospective analysis of clinical practice. Respiration. 2019; 97(1): 52-9.
Ashraf SF, Lau KKW. Navigation bronchoscopy: a new tool for pulmonary infections. Med Mycol. 2019; 57(Suppl 3): S287-93.
Adamczyk M, Tomaszewski G, Naumczyk P, et al. Usefulness of computed tomography virtual bronchoscopy in the evaluation of bronchi divisions. J Radiol. 2013; 78(1): 30-41.
Ruiz-Cordero R, Devine WP. Targeted therapy and checkpoint immunotherapy in lung cancer. Surg Pathol Clin. 2020; 13(1): 17-33.
Reck M, Remon J, Hellmann MD. first-line immunotherapy for non-small-cell lung cancer. J Clin Oncol. 2022; 40(6): 586-97
Hirsch FR, Scagliotti GV, Mulshine JL, et al. Lung cancer: current therapies and new targeted treatments. Lancet. 2017; 389(10066): 299-311.
Авторы:
Черниченко Наталья Васильевна, д. м. н., вед. науч. сотр. научно-исследовательского отдела хирургии и хирургических технологий в онкологии ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России;
Лагкуева Ирина Джабраиловна, к. м. н., заведующая отделением рентгеновской диагностики с кабинетами рентгеновской и магнитно-резонансной компьютерной томографии ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России;
Сусарев Илья Олегович, врач-эндоскопист отделения внутрипросветной эндоскопической диагностики и лечения консультативно-диагностического клинического центра ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России;
Джигкаева Марина Михайловна, врач-рентгенолог отделения рентгеновской диагностики с кабинетами рентгеновской и магнитно-резонансной компьютерной томографии ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России;
Чхиквадзе Владимир Давидович, д. м. н., профессор, заведующий лабораторией хирургических технологий в онкологии ФГБУ «Российский научный центр рентгенорадиологии» Минздр
Лагкуева Ирина Джабраиловна, к. м. н., заведующая отделением рентгеновской диагностики с кабинетами рентгеновской и магнитно-резонансной компьютерной томографии ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России;
Сусарев Илья Олегович, врач-эндоскопист отделения внутрипросветной эндоскопической диагностики и лечения консультативно-диагностического клинического центра ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России;
Джигкаева Марина Михайловна, врач-рентгенолог отделения рентгеновской диагностики с кабинетами рентгеновской и магнитно-резонансной компьютерной томографии ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России;
Чхиквадзе Владимир Давидович, д. м. н., профессор, заведующий лабораторией хирургических технологий в онкологии ФГБУ «Российский научный центр рентгенорадиологии» Минздр
Теги: легкие
234567 Начало активности (дата): 05.09.2024 00:50:00
234567 Кем создан (ID): 989
234567 Ключевые слова: очаг; легкие; компьютерная томография; мультипланарная реконструкция; бронхобиопсия
12354567899
Похожие статьи
Гамартома легкого: моноцентровый аналитический обзор 142 случаевРентген на дому 8 495 22 555 6 8
Повышение эффективности хирургического восстановления больших костных дефектов при посттравматическом остеомиелите конечностей
Таможня Литвы хочет полностью избавиться от китайских рентген-аппаратов
Литва усилит рентген-контроль на границе с РФ и Белоруссией



