 10.01.2024
10.01.2024
Эндопротезирование коленного сустава у пациентов, находящихся на хроническом гемодиализе: стандартная операция или сложный случаи?
Хронический гемодиализ существенно увеличивает риски при эндопротезировании коленного сустава (ЭП КС)
Введение
Эндопротезирование коленного сустава (ЭП КС) является самым эффективным хирургическим способом лечения всех этиологических форм гон- артроза II-III степеней.
Современные зарубежные и отечественные публикации указывают на ежегодное увеличение количества имплантируемых эндопротезов КС с хорошими долгосрочными показателями выживаемости компонентов [1, 2, 3, 4, 5].
Наличие у пациента терминальной стадии хронической болезни почек (ХБП) существенно увеличивает риски развития осложнений оперативного вмешательства, таких как кровотечения, острые сердечно-сосудистые нарушения (пароксизмы мерцательной аритмии, инфаркт миокарда, отек легких, ТЭЛА и пр.) и интраоперационные перипротезные переломы [6, 7, 8]. Среди поздних осложнений тотальной артропластики КС у гемодиализных пациентов отмечаются: глубокая пе- рипротезная инфекция (ППИ) — до 18% [9, 10, 11] и асептическое расшатывание — 16% [12, 13]. В отечественных публикациях данная проблема освещена недостаточно.
Частота распространения терминальной стадии ХБП возрастатет во всех странах экспоненци- онально [14]. С учетом ежегодно увеличивающейся потребности в выполнении ЭП КС, в том числе и у пациентов гемодиализного профиля, возможно в ближайшей перспективе увеличение ревизионных хирургических вмешательств. В связи с этим возрастает необходимость более тщательного анализа результатов первичного ЭП КС у пациентов, находящихся на хроническом гемодиализе, и разработки схем предоперационной подготовки, заключающихся в коррекции нарушений кальцийфосфорного обмена, кислотно-основного состояния организма, анемии, минеральной плотности костной ткани, тромбопрофилактики и снижения рисков инфекционных осложнений.
Цель исследования — на основании оценки пе- риоперационных показателей и среднесрочных результатов первичного эндопротезирования коленного сустава у пациентов, находящихся на хроническом гемодиализе, обосновать необходимость отнесения данной категории операций к сложным случаям.
Материалы и методы
Дизайн исследоания
Проведено ретроспективное рандомизированное одноцентровое когортное исследование, в которое вошли 62 пациента с различными патогенетическими формами гонартроза, которым в клинике ПСПбГМУ им. акад. И.П. Павлова в период с 2016 по 2022 г. было выполнено ЭП КС одной хирургической бригадой.
Критерии включения в исследование:
- 2-3 стадии деформирующего артроза КС по классификации Н.С. Косинской [15];
- костные дефекты 1-2А типа по классификации AORI [16];
- отсутствие предшествующих операций на КС в анамнезе;
- отсутствие тяжелых травм КС с наличием гемартроза;
- сроки полноценной осевой нагрузки не ранее 4 нед. с момента операции.
Критерии невключения в исследование:
- 1 стадия деформирующего артроза КС по классификации Н.С. Косинской;
- тяжелые варусные/вальгусные деформации КС;
- наличие в анамнезе разрывов/повреждений латеральной или медиальной коллатеральной связки, приведших к нестабильности КС;
- наличие активного инфекционного процесса в области КС в предоперационном периоде.
Все пациенты были разделены на две группы исследования: группу 1 составили 29 (46,8%) пациентов (34 операции ЭП КС) с терминальной стадией ХБП 5Д степени (хронический гемодиализ), в группу 2 вошли 33 (53,2%) пациента (37 операций) с различными формами гонартроза без патологии почек. Средний период наблюдения в обеих группах составил 3,7 года (min — 1, max — 6). Основные характеристики пациентов представлены в таблице 1.
Пациенты обеих групп были сопоставимы по тяжести деформирующего артроза КС, объему предоперационного обследования, а также послеоперационному ведению. В выборку обеих групп исследования рандомизированно были включены пациенты, которым имплантировались эндопротезы одного производителя (Zimmer NexGen, Warsaw, США), но с различными вариантами степени связанности: от CR (cruciate retaining) до VVC (varus-valgus constrained). Полностью связанные системы (RHK — rotational hinge knee) из исследования исключались на этапе выборки групп исследования (табл. 2).
В обеих группах исследования для фиксации компонентов эндопротеза применялся костный цемент с гентамицином (Synicem 1G, 40 г).
Таблица 1
|
Показатель |
Группа I (n = 29) 34 операции |
Группа 2 (n = 33) 37 операции |
Р |
|
Пол, n (%) |
|
|
|
|
муж. |
6 (20,6) |
9 (27,7) |
- |
|
жен. |
23 (79,4) |
24 (72,3) |
|
|
Средний возраст, лет, |
57,1±8,7; 58 |
66,7±9,5; 64 |
0,00002 |
|
M±SD; Me (Q1-Q3) |
(53,25-63,00) |
(60,00-76,00) |
|
|
ИМТ, M±SD |
23,8±3,1 |
30,9±4,3 |
0,00001 |
|
Сторона поражения, n (%) |
|
|
|
|
правая |
19 (55,9) |
18 (48,6) |
- |
|
левая |
15 (44,1) |
19 (51,4) |
|
|
Деформация КС, n (%) |
|
|
|
|
варусная |
30 (88,3) |
34 (91,9) |
- |
|
вальгусная |
4 (11,7) |
3 (8,1) |
|
|
Средний срок стационарного лечения, койко-дней; |
15,3; |
8,8; |
0,00001 |
|
Me (min/max) |
14 (8/33) |
9(5/15) |
|
|
Морфокортикальный индекс большеберцовой кости |
35,3; 33 |
40,8; 40 |
0,002 |
|
(Бернарда - Лаваля - Жентета)*, ед.; Me (min/max) |
(21/57) |
(28/51) |
Маркс В.О. Ортопедическая диагностика. Минск: Наука и техника. 1978. С. 504-505.
Основные характеристики имплантированных эндопротезов
Таблица 2
|
Характеристика имплантатов |
Группа 1 (n = 34) |
Группа 2 (n = 37) |
|
Степень связанности эндопротеза: |
|
|
|
CR |
2 (5,9%) |
31 (83,8%) |
|
PS (posterior stabilized) |
28 (82,4%) |
5 (13,5%) |
|
VVC |
4 (11,7%) |
1 (2,7%) |
|
Модульность тибиального компонента: |
|
|
|
All Poly |
7 (20,6%) |
29 (78,4%) |
|
Metal-back |
24 (70,6%) |
7 (18,9%) |
|
Precoat + ножка |
3 (8,8%) |
1 (2,7%) |
|
Модульность бедренного компонента: |
|
|
|
стандартный бедренный компонент |
33 (97,1%) |
37 (100%) |
|
ревизионный компонент + ножка |
1 (2,9%) |
0 |
|
Замещение костного дефекта: |
|
|
|
цемент |
4 (11,7%) |
2 (5,4%) |
|
аутокость |
2 (5,9%) |
3 (8,1%) |
|
аллокость |
0 |
0 |
|
металлический аугмент |
4 (11,7%) |
1 (2,7%) |
Средняя продолжительность гемодиализа до операции у пациентов группы 1 составила 7,7 лет (min — 1, max — 15 лет). Процедура гемодиализа выполнялась не позднее чем за 24 ч. до эндопротезирования с целью минимизации осложнений со стороны сердечно-сосудистой системы и водно-электролитной нагрузки во время операции. Оценка качества гемодиализа оценивалась посредством определения индекса kt/V (коэффициентом очищения), который у всех пациентов составлял 1,34, что свидетельствовало об адекватности использованных в предоперационном периоде диализатов.
Пациентам обеих групп перед операцией выполнялись инфузия транексамовой кислоты, а также тромбопрофилактика согласно новым методическим рекомендациям по профилактике, диагностике и лечению тромбоэмболических осложнений в травматологии и ортопедии, утвержденным в 2022 г. [17]. Стандартная антибиотикопрофилактика пациентам гемодиализного профиля, утвержденная локальным приказом, предполагала использование защищенных пени- циллинов в уменьшенной дозировке и в меньшей кратности введения в течение 5 дней после процедуры гемодиализа. Полноценная нагрузка разрешалась только через 4-6 нед. после операции.
Степень выраженности остеопороза у пациентов обеих групп исследования определялась рентгенометрическим методом согласно морфо-кортикальному индексу Бернарда- Лаваля - Жентета. Нормальные показатели данного индекса находятся в пределах 48±9 ед., при индексе менее 40 ед. устанавливался диагноз остеопороза проксимального отдела большеберцовой кости.
Оценка результатов
В предоперационном периоде производилась оценка состояния и функции коленного сустава по шкале KSS Function Score [18]. В процессе клинического обследования выполняли тесты на варус- вальгусный стресс, Лахмана, «переднего и заднего выдвижного ящика», оценивали степень выраженности остеопороза по стандартным рентгенограммам и при необходимости — по данным МСКТ. В процессе хирургического вмешательства оценивали среднюю продолжительность операции, объем периоперационной кровопотери, показатели стабильности гемодинамики, тип связанности эндопротеза в зависимости от степени балансировки коллатеральных связок и состоятельности задней крестообразной связки (ЗКС). Функциональные показатели по шкале KSS Function Score оценивались через 6 и 12 мес., затем ежегодно. Показатели по шкале FJS-12 после ЭП КС оценивались через 12 мес. и далее ежегодно [19]. Расчет рентгенологических критериев асептического расшатывания компонентов эндопротеза по системе KRESS (Total Knee Arthroplasty Roentgenographic Evaluation and Scoring System) производился в баллах в среднем через 43 мес. (min -13, max — 72) [20]. Также оценивалась частота различных осложнений в течение всего периода наблюдения.
Статистический анализ
Статистическая обработка полученных данных производилась при помощи программы IBM SPSS v. 20.
Нормальность распределения количественных показателей,таких как возраст, продолжительность стационарного лечения, морфо-кортикальный индекс, ИМТ, длительность гемодиализа, функциональные характеристики коленного сустава в баллах по KSS Function Score, шкале FJS-12 и рентгенологические показатели по шкале KRESS, проводилась на основании критерия Шапиро - Уилка (в модификации J.P. Royston). При ненормальном распределении связанных выборок использовался критерий Вилкоксона, для несвязанных — критерий Манна - Уитни, при нормальном — критерий Стьюдента для связанных и несвязанных выборок. Для оценки значимости влияния вероятности развития осложнений в зависимости от наличия или отсутствия хронического гемодиализа использовался критерий х2 с поправкой на правдоподобие и оценкой силы связи по коэффициенту сопряженности Пирсона.
Результаты
Средние сроки стационарного лечения отличались между группами. У пациентов группы 1, получавших гемодиализ 3 раза в неделю, продолжительность стационарного лечения была больше в 1,7 раза, что косвенно свидетельствует о больших экономических затратах на лечение одного пациента.
Функциональные результаты по шкале KSS Function Score в предоперационном периоде статистически не отличались между группами и в среднем составили 48 баллов (рис. 1). Через 6, 12, 24 и 36 мес. после операции статистически значимой разницы между группами по шкале KSS Function Score также не выявлено. Однако к 4-му году после первичного ЭП КС в группе пациентов, получавших гемодиализ, средние показатели по шкале KSS Function Score снизились до 77,3 баллов, что, скорее всего, обусловлено инфекционными осложнениями сразу у 5 пациентов. В группе 2 отмечено лишь одно инфекционное осложнение спустя 48 мес. после эндопротезирования.
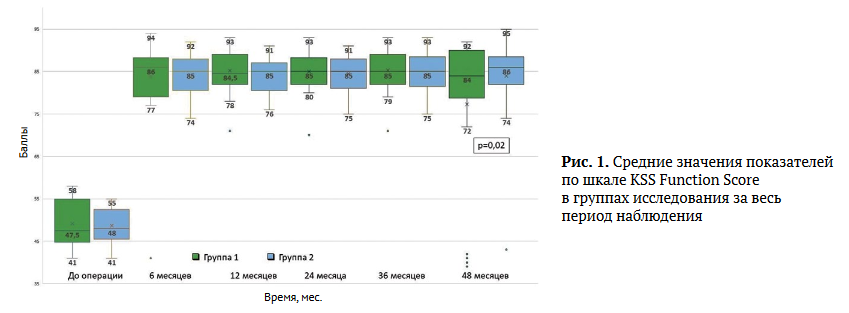
Оценка по шкале FJS-12 в сроки 12-36 мес. после тотального ЭП КС у пациентов группы 1 в среднем составила 77,04 баллов (SD = 3,9) (рис. 2).
В группе 2 (без терминальной почечной патологии) показатель по шкале FJS-12 был хуже и составлял в среднем 68,72 балла (SD = 4,8). Получена статистически значимая разница (р<0,0001) в результатах по шкале FJS-12 между группами исследования в первые три года после эндопротезирования КС (рис. 2). Но в сроки более трех лет разницы между группами уже не выявлено, что связано с увеличением количества осложнений в группе 1.
Лучшие показатели по шкале FJS-12 в группе 1 на ранних сроках после операции, скорее всего, связаны с наличием тяжелых форм полинейропатии, развивающейся на поздних стадиях ХБП, что обуславливает резкое снижение порога болевой чувствительности. Поэтому любое улучшение физического и функционального статуса, а также состояния ноцицептивной системы у пациентов гемодиализного профиля приводит к лучшим показателям по шкале FJS-12.
Рентгенологические результаты по шкале KRESS через 43 мес. статистически не отличались между группами исследования (min — 12, max — 72). В таблице 3 отражены результаты в зависимости от количества баллов, полученных методом подсчета линий просветления в различных зонах на границе «кость — имплантат» по стандартным рентгенограммам в прямой и боковой проекциях. У пациентов обеих групп не выявлено миграции компонентов эндопротеза после первичного ЭП КС. Однако большое число наблюдений с пограничными значениями (Ме = 3; 1-7) в группе 1 свидетельствует о возрастающем риске ревизионных вмешательств у пациентов с терминальной стадией ХБП после ЭП КС. Также необходимо отметить, что по шкале KRESS в 89% случаев линии просветления диагностированы со стороны тибиального компонента эндопротеза.
Клиническим примером асептического расшатывания большеберцового компонента эндопротеза, приведшего к инфекционному осложнению у пациента группы 1 после первичного ЭП КС, может служить наблюдение, продемонстрированное на рисунке 3.
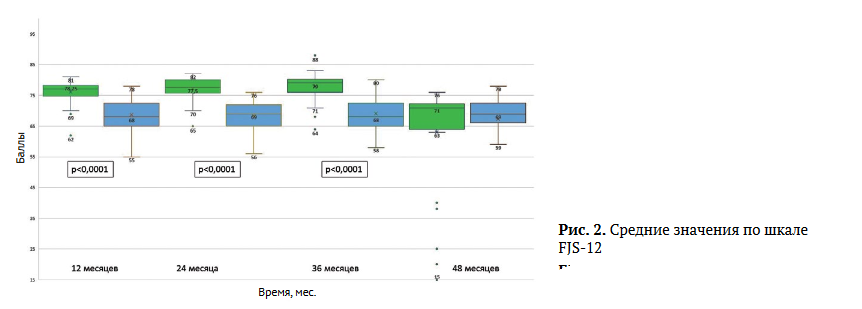
Оценка рентгенологических результатов по шкале KRESS в средние сроки наблюдения 43 мес.
Таблица 3
|
Линия просветления |
Группа 1 (n = 34) |
Группа 2 (n = 37) |
Р |
|
Менее 4 баллов — несущественная |
23 (67,7%) |
34 (91,9%) |
0,06 |
|
5-9 баллов — необходимо наблюдение в динамике |
11 (32,3%) |
3 (8,1%) |
0,05 |
|
Более 10 баллов — миграция компонентов |
- |
- |
- |
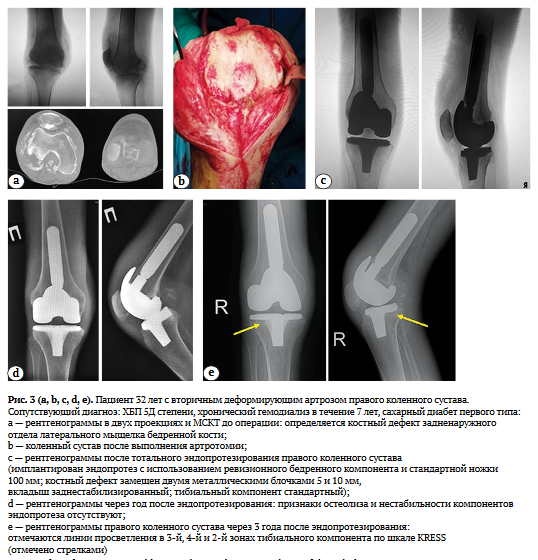
Таблица 4
Структура ортопедических осложнений в группах исследования
|
Осложнение |
Группа 1 (n = 34) |
Группа 2 (n = 37) |
Р |
|
Асептическое расшатывание |
0 |
0 |
- |
|
Перипротезный перелом |
1 (2,9%) |
0 |
>0,05 |
|
Глубокая перипротезная инфекция |
6 (17,6%) |
1 (2,7%) |
>0,05 |
|
Остаточная контрактура сустава |
1 (2,9%) |
1 (2,7%) |
>0,05 |
|
Всего |
8 (23,5%) |
2 (5,4%) |
0,05 |
Ортопедических осложнений после первичного ЭП КС было прогнозируемо больше в группе 1 (табл. 4).
Необходимо отметить, что суммарное количество осложнений не отличалось между группами, но отсутствие статистической значимости свидетельствует о необходимости дальнейших исследований в этом направлении.
Возможно, при увеличении выборки пациентов и на более поздних сроках наблюдения частота ортопедических осложнений будет статистически отличаться между пациентами, перенесшими ЭП КС с терминальной стадией ХБП, и пациентами без патологии почек. Тем не менее частота ППИ была существенно выше среди пациентов, получающих гемодиализ. Кроме того, у одного пациента группы 1 при имплантации тибиального компонента произошла перфорация латеральной стенки большеберцовой кости в связи с выраженным остеопорозом. После дополнительной оценки степени тяжести пери- протезного перелома было принято решение об иммобилизации КС в ортезе и ограничении осевой нагрузки сроком до 6 нед.
Обсуждение
Анализируя средний возраст пациентов гемодиализного профиля, перенесших тотальное ЭП КС, мы обнаружили, что данный показатель (57,1±8,7; Me — 58) был существенно ниже по сравнению со средним возрастом пациентов без терминальной стадии ХБП (66,7±9,5; Me — 64 года). Это соответствует данным N. Venishetty с соавторами [21]. Согласно последним отчетам регистра артро- пластики Швеции, средний возраст пациентов, перенесших ЭП КС, составляет 69,1±9,0 лет, регистра артропластики Англии и Уэльса — 70,0±7,0 лет, регистра эндопротезирования США — 67,2±9,4 года [22, 23, 24].
По данным регистра эндопротезирования НМИЦ ТО им. Р.Р. Вредена, этот показатель в 2019 г. составлял 63,4 года, увеличиваясь за предыдущие несколько лет [25]. Гендерное соотношение мужчин и женщин с дегенеративно-дистрофическими изменениями коленного сустава, получающих заместительную почечную терапию, соответствует общей популяции (мужчин — 20,6%, женщин — 79,4%; соотношение 1:5).
Особого внимания заслуживают данные, полученные при анализе степени связанности компонентов эндопротеза КС у пациентов гемодиализного профиля, в сравнении с пациентами группы 2 (см. табл. 2). Согласно данным регистра артропла- стики Англии и Уэльса за 2022 г., частота имплантации цементных эндопротезов с сохранением ЗКС составила 62,7%, заднестабилизированных (PS) — 15,3%, варус-вальгус связанных (VVC) — 1,7% [23].
Примерно такие же данные демонстрирует регистр эндопротезирования США: CR эндопротезы — 57,4%, PS — 42,5%, VVC — 0,2% с тенденцией к ежегодному увеличению частоты использования менее связанных эндопротезов, применяемых при первичном ЭП КС [24]. Несмотря на отсутствие в современной литературе сообщений об отдаленных результатах ЭП КС с применением CR и PS систем [26], в некоторых исследованиях, таких как работа G. Thuysbaert с соавторами, говорится о статистически значимых различиях в показателях по шкале FJS-12 при использовании эндопротезов CR и PS [27]. Именно этим во многом обусловлено увеличение частоты использования менее связанных систем в западноевропейских странах. Однако в нашем исследовании доля CR эндопротезов у гемодиализных пациентов составила всего 5,9%, PS — 82,4% и VVC — 11,7%.
Окончательный выбор степени связанности эндопротеза производился интраоперационно в обеих группах исследования в зависимости от состояния параартикулярных мягких тканей, эластичности коллатеральных связок и ЗКС, степени выраженности остеопороза, а также наличия и величины костных дефектов. У пациентов гемодиализного профиля в большинстве случаев отмечались слабость и гиперэластичность мягких тканей, задней капсулы, связок и мышц, окружающих КС, которые были связаны как с наличием сопутствующей ренальной миодистрофии, так и с отложениями р-2 микроглобулиновых амилоидных фибрилл вокруг КС, подтвержденных гистологическими исследованиями. Кроме того, происходило формирование костных кист в мыщелках бедренной и/или большеберцовой костей, также заполненных р-2 микроглобулиновыми амилоидными комплексами (рис. 4).
Схожие результаты были получены при анализе модульности тибиального компонента. Так, у пациентов группы 1, получавших гемодиализ, в 79% случаев имплантировали большеберцовые компоненты на металлической основе и лишь в 20,6% наблюдений — полиэтиленовые моноблоки, что отличается от показателей применения большеберцовых компонентов в группе больных без патологии почек. В работе K.A. Gustke с соавторами сообщается о более частом использовании полиэтиленовых тибиальных моноблоков у пациентов пожилого и старческого возраста [28]. V. Apostolopoulos с соавторами сообщают о лучших показателях 10-летней выживаемости эндопротезов All Poly Tibial (97,1%) в сравнении с Metal-back Tibial (93,2%) [29].
У пациентов группы 1, длительно находящихся на хроническом гемодиализе, в 29,4% случаев потребовалось применение различных методик замещения костных дефектов.
Такая высокая частота компенсации дефицита костной массы обусловлена формированием костных кист в мыщелках бедренной и/или большеберцовой костей, также заполненных р-2 микроглобулиновыми амилоидными комплексами.
По данным G.F. Scheumann с соавторами, наиболее типичными локализациями формирования костных кист у пациентов, длительное время получающих гемодиализ, являются головка и шейка бедренной кости, позвоночник, дистальный метаэпифиз лучевой кости, мыщелки бедра [30].
Одним из наиболее частых осложнений ЭП КС является глубокая ППИ. По данным A.I. Stavrakis с соавторами, частота развития ППИ в течение 90 дней после ЭП КС у пациентов гемодиализного профиля составляет 2,66% [12]. В более поздние сроки наблюдения инфекционные осложнения у больных, находящихся на гемодиализе, достигают 18% и более [9]. В нашем исследовании частота инфекционных осложнений среди пациентов с терминальной стадией ХБП через 3,4 года составила 17,6%, что сопоставимо с данными литературы. При этом мы не наблюдали ранних инфекционных осложнений в первый год после ЭП КС, что может быть связано как с рутинным использованием цемента с антибиотиком для фиксации компонентов эндопротеза, так и с индивидуальным подходом к продленной антибиотикопрофилактике у данной категории пациентов.
Первичное ЭП КС у пациентов, получающих лечение в виде хронического гемодиализа, можно отнести к категории первичных сложных вмешательств. Это связано с возрастными и конституциональными характеристиками пациентов гемодиализного профиля, которые существенно отличаются от пациентов без патологии почек. Средние сроки стационарного лечения пациентов с терминальной стадией ХБП больше в 1,7 раза, а частота осложнений составила 23,5% в средние сроки наблюдения 3,7 года. При этом в первые три года отмечались лучшие показатели по шкалам KSS Function Score и FJS-12, что может быть обусловлено сопутствующей ренальной полинейропатией, снижающей порог болевой чувствительности, а также менее выраженной требовательностью к результатам артроплас- тики коленного сустава. Пациентам, получавшим гемодиализ, чаще имплантировали более связанные эндопротезы коленного сустава (PS и VVC) по сравнению с пациентами обычной популяции, а также модульные большеберцовые и бедренные компоненты, что связано как с наличием выраженного сопутствующего системного остеопороза, так и с формированием р-2 микроглобулиновых амилоидных комплексов вдоль капсулы сустава, связок, мышечных волокон и формированием костных кист в мыщелках бедренной и большеберцовой костей.
Литература1. Преображенский П.М., Филь А.С., Корнилов Н.Н., Пантелеев А.Н., Гуацаев М.С., Каземирский А.В. и др. Эндопротезирование коленного сустава в клинической практике: анализ 36 350 наблюдений из регистра НМИЦ ТО имени Р.Р. Вредена. Травматология и ортопедия России. 2023;29(3):73-85. doi: 10.17816/2311-2905-9349.
2. Середа А.П., Кочиш А.А., Черный А.А., Антипов А.П., Алиев А.Г., Вебер Е.В. и др. Эпидемиология эндопротезирования тазобедренного и коленного суставов и перипротезной инфекции в Российской Федерации. Травматология и ортопедия России. 2021;27(3):84-93. doi: 10.21823/2311-2905-2021-27-3-84-93..
3. Singh J.A. Epidemiology of knee and hip arthroplasty: a systematic review. Open Orthop J. 2011;5:80-85. doi: 10.2174/1874325001105010080.
4. Evans
J.T., Walker R.W., Evans J.P., Blom A.W., Sayers A., Whitehouse M.R. How long
does a knee replacement last? A systematic review and meta-analysis of case
series and national registry reports with more than 15 years of follow-up.
5. Pollock M., Somerville L., Firth A., Lanting B. Outpatient Total Hip Arthroplasty, Total Knee Arthroplasty, and Unicompartmental Knee Arthroplasty: A Systematic Review of the Literature. JBJS Rev. 2016;4(12):e4.
6. Муштин Н.Е., Цед А.Н., Дулаев А.К., Леонтьева Н.В., Румянцев А.Ш. Возможности использования фракционированных и нефракционированных гепаринов после первичного эндопротезирования тазобедренного и коленного суставов у пациентов, получающих программный гемодиализ. Нефрология. 2020;24(6): 55-64. doi: 10.36485/1561-6274-2020-24-6-55-64. Mushtin N.E., Tsed A.N., Dulaev A.K., Leontyeva N.V., Rumyantsev A.Sh. Comparison of using fractionated and unfractionated heparins after primary hip and knee arthroplasty in patients receiving programmed hemodialysis. Nephrology (Saint-Petersburg). 2020;24(6):55-64. (In Russian). doi: 10.36485/1561-6274-2020-24-6-55-64.
7. Петрова Е.Н., Полушин Ю.С., Шлык И.В., Цед А.Н. Особенности периоперационного ведения пациентов с терминальной стадией хронической болезни почек при эндопротезировании тазобедренного и коленного суставов. Альманах клинической медицины.
8. Цед А.Н., Дулаев А.К., Муштин Н.Е., Ильющенко К.Г., Шмелев А.В. Среднесрочные результаты первичного эндопротезирования тазобедренного сустава у пациентов с терминальной стадией хронической болезни почек. Травматология и ортопедия России. 2019;25(2):44-54. doi: 10.21823/2311-2905-2019-25-2-44-54.
9. Inoue
D., Yazdi H., Goswami K., Tan T.L., Parvizi J. Comparison of Postoperative
Complications and Survivorship of Total Hip and Knee Arthroplasty in Dialysis
and Renal Transplantation Patients. J Arthroplasty. 2020;35(4):971-975.
10. Gkiatas I., Xiang W., Karasavvidis T., Windsor E.N., Sharma A.K., Sculco P.K. Total knee arthroplasty in dialysis patients: Is it safe? A systematic review of the literature. J Orthop. 2021;25:199-206. doi: 10.1016/j.jor.2021.05.025.
11. Мурылев В.Ю., Цыгин Н.А., Шутов Е.В., Жучков А.Г., Рукин Я.А., Сорокина Г.Л. и др. Эндопротезирование крупных суставов у больных, получающих лечение программным диализом. Результаты лечения в одном центре и обзор литературы. Нефрология и диализ. 2019;21(2):221-233.
12. Stavrakis A.I., Li A.K., Uquillas C., Photopoulos C. Comparison of Total Knee Arthroplasty Outcomes Between Renal Transplant and End Stage Renal Disease Patients. J Am Acad Orthop Surg Glob Res Rev. 2022; 6(3):e21.00288. doi: 10.5435/JAAOSGlobal-D-21-00288.
13. Мурылев В.Ю., Цыгин Н.А., Шутов Е.В., Жучков А.Г., Рукин Я.А. Тотальное эндопротезирование тазобедренных и коленных суставов у пациентов с хронической болезнью почек (обзор литературы). Травматология и ортопедия России. 2018;24(2):138- 145. doi: 10.21823/2311-2905-2018-24-2-138-145. Murylev V.Y., Tsygin N.A., Shutov E.V., Zhuchkov A.G., Rukin Y.A. Total hip and knee arthroplasty in patients with chronic kidney disease (review). Traumatology and Orthopedics of Russia. 2018;24(2):138-145. (In Russian). doi: 10.21823/2311-2905-2018-24-2-138-145.
14. Цед А.Н., Смирнов А.В., Дулаев А.К., Румянцев А.Ш., Ананьев А.Н. Патологические повреждения костей и суставов у больных на программном гемодиализе в Санкт-Петербурге. Нефрология.2019;23(6):73-82. doi: 10.36485/1561-6274-2019-236-73-82.
15. Косинская Н.С. Дегенеративно-дистрофические поражения костно-суставного аппарата. Медгиз: Ленинград; 1961. с. 98.
16. Engh G.A., Ammeen D.J. Classification and preoperative radiographic evaluation: knee. Orthop Clin North Am. 1998;29(2):205-217. doi: 10.1016/s0030-5898(05)70319-9.
17. Божкова С.А., Тихилов Р.М., Андрияшкин В.В., Ахтямов И.Ф., Белов М.В., Дианов С.В. и др. Профилактика, диагностика и лечение тромбоэмболических осложнений в травматологии и ортопедии: методические рекомендации. Травматология и ортопедия России. 2022;28(3):136-166. doi: 10.17816/2311-2905-1993.
18. Lingard E.A., Katz J.N., Wright R.J., Wright E.A,. Sledge C.B.; Kinemax Outcomes Group. Validity and responsiveness of the Knee Society Clinical Rating System in comparison with the SF-36 and WOMAC. J Bone Joint Surg Am. 2001; 83(12):1856-1864. doi: 10.2106/00004623-200112000-00014.
19. Behrend H., Giesinger K., Giesinger J.M., Kuster M.S. The “forgotten joint” as the ultimate goal in joint arthroplasty: validation of a new patient-reported outcome measure. J Arthroplasty. 2012;27(3):430-436.e1. doi: 10.1016/j.arth.2011.06.035.
20. Ewald F.C. The Knee Society total knee arthroplasty roentgenographic evaluation and scoring system. Clin Orthop Relat Res. 1989;(248):9-12.
21. Venishetty N., Wukich D.K., Beale J., Riley Martinez J., Toutoungy M., Mounasamy V. et al. Total knee arthroplasty in dialysis patients: a national inpatient sample-based study of perioperative complications. Knee Surg Relat Res. 2023;35(1):22. doi: 10.1186/s43019-023-00196-0.
22. Swedish Arthroplasty Register The Swedish arthroplasty register annual report 2021.
23. The
National Joint Registry 19-th Annual Report 2022 [Internet]. London: National
Joint Registry; 2022 Oct.
24. The Ninth Annual Report
of the American Joint Replacement Registry on Hip and Knee Arthroplasty, 2022.
25. Филь А., Тараканов В., Куляба Т., Корнилов Н. Тренды в первичной артропластике коленного сустава в Национальном медицинском исследовательском центре травматологии и ортопедии им. Р.Р. Вредена и их сравнительный анализ с данными международных национальных регистров: схож ли наш путь? Гений ортопедии. 2020;26(4):476-483. doi: 10.18019/1028-4427-2020-26-4-476-483.
26. Li N., Tan Y., Deng Y., Chen L. Posterior cruciate-retaining versus posterior stabilized total knee arthroplasty: a meta-analysis of randomized controlled trials. Knee Surg Sports Traumatol Arthrosc. 2014;22(3):556-564. doi: 10.1007/s00167-012-2275-0.
27. Thuysbaert G., Luyckx T., Ryckaert A., Gunst P., Noyez J., Winnock De Grave P. Reduced joint awareness after total knee arthroplasty with a cruciate retaining design. Acta Orthop Belg. 2020;86(3):482-488.
28. Gustke K.A., Gelbke M.K. All-polyethylene tibial component use for elderly, low-demand total knee arthroplasty patients. J Arthroplasty. 2017;32(8):2421- 2426. doi: 10.1016/j.arth.2017.02.077.
29. Apostolopoulos V., Nachtnebl L., Mahdal M., Pazourek L., Bohac P., Jamcek P. et al. Clinical outcomes and survival comparison between NexGen all-poly and its metal-backed equivalent in total knee arthroplasty. Int Orthop. 2023;47(9):2207-2213. doi: 10.1007/s00264-023-05772-3.
30. Scheumann G.F., Holch M., Nerlich M.L., Brandis A., Ostertag H., Tscherne H. Pathological fractures and lytic bone lesion of the femoral neck associated with beta 2-microglobulin amyloid deposition in longterm dialysis patients. Arch Orthop Trauma Surg. 1991;110(2):93-97. doi: 10.1007/BF00393881.
Сведения об авторах
Муштин Никита Евгеньевич — канд. мед. наук
Цед Александр Николаевич — д-р мед. наук
Дулаев Александр Кайсинович — д-р мед. наук, профессор
Шмелев Антон Владимирович
Теги: эндопротезирование коленного сустава
234567 Начало активности (дата): 10.01.2024 18:06:00
234567 Кем создан (ID): 989
234567 Ключевые слова: эндопротезирование коленного сустава, хронический гемодиализ, хроническая болезнь почек
12354567899
Похожие статьи
Результаты лечения пациентов с переломами лодыжек и заднего края большеберцовой кости с использованием различных вариантов хирургической техникиРентген на дому 8 495 22 555 6 8
Среднесрочные результаты лечения перипротезной инфекции с применением спейсеров с углеродным покрытием, импрегнированных серебром
Перипротезная инфекция коленного и тазобедренного суставов - можно ли сравнивать результаты лечения?
Оригинальный направитель для малоинвазивной дистальной остеотомии первой плюсневой кости при лечении вальгусной деформации первого пальца стопы



