 30.11.2023
30.11.2023
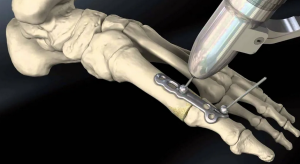
Хондропластика в лечении больных с остеоартритом первого плюснефалангового сустава
В мировой литературе только один автор предлагает метод хирургического лечения ОА I ПФС, схожий с тем, который использовался в нашем исследовании - модифицированный вариант хондропластики - MAST
Актуальность темы исследования
- Остеоартрит (ОА) I плюснефалангового сустава (I ПФС) - заболевание, характеризующееся наличием боли, усиливающейся при ходьбе, скованностью в суставе и снижением объема движений, особенно тыльного сгибания. В литературе ОА I ПФС чаще всего обозначается термином halluxrigidus(ригидный I палец стопы) [McNeil, D., 2013; Mackey, R., 2010; Бобров, Д., 2014].
Hallux rigidus (HR) является вторым по частоте после вальгусной деформации I пальца патологическим состоянием стопы и встречается, по данным литературы, у 2,5-10% взрослого населения [Бобров, Д., 2014; Бережной, С., 2017; Konkel, K., 2008].
В настоящее время общего подхода к выбору хирургической тактики при hallux rigidus не существует [Бережной, С., 2017; Мазалов, А., 2011; Polzer, H., 2014]. Основные методы хирургического лечения на сегодняшний день - хейлэктомия и артродез I ПФС. Тем не менее при хейлэктомии авторы отмечают рецидив развития дорсального остеофита в 30% случаев; более чем у 40% прооперированных пациентов сохраняется боль в среднем диапазоне движений, а на поздних стадиях ОА I ПФС у большинства пациентов возникала необходимость в повторном хирургическом лечении в виде артродеза I ПФС [Coughlin, M., 2003; Ho, B., 2017].
Артродез I ПФС чаще всего применяется на поздних стадиях ОА I ПФС. Данный метод считается «золотым стандартом», так как обеспечивает быстрое купирование болевого синдрома [Garras, D., 2013; Fazal, M., 2018]; однако после артродеза I ПФС могут развиваться такие осложнения, как метатарзалгия (9,8%), несостоятельность артродеза (7,8%), смещение артродезируемых поверхностей (7,8%), боль в межфаланговом суставе (3,9%), замедленная консолидация (2%) [Kim, P., 2012].
В свою очередь, известно, что при наличии костно-хрящевых дефектов в коленном, тазобедренном и голеностопном суставах довольно успешно применяется техника хондропластики с использованием коллагеновой матрицы, индуцирующей процесс аутологичного хондрогенеза, при котором происходит формирование из стволовых клеток гиалиноподобной ткани [Panni, A., 2018; Kaiser, N., 2020; Bertho, P., 2018; Лазишвили, Г., 2020; Егиазарян, К., 2020].
В связи с описанной эффективностью данного метода при наличии дефектов хряща в коленном, тазобедренном и голеностопном суставах [Panni, A., 2018; Kaiser, N., 2020; Bertho, P., 2018; Лазишвили, Г., 2020; Егиазарян, К., 2020] нами предложено применение хондропластики с использованием коллагеновой матрицы в качестве нового способа хирургического лечения пациентов с ОА I ПФС.
В мировой литературе только один автор предлагает метод хирургического лечения ОА I ПФС, схожий с тем, который использовался в нашем исследовании - модифицированный вариант хондропластики - MAST (matrix-associated stem cell transplantation) [Richter, M., 2017; Richter, M., 2019; Richter, M., 2020]. M. Richter проводил наблюдение за пациентами (n = 20) в течение 2 лет после выполненной хондропластики I ПФС, при этом отмечал значительное улучшение клинических показателей как в раннем послеоперационном периоде, так и через вышеуказанный промежуток времени, в том числе, увеличение объема движений в I ПФС [Richter, M., 2019].
Таким образом, существующие хирургические методики, в отличие от хондропластики, не позволяют достичь хороших результатов лечения пациентов с ОА I ПФС.
Цель исследования - улучшить результаты хирургического лечения пациентов с ОА I ПФС путём разработки суставсберегающего метода с использованием коллагеновой матрицы, индуцирующей хондрогенез.
Задача исследования
1. Проанализировать исходы лечения больных с ОА I ПФС после хейлэктомии и артродеза I ПФС.
2. Разработать хирургическую технику суставсберегающей операции при ОА I ПФС с использованием коллагеновой матрицы для стимуляции хондрогенеза.
3. Определить показания и противопоказания к выполнению разработанного способа хондропластики I ПФС.
4. Проанализировать ближайшие и среднесрочные результаты разработанной хирургической методики.
5. Оценить эффективность методики у пациентов разных возрастных групп, а также у пациентов, страдающих системными ревматическими заболеваниями (РЗ).
Научная новизна. Научная новизна диссертационной работы заключается в том, что разработан новый способ суставсберегающей операции при ОА I ПФС по технике хондропластики на коллагеновой матрице (получен патент РФ № 2737710 на изобретение: «Способ лечения артроза первого плюснефалангового сустава» от 02.12.2020); определены показания и противопоказания к разработанной методике хондропластики I ПФС; доказана эффективность хондропластики у больных с ОА I ПФС на всех стадиях заболевания; обоснована возможность применения разработанной операции у больных с системными воспалительными РЗ.
Практическая значимость работы. Разработанная новая хирургическая методика позволит улучшить функциональные результаты хирургического лечения пациентов с ОА I ПФС и сократить сроки послеоперационной реабилитации
Положеня:
1. Разработанная хирургическая техника хондропластики I ПФС с использованием коллагеновой матрицы является эффективным методом хирургического лечения, позволяющим купировать боль и улучшить функцию стопы у больных с ОА I ПФС как на ранних, так и на поздних стадиях заболевания.
2. Хондропластика I ПФС с использованием коллагеновой матрицы может применяться у пациентов, страдающих системными воспалительными РЗ с низкой активностью или в ремиссии заболевания (при ревматоидном артрите активность по DAS28 < 3,2; при анкилозирующем спондилите активность по BASDAI < 2,0).
3. Разработанная операция может быть использована для лечения пациентов с ОА I ПФС как молодого, так и пожилого возраста.
Степень достоверности результатов исследования. Достоверность данных подтверждается достаточным количеством больных в исследовании (41 пациентов, 44 стопы) для реализации поставленных цели и задач. Для анализа полученных результатов и осложнений использовали современные методы статистической обработки данных с применением компьютерной программы BioStat®. Выводы и практические рекомендации подкреплены данными, представленными в таблицах и рисунках, демонстрирующих результаты исследования и подтверждающих положения, выносимые на защиту.
Внедрение результатов исследования. Разработанная хирургическая техника применяется у пациентов, страдающих ОА I ПФС, в том числе на поздних стадиях заболевания. Результаты диссертационной работы внедрены в практическую работу травматолого-ортопедического отделения ФГБНУ НИИР имени В. А. Насоновой.
Методология и методы исследования. Хондропластику выполняли пациентам, страдающим ОА I ПФС 1-4 стадии по классификации Coughlin- Shumas. Группу контроля №1 составили 22 больных, которым была выполнена хейлэктомия без хондропластики. В группу контроля №2 были включены 27 пациентов, которым выполнялся артродез I ПФС. В основной группе 41 пациентам выполняли хондропластику I ПФС с применением разработанной хирургической техники с использованием коллагеновой матрицы (44 операции). Пациенты основной группы были также разделены на две группы сравнения в зависимости от возраста, а также наличия или отсутствия системного ревматического заболевания. При выполнении работы использовались общие и специальные методы исследования.
Апробация диссертации. Результаты исследования были представлены на Российских и международных съездах, конференциях, конгрессах, форумах: Научно-практическая конференция «Новые концепции диагностики и лечения остеоартроза» (Астрахань, 2018 г.); II Международный конгресс ассоциации ревмоортопедов, (Москва, 2018 г.); 39th SICOT Orthopaedic World Congress (Монреаль, 2018 г.); XIV Межрегиональная научно-практическая конференция «Организационные и клинические вопросы оказания помощи больным в травматологии и ортопедии», (Воронеж, 2018 г.); III Конгресс Российской ассоциации хирургов стопы и голеностопного сустава, (Санкт-Петербург, 2019 г.); 40th SICOT Orthopaedic World Congress., (Маскат, 2019 г.); III Международный конгресс ассоциации ревмоортопедов (Москва, 2019 г.).
Личный вклад автора. Автором изучены существующие в настоящее время методы хирургического лечения ОА I ПФС. Автор участвовал в разработке хирургической техники хондропластики I ПФС с использованием коллагеновой матрицы, принимал непосредственное участие в операциях. Автором осуществлен сбор, статистическая и компьютерная обработка первичного материала; проведен анализ обобщенных данных; сформулированы выводы; оформлены результаты исследования и представлены в виде диссертационной работы.
Соответствие диссертации паспортам научных специальностей. Научные положения диссертации соответствуют паспорту специальности 14.01.15 - травматология и ортопедия. Результаты проведенного исследования соответствуют области исследования специальности 14.01.15 - травматология и ортопедия.
Публикации по теме диссертации. Основные результаты диссертации опубликованы в 15 научных работах, из них 3 статьи в журналах, рекомендованных ВАК, 1 статья в журнале международной базы Scopus. Получен патент Российской Федерации № 2737710 на изобретение: «Способ лечения артроза первого плюснефалангового сустава» от 02.12.2020.
Структура и объем работы. Диссертация состоит из введения, 4 глав, заключения, выводов и практических рекомендаций. Текст диссертации представлен на 118 страницах компьютерного текста, содержит 16 таблиц, 33 графика и 59 рисунков. Указатель литературы включает 113 источников, из них 12 отечественных.
Работа основана на исследовании результатов хондропластики с использованием коллагеновой матрицы у пациентов с ОА I ПФС. В лаборатории ревмоортопедии и реабилитации ФГБНУ НИИР имени В. А. Насоновой за период с 2015 по 2020 гг. по разработанной нами хирургической технике было выполнено 44 хондропластики I ПФС у 41 пациента. Эти пациенты составили основную группу. Для оценки эффективности разработанной методики созданы две контрольные группы. Первую группу составили пациенты с ОА I ПФС, которым выполнялась хейлэктомия без хондропластики (13 пациентов с ОА на 1-2-й стадиях и 9 пациентов с ОА на 3-4-й стадиях заболевания). Во вторую контрольную группу были включены пациенты, которым выполнялся артродез I ПФС (27 пациентам на поздних стадиях ОА). Пациенты основной группы были также разделены на две группы сравнения в зависимости от следующих характеристик:
1) возраст: 18-59 лет (23 пациентов, 25 операций) / 60-74 года (18 пациентов, 19 операций)
2) наличие / отсутствие системного ревматического заболевания (из 41 прооперированных пациентов 18 страдали системными РЗ)
Критерии включения: боль по ВАШ > 40 мм, амплитуда движений в I ПФС < 75 градусов, нарушение переката стопы, затруднение подбора и ношения обычной обуви, рентгенологическая картина ОА I ПФС 1-4-й стадий.
Критерии исключения: пациенты моложе 18 и старше 74 лет, индекс массы тела > 40, наличие системных заболеваний средней и высокой активности, наличие инфекционных заболеваний, грибковых поражений.
На этапе поступления в стационар пациенты заполняли индивидуальные карты и специальные опросники: ВАШ, по которой оценивали интенсивность боли в I ПФС; шкалу Американского ортопедического общества стопы и голеностопного сустава (American Orthopedic Foot & Ankle Society - AOFAS) и визуальную аналоговую шкалу оценки функционального состояния стопы и голеностопного сустава (Visual Analogue Scale Foot and Ankle - VAS FA), по которым оценивали функциональное состояние стоп. Также определяли объем пассивных движений в I ПФС.
Хондропластику I ПФС выполняли под спинальной анестезией на ортопедическом столе в положении лежа на спине под пневматическим жгутом, наложенным на границе верхней и средней трети бедра, либо под ленточным жгутом, наложенным на среднюю треть голени.
Послеоперационное ведение больных включало: немедикаментозную (компрессионный трикотаж на нижние конечности, криотерапия, ношение обуви Барука) и медикаментозную (антибактериальная, анальгетическая, симптоматическая) терапию, выполнение перевязок операционной раны, рентген-контроль, первичную реабилитацию в пределах стационара.
После выписки из стационара больные продолжали ходить в обуви Барука. Пациенты приступали к разработке пассивных движений в I ПФС через неделю после операции. Через 3 недели после операции мы рекомендовали пациентам начать разработку активных движений. После перехода к ношению обычной обуви (через 6 недель после операции) пациентам рекомендовали использование индивидуальных стелек. По прошествии 3 месяцев со дня операции выполняли контрольные рентгенограммы оперированной стопы, заполняли опросники.
Дальнейшее амбулаторное наблюдение и сопутствующее им выполнение рентгенограмм и МРТ оперированных стоп, заполнение опросников осуществляли по прошествии 6 и 12 месяцев после хондропластики I ПФС. Соответственно, через 3 месяца результат операции был оценен в 38 случаях, через 6 месяцев - в 35, через 12 месяцев - в 32.
Результат лечения оценивали в соответствии с изменением интенсивности боли по ВАШ, объема движений в I ПФС, а также функциональных шкал AOFAS и VAS FA.
Статистическую обработку полученных данных проводили на персональном компьютере с использованием приложения Microsoft Excel и программы статистического анализа данных BioStat®. Результаты считали достоверными при p < 0,05.
Наличие и размер дефекта хрящевого покрытия головки I ПК определяли интраоперационно. Хондропластику I ПФС осуществляли с использованием коллагеновых матриц Chondro-Gide® и Aesculap Novocart Basic®. Техника операции заключалась в следующем: выполняли прямой медиальный кожный разрез в проекции I ПФС длиной 4 см (рис. 1) с последующей мобилизацией кожи с подкожно-жировой клетчаткой, обнажением капсулы сустава и артротомией (рис. 2). Осуществляли удаление остеофитов с головки I ПК и основания проксимальной фаланги первого пальца - хейлэктомия (рис. 3); обрабатывали зону дефекта хряща на головке плюсневой кости до субхондральной кости, выполняли микрофрактурирование данного участка с помощью тонкой спицы или шила (рис. 4, 5), и дефект укрывали предварительно подготовленной двуслойной коллагеновой матрицей (рис. 6), которую фиксировали по краям к надкостнице с помощью тонких рассасывающихся нитей пористым слоем к поверхности кости (рис. 7).
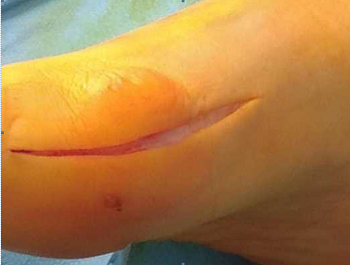
Рисунок 1 - Доступ к I ПФС
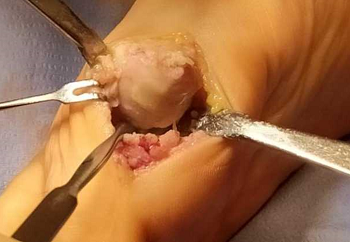
Рисунок 2 - Артротомия
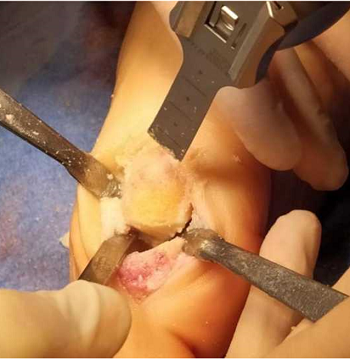
Рисунок 3 - Хейлэктомия, удаление остатков поврежденного хряща
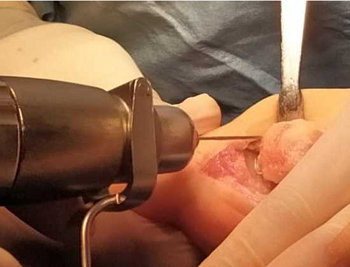
Рисунок 4 - Микрофрактурирование зоны дефекта
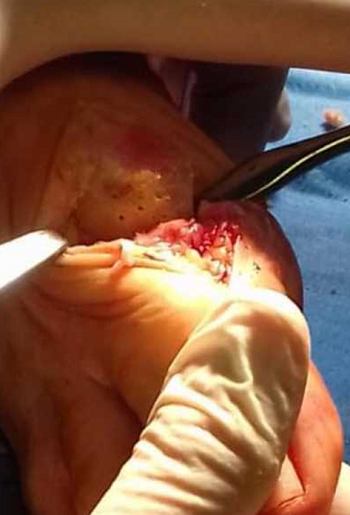
Рисунок 5 - Нанесенные микроперфорации на головке I ПК
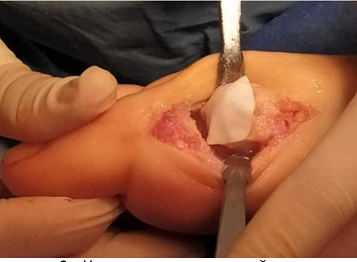
Рисунок 6 - Укладка коллагеновой матрицы
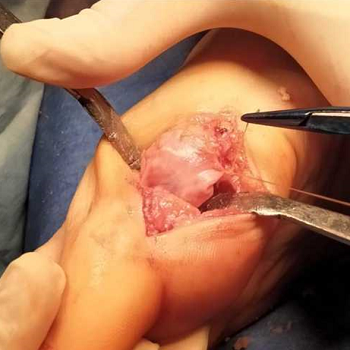
Рисунок 7 - Фиксация матрицы тонкими рассасывающимися нитями
Послеоперационное ведение больных включало в себя анальгетическую и антибактериальную терапию. Пациентам разрешали ходьбу на следующие сутки после операции, при этом обязательным условием послеоперационной реабилитации было ношение обуви Барука для разгрузки переднего отдела стопы в течение 6 недель. Через неделю после операции мы рекомендовали нашим пациентам приступить к постепенной разработке пассивных движений в I ПФС. Через 3 недели после операции рекомендовали начать разработку активных движений. После перехода к ношению обычной обуви пациентам было рекомендовано использование индивидуальных стелек.
Результаты проведенного хирургического лечения оценивали по вышеуказанным опросникам через 3, 6 и 12 месяцев после операции.
За 12 месяцев исследования мы наблюдали положительную динамику состояния пациентов на 1-2-й стадиях ОА I ПФС после хейлэктомии: уровень боли по ВАШ снизился с 80 мм до 15 мм, в то время как AOFAS увеличился с 52 до 77, VAS FA - c 5,2 до 8,3, а объем движений в I ПФС - с 30о до 70о.
Тем не менее, после хондропластики у пациентов на ранних стадиях HR мы наблюдали более выраженную положительную динамику, чем у пациентов после хейлэктомии. У пациентов c 1-2-й стадиями ОА I ПФС через 12 месяцев после хондропластики медиана уровня боли по ВАШ снизилась с 77,5 мм до 2,5 мм, медиана AOFAS увеличилась с 50 до 90, VAS FA - с 4,6 до 9,6; при этом медиана объема движений в I ПФС увеличилась с 25о до 78о.
Совершенно другую динамику мы наблюдали после выполненной хейлэктомии у пациентов с 3-4-й стадиями ОА I ПФС. Через 12 месяцев после операции уровень боли по ВАШ снизился с 80 мм до 45 мм, в то время как AOFAS увеличился с 45 всего лишь до 62, VAS FA - с 4,1 до 6,8, а объем движений в I ПФС - с 17о до 45о.
Таким образом, исходя из результатов видно, что хейлэктомия эффективна при 1 -2-й стадии ОА I ПФС, так как наблюдается снижение боли по ВАШ к концу первого года наблюдения до 15 мм, увеличение амплитуды движений в I ПФС до 75о. Однако данный метод хирургического лечения неэффективен при 34-й стадии HR, так как сохраняется высокий уровень боли (по ВАШ 45 мм) и низкая амплитуда движений - 45о.
Напротив, у пациентов с 3-4 стадиями ОА I ПФС через 12 месяцев после хондропластики медиана уровня боли по ВАШ снизилась с 70 мм до 7,5 мм, медиана AOFAS увеличилась с 50 до 85, VAS FA - с 4,4 до 9,5; при этом медиана объема движений увеличилась с 18о до 76о.
В группе пациентов после артродеза I ПФС через 12 месяцев после операции медиана уровня боли по ВАШ снизилась с 80 мм до 0 мм, в то время как медиана AOFAS увеличилась с 32 до 80, VAS FA - c 3,6 до 8,0, но при этом объем движений в I ПФС был полностью утрачен (Графики 1-4).
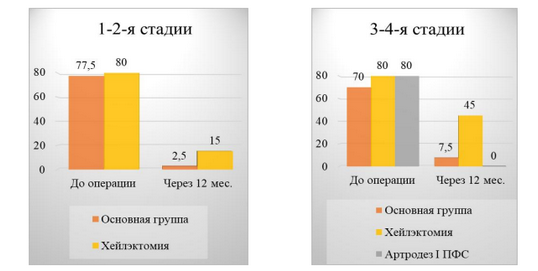
График 1 - Динамика уровня боли по ВАШ в основной и контрольных группах в зависимости от стадии ОА I ПФС
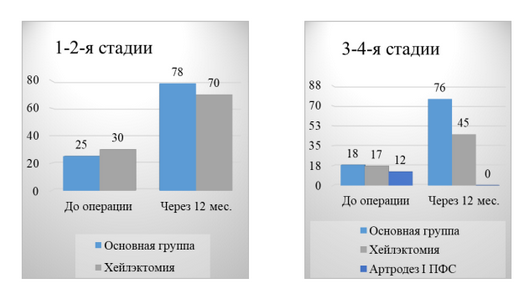
График 2 - Динамика объема движений в I ПФС в основной и контрольных группах в зависимости от стадии ОА I ПФС
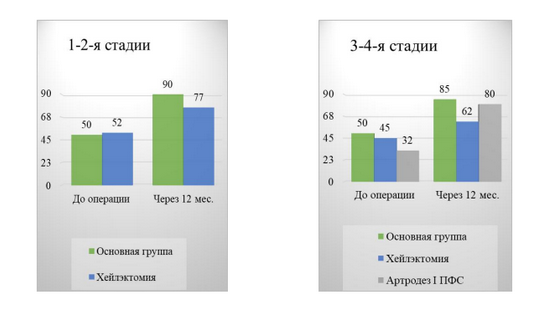
График 3 - Динамика по AOFAS в основной и контрольных группах в зависимости от стадии ОА I ПФС
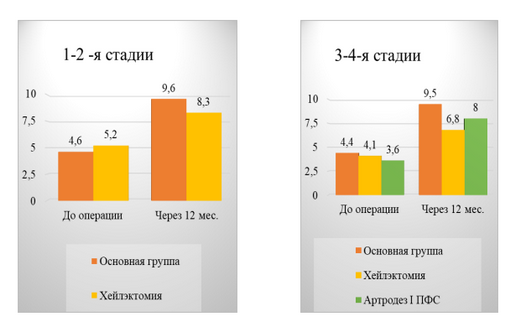
График 4 - Динамика по VAS FA в основной и контрольных группах в зависимости от стадии ОА I ПФС
Артродез не состоялся в 7,4% случаев. Также в связи с отсутствием движений в I ПФС нарушается биомеханика ходьбы, что проявлялось в развитии метатарзалгий у 14,8% пациентов.
Таким образом, хондропластику I ПФС можно считать эффективной суставсберегающей альтернативой артродезу I ПФС на поздних стадиях ОА I ПФС.
Как указывалось выше, пациенты основной группы были разделены на две подгруппы в зависимости от возраста, а также на две подгруппы в зависимости от наличия или отсутствия системного РЗ.
У пациентов в возрасте до 59 лет к концу первого года наблюдения медиана уровня боли по ВАШ снизилась с 70 мм до 0, медиана AOFAS увеличилась с 50 до 90; при этом медиана объема движений в I ПФС увеличилась с 20о до 78о, VAS FA - с 4,3 до 9,6.
В подгруппе пациентов старше 60 лет через 12 месяцев после операции медиана боли снизилась с 80 мм до 10 мм, AOFAS - увеличилась с 49,5 до 85; в свою очередь, медиана VAS FA увеличилась с 4,0 до 9,3, объем движений в I ПФС - c 20o до 71о.
У пациентов с РЗ за 12 месяцев наблюдения медиана уровня боли по ВАШ снизилась с 75 мм до 2,5 мм, медиана AOFAS увеличилась с 51 до 87,5, VAS FA - с 4,6 до 9,6; при этом медиана объема движений в I ПФС увеличилась с 20о до 78о.
В подгруппе пациентов, не страдающих РЗ, через год после операции медиана уровня боли по ВАШ снизилась с 75 мм до 10 мм, медиана AOFAS увеличилась с 48 до 85, VAS FA - с 3,8 до 9,4; при этом медиана объема движений увеличилась с 20о до 72о (Графики 5-8).
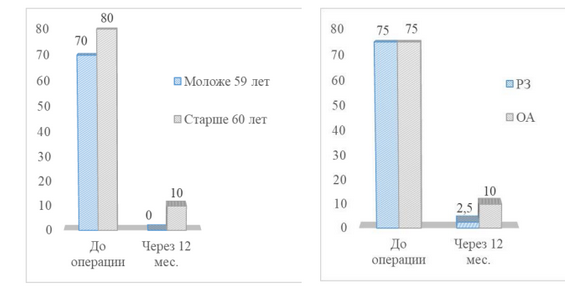
График 5 - Динамика уровня боли по ВАШ в основной группе в зависимости от возраста, а также от наличия или отсутствия системного РЗ
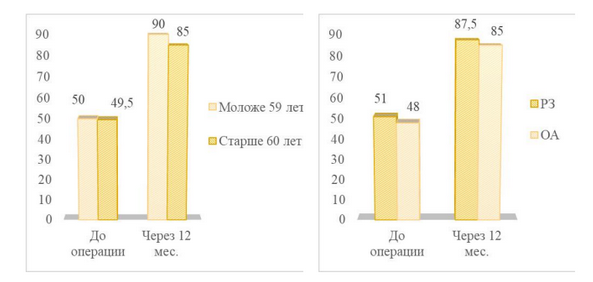
График 6 - Динамика по AOFAS в основной группе в зависимости от возраста, а также от наличия или отсутствия системного РЗ
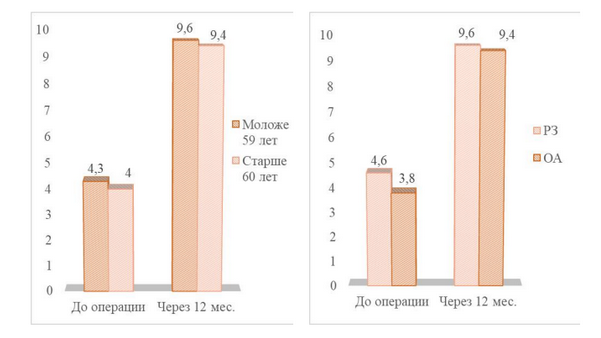
График 7 - Динамика по VAS FA в основной группе в зависимости от возраста, а также от наличия или отсутствия системного РЗ
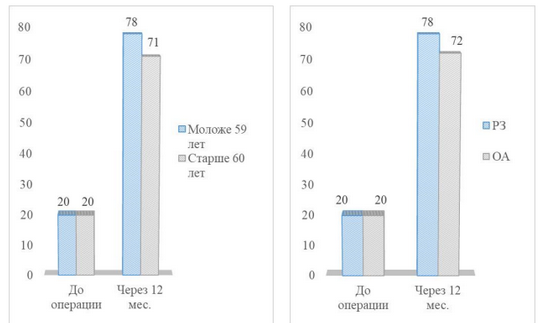
График 8 - Динамика объема движений в I ПФС в основной группе в зависимости от возраста, а также от наличия или отсутствия системного РЗ
После хондропластики I ПФС мы наблюдали одно осложнение: пациентка, страдающая анкилозирующим спондилитом, у которой была 4-я стадия ОА I ПФС, к 6 месяцу после операции отметила ухудшение состояния. Пациентка жаловалась на постоянные боли и припухлость в оперированном I ПФС. Больная не принимала регулярно базисную терапию, и мы предположили, чтоэто могло быть связано с обострением основного заболевания. На рентгенограмме суставная щель I ПФС практически не определялась, движения в суставе были резко ограничены. Данной пациентке была выполнена повторная операция в виде артродеза I ПФС.
Выводы
1. Анализ результатов лечения больных с ОА I ПФС показал, что уровень боли по ВАШ после хейлэктомии при 3-4-й стадиях HR оставался высоким (45 мм), объем движений увеличивался только до 45 градусов; при артродезе I ПФС отсутствие движений в I ПФС приводит к нарушению нормальной перекатной функции стопы и развитию метатарзалгии в 14,8% случаев.
2. Разработан новый способ суставсберегающей операции при ОА I ПФС по технике хондропластики, заключающейся в выполнении хейлэктомии, микрофрактурировании зоны дефекта и подшивании коллагеновой матрицы. Результатом данной операции является стойкое купирование боли (5 мм по ВАШ через 1 год после операции) и восстановление нормальной амплитуды движений в I ПФС (до 77о), даже у пациентов с 3-4-й стадиями заболевания.
3. Показаниями к выполнению хондропластики I ПФС являются выраженная боль (по ВАШ > 40 мм), амплитуда движений в I ПФС < 75о, нарушение переката стопы, затруднение подбора и ношения обычной обуви, рентге-нологическая картина ОА I ПФС 1-4-й стадий; противопоказаниями к данной операции являются возраст моложе 18 и старше 74 лет, индекс массы тела > 40, средняя и высокая активность системных заболеваний, наличие инфекционных заболеваний.
4. Ближайшие и среднесрочные результаты лечения показали, что на ранних стадиях ОА I ПФС эффективность хейлэктомии и хондропластики I ПФС сопоставимы. На поздних стадиях заболевания очевидным является преимущество хондропластики как над хейлэктомией, так и над артродезом I ПФС. Хондропластика может быть суставсберегающей альтернативой артродезу на 3-й и 4-й стадиях ОА I ПФС.
5. Разработанная методика хондропластики I ПФС может успешно использоваться у пациентов как молодого, так и пожилого возраста, а также у пациентов, страдающих системными РЗ. При этом обязательным условием выполнения данной операции у таких пациентов является низкая активность или ремиссия заболевания на фоне продолжающегося приема базисной терапии.
Рекомендации
1. С целью планирования операции в предоперационном периоде показано выполнение рентгенографии в прямой и боковой проекции и МРТ стопы (оценка стадии ОА I ПФС, размера дефекта хряща головки I ПК).
2. При выполнении операции следует осуществлять удаление остеофитов головки I ПК и основания проксимальной фаланги, релиз плантарной фасции. Микрофрактурирование зоны дефекта выполняется с помощью тонкой спицы, расстояние между перфорациями - 2-3 мм. Перед имплантацией коллагеновую матрицу следует выдержать в 0,9%-м растворе NaCl в течение 2-7 минут.
3. Для профилактики послеоперационных осложнений следует проводить терапию: антибактериальную и анальгетическую, а также криотерапию в первые трое суток после операции.
4. Активизация больного осуществляется на следующий день после операции. Обязательным условием послеоперационной реабилитации является ношение обуви Барука для разгрузки переднего отдела стопы в течение 6 недель. Показана пассивная разработка движений в I ПФС через неделю после операции, а также активная разработка движений через 3 недели после операции. После перехода к ношению обычной обуви рекомендовано изготовление и постоянное использование индивидуально подобранных стелек.
Литература
1. Нурмухаметов, М. Р. Комплексное хирургическое лечение стойкой деформации переднего отдела стопы у больных с ревматоидным артритом. Влияние состояния костной ткани на способ фиксации артродеза 1 плюснефалангового сустава / М. Р. Нурмухаметов // VII Научно-образовательная конференция с международным участием «Проблема остеопороза в травматологии и ортопедии». Сборник тезисов. - Москва, 2018. - С. 154.
2. Нурмухаметов, М. Р. Хондропластика по технике AMIC в лечении больных с hallux rigidus / М. Р. Нурмухаметов, М. А. Макаров, С. А. Макаров, Е. И. Бялик, Я. Б. Хренников, В. Е. Бялик, В. А. Нестеренко // Научно-практическая конференция «Новые концепции диагностики и лечения остеоартроза». Сборник тезисов. - Астрахань, 2018. - С. 27.
3. Нурмухаметов, М. Р. Принципы хирургического лечения больных с остеоартритом первого плюснефалангового сустава / М. Р. Нурмухаметов // Научно-практическая ревматология. - 2018. Т. 56. - № 3. - С. 363-372
4. Нурмухаметов, М. Р. Аутологичный матрикс-индуцированный хондрогенез (AMIC) в лечении больных с hallux rigidus / М. Р. Нурмухаметов, М. А. Макаров, С. А. Макаров, Е. И. Бялик, Я. Б. Хренников, В. Е. Бялик, В. А. Нестеренко // Материалы XXI Всероссийской научно-практической конференции 25-26 мая 2018г. «Многопрофильная больница: проблемы и решения». ООО «Примула» г. Кемерово. - С. 72.
5. Нурмухаметов, М. Р. Хирургическое лечение больных с hallux rigidus. Современные методы и возможности / М. Р. Нурмухаметов, М. А. Макаров, С. А. Макаров, Е. И. Бялик, Я. Б. Хренников, В. Е. Бялик, В. А. Нестеренко II Международный конгресс ассоциации ревмоортопедов. Тезисы докладов. Воронеж. Издательско-полиграфический центр «Научная книга» 2018. - С. 113-114.
6. Нурмухаметов, М. Р. Проблемы хирургического лечения стойкой деформации переднего отдела стопы у больных ревматоидным артритом. Способы фиксации артродеза I плюснефалангового сустава в зависимости от состояния костной ткани / М. Р. Нурмухаметов, М. А. Макаров, С. А. Макаров, Е. И. Бялик, Я. Б. Хренников, В. Е. Бялик, В. А. Нестеренко, А. Э. Храмов, А. В. Рыбников, Е. А. Нарышкин, В. П. Павлов // Тезисы IV Евразийского конгресса ревматологов. Москва, 26-28 сентября 2018г. Научно-практическая ревматология. 2018; 56 (3, прил.2). С. 59.
7. Nurmukhametov, M. R. Autologous matrix-induced chondrogenesis in treatment of patients with hallux rigidus / M. R. Nurmukhametov, M. A. Makarov, S. A. Makarov, E. I. Bialik, Y. B. Khrennikov, V. E. Bialik, V. A. Nesterenko // 39th SICOT Orthopaedic World Congress. 10-13 October 2018. Abstract book. Free Papers. №49812. P. 127.
8. Нурмухаметов, М. Р. Проблемы хирургического лечения больных с hallux rigidus. Возможность применения хондропластики 1 плюснефалангового сустава / М. Р. Нурмухаметов, М. А. Макаров, С. А. Макаров, Е. И. Бялик, Я. Б. Хренников, В. Е. Бялик, В. А. Нестеренко // XIV Межрегиональная научнопрактическая конференция Организационные и клинические вопросы оказания помощи больным в травматологии и ортопедии 30 ноября - 1 декабря 2018г. Сборник тезисов. - С. 100-101.
9. Нурмухаметов, М. Р. Современные методы и возможности хирургического лечения больных остеоартритом 1 плюснефалангового сустава / М. Р. Нурмухаметов, С. А. Макаров, М. А. Макаров, Е. И. Бялик, Я. Б. Хренников, В. Е. Бялик, В. А. Нестеренко // Opinion Leader. 2018. №5 (13). С. 6873.
10. Нурмухаметов, М. Р. Использование хондропластики по технике аутологичного индуцированного матрицей хондрогенеза (AMIC) в лечении пациентов с hallux rigidus / М. Р. Нурмухаметов, М. А. Макаров, С. А. Макаров, Е. И. Бялик, Я. Б. Хренников, В. Е. Бялик, В. А. Нестеренко // III Конгресс Российской ассоциации хирургов стопы и голеностопного сустава. Сборник тезисов. - Санкт-Петербург, 5-6 апреля 2019 г.
11. Нурмухаметов, М. Р. Хондропластика по технике аутологичного индуцированного матрицей хондрогенеза (AMIC) как новый метод хирургического лечения пациентов с hallux rigidus. Ближайшие и среднесрочные результаты / М. Р. Нурмухаметов, М. А. Макаров, С. А. Макаров, Е. И. Бялик, Я. Б. Хренников, В. Е. Бялик, В. А. Нестеренко // III Международный конгресс ассоциации ревмоортропедов: тезисы докладов конгресса - Воронеж : Издательско-полиграфический центр «Научная книга», 2019. - С. 136
12. Nurmukhametov, M. R. Features of the First Metatarsophalangeal Joint Chondroplasty by Autologous Matrix-Induced Chondrogenesis (AMIC) in Treatment of Patients with First Metatarsophalangeal Joint Osteoarthritis / M. R. Nurmukhametov, M. A. Makarov, S. A. Makarov, E. I. Bialik, Y. B. Khrennikov, V. E. Bialik, V. A. Nesterenko // 40th SICOT Orthopaedic World Congress. 4-7 December 2019. Abstract book. Free Papers. №53385. P. 103.
13. Нурмухаметов, М. Р. Использование хондропластики I плюснефалангового сустава по технике аутологичного индуцированного матрицей хондрогенеза для лечения пациентов с hallux rigidus: ближайшие результаты / М. Р. Нурмухаметов, М. А. Макаров, Е. И. Бялик, В. Е. Бялик, В.А. Нестеренко // Научно-практическая ревматология. - 2020. -N 58 (1). - C. 97101.
14. Nurmukhametov, M. R. The Use of Autologous Matrix-Induced Chondrogenesis as a Surgical Treatment for Patients with the First Metatarsophalangeal Joint Osteoarthritis. Immediate and Medium-Term Results / M.
15. Нурмухаметов, М. Р. Хондропластика первого плюснефалангового сустава по технике аутологичного индуцированного матрицей хондрогенеза в лечении пациентов с hallux rigidus. Анализ ближайших и среднесрочных результатов / М. Р. Нурмухаметов, М. А. Макаров, С. А. Макаров, Е. И. Бялик, Я. Б. Хренников // Вестник травматологии и ортопедии им. Н. Н. Приорова. - 2020. - Т. 27. - №. 3. - С. 32-41.
Работа выполнена в Федеральном государственном бюджетном научном учреждении «Научно-исследовательский институт ревматологии им. В. А. Насоновой»
доктор медицинских наук, профессор Бялик Евгений Иосифович
доктор медицинских наук Процко Виктор Г еннадьевич
Федеральное государственное автономное образовательное учреждение высшего образования «Российский университет дружбы народов», кафедра травматологии и ортопедии Медицинского института, доцент кафедры
Федеральное государственное автономное образовательное учреждение высшего образования Первый Московский государственный медицинский университет имени И.М. Сеченова Министерства здравоохранения Российской Федерации (Сеченовский Университет), доцент кафедры травматологии, ортопедии и хирургии катастроф Института клинической медицины им. Н.В. Склифосовского, руководитель центра хирургии стопы, голеностопного сустава и кисти Университетской клинической больницы №1
Теги: хондропластика
234567 Начало активности (дата): 30.11.2023 11:10:00
234567 Кем создан (ID): 989
234567 Ключевые слова: первая плюсневая кость,хондропластика, остеоартрит, анкилозирующий спондилит
12354567899
Похожие статьи
Гонатроз и сходные с ним клинические состояния (клинические рекомендации)Рентген на дому 8 495 22 555 6 8
Способ хирургического лечение деформирующего артроза I плюснефалангового сустава
Дистракционная артропластика голеностопного сустава с использованием аппарата Илизарова и артроскопической техники: первый клинический опыт
Эффективность артроскопии тазобедренного сустава как метода хирургической коррекции фемороацетабулярного импинджмента. Оценка результатов лечения в течение двух лет после операции



