 31.07.2023
31.07.2023
Проблемы и успехи комбинированного применения технологий Илизарова и Masquelet
Основываясь на оценке проблем и эффективности применения индуцированной мембраны и транспорта кости, предложен новый дизайн технологических решений, базирующийся на авторских методиках Masquelet и Илизарова при восстановительном лечении пациентов с костными дефектами и ложными суставами
ВВЕДЕНИЕ
Рассматривая исторические аспекты применения несвободной костной пластики по Илизарову и техники формирования индуцированной мембраны (IMT) по Masquelet необходимо отметить эффективность их использования с 80-х годов XX века при восполнении приобретенных костных дефектов [1, 2, 3].
Транспорт кости по Илизарову подразумевает дискретное и управляемое перемещение кровоснабжаемого аутотрансплантата с сохраненным покровом мягких тканей в межотломковом диастазе с восполнением костного дефекта новообразованной костной тканью [2, 4].
Техника Masquelet включает реконструкцию сегмента в две операционные сессии. На первом этапе лечения выполняют радикальную санирующую обработку мягких тканей и некротической кости, в сформированный дефект имплантируют полиметилметакрилатовый цементный спейсер. Костный сегмент обычно фиксируют аппаратами внешней фиксации. Через 6-8 недель спей- сер удаляют, дефект заполняют свободными костными аутотрансплантатами из гребня подвздошной кости [3].
Необходимо признать, что для ликвидации костных дефектов, в том числе в условиях гнойной инфекции, в настоящее время не существует идеальных костно-пластических материалов и лишенных недостатков реконструктивно-восстановительных оперативных вмешательств.
Сторонники чрескостного остеосинтеза признают определенные недостатки внешней фиксации, связанные, в первую очередь, со снижением качества жизни пациентов, длительным и многоэтапным лечением, риском воспаления мягких тканей в области чрескостных элементов фиксации, развитием контрактур смежных суставов и т.д. [2, 5].
По данным литературы, использование технологии Masquelet ограничено у пожилых пациентов в связи с длительной и незавершенной перестройкой массивных имплантатов, риском патологических переломов, инфекционными осложнениями, проблемным заживлением ран, в том числе в донорских зонах, развитием костных несращений и т.д. [3, 6, 7].
При сравнительном анализе опубликованных результатов лечения пациентов с использованием транспорта кости по Илизарову (37 статей, средняя величина дефекта 6,9 см) и исходов костной пластики по Masquelet (принята во внимание 41 статья, средняя величина дефекта 6,32 см) выявлено, что достигнутые результаты не имеют статистически значимых и достоверных преимуществ по восстановлению анатомической целостности конечности, формированию неправильного сращения отломков, рискам развития инфекционных осложнений [8].
По нашему мнению, дифференцированное и рациональное комбинирование различных подходов и альтернативных оперативных технологий позволяет оптимизировать лечебный процесс, сократить продолжительность и этапность остеосинтеза, снизить риски возможных осложнений [9].
В свою очередь, мы имеем опыт успешного замещения врожденных ложных суставов костей голени при формировании индуцированной мембраны в условиях несвободной костной пластики по Илизарову. По нашим данным, комбинация технологии Masquelet и транспорта кости по Илизарову обеспечивает оптимальный объем восполнения утраченной костной массы и снижает риски рецидивов несращений в отдаленном периоде наблюдений у пациентов с врожденными ложными суставами [10].
Цель работы - поиск новых технологических решений для улучшения результатов хирургической реабилитации пациентов с приобретенными костными дефектами в условиях активной гнойной инфекции и ремиссии.
МАТЕРИАЛЫ И МЕТОДЫ
Работа основана на ретроспективном и проспективном исследовании результатов восстановительного лечения 24 пациентов, которым для восполнения дефектов длинных костей применили комбинацию технологий костной пластики по Г.А. Илизарову и Masquelet.
Пациенты были разделены на две группы. Первая группа пациентов (17 клинических наблюдений) имела костные дефекты в условиях ремиссии остеомиелитического процесса и прошла лечение в профильном отделении ФГБУ «НМИЦ ТО имени академика Г.А. Илизарова». Вторая группа (7 наблюдений) была представлена пациентами с костными дефектами и активными проявлениями остеомиелитического процесса, прошедшими лечение в ГАУЗ СО ЦГКБ № 23, г. Екатеринбург.
Все пациенты были в трудоспособном возрасте от 18 до 62 лет, имели приобретенную этиологию псевдоартрозов и дефектов. Давность травмы была от одного года до 7 лет (3,7 ± 1,5). Все пациенты были ранее безуспешно оперированы, 8 из них (33 %) многократно, точное количество операций они указать не могли, полная медицинская документация у больных отсутствовала. При сборе анамнеза и знакомства с медицинской документацией удалось выяснить, что на разных этапах лечения пациентам был применен интрамедуллярный блокируемый остеосинтез, накостный остеосинтез и чрескостный остеосинтез (табл. 1). В результате травм, неоднократных и безуспешных оперативных вмешательств мягкие ткани у всех пациентов были рубцовоиз- менены и спаяны на протяжении с костными отломками.
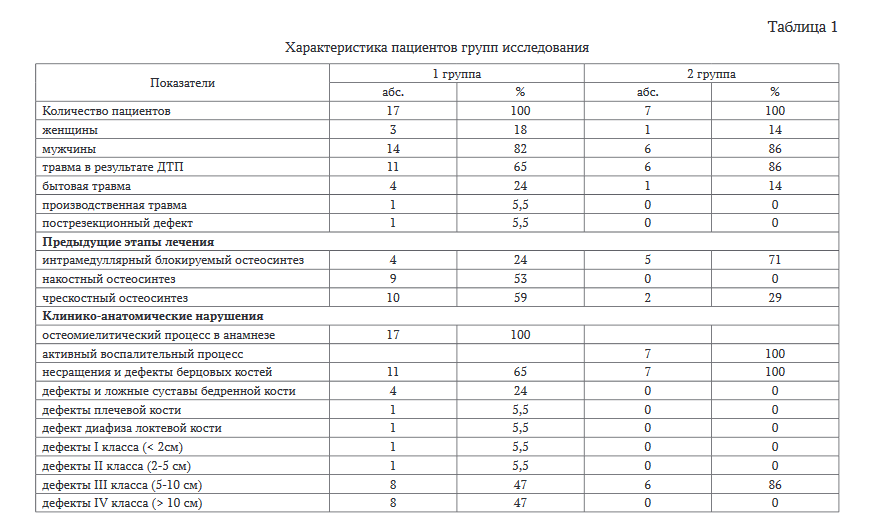
Анамнез заболевания у 17 пациентов был осложнен остеомиелитическим процессом. Все пациенты второй группы имели активный воспалительный процесс с гнойным отделяемым из свищей и ран. При активном гнойном процессе остеомиелит был классифицирован по Cierny-Mader у пациентов второй группы как IV тип (диффузный остеомиелит) с поражением всего диаметра кости и потерей стабильности сегмента [11].
В результате травм и безуспешных оперативных вмешательств у 18 пациентов (75 %) были сформированы несращения и дефекты берцовых костей. У 4-х больных были выявлены дефекты и ложные суставы бедренной кости.
Дефект плечевой кости величиной 7 см верифицирован у одной пациентки, дефект диафиза локтевой кости на протяжении 5 см был выявлен у одного больного.
Комбинация технологий костной пластики по Г.А. Илизарову и Masquelet включала реконструкцию сегмента в две операционные сессии. На первом этапе лечения выполняли радикальную санирующую обработку мягких тканей и костей в зоне дефекта и ложного сустава с чрескостной фиксацией сегмента аппаратом Илизарова. При нашем дизайне исследования компоновка аппарата подразумевала возможность после удаления спейсера выполнения остеотомий (кортикотомий) отломков для замещения пострезекционного дефекта удлинением отломков по Г.А. Илизарову. Из зоны сформированного дефекта и скомпрометированных тканей брали посевы. Начинали эмпирическую антибактериальную терапию в отношении широко
Сформированные дефекты были классифицированы по Karger C. et all [12]. Дефекты I класса (< 2 см) встретили у одного пациента, II (2-5 см) класс был представлен 14 клиническими наблюдениями, III (5-10 см) класс был выявлен у 8 больных. У одной пациентки был верифицирован дефект IV (> 10 cм) класса.
По классификации В.И. Шевцова с соавт. [13] выявленные несращения были характерными для дефектпсевдоартрозов с анатомическим укорочением у 14 пациентов (58 %), без анатомического укорочения сегмента были верифицированы дефект-псевдоартрозы в 10 клинических наблюдениях (42 %). Анатомические укорочения сегментов были выявлены от 1 до 7 см (4,6 ± 2,2).
В работе использованы методы описательной статистики (среднее значение показателя и его стандартное отклонение).
го спектра возбудителей, включая метициллинрези- стентные штаммы стафилококков. После верификации микробного пейзажа биоматериала и определения особенностей чувствительности к антибиотикам проводили коррекцию антибактериальной терапии.
В межотломковый диастаз имплантировали поли- метилметакрилатовый цементный спейсер. Спейсеры формировали цилиндрической формы на величину ме- жотломкового диастаза длиной от 3 до 6 см (4,2 ± 1,1) с добавлением одной профилактической дозы гентамицина или ванкомицина (рис. 1).
В одном клиническом наблюдении при субтотальном дефекте большеберцовой кости в межотломковый диастаз был имплантирован спейсер длиной 13 см.
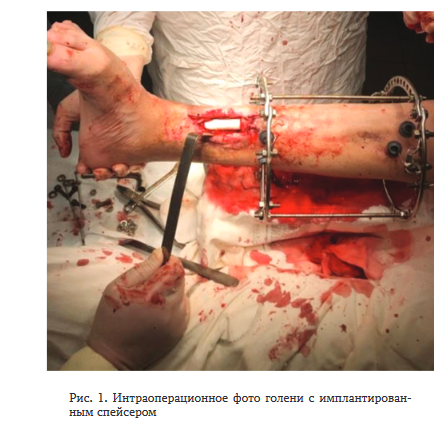
У наших пациентов продолжительность имплантации спейсера была от 26 до 51 дня (39,0 ± 7,7). В двух наблюдениях задержка второго этапа лечения составила 2-3 месяца.
Различные сроки в выполнении второго этапа лечения были связаны с нахождением пациентов на амбулаторном лечении в различных регионах РФ и организационными сложностями, связанными, в том числе, с COVID. Вместе с тем, по данным литературы, секреция индуцированной мембраной факторов роста более продолжительна, с достижением пиковых показателей между 4 и 6 неделей после имплантации спей- сера [15].
У всех пациентов 1 группы раны в области имплантированных спейсеров зажили первичным натяжением. У двух пациентов 2-ой группы (29 %) к моменту удаления спейсеров были сформированы гнойные свищи, и раны заживали вторичным натяжением.
Клинический пример пациентки второй группы
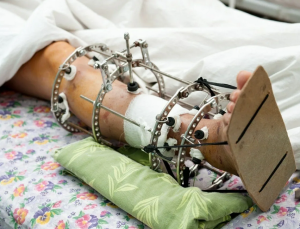
Пациентка М., 60 лет. Приобретенный субтотальный дефект большеберцовой кости замещен спейсером длиной 13 см. Голень фиксирована аппаратом Илизарова. После имплантации спейсера послеоперационная рана заживала вторичным натяжением со скудным гнойным отделяемым (рис. 2).
В посевах биоматериала была выявлена микрофлора: S. Aureus (MRSA) и Pseudomonas aeruginosa. После удаления спейсера была назначена антибактериальная терапия с учетом выявленного микробного пейзажа и чувствительности микрофлоры к антибиотикам. Восполнить субтотальный дефект большеберцовой кости предполагалось за счет полилокального формирования дистракционных регенератов и удлинения противолежащих отломков. Замещение дефекта осуществляли полилокальным удлинением отломков [16]. После выполнения остеотомий противолежащих отломков дистракция начата на 10-й день, темп дистракции по 0,75 мм при удлинении проксимального отломка и по 0,5 мм в сутки при удлинении дистального. В настоящее время пациентка продолжает лечение (рис. 3).
У другого пациента 2 группы послеоперационная рана зажила первичным натяжением, свищ с гнойным отделяемым сформировался на 6-й неделе после имплантации спейсера. В посеве из раны верифицировали S. Aureus (MRSA) и Enterobacter spp.
После удаления спейсера и повторной радикальной санации очага послеоперационная рана зажила первичным натяжением, при этом мембрана не была повреждена.
Дефект большеберцовой кости был восполнен удлинением проксимального отломка.
Продолжительность дистракции для транспорта сформированных фрагментов в I группе составила 45,4 ± 9,8 дня.
Перемещение фрагментов у II группы пациентов выполняли в течение 52,8 ± 5,3 дня. К моменту стыковки перемещаемых фрагментов с противолежащими отломками замыкательные пластинки на концах отломков не были сформированы. Кроме того, после удаления спейсеров концы отломков дополнительно экономно, а при наличии свищей в двух клинических наблюдениях, дополнительно радикально обрабатывали. Отсутствие замыкательных пластинок позволило выполнять закрытую репозицию и адаптацию концевых отделов костных отломков.
На стыке отломков поддерживали компрессию до достижения консолидации отломков. Манипуляцию для поддержания компрессии между концами отломков выполняли по 1,0 мм 1 раз в 10-14 дней. Продолжительность фиксации сегментов аппаратом составила в I группе пациентов 195,1 ± 9,9 дня. Во II группе пациентов период фиксации занял 181,8 ± 11,4 дня. У всех пациентов, закончивших лечение, было достигнуто восстановление целостности и опороспособности поврежденного сегмента. При контрольных явках остаточное анатомическое укорочение от одного до 6,0 см выявлено у трех пациентов (3,3 ± 1,8 см).
ОБСУЖДЕНИЕ
Технология Masquelet создает благоприятные условия для регенерации тканей, в том числе, и для дистракционного остеогенеза. Имеются сведения, что формируемая вокруг спейсера мембрана адекватно кровоснабжаема, богата мезенхимальными стволовыми и эпителиоподоб- ными клетками, фибробластами, миофибробластами, продуцирует факторы роста (VEGF, TGF-бета 1) и морфогенетические белки ВМР-2 и ВМР-7 [17-19].
По данным литературы, индуцированная мембрана обладает антимикробной активностью, что связано с присутствием антиоксидантных химических веществ, локально секретируемых с факторами роста, которые могут вызывать деградацию ДНК существующих микроорганизмов, приводящую к цитолизу. Присутствие некоторых пептидов также может вызывать бактериостатический эффект путем ингибирования клеточного деления. Другим предполагаемым механизмом является присутствие местных пептидов, которые могут ингибировать секрецию бактериальной биопленки и, следовательно, предотвращать адгезию микроорганизмов к окружающим поверхностям [20].
Ранее в наших работах были представлены результаты успешного лечения 10 пациентов с дефектами голени в условиях отсутствия активной инфекции при комбинации технологии Masquelet и несвободной костной пластики по Г.А. Илизарову. Ни в одном клиническом наблюдении мы не наблюдали обострения гнойного процесса. При этом мы выбрали основной задачей радикальную дебридментацию потенциального очага инфекции. Временной интервал между операционными сессиями мы использовали для верификации микробного состава взятого биоматериала и для целевого подбора антибиотикотерапии [21].
Однако, по данным литературы, из полиметилме- такрилатового цементного спейсера элиминация антибиотика в окружающие ткани не превышает 10 % от первоначальной дозы [22].
По мнению Masquelet A.C., технология формирования индуцированной мембраны не является методом лечения костной инфекции. Является заблуждением, что использование спейсера, насыщенного антибиотиками, позволяет стойко подавить гнойную инфекцию без проведения тщательной хирургической обработки раны [23].
По мнению авторитетных авторов, стойкое подавление гнойной инфекции обеспечивается радикальной хирургической санацией очага и локальным созданием депо антибиотика в скомпрометированных тканях [8, 24].
Вероятно, в нашем исследовании заживление послеоперационных ран вторичным натяжением и формирование свищей с гнойным отделяемым в области имплантированных спейсеров в двух клинических наблюдениях второй группы было связанно с нерадикальной хирургической санацией гнойных очагов, недостаточной дозой антибиотика и массивностью имплантированного спейсера.
По данным литературы, при использовании костной пластики по Masquelet в дизайне монотехнологии не удается купировать гнойный процесс в 8,09-8,8 % клинических наблюдений [8, 25].
Полученные нами результаты вполне соотносятся с литературными данными: так, на первом этапе комбинированного применения технологий в условиях активной гнойной инфекции не удалось стойко купировать гнойный процесс у двух пациентов. После удаления спейсера, повторной санации очага и проведения этиотропной антибактериальной терапии была достигнута ремиссия гнойного процесса. Необходимо отметить, что при комбинации технологий Илизарова и Masquelet происходит удлинение отломков в благоприятных для дистракционного остеогенеза условиях. Перемещение несвободного костного аутотрансплантата осуществляется без технических проблем через туннель, стенками которого является индуцированная мембрана, через ранее скомпрометированные ткани, санированные на момент перемещения костного фрагмента [26].
В группах пациентов, принятых во внимание, на этапах удлинения отломков и последующей фиксации обострения остеомиелитического процесса нами выявлено не было. Вместе с тем, по нашим предварительным данным, нерадикальная санация очага, имплантация массивных спейсеров с профилактической дозой антибиотиков не гарантирует стойкого подавления очага гнойной инфекции.
ЗАКЛЮЧЕНИЕ
На начальном этапе применения комбинации техники Masquelet и несвободной костной пластики по Илизарову сохраняются риски активности гнойного процесса при нерадикальной санации очага инфекции, имплантации массивных спейсеров с профилактической дозой антибиотиков и эмпирической антибактериальной терапии. На этапах чрескостного остеосинтеза имеются невысокие риски воспаления мягких тканей в области чрескостных элементов, в наших наблюдениях воспаления мягких тканей в области спиц, потребовавшего их удаления и ликвидации очага спицевого остеомиелита, встречено не было. Транспорт кости по Илизарову осуществляется в благоприятных для гистогенеза условиях. Вокруг перемещаемого несвободного аутотрансплантата и формируемой новообразованной костной ткани имеется биологически активная капсула, основой которой является индуцированная мембрана, обладающая остеоиндуктивными и бактерицидными свойствами. Формирование на втором этапе хирургического лечения индуцированной мембраны (IMT), обладающей бактерицидной активностью, создание благоприятных условий для удлинения отломков, адекватная санация гнойного очага и проведение целевой антибактериальной терапии обеспечивает стойкое подавление активности гнойного процесса. В исходе хирургической реабилитации пациентов с сегментарными инфицированными дефектами мы имеем восполнение костных дефектов дистракционными регенератами, претерпевающими полную органотипическую перестройку, что исключает вероятность формирования деформаций или переломов на уровне новообразованных участков кости и снижает риски рецидивов остеомиелитического процесса.
СПИСОК ИСТОЧНИКОВ
1. Gubin A., Borzunov D., Malkova T. Ilizarov Method for Bone Lengthening and Defect Management Review of Contemporary Literature // Bull. Hosp. Jt. Dis. 2016. Vol. 74, No 2. P. 145-154.
2. Gubin A.V., Borzunov D.Y., Malkova T.A. The Ilizarov paradigm: thirty years with the Ilizarov method, current concerns and future research // Int. Orthop. 2013. Vol. 37, No 8. P. 1533-1539. DOI: 10.1007/s00264-013-1935-0.
3. Masquelet A.C., Fitoussi F., Begue T., Muller G.P. Reconstruction des os longs par membrane induite et autogreffe spongieuse // Ann. Chir. Plast. Esthet. 2000. Vol. 45, No 3. P. 346-353.
4. Management of segmental defects by the Ilizarov intercalary bone transport method / S.A. Green, J.M. Jackson, D.M. Wall, H. Marinow, J. Ishkanian // Clin. Orthop. Relat. Res. 1992. No 280. P. 136-142.
5. Paley D. Problems, obstacles, and complications of limb lengthening by the Ilizarov technique // Clin. Orthop. Relat. Res. 1990. No 250. P. 81-104.
6. Lasanianos N.G., Kanakaris N., Giannoudis P. Current management of long bone large segmental defects // Orthop. Trauma. 2010. Vol. 24, No 2. P. 149-163. DOI: 10.1016/j.mporth.2009.10.003.
7. Complications following autologous bone graft harvesting from the iliac crest and using the RIA: a systematic review / R. Dimitriou, G.I. Mataliotakis, A.G. Angoules, N.K. Kanakaris, P.V. Giannoudis // Injury. 2011. Vol. 42, No Suppl. 2. P. S3-S15. DOI: 10.1016/j.injury.2011.06.015.
8. Mixed results with the Masquelet technique: A fact or a myth? / M. Mi, C. Papakostidis, X. Wu, P.V. Giannoudis // Injury. 2020. Vol. 51, No 2. P. 132-135. DOI: 10.1016/j.injury.2019.12.032.
9. Borzunov D.Y., Kolchin S.N. Nonunion of the femoral shaft associated with limb shortening treated with a combined technique of external fixation over an intramedullary nail versus the Ilizarov method // Arch. Orthop. Trauma Surg. 2021. DOI: 10.1007/s00402-021-03804-4.
10. Комбинированные костнопластические вмешательства при реабилитации пациентов с врожденным ложным суставом костей голени / Д.Ю. Борзунов, Е.Н. Горбач, Д.С. Моховиков, С.Н. Колчин // Гений ортопедии. 2019. Т. 25, No 3. С. 304-311. DOI: 10.18019/1028-4427- 2019-25-3-304-311.
11. Cierny G., Mader J.T. Adult chronic osteomyelitis // Orthopedics. 1984. Vol. 7, No 10. P. 1557-1564. DOI: 10.3928/0147-7447-19841001-07.
12. Treatment of posttraumatic bone defects by the induced membrane technique / Karger C., Kishi T., Schneider L., Fitoussi F., Masquelet A.C.; French Society of Orthopaedic Surgery and Traumatology (SoFCOT) // Orthop. Traumatol. Surg. Res. 2012. Vol. 98, No 1. P. 97-102. DOI: 10.1016/j. otsr.2011.11.001.
13. Шевцов В.И., Макушин В.Д., Куфтырев Л.М. Дефекты костей нижней конечности. Чрескостный остеосинтез по методикам Российского научного центра «ВТО» им. акад. Г.А. Илизарова. Курган : Зауралье, 1996. 504 с.
14. Masquelet technique for the treatment of bone defects: tips-tricks and future directions / Giannoudis P.V., Faour O., Goff T., Kanakaris N., Dimitriou
R. // Injury. 2011. Vol. 42, No 6. P. 591-598. DOI: 10.1016/j.injury.2011.03.036.
15. Restoration of long bone defects treated with the induced membrane technique: protocol and outcomes / P.V. Giannoudis, P.J. Harwood, T. Tosounidis, N.K. Kanakaris // Injury. 2016. Vol. 47, No Suppl. 6. P. S53-S61. DOI: 10.1016/S0020-1383(16)30840-3.
16. Borzunov D.Y. Long bone reconstruction using multilevel lengthening of bone defect fragments // Int. Orthop. 2012. Vol. 36, No 8. P. 1695-1700. DOI: 10.1007/s00264-012-1562-1.
17. Masquelet A.C., Begue T. The concept of induced membrane for reconstruction of long bone defects // Orthop. Clin. North Am. 2010. Vol. 41, No 1. P. 27-37. DOI: 10.1016/j.ocl.2009.07.011.
18. Induced membranes secrete growth factors including vascular and osteoinductive factors and could stimulate bone regeneration / P. Pelissier, A.C. Masquelet, R. Bareille, S.M. Pelissier, J. Amedee // J. Orthop. Res. 2004. Vol. 22, No 1. P. 73-79. DOI: 10.1016/S0736-0266(03)00165-7.
19. Induced membrane technique: Advances in the management of bone defects / W. Han, J. Shen, H. Wu, S. Yu, J. Fu, Z. Xie // Int. J. Surg. 2017. Vol. 42. P. 110-116. DOI: 10.1016/j.ijsu.2017.04.064.
20. Does the induced membrane have antibacterial properties? An experimental rat model of a chronic infected nonunion / S. Roukoz, G. El Khoury, E. Saghbini, I. Saliba, A. Khazzaka, M. Rizkallah // Int. Orthop. 2020. Vol. 44, No 2. P. 391-398. DOI: 10.1007/s00264-019-04453-4.
21. Ilizarov bone transport combined with the Masquelet technique for bone defects of various etiologies (preliminary results) / D.Y. Borzunov, S. N. Kolchin, D.S. Mokhovikov, T.A. Malkova // World J. Orthop. 2022. Vol. 13, No 3. P. 278-288.
22. Zilberman M., Elsner J.J. Antibiotic-eluting medical devices for various applications // J. Control. Release. 2008. Vol. 130, No 3. P. 202-215. DOI: 10.1016/j.jconrel.2008.05.020.
23. Masquelet A.C. Induced Membrane Technique: Pearls and Pitfalls // J. Orthop. Trauma. 2017. Vol. 31, No Suppl. 5. P. S36-S38. DOI: 10.1097/ BOT.0000000000000979.
24. Pande K.C. Optimal management of chronic osteomyelitis: current perspectives // Orthop. Res. Rev. 2015. Vol. 7. P. 71-81. DOI: 10.2147/ORR. S50753.
25. Masquelet technique: myth or reality? A systematic review and meta-analysis / I. Morelli, L. Drago, D.A. George, E. Gallazzi, S. Scarponi, C.L. Romano // Injury. 2016. Vol. 47, No Suppl. 6. P. S68-S76. DOI: 10.1016/S0020-1383(16)30842-7.
26. Комбинированное применение несвободной костной пластики по Илизарову и техники Masquelet при реабилитации пациентов с приобретенными костными дефектами и ложными суставами / Д.Ю. Борзунов, Д.С. Моховиков, С.Н. Колчин, Е.Н. Горбач // Гений ортопедии. 2020. Т. 26, № 4. С. 532-538. DOI: 10.18019/1028-4427-2020-26-4-532-538.
Информация об авторах:
1. Дмитрий Юрьевич Борзунов - доктор медицинских наук, доцент
3. Сергей Николаевич Колчин - кандидат медицинских наук
4. Сергей Владимирович Люлин - доктор медицинских наук
5. Сергей Михайлович Кутепов - доктор медицинских наук, профессор, член-корр. РАН;
6. Ринат Тимурович Гильманов - врач травматолог-ортопед.
Теги: Илизаров
234567 Начало активности (дата): 31.07.2023 15:03:00
234567 Кем создан (ID): 989
234567 Ключевые слова: комбинация, Masquelet, Илизаров, индуцированная мембрана, дистракционный регенерат
12354567899
Похожие статьи
Проблемы и успехи комбинированного применения технологий Илизарова и MasqueletДоклиническая оценка эффективности и безопасности нового костнопластического материала ксеногенного происхождения, содержащего в своем объеме ванкомицин и меропенем
Оценка синовита голеностопного сустава при диабетической нейроостеоартропатии в зависимости от воспалительной фазы хронического остеомиелита
Рентген на дому 8 495 22 555 6 8



