 07.03.2020
07.03.2020
Оценка эффективности двухэтапного хирургического лечения больных с перипротезной инфекцией коленного и тазобедренного суставов
Двухэтапное хирургическое лечение перипротезной инфекции является “золотым стандартом” для большинства отечественных и зарубежных клиник.
ВВЕДЕНИЕ
К несомненным положительным факторам эндопротезирования следует отнести быстрое восстановление безболезненных движений в суставе, а также опороспособности конечности и короткий реабилитационный период [1, 2, 3]. К сожалению, как и любое хирургическое вмешательство, эндопротезирование имеет ряд серьезных осложнений: нестабильность и вывихи компонентов, разная длина конечностей, перипротезные переломы, фрактура имплантата, гетеротопическая оссификация, износ вкладыша, артрофиброз [4, 5, 6, 7]. Зарубежные авторы считают инфекцию наиболее разрушительным осложнением [8, 9].
Перипротезная инфекция является тяжелым бременем для больных ввиду высокого уровня ее рецидива и смертности.
Стоимость лечения одного пациента с перипротезной инфекцией в зарубежных клиниках варьирует от 30 000 до 78 000 $, не включая амбулаторные расходы, затраты за длительную нетрудоспособность и потерянную заработную плату [10, 11, 12].
Сложившаяся система лечения больных с перипротезной инфекцией включает в себя несколько подходов с присущими им методическими приемами и используемыми техническими средствами.
Основным из них является оперативное лечение, проводимое в сочетании с курсами этиотропной терапии. Использование того или иного хирургического подхода в значительной степени зависит от времени манифестации инфекции, стабильности имплантата, чувствительности микроорганизмов к антибактериальным препаратам, наличия сопутствующих заболеваний и т.д. [13, 14, 15, 16].
Двухэтапное хирургическое лечение перипротезной инфекции является “золотым стандартом” для
большинства отечественных и зарубежных клиник [17, 18, 19]. Данная методика предусматривает удаление эндопротеза, хирургическую обработку гнойно-воспалительного очага и установку цементного спейсера с последующей его заменой на постоянный эндопротез
Цель исследования.
Оценить среднесрочные результаты двухэтапного хирургического лечения больных с перипротезной инфекцией коленного и тазобедренного суставов.МАТЕРИАЛЫ И МЕТОДЫ
Проведен анализ результатов лечения 172 больных-с перипротезной инфекцией, прошедших процедуру двухэтапного хирургического лечения с использованием цементного спейсера в период с 2011 по 2015 год.
При этом у 113 больных наблюдалась инфекция после эндопротезирования тазобедренного сустава и у 59 пациентов – коленного сустава. Средний возраст пациентов составил 51,93 ± 10,9 года (от 22 до 80 лет).
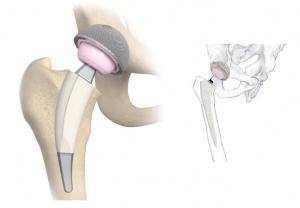
Исследование было одобрено комитетом по этике в соответствии со стандартами, изложенными в Хельсинской декларации 1975 г., пересмотренными в 2008 г. Всем больным проводилась диагностика перипротезной инфекции согласно рекомендациям Proceedings of the International Consensus Meeting on Periprosthetic Joint Infection [24, 25]. После тщательного предоперационного планирования известными способами осуществлялся хирургический доступ к инфицированному суставу, с помощью ревизионного инструментария бережно удалялись все элементы эндопротеза, проводилась радикальная обработка гнойно-воспалительного очага с последующей установкой цементного спейсера (преформированного или блоковидного) соответствующего размера с антибактериальными препаратами (ванкомицин и/или гентамицин, и/или цефазолин) (рис. 1).
На амбулаторном этапе осуществлялся контроль клинико-рентгенологического состояния больных, острофазовых показателей крови (лейкоциты, СОЭ и СРБ) и микробиологических данных суставного содержимого. При отсутствии клинико-лабораторных признаков наличия гнойно-воспалительного процесса проводили второй этап лечения, в ходе которого удаляли элементы цементного спейсера и имплантировали компоненты эндопротеза (рис. 2). Средний срок между этапами лечения составил 8,84 ± 5,8 (от 4 до 32) месяца.
.png)
Оценка результатов купирования гнойно-воспалительного процесса у больных с перипротезной инфекцией производилась нами на основе международного многопрофильного соглашения Delphi, согласно которому использовались следующие критерии [26]:
а) искоренение инфекции (отсутствие ран, свищей, дренажей, боли, а также рецидива инфекции, вызванного тем же штаммом микроорганизма)
а) искоренение инфекции (отсутствие ран, свищей, дренажей, боли, а также рецидива инфекции, вызванного тем же штаммом микроорганизма)
б) отсутствие хирургического вмешательства с целью купирования инфекции после последней операции (реимплантации);
в) отсутствие летального исхода по причине сепсиса.
Прослежены результаты лечения всех 172 больных в сроки от 2 до 6 лет, средний срок наблюдения
составил 4 ± 1,58 года. Статистическая обработка проводилась при помощи программного обеспечения
“Microsoft Excel” с вычислением среднего значения и статистического отклонения.
РЕЗУЛЬТАТЫ
Согласно классификации D.T. Tsukayama у 90 (52%) больных отмечалась острая послеоперационнаяинфекция, поздняя хроническая – у 36 (21 %) пациентов и острая гематогенная – у 34 (20 %).
Положительная интраоперационная культура выявлена у 12 (7 %) больных. Однако на момент поступления в нашу клинику у всех пациентов время манифестации инфекции составило более 4 недель, что являлось абсолютным показанием для удаления инфицированного сустава.
После клинико-рентгенологического обследования у 144 (84 %) больных были выявлены свищи, раны – у 7 (4 %), отек и гиперемия области послеоперационного шва – у 21 (12 %) пациента. При поступлении в клинику у пациентов с локализацией перипротезной инфекции в тазобедренном суставе отмечались следующие типы дефектов согласно классификации Paprosky W.G. [27]. Дефекты вертлужной впадины I типа наблюдались у 36 % пациентов, у 55 % пациентов отмечался II тип и лишь у 9 % больных был III тип.
Вместе с тем, среди дефектов бедренной кости доминировали I и II типы (38 % и 33 % соответственно), в 25 % случаев выявлены дефекты III типа и IV типа – у 4 % пациентов.
У пациентов с локализацией инфекции в коленном суставе дефекты костей классифицировали согласно AORI [28]. Среди дефектов коленного сустава преобладал I тип, который наблюдался в 37 % случаев, II А тип и II В тип отмечались в 21 % и 18 % соответственно, а также III тип был выявлен у 24 % больных.
По клиническим показаниям проведено микробиологическое исследование биоматериалов 172 больных, результаты которого представлены на рисунке 3.
.png)
.png)
.png)
Из таблицы видно, что после удаления инфицированного эндопротеза тазобедренного сустава и установки цементного спейсера в 37 (32,7 %) случаях наблюдался рецидив инфекции, из них 15 больным с ранним рецидивом выполнен дебридмент сустава без удаления спейсера, 14 пациентам произведена переустановка спейсера, еще 4 – резекционная артропластика и 4 других отказались от замены спейсера на эндопротез. После второго этапа лечения рецидив гнойного процесса отмечался лишь у 3 (2,6 %) больных, которые повторно прошли процедуру двухэтапного лечения. В целом, из 113 больных с перипротезной инфекцией тазобедренного сустава 102 (90,2 %) было успешно проведено двухэтапное лечение.
59 пациентам с перипротезной инфекцией коленного сустава выполнено 60 процедур двухэтапного реэндопротезирования, так как у одной больной было двустороннее поражение суставов. После первого этапа лечения (установки спейсера) рецидив гнойно-воспалительного процесса выявлен в 17 (28,3 %) случаях, из них 4 больным с ранним рецидивом выполнен дебридмент сустава без удаления спейсера, 6 пациентам произведена переустановка спейсера, еще 7 – артродез сустава.
После второго этапа лечения рецидив гнойного процесса отмечался лишь у 2 (3,3 %) больных, одному из которых повторно проведена процедура двух этапного лечения и другому – артродез. В целом из 60 случаев двухэтапных ревизий, выполненных 59 больным, 50 (83,3 %) были успешными.
ОБСУЖДЕНИЕ
Двухэтапное ревизионное эндопротезирование суставов с использованием цементного спейсера –
сложная медицинская процедура, которая позволяет хирургам надеяться на благополучный результат лечения в плане купирования гнойного процесса. Это обеспечивается возможностью проведения двукратной хирургической обработки сустава в сочетании с курсами этиотропной терапии и последующего эндопротезирования сустава [29, 30]. Однако в последнее время отмечаются публикации, которые подвергают сомнению высокую эффективность данной методики лечения [31, 32].
Нами проведен анализ современной литературы в отношении степени эффективности двухэтапного ревизионного эндопротезирования. Эти данные отражены в таблице 2.
.png)
ревизии в 93 % с хорошими функциональными результатами [18]. Наиболее успешно были пролечены
пациенты в американских клиниках с купированием гнойно-воспалительного процесса в 94 % случаев [33].
Pelt C.E. c коллегами продемонстрировали наибольший уровень рецидива инфекции после двухэтапного лечения с 22 % уровнем летального исхода [34].
Claassen L. также констатирует значительный уровень рецидива, который достигает 24 % [35]. Citak M. после обзора статей делает вывод, что нет никаких различий в отношении контроля инфекции между различными видами спейсеров [36].
Уровень подавления гнойного процесса в нашей клинике составил 86,7 % (83,3 % для коленного и 90,2 % для тазобедренного суставов) случаев при среднем сроке наблюдения 4,1 года и рецидивом инфекции в 13,3 % (9,8 % для тазобедренного и 16,7 % для коленного суставов) случаев.
ВЫВОДЫ
Двухэтапное ревизионное эндопротезирование суставов с использованием цементного спейсера является достаточно эффективным вариантом лечения перипротезной инфекции, который обеспечивает подавление гнойно-воспалительного процесса в 86,7 % (83,3 % для коленного и 90,2 % для тазобедренного суставов) случаев в среднесрочном периоде наблюдения до 5 лет.
Однако уровень рецидива гнойного процесса остается значительным, достигая 13,3 % (9,8 % для тазобедренного и 16,7 % для коленного суставов) случаев.
Конфликт интересов: не заявлен.
ЛИТЕРАТУРА
1.Early postoperative complications after total hip arthroplasty: current strategies for prevention and treatment / M. Khan, C.J. Della Valle, D.J. Jacofsky, R.M.Meneghini, F.S. Haddad // Instr. Course Lect. 2015. Vol. 64. P.
337-346.
2.Advanced age and comorbidity increase the risk for adverse events after revision total hip arthroplasty / K. Koenig, J.I. Huddleston 3rd, H. Huddleston, W.J.Maloney, S.B. Goodman // J. Arthroplasty. 2012. Vol. 27, No 7. P. 1402-1407. DOI: 10.1016/j.arth.2011.11.013.
3.Singh J.A., Lewallen D.G. Ninety-day mortality in patients undergoing elective total hip or total knee arthroplasty // J. Arthroplasty. 2012. Vol. 27, No 8. P. 1417-1422. DOI: 10.1016/j.arth.2012.03.008.
4.Why are total knee arthroplasties failing today – has anything changed after 10 years? / P.F. Sharkey, .M.Lichstein, C. Shen, A.T. Tokarski, J. Parvizi // J. Arthroplasty. 2014. Vol. 29, No 9. P. 1774-1778. DOI: 10.1016/j.arth.2013.07.024.
5.Causes of early failure after total hip arthroplasty / T. Zhang, C. Zheng, H. Ma, C. Sun // Zhonghua Yi Xue Za Zhi. 2014. Vol. 94, No 48. P. 3836-3838.
6.Iamthanaporn K., Chareancholvanich K., Pornrattanamaneewong C. Revision primary total hip replacement: causes and risk factors // J. Med. Assoc. Thai. 2015. Vol. 98, No 1. P. 93-99.
7.Huang Z., Sun C. Causes of failure after total knee arthroplasty // Zhonghua Yi Xue Za Zhi. 2015. Vol. 95, No 20. P. 1606-1608.
8.Periprosthetic joint infection / B.H. Kapadia, R.A. Berg, J.A. Daley, J. Fritz, A. Bhave, M.A. Mont // Lancet. 2016. Vol. 387, No 10016. P. 386-394.
9.Antibiotic-loaded bone cement in total joint arthroplasty / D. Soares, P. Leite, P. Barreira, R. Aido, R. Sousa // Acta Orthop. Belg. 2015. Vol. 81, No 2. P.184-190.
10.Periprosthetic infections after total hip and knee arthroplasty – a review / G. Vrgoc, M. Japjec, G. Gulan, J. Ravlić-Gulan, M. Marinović, A. Bandalović // Coll. Antropol. 2014. Vol. 38, No 4. P. 1259-1264.
11.Monitoring bacterial burden, inflammation and bone damage longitudinally using optical and μCT imaging in an orthopaedic implant infection in mice / J.A. Niska, J.A. Meganck, J.R. Pribaz, J.H. Shahbazian, E. Lim, N. Zhang, B.W. Rice, A. Akin, R.I. Ramos, N.M. Bernthal, K.P. Francis, L.S. Miller // PLoS One. 2012. Vol. 7, No 10. P. e47397. DOI: 10.1371/journal.pone.0047397.
12.Descriptive analysis of the economic costs of periprosthetic joint infection of the knee for the public health system of Andalusia / J. Garrido-Gómez, M.A.Arrabal-Polo, M.S. Girón-Prieto, J. Cabello-Salas, J. Torres Barroso, J. Parra-Ruiz // J. Arthroplasty. 2013. Vol. 28, No 7. P. 1057-1060.
13.Анализ эффективности санирующих операций при параэндопротезной инфекции / Б. Лю, Р.М. Тихилов, И.И. Шубняков, С.А. Божкова, Артюх, А.О. Денисов // Травматология и ортопедия России. 2014. No 2 (72). С. 22-29. DOI:10.21823/2311-2905-2014-0-2-22-29.
14.Two-stage revision of infected hip arthroplasty using an antibiotic-loaded spacer: retrospective comparison between short-term and prolonged antibiotic therapy / P.H. Hsieh, K.C. Huang, P.C. Lee, M.C. Lee // J. Antimicrob. Chemother. 2009. Vol. 64, No 2. P. 392-397. DOI: 10.1093/jac/dkp177.
15.Moran E., Byren I., Atkins B.L. The diagnosis and management of prosthetic joint infections // J. Antimicrob. Chemother. 2010. Vol. 65, No Suppl. 3. P.45-54. DOI: 10.1093/jac/dkq305.
16.Infectiological, functional, and radiographic outcome after revision for prosthetic hip infection according to a strict algorithm / F.H. de Man, P. Sendi, W.Zimmerli, T.B. Maurer, P.E. Ochsner, T. Ilchmann // Acta Orthop. . Vol. 82, No 1. P. 27-34. DOI: 10.3109/17453674.2010.548025.
17.Parvizi J., Zmistowski B., Adeli B. Periprosthetic joint infection: treatment options // Orthopedics. 2010. Vol. 33, No 9. P. 659. DOI: 10.3928/01477447-20100722-42.
18.Two-stage hip revision arthroplasty with a hexagonal modular cementless stem in cases of periprosthetic infection / R. Dieckmann, D. Schulz, G. Gosheger, K. Becker, K. Daniilidis, A. Streitbürger, J. Hardes, S. Hoell // BMC Musculoskelet. Disord. 2014. Vol. 15. P. 398. DOI: 10.1186/1471-2474-15-398.
19.Преображенский П.М., Каземирский А.В., Гончаров М.Ю. Современные взгляды на диагностику и лечение пациентов с перипротезной инфекцией после эндопротезирования коленного сустава // Гений ортопедии. 2016. No 3. С. 94-104.
20.Management of periprosthetic joint infection after total hip arthroplasty using a custom made articulating spacer (CUMARS); the Exeter experience / J.D. Tsung, J.A. Rohrsheim, S.L. Whitehouse, M.J. Wilson, J.R. Howell // J. Arthroplasty. 2014. Vol. 29, No 9. P. 1813-1818. DOI: 10.1016/j.arth.2014.04.013.
21.Fungal periprosthetic joint infection in total knee arthroplasty: a systematic review / O. Jakobs, B. Schoof, T.O. Klatte, S. Schmidl, F. Fensky, D. Guenther, L. Frommelt, T. Gehrke, M. Gebauer // Orthop. Rev. (Pavia). 2015. Vol. 7, No 1. P. 5623. DOI: 10.4081/or.2015.5623.
22.Two-stage revision protocol in multidrug resistant periprosthetic infection following total hip arthroplasty using a long interval between stages / G.C. Babis, V.I. Sakellariou, P.G. Pantos, G.G. Sasalos, N.A. Stavropoulos // J. Arthroplasty. 2015. Vol. 30, No 9. P. 1602-1606. DOI: 10.1016/j.arth.2015.04.004.
23.Тактика лечения инфекционных осложнений после эндопротезирования тазобедренного сустава / Р.Н. Комаров, В.Н. Митрофанов, А.В. Новиков, С.Б. Королёв // Травматология и ортопедия России. 2016. Т. 22, No 4. С. 25-34.
24.Enayatollahi M.A., Parvizi J. Diagnosis of infected total hip arthroplasty // Hip Int. 2015. Vol. 25, No 4. P. 294-300. DOI: 10.5301/hipint.5000266.
25.Definition of periprosthetic joint infection: is there a consensus? / J. Parvizi, C. Jacovides, B. Zmistowski, K.A. Jung // Clin. Orthop. Relat. Res. 2011. Vol.469, No 11. P. 3022-3030. DOI: 10.1007/s11999-011-1971-2.
26.Diaz-Ledezma C., Higuera C.A., Parvizi J. Success after treatment of periprosthetic joint infection: A Delphi-based international multidisciplinary consensus // Clin. Orthop. Relat. Res. 2013. Vol. 471, No 7. P. 2374-2382. DOI: 10.1007/s11999-013-2866-1.
27.Della Valle C.J., Paprosky W.G. The femur in revision total hip arthroplasty evaluation and classification // Clin. Orthop. Relat. Res. 2004. No 420. P. 55-62.
28.Review article: bone defect classifications in revision total knee arthroplasty / Y.Y. Qiu, C.H. Yan, K.Y. Chiu, F.Y. Ng // J. Orthop. Surg. (Hong Kong). 2011. Vol. 19, No 2. P. 238-243. DOI: 10.1177/230949901101900223.
29.Two-stage treatment of hip periprosthetic joint infection is associated with a high rate of infection control but high mortality / K.R. Berend, A.V. Lombardi Jr., M.J. Morris, A.G. Bergeson, J.B. Adams, M.A. Sneller // Clin. Orthop. Relat. Res. 2013. Vol. 471, No 2. P. 510-518. DOI: 10.1007/s11999-012-2595-x.
30.One-stage revision of infected hip arthroplasty: outcome of 39 consecutive hips / T. Ilchmann, W. Zimmerli, P.E. Ochsner, B. Kessler, L. Zwicky, P. Graber, M. Clauss // Int. Orthop. 2016. Vol. 40, No 5. P. 913-918. DOI: 10.1007/s00264-015-2833-4.
31.Management of deep postoperative shoulder infections: is there a role for open biopsy during staged treatment? / A.L. Zhang, B.T. Feeley, B.S. Schwartz, T.T. Chung, C.B. Ma // J. Shoulder Elbow Surg. 2015. Vol. 24, No 1. P. 15-20. DOI: 10.1016/j.jse.2014.04.007.
32.Two-stage exchange arthroplasty for infected total knee arthroplasty: predictors of failure / S.M. Mortazavi, D. Vegari, A. Ho, B. Zmistowski, J. Parvizi // Clin. Orthop. Relat. Res. 2011. Vol. 469, No 11. P. 3049-3054. DOI: 10.1007/s11999-011-2030-8.
33.Treatment of periprosthetic knee infection with a two-stage protocol using static spacers / P. Lichstein, S. Su, H. Hedlund, G. Suh, W.J. Maloney, S.B.Goodman, J.I. Huddleston 3rd // Clin. Orthop. Relat. Res. 2016.
Vol. 474, No 1. P. 120-125. DOI: 10.1007/s11999-015-4443-2.
34.Two-stage revision TKA is associated with high complication and failure rates / C.E. Pelt, R. Grijalva, L. Anderson, M.B. Anderson, J. Erickson, C.L. Peters // Adv. Orthop. 2014. Vol. 2014. P. 659047. DOI: 10.1155/2014/659047.
35.Two-stage revision total knee arthroplasty in cases of periprosthetic joint infection: an analysis of 50 cases / L. Claassen, C. Plaass, K. Daniilidis, T. Calliess, G. von Lewinski // Open Orthop. J. 2015. Vol. 9. P. 49-56. DOI: 10.2174/1874325001509010049.
36.Citak M., Citak M., Kendoff D. Dynamic versus static cement spacer in periprosthetic knee infection: A meta-analysis // Orthopade. 2015. Vol. 44, No 8. P.599-606.
А.М. Ермаков, Н.М. Клюшин, Ю.В. Абабков, А.С. Тряпичников, А.Н. Коюшков
Федеральное государственное бюджетное учреждение "Российский научный центр "Восстановительная травматология и ортопедия" им. акад. Г.А. Илизарова»
Министерства здравоохранения Российской Федерации, г. Курган, Россия;
Федеральное государственное бюджетное образовательное учреждение высшего образования
«Тюменский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Тюмень, Россия
Теги: коленный сустав
234567 Начало активности (дата): 07.03.2020 14:47:00
234567 Кем создан (ID): 989
234567 Ключевые слова: эндопротезирование, коленный сустав, тазобедренный сустав, перипротезная инфекция, лечение, двухэтапная ревизия
12354567899
Похожие статьи
Опыт ультразвуковой диагностики поражений коленных суставовРентген на дому 8 495 22 555 6 8
Коленный сустав
Оперативное лечение пациентов с гонартрозом и варусной деформацией коленного сустава с применением аппарата Илизарова
Магнитно-резонансная томография в выявлении недиагностированных переломов костей коленного сустава



