 11.05.2026
11.05.2026
Артериовенозная мальформация в легком у мужчины 43 лет
Артериовенозная мальформация легких (АВМЛ) – это эмбриональное нарушение формирования сосудов легкого, при котором возникает сообщение между артериальными и венозными сосудами.
Введение
Артериовенозная мальформация легких (АВМЛ) – это нарушение развития сосудов легкого, возникающее на эмбриональном этапе развития, при котором формируется локальная сеть анастомозов между артериальными и венозными сосудами. На практике данная патология отмечается у 2–3 человек на 100 тыс. населения [1]. Однако лишь в 10% случаев клинические проявления наблюдаются в детском возрасте, а у 90% пациентов АВМЛ диагностируется во втором-четвертом десятилетиях жизни. У мужчин и женщин она встречается с одинаковой частотой [2, 3].
Этиология АВМЛ, как и прочих пороков развития легких, связана с различными пренатальными нежелательными факторами: радиационное, электромагнитное, химическое, биологическое воздействие на плод, токсикозы и заболевания беременных [4]. В первую очередь, влияние на ангиогенез и процессы ремоделирования сосудистой стенки оказывают генетические факторы [5]. Патология сосудов проявляется поражением любого из слоев их стенки [6].
АВМЛ представлены как самостоятельными аномалиями, так и частью врожденных синдромов. В 60–70% случаев АВМЛ могут быть единичными, в 30–40% – множественными, при этом у 75% пациентов наблюдается одностороннее поражение. Для систематизации сосудистых патологий используют классификацию Международного общества изучения сосудистых аномалий (International Society for the Study of Vascular Anomalies, ISSVA) 1996 г., которая постоянно обновляется [7–9]. Эта система основана на исследованиях гемодинамики, проведенных J.B. Mulliken и J. Glowacki в 1982 г. [10]. Сосудистые аномалии подразделяются на опухоли (гемангиомы) и мальформации. Сосудистая мальформация – это врожденный дефект строения сосудов, возникший в результате нарушения эмбрионального ангиогенеза.
Среди сосудистых мальформаций различают [9]: – мальформации с медленным кровотоком, среди которых несколько подтипов капиллярных, венозных и лимфатических мальформаций;
– мальформации с быстрым кровотоком, которые, в свою очередь, делятся на артериальные, артериовенозные фистулы и артериовенозные мальформации;
– комбинированные сложные сосудистые мальформации.
Артериовенозные анастомозы могут возникать на уровне сегментарного, субсегментарного и более мелкого деления сосудов легких [11]. АВМЛ небольших размеров протекают бессимптомно и часто становятся случайной находкой при компьютерной визуализации легких с контрастированием сосудов. Клиническими проявлениями и осложнениями сосудистой мальформации легких могут быть легочные кровотечения, гемоторакс, инфаркт и абсцесс легкого [1].
Основными методами диагностики АВМЛ являются ангиопульмонография и мультиспиральная компьютерная томография (МСКТ) – ангиография с контрастированием легочных сосудов, реже перфузионная сцинтиграфия легких.
Рентгеноконтрастные исследования обеспечивают визуализацию питающего и дренирующего сосудов [4]. Дифференциальная диагностика чаще проводится с лобарной эмфиземой, туберкуломой и солитарными воздушными кистами легких.
Представляем собственное клиническое наблюдение АВМЛ в S4, S5 левого легкого, диагностированной при МСКТ с контрастированием у взрослого мужчины. От пациента получено письменное информированное добровольное согласие на публикацию его изображений с научной целью (дата подписания 15.02.2025).
Описание случая
Мужчина 43 лет поступил с жалобами на непродуктивный кашель, одышку инспираторного характера при незначительных физических нагрузках, головные боли, выраженную общую слабость.
Из анамнеза известно, что пациент в возрасте 22 лет впервые отметил одышку при умеренной физической нагрузке, в связи с чем обратился за медицинской помощью. Была выполнена МСКТ органов грудной клетки, при которой выявлена артериовенозная мальформация верхней доли левого легкого. Пациенту было рекомендовано динамическое наблюдение. С периодичностью в 5 лет проводились рентгенологические исследования, увеличения мальформации в динамике не отмечалось. В течение последнего года пациент дважды перенес левостороннюю верхнедолевую пневмонию, после второго эпизода отметил ухудшение состояния в виде нарастания одышки, снижения толерантности к физическим нагрузкам. Также его стала беспокоить головная боль – после осмотра невролога установлен диагноз «мигрень без ауры». В связи с ухудшением состояния больной обратился к торакальному хирургу, был планово госпитализирован в отделение торакальной хирургии.
При поступлении общее состояние пациента было расценено как средней степени тяжести. При физикальном осмотре отмечался диффузный цианоз, изменение ногтевых пластин по типу часовых стекол (рис. 1).

Температура тела 36,6 °С, частота дыхательных движений 21 в минуту. Сатурация крови кислородом (SpO2) на воздухе в покое 87%, при ходьбе по палате десатурация до 85%, на фоне инсуффляции увлажненным кислородом 4–5 л/мин – 89–91%. По данным теста 6-минутной ходьбы: до нагрузки SpO2 86%, пульс 79 уд/мин, одышка по шкале Борга 3 балла; на 6-й минуте – 84%, 107 уд/мин, 5 баллов соответственно. Пациент прошел 408 м, что составило 58% от должного. Восстановление после нагрузки произошло через 1 мин. По данным бодиплетизмографии и спирометрии объемные и скоростные показатели в пределах нормы. При проведении пробы с бронхолитиком данных за бронхоспазм не получено.
Диффузионная способность легких по монооксиду углерода (diffusion capacity of the lungs for carbon monoxide, DLCO) была умеренно снижена (81% от должного до коррекции по гемоглобину, 77% от должного после нее; гемоглобин 165 г/л). Альвеолярный объем (АО) в пределах нормы (7,91 л – 115% от должного). Отношение DLCO к АО после коррекции по гемоглобину снижено (66% от должного). Жизненная емкость легких в пределах нормы (5,95 л – 115% от должного). Легочный газообмен умеренно снижен. При исследовании газового состава артериальной крови: водородный показатель (pH) 7,43, парциальное давление углекислого ваза (PaCO2) 30 мм рт. ст., парциальное давление кислорода (PaO2) 56,1 мм рт. ст., SpO2 89%, уровень лактата 0,8 ммоль/л, дефицит оснований (cBase) 3,7 ммоль/л, содержание бикарбоната (HCO3 –) 22 ммоль/л, что свидетельствует о гипоксемии средней степени тяжести и гипокапнии, обусловленной явлениями гипервентиляции.
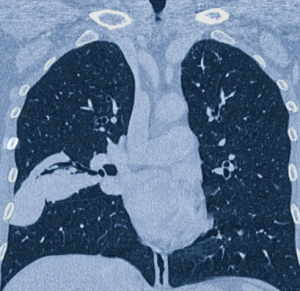
По данным фибробронхоскопии выявлена картина диффузного двустороннего бронхита, кисты правой валекулы. При МСКТ органов грудной клетки в сегментах S4 и S5 левого легкого обнаружены субплеврально расположенные клубки извитых сосудов общей протяженностью до 46 мм, сообщающиеся с расширенными до 6,9 мм четырьмя и пятью сегментарными ветвями легочной артерии и расширенными до 8,4 мм ветвями левой верхней легочной вены (рис. 2).
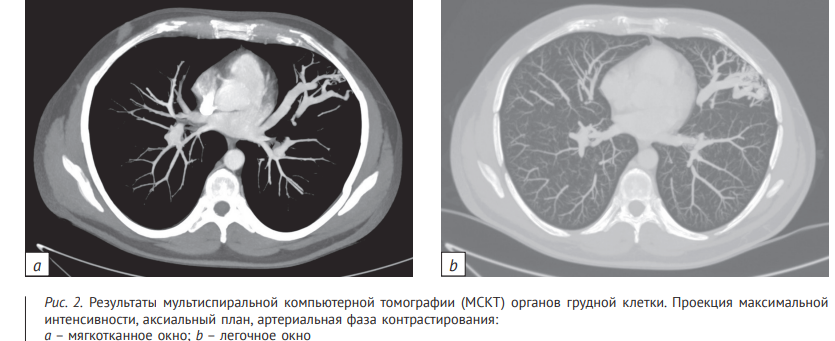
С помощью 3D-реконструкции, выполненной при исследовании в артериальную фазу контрастирования, визуализированы расширенные анастомозирующие ветви легочных артерии и вены (рис. 3).
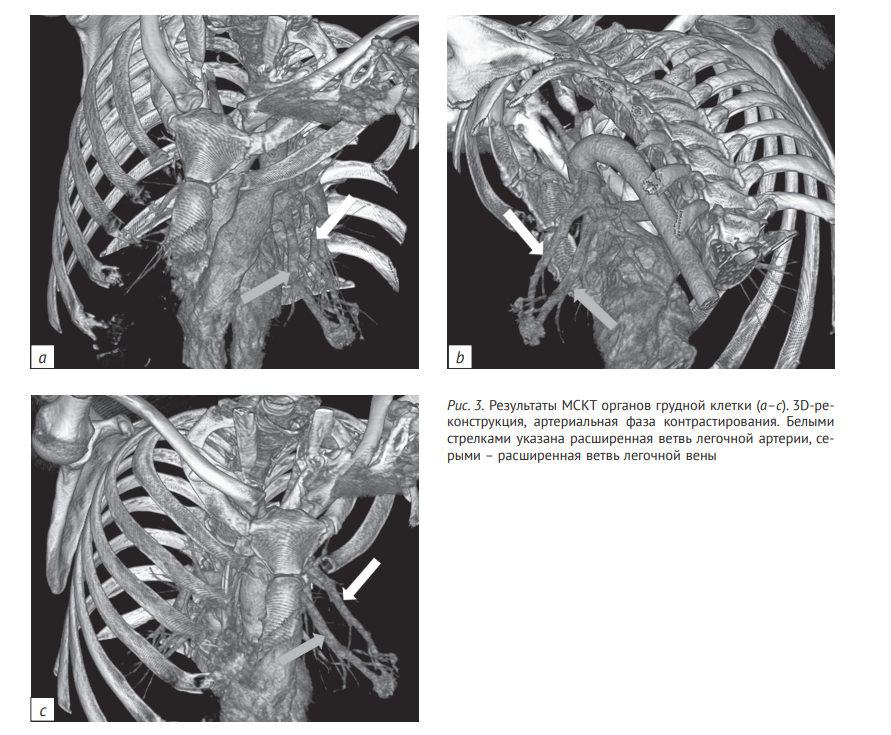
Таким образом, МСКТ-картина соответствовала крупной артериовенозной мальформации язычковых сегментов левого легкого. Выполнена видеоассистированная торакоскопия (ВАТС) левого легкого. При ревизии: легкое повышенной воздушности, в области S4, S5 субплеврально пальпируются АВМЛ до 30 мм и до 15 мм.
Во время оперативного вмешательства при проведении однолегочной вентиляции до момента пересечения основной артерии язычковых сегментов фракция кислорода во вдыхаемой смеси (FiO2) составляла 100%, PaO2 артериальной крови – 56,1 мм рт. ст., SpO2 – 89%. После пересечения приносящего сосуда FiO2 была снижена до 50%, на фоне чего РаO2 составило 102 мм рт. ст., SpO2 – 97,7%. Проведена анатомическая сегментэктомия S4, S5 левого легкого. Участок легкого с изменениями направлен на плановое гистологическое исследование. Время операции составило 70 мин, время нахождения пациента в отделении интенсивной терапии – 1 сут. В раннем послеоперационном периоде SpO2 составила 96–98% на воздухе в покое, обращало на себя внимание уменьшение выраженности цианоза, а таже ощущение пациентом одышки. Срок госпитализации после оперативного вмешательства – 4 сут.
При макроскопической оценке фрагмента ткани легкого размеры составили 13×8×4 см, висцеральная плевра с поверхности серовато-розовая, гладкая, на разрезе параллельно сегментарному бронху диаметром 0,8 см расположена вена диаметром 1,5 см, которая заканчивалась субплеврально в красно-черных многокамерных образованиях диаметром от 1,5 до 3 см, расположенных на расстоянии до 1 см друг от друга, заполненных кровяными сгустками.
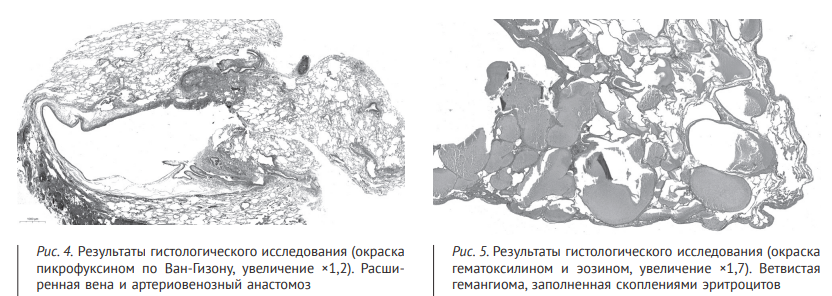
При гистологическом исследовании обнаружена расширенная вена и артериовенозный анастомоз (рис. 4), заканчивающиеся множественными близко прилежащими друг к другу полнокровными тонкостенными сосудами, образующими целую сеть (рис. 5). Здесь же имели место расширенные сосуды, местами напоминающие артериовенозные анастомозы, значительная часть лимфатических сосудов также была резко расширена, встречались единичные сосудистые плексусы, в просветах части окружающих альвеол выявлены скопления эритроцитов. При окраске пикрофуксином по Ван-Гизону практически все сосуды, как и расширенная вена, имели одну эластическую мембрану, местами наблюдался фиброэластоз интимы. В одном из участков виден переход вены в артерию (см. рис. 4). На основании полученных данных сформулирован клинический диагноз: «Основное заболевание: Q27.3. Артериовенозная мальформация средней доли левого легкого.
Осложнение основного заболевания: хроническая гипоксемическая дыхательная недостаточность средней степени тяжести».
Обсуждение
Поражение нижних долей легких при АВМЛ описано в 63–70% случаев [12]. В 75% наблюдений повреждено одно легкое [13, 14], множественные мальформации встречаются в 36%, среди которых в половине наблюдений имеет место двустороннее нарушение. У 81% пациентов в процесс вовлечена висцеральная плевра [15].
В представленном наблюдении поражение было односторонним в S4, S5 левого легкого, при этом гемангиоматоз имел место в висцеральной плевре и под ней. Следует отметить, что перед оперативным вмешательством при пульсоксиметрии значение SpO2 составило 86% и было практически неизменным при тесте 6-минутной ходьбы (снижение до 84%), что обусловлено наличием внутрилегочного шунтирования крови при артериовенозной мальформации. Пациент был адаптирован к гипоксемии, что обусловлено ее длительным существованием.
Профессия больного не связана с физическим трудом, он является офисным работником. Также, с его слов, в семье не известно о родственниках с диагностированной АВМЛ, сам он имеет двух здоровых детей. Дважды перенесенные эпизоды внебольничной пневмонии привели к снижению респираторной функции, что заставило пациента обратиться за медицинской помощью. Важно обратить внимание на локализацию воспалительных изменений в легких, которые соответствовали расположению АВМЛ, что обусловлено локальным нарушением вентиляции и перфузии окружающей легочной ткани и может явиться одной из причин развития инфекционного процесса. Нечасто в литературе описаны головные боли, обусловленные АВМЛ и шунтированием крови. Нашему пациенту устанавливался диагноз мигрени без ауры, назначались анальгетические препараты различных групп, однако после операции он отметил отсутствие необходимости в приеме лекарственных средств, что свидетельствует об улучшении качества жизни.
Гистологически АВМЛ имеют ряд отличительных особенностей [12]:
– тонкостенные сосудистые каналы (по типу папиросной бумаги), выстланные тонким слоем эндотелия;
– строма состоит из соединительной ткани и не связана с прилежащей легочной тканью;
– стенка артериовенозного образования уплотнена за счет разрастаний фиброзной ткани и эластических волокон.
По форме АВМЛ могут быть округлыми, овальными, грушевидными или гроздьевидными, состоящими из нескольких полостей размерами от 1 до 10 см. По строению различают простой тип мальформаций (80–90%), когда одна питающая сегментарная артерия соединяется с одной дренирующей веной, и сложный (комплексный), когда мальформация образована двумя и более питающими артериями и дренирующими венами [14]. В нашем наблюдении имелась одна дренирующая вена диаметром 1,5 см, по периферии сформировалось гемангиоматозное сосудистое сплетение.
МСКТ является наиболее информативным методом диагностики артериовенозных мальформаций с очень высоким пространственным разрешением [15]. В представленном случае выявление АВМЛ при МСКТ с контрастированием и подтверждение полученных результатов с помощью 3D-реконструкции способствовали правильной диагностике и позволили выбрать наиболее щадящий метод лечения.
Рентгеноэндоваскулярная эмболизация АВМЛ – наименее инвазивное и достаточно эффективное вмешательство, которое при необходимости легко повторить в различные сроки, однако этот метод не является общедоступным [16]. Открытая торакотомия, как правило, показана при больших центрально расположенных очагах с короткими приводящими артериями, при субплеврально расположенных мальформациях, а также при наличии противопоказаний к рентгеноэндоваскулярным вмешательствам и при их низкой эффективности. После открытой торакотомии вероятность рецидива заболевания низка. Все чаще, особенно при небольших мальформациях, рекомендуется резекционная ВАТС в виде лобэктомии либо удаления одного или нескольких сегментов легкого [17], как и было выполнено в нашем наблюдении. Все пациенты подлежат динамическому наблюдению, особенно в первый год после процедуры [18].
Заключение
АВМЛ в двух сегментах левого легкого – крайне редкая патология у взрослых. В описанном клиническом случае она выявлена у пациента 43 лет с помощью МСКТ с контрастированием, которая позволила оценить риск оперативного вмешательства. Успешно проведена ВАТС с анатомической резекцией двух сегментов левого легкого, послеоперационный период протекал без осложнений. Вероятнее всего, данное нарушение у взрослого человека носило врожденный характер. Радикальное лечение привело к нормализации показателей респираторной функции и значительному улучшению качества жизни пациента.
Литература
1. Филинов И.В., Петров Е.И., Цыгина Е.Н. и др. Лучевая диагностика артериовенозной мальформации легких у детей. Российский электронный журнал лучевой диагностики. 2013; 3(3): 32–41.
2. Nosher L, Murillo PG, Liszewski M, et al. Vascular anomalies: a pictorial review of nomenclature, diagnosis and treatment. World J Radiol. 2014; 6(9): 677–92.
3. Jha AK, Sunder A. An unusual case of pulmonary arterio-venous fistula (PAVF). J Family Med Prim Care. 2019; 8(10): 3408–11.
4. Урыков А.Д. Морфология артериовенозных мальформаций головного мозга. Современные технологии в медицине. 2011; 3: 116–8.
5. Эркинова С.А., Киселёв В.С., Стрельников Н.В. и др. Исследование ассоциации полиморфных вариантов rs1333040 и rs7865618 хромосомы 9p21 с развитием артериовенозных мальформаций. Медицинская генетика. 2016; 15(5): 61–4.
6. Кострова О.Ю., Михайлова М.Н., Семенова О.В. и др. Случаи выявления артериовенозных мальформаций лeгких и селезенки. Acta Medica Eurasica. 2020; 4: 25–32.
7. 2025 ISSVA Classification
8. Enjolras O, Wassef M, Chapot R. Color atlas of vascular tumors and vascular malformations. Cambridge University Press; 2007: 1–11.
9. Гончарова Я.А. Гемангиомы и сосудистые мальформации. Современные теории и лечебная тактика. Здоровье ребенка. 2013; 6: 148–52.
10. Milliken JB, Glowacki J. Hemangiomas and vascular malformations in infants and children: a classification based on endothelial characteristics. Plast Reconstr Surg. 1982; 69(3): 412–22.
11. Цап Н.А., Виноградова И.А., Некрасова Е.Г. Редкий порок развития легких у детей – артериовенозная мальформация нижней доли правого легкого (случай из практики). Детская больница. 2011; 1: 56–9.
12. Цап Н. А., Виноградова И. А., Некрасова Е. Г. Редкий порок развития лёгких у детей - артериовенозная мальформация нижней доли правого лёгкого // Детская больница. 2011. № 1. С. 56-59.
13. Цой Е. Г., Игишева Л. Н., Карташян Э. С. Артериовенозная мальформация нижней доли левого лёгкого у пациента раннего возраста // Комплексные проблемы сердечно-сосудистых заболеваний. 2013. № 4. С. 50-55.
14. Anabtawi I. N., Ellison R. G., Ellison L. T. Pulmonary arteriovenous aneurysms and fistulas: Anatomical variations, embryology and classification // Ann. Thorac. Surg. 1965. № 122. P. 277-285.
15. Ando K., Mochizuki A., Kurimoto N. et al. Coil embolization for pulmonary arteriovenous malformation as an organ-sparing therapy: outcome of long-term follow-up // Ann. Thorac. Cardio vasc. Surg. 2011. Vol. 17, № 2. P. 118-123.
16. Angriman F., Ferreyro B. L., Wainstein E. J., Serra M. M. Pulmonary arteriovenous malformations and embolic complications in patients with hereditary hemorrhagic telangiectasia // Arch. Bronco neumol. 2014. Vol. 50, № 7. P. 301-304.
17. Babaker M., Breault S., Beigelman C. et al. Endovascular treatment of pulmonary arteriovenous malformations in hereditary haemorrhagic telangiectasia // Swiss. Med. Wkly. 2015. Vol. 28, № 145. P. 14151.
18. Bélanger C., Chartrand-Lefebvre C., Soulez G. et al. Pulmonary arteriovenous malformation (PAVM) reperfusion after percutaneous embolization: Sensitivity and specificity of non-enhanced CT // Eur. J. Radiol. 2016. Vol. 85, № 1. P. 150-157.
19. Conrad M. B., Ishaque B. M., Surman A. M. et al. Intraprocedural safety and technical success of the MVP micro vascular plug for embolization of pulmonary arteriovenous malformations // J. Vasc. Interv. Radiol. 2015. Vol. 26, № 11. P. 1735-1739.
20. Duch P. M., Chandrasckaran K., Mulhern C. B. et al. Transesophageal echocardiographic diagnosis of pulmonary arteriovenous malformation: role of contrast and pulsed Doppler echocardiography // J. Chest. 1994. № 105. P. 1604-1605.
21. Faugnan M. E., Granton J. T., Young L. H. The pulmonary vascular complications of hereditary haemorrhagic telangiectasia // Eur. Respir. J. 2009. Vol. 33, № 5. P. 1186-1194.
22. Faughnan M. E., Palda V.A., Garcia-Tsao G. et al. International guidelines for the diagnosis and management of hereditary hemorrhagic telangiectasia // J. Med. Genet. 2011. Vol. 48, № 2. P. 73-87.
23. Fraga J. C., Favero E., Contelli F. et al. Surgical treatment of congenital pulmonary arteriovenous fistula in children // Pediatr. Surg. 2008. Vol. 43. P. 1365-1367.
24. Gamondès D., Si-Mohamed S., Cottin V. et al. Vein diameter on unenhanced multidetector CT: predicts reperfusion of pulmonary arteriovenous malformation after embolotherapy // Eur. J. Radiol. 2016. Vol. 85, № 1. P. 150-157.
25. Gill S. S., Roddie M. E., Shovlin C. L., Jackson J. E. Pulmonary arteriovenous malformations and their mimics // Clin. Radiol. 2015. Vol. 70, № 1. P. 96-110.
26. Gossage J. R. Role of contrast echocardiography in screening for pulmonary arteriovenous malformation in patients with hereditary hemorrhagic telangiectasia // Chest. 2010. Vol. 138, № 4. P. 769-771.
27. Gossage J. R., Kanj G. Pulmonary arteriovenous malformations: A state of the art review // Amer. J. Respir. Crit. Care. Med. 1998. Vol. 158, № 2. P. 643-661.
28. Hsu C. C., Kwan G. N., Thompson S. A. et al. Embolisation for pulmonary arteriovenous malformation // Cochrane Database Syst. Rev. 2015. Vol. 29, № 1. CD008017.
29. Kaleda V.I., Barbuhatti K. O., Porhanov V.A. Multiple pulmonary arteriovenous malformations // Asian Cardiovasc. Thorac. Ann. 2015. Vol. 31. pii: 0218492315579557.
30. Kawai T., Shimohira M., Kan H. et al. Feasibility of time-resolved MR angiography for detecting recanalization of pulmonaryarteriovenous malformations treated with embolization with platinum coils // J. Vasc. Interv. Radiol. 2014. Vol. 25, № 9. P. 1339-1347.
31. Kerut E. K. Intrapulmonary shunts and their clinical implications for the echocardiographer // Echocardiography. 2015. Vol. 32, № 3. P. 189.
32. Khurshid I., Downie G. H. Pulmonary arteiovenous malformation // Postgrad Med. J. 2002. № 78. P. 191-197.
33. Kim H. J., Lee J. S., Oh Y. M. et al. Clinical characteristics of pulmonary arteriovenous malformations in Koreans // Respirology. 2015. Vol. 20, № 1. P. 155-159.
34. Kraemer N., Krombach G. A. Images in clinical medicine: Pulmonary arteriovenous fistula // Engl. J. Med. 2009. Vol. 360. P. 1769.
35. Kucukay F., Özdemir M., Şenol E. et al. Large pulmonary arteriovenous malformations: long-term results of embolization with AMPLATZER vascular plugs // J. Vasc. Interv. Radiol. 2014. Vol. 25, № 9. P. 1327-1332.
36. Lacombe P., Lacout A., Marcy P. Y. et al. Diagnosis and treatment of pulmonary arteriovenous malformations in hereditary hemorrhagic telangiectasia: An overview // Diagn. Interv. Imaging. 2013. Vol. 94, № 9. P. 835-848.
37. Lacout A., Marcy P.Y., El Hajjam M., Lacombe P. Metformin as possible therapy of pulmonary arterio venous malformation in HHT patients // Med. Hypotheses. 2015. Vol. 85, № 3. P. 245-248.
38. Lange S., Walsh G. Лучевая диагностика заболеваний органов грудной клетки: Пер. с англ. / Под ред. акад. РАМН С. К. Тернового, проф. А. И. Шехтера. М.: ГЭОТАР-Медиа, 2010. 80 с.
39. Letteboer T. G., Benzinou M., Merrick C. B. et al. Genetic variation in the functional ENG allele inherited from the non-affected parent associates with presence of pulmonary arteriovenous malformation in hereditary hemorrhagic telangiectasia 1 (HHT1) and may influence expression of PTPN14 // Front Genet. 2015. Vol. 12, № 6. P. 67.
40. Mager J. J., Zanen P., Verzijlbergen F. et al. Quantification of rightto-left shunt with (99m)Tc-labelled albumin macroaggregates and 100 % oxygen in patients with hereditary haemorrhagic telangiectasia // Clin. Sci (Lond). 2002. № 102. P. 127-134.
41. Makimoto S., Hiraki T., Gobara H. et al. Association between reperfusion and shrinkage percentage of the aneurysmal sac after embolization of pulmonary arteriovenous malformation: evaluation based on contrast-enhanced thin-section CT images // Jpn. J. Radiol. 2014. Vol. 32, № 5. P. 266-273.
42. McMullan D. M., Riemer R. K. Embryology and anatomy of intrapulmonary shunts // Echocardiography. 2015. Vol. 32, № 3. P. 190-194.
43. Park J., Kim H. J., Kim J. M., Park Y. S. Successful Treatment of a Large Pulmonary Arteriovenous Malformation by Repeated Coil Embolization // Tuberc. Respir. Dis. (Seoul). 2015. Vol. 78, № 4. P. 408-411.
44. Pereira-da-Silva T., Martins J. D., de Sousa L. et al. Percutaneous occlusion of vascular malformations in pediatric and adult patients: 20-Year Experience of a Single Center // Catheter Cardiovasc. Interv. 2015. Vol. 31.
45. Rabellino M., Serra M., Peralta O. et al. Early experience with the AMPLATZER vascular plug IV for the occlusion of pulmonaryarteriovenous malformations // J. Vasc. Interv. Radiol. 2014. Vol. 25, № 9. P. 1333-1337.
46. Reichert M., Kerber S., Alkoudmani I., Bodner J. Management of a solitary pulmonary arteriovenous malformation by video-assisted thoracoscopic surgery and anatomic lingula resection: video and review // Surg. Endosc. 2015. Vol. 9.
47. Sano A., Tsuchiya T. Thoracoscopic surgery for multiple peripheral pulmonary arteriovenous fistulas // Ann. Thorac. Surg. 2015. Vol. 99, № 5. P. 1808-1809.
48. Shimohira M., Hashizume T., Kawai T. et al. Triaxial system in re-embolization for recanalization of pulmonary arteriovenous malformations // Pol. J. Radiol. 2015. Vol. 7, № 80. P. 67-71.
49. Shimohira M., Kawai T., Hashizume T. et al. Reperfusion Rates of Pulmonary Arteriovenous Malformations after Coil Embolization: Evaluation with Time-Resolved MR Angiography or Pulmonary Angiography // J. Vasc. Interv. Radiol. 2015. Vol. 26, № 6. P. 856-864.
50. Yazdi R., Saberi A. Coil Embolotherapy of Unilateral Diffuse Pul monary Arteriovenous Malformations in a Nineteen-Year-Old Woman // Iran J. Radiol. 2015. Vol. 22, № 12 (3). P. 9632.
Авторы;
Самсонова Мария Викторовна, д. м. н., заведующая лабораторией патологической анатомии ФГБУ «Научно-исследовательский институт пульмонологии» ФМБА России, ст. науч. сотр. лаборатории инновационной патоморфологии ГБУЗ «Московский клинический научный центр им. А.С. Логинова ДЗМ»/
Никитин Павел Алексеевич, к. м. н., заведующий отделением лучевой диагностики ФГБУ «Научно-исследовательский институт пульмонологии» ФМБА России
Черняев Андрей Львович, д. м. н., профессор, заведующий отделом фундаментальной пульмонологии ФГБУ «Научно-исследовательский институт пульмонологии» ФМБА России, вед. науч. сотр. лаборатории клинической морфологии Научно-исследовательского института морфологии человека им. академика А.П. Авцына ФГБНУ «Российский научный центр хирургии им. академика Б.В. Петровского»
Микушина Марина Анатольевна, врач-патологоанатом ФГБУ «Научно-исследовательский институт пульмонологии» ФМБА России
Данилов Виталий Владимирович, к. м. н., заведующий отделением торакальной хирургии ФГБУ «Научно-исследовательский ин ститут пульмонологии» ФМБА России
Омарова Жанна Рубеновна, к. м. н., заведующая патолого-анатомическим отделением ФГБУ «Научно-исследовательский институт пульмонологии» ФМБА России, доцент кафедры патологической анатомии и клинической патологической анатомии детского воз раста Института биологии и патологии человека ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России;
Крюкова Надежда Олеговна, к. м. н., врач-терапевт ФГБУ «Научно-исследовательский институт пульмонологии» ФМБА России, до цент кафедры госпитальной терапии Института материнства и детства ФГАОУ ВО «Российский национальный исследовательский медицинский университет им. Н.И. Пирогова» Минздрава России
Бостанова Алина Магомедовна, врач анестезиолог-реаниматолог ФГБУ «Научно-исследовательский институт пульмонологии» ФМБА России
Теги: компьютерная томография
234567 Начало активности (дата): 11.05.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: артериовенозная мальформация; компьютерная томография; патологическая анатомия; клинический случай
12354567899
Похожие статьи
Компьютерная томография и магнитно-резонансная томография в диагностике острого нарушения мозгового кровообращения у детейРентген на дому 8 495 22 555 6 8
Мультиспиральная компьютерная томография (МСКТ)в оценке качества кости у больных врожденным ложным суставом голени
Магнитно-резонансная и рентгеновская компьютерная томография в диагностике повреждений костных элементов коленного сустава
Компьютерная томография: история создания и современное состояние



