 01.05.2026
01.05.2026
Применение обогащенной тромбоцитами плазмы при возмещении дефектов костной ткани керамическими имплантами
ВВЕДЕНИЕ
Возмещение дефектов кости является одной из ключевых задач современной травматологии и ортопедии. С каждым годом отмечается рост числа травм, дегенеративных заболеваний и онкологических патологий, связанных с костной тканью, которые требуют оперативного лечения, а в ряде случаев — возмещения полученных дефектов. Количество хирургических вмешательств при внутрисуставных и многооскольчатых переломах с костными дефектами растет с каждым годом [1, 2, 3].
Для замещения дефектов используют различные остеопластические материалы. «Золотым стандартом» признают аутотрансплантат, однако его применение сопряжено с возможными осложнениями, как в донорском участке, так и в месте замещения дефекта [4]. Использование алло- и ксенотрансплантатов также имеет существенные недостатки [5].
Дефицит натуральных источников на фоне роста потребности в имплантатах стимулировал поиск и разработку искусственных материалов для остеопластики.
Одним из перспективных направлений в возмещении дефектов кости является применение керамических материалов. Широкий спектр свойств биокерамики и хорошая совместимость с тканями человека делает этот материал потенциально приемлемым для решения большого круга проблем травматологии и ортопедии [6]. Важное место занимает биокерамика на основе стабилизированного иттрием диоксида циркония. Этот материал демонстрирует исключительные механические свойства и биосовместимость, не вызывает цитотоксических эффектов или аллергических реакций в окружающих тканях [7, 8].
Цель работы — определить эффективность применения обогащенной тромбоцитами плазмы при возмещении дефектов костной ткани керамическими имплантатами из диоксида циркония, допированного оксидом иттрия.
В силу своих физико-химических свойств биокерамика, применяемая для костной пластики, обладает, главным образом, остеокондуктивными свойствами [9]. С целью улучшения свойств остеопластических материалов и повышения их регенераторного потенциала используют различные ортобиологичские препараты [10]. Особое внимание в последние годы уделяется тромбоцитарным биопрепаратам [11]. Отмечено, что применение обогащенной тромбоцитами плазмы (PRP, англ.: platelet rich plasma) не только улучшает пролиферацию мезенхимальных стволовых клеток [12], но и способствует их остеогенной дифференцировке [13]. Исследования показывают, что применение PRP в комбинации с керамическими или композитными имплантатами может способствовать остеоиндукции [14] и значительно улучшать исходы лечения [15]. Результаты комбинированного применения PRP-терапии с костнопластическими материалами признаются многообещающими [16]. Вместе с тем отмечено, что, несмотря на дополнительные преимущества сочетания керамических остеозамещающих материалов с тромбо- цитарными ортобиологическими продуктами, необходимы дальнейшие экспериментальные и клинические исследования.
МАТЕРИАЛЫ И МЕТОДЫ
Лабораторные животные
В качестве экспериментальных животных выбраны самцы кроликов породы шиншилла, которых содержали на базе вивария Уральского государственного медицинского университета при температуре 23-25 °C, цикле освещения 12 ч день/ночь, с доступом к еде и воде ad libitum. Все эксперименты проводили в соответствии с «Правилами надлежащей лабораторной практики» (приказ МЗ РФ № 199н от 01.04.2016г.), Межгосударственными стандартами (ГоСт 33215-2014, ГОСТ 33216-2014 «Руководство по содержанию и уходу за лабораторными животными»), Европейской конвенцией о защите позвоночных животных, используемых в экспериментах и в других научных целях (ETS № 123, Страсбург, 18 марта 1986 г. c приложением от 15.06.2006). Исследования одобрены локальным этическим комитетом ФГБОУ ВО УГМУ Минздрава России (протокол № 4 от 26.05.23).
Все кролики разделены на две группы: в группу 1 (п = 10) включены животные, которым билатерально в бедренных костях моделировали метафизарные костные дефекты с имплантацией керамических аугментов; в группу 2 (п = 10) вошли животные, которым также билатерально в бедренных костях моделировали метафизарные костные дефекты, но имплантацию керамических аугментов не проводили. Кроликам обеих групп в костный дефект на правом бедре вводили PRP, в дефект на левом бедре PRP не вводили.
Хирургическое моделирование костного дефекта в области дистального метафиза бедренной кости
Для создания модели костного дефекта экспериментальное животное укладывали на бок, заднюю конечность обрабатывали растворами антисептиков, операционное поле обкладывали стерильным хирургическим бельем.
Выполняли продольный кожный разрез длиной 1 см по латеральной поверхности нижней трети бедра в проекции бедренной кости. Мягкие ткани по ходу доступа отсепаровы- вали тупым способом. Спицей Киршнера диаметром 2,0 мм формировали костный дефект в области дистального метафиза бедренной кости параллельно суставной поверхности коленного сустава. Моделирование костного дефекта производили билатерально. На правой конечности в костный дефект вводили PRP, на левой конечности в костный дефект PRP не вводили.
В группе 1 в костные дефекты обоих бедер имплантировали керамические аугменты (размер 0,15 х 0,15 х 1 см). В группе 2 в костные дефекты обоих бедер аугменты из керамики не имплантировали.
Рану ушивали послойно, кожные покровы обрабатывали антисептиком, накладывали асептическую повязку. В каждой из групп пять животных выводили из эксперимента через четыре недели после операции, пять животных — через восемь недель после операции.
Материал для аугментации костных дефектов
Образцы биокерамики, представленной диоксидом циркония (ZrO2), допированным оксидом иттрия (Y2O3 5 масс %), получены в Институте высокотемпературной электрохимии Уральского отделения Российской академии наук. Материал — с закрытым типом пористости, объемная доля пор — около 15 %. Поры — размером от 1-2 до 30 мкм, сложной формы. Керамические имплантаты имели размер 0,15 х 0,15 х 1 см (рис. 1).

Приготовление плазмы, сыворотки, PRP
Процедуру отбора крови у животных обеих групп проводили перед операцией и при выводе из эксперимента через четыре и восемь недель после операции.
Отбор крови осуществляли из краевой вены уха кроликов:
в пробирки с ЭДТА-К2 (этилендиаминтетраацетет калия) для определения гематологических параметров;
в пробирки без антикоагулянта для получения сыворотки, которую далее замораживали и хранили при температуре -80 °С до проведения иммуноферментного анализа (ИФА);
в пробирки с 3,2 % цитратом натрия в соотношении 9:1.
Для получения PRP кровь с цитратом натрия центрифугировали в течение 7 мин. при скорости 1500 об/мин. Полученную плазму оттягивали стерильным инсулиновым шприцем, 200 мкл помещали в пробирку Эппендорфа для определения количества тромбоцитов на гематологическом анализаторе Cell-70 (Biocode- Hygel, France) и последующего замораживания, остальную PRP (1 мл) вводили в место сформированного метафизарного дефекта правого бедра.
Лабораторные исследования
Лабораторные исследования проводили на базе ЦНИЛ ФГБОУ ВО УГМУ. Основные показатели крови определяли на автоматическом гематологическом анализаторе Cell-70 (Biocode-Hygel, France). Тромбоцитарный фактор роста (PDGF subunit A, rabbit) после процедуры замораживания-оттаивания PRP определяли с использованием наборов для ИФА (Cloud-Clone Corp., Китай). Также методом ИФА определяли С-реактивный белок (CRP, rabbit, Cloud-Clone Corp), остеокальцин (Osteocalcin, rabbit, Cloud-Clone Corp). Для выполнения анализа применяли комплекс, включающий планшетный иммуноферментный анализатор Termo Scirntific Multiskan GO (Япония); вошер Thermo Scientific Wellwash (Япония), шейкер-термостат Elmi ST-3L (Латвия).
Гистологическое исследование
После вывода животного из эксперимента забирали образец костной ткани в области дистального метафиза бедра в виде блока, фиксировали путем погружения в 10 % забуференный формальдегид при комнатной температуре в течение минимум семи дней. После фиксации образцы декальцини- ровали в течение 48 часов в растворе соляной (11,5 ± 0,5 %) и муравьиной (5,8 ± 0,3 %) кислот, который заменяли каждые 24 часа.
Декальцинированные образцы разрезали в области костного дефекта с формированием пластин толщиной от 2 до 4 мм. Полученные пластины обезвоживали в этаноле восходящей крепости и заливали в парафин с формированием блоков, после чего изготавливали срезы парафиновых блоков толщиной от 3 до 4 мкм, материал окрашивали гематоксилином и эозином. Керамические имплантаты извлекали при вырезке образцов для гистологического исследования после проведения декальцинации. Гистологические срезы готовили с использованием механического ротационного микротома CUT 4062. Гистологическое и морфометрическое исследования осуществляли при помощи микроскопа Olympus CX-31, камеры Olympus DP27. Выполняли оценку степени фиброза, наличия и выраженности костно-хрящевой мозоли, регенерирующих костных балок, определяли наличие воспалительного инфильтрата.
Статистическая обработка данных
Применяли методы вариационной статистики, использовали программу Statistica 10. Для сравнения исследуемых групп использовали критерий Манна - Уитни. Уровень р < 0,05 принимали статистически значимым. Данные представлены как медиана [интерквартильный размах].
РЕЗУЛЬТАТЫ
Для оценки влияния вводимого керамического материала на общее состояние организма экспериментальных животных проводили определение общих гематологических параметров в динамике (до и после операции).
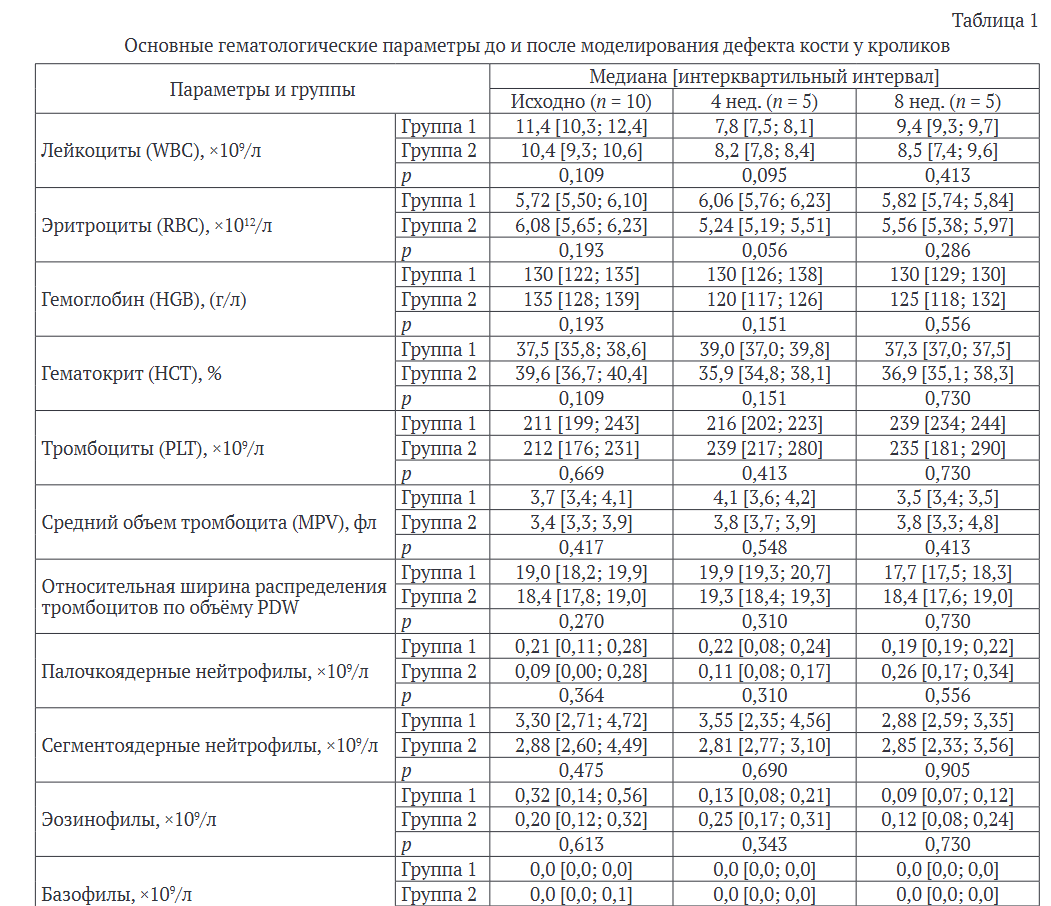
Общий анализ крови (табл. 1) не выявил существенных различий по основным показателям лейкоцитов, эритроцитов и тромбоцитов между группами 1 и 2 ни до операции, ни в послеоперационном периоде.
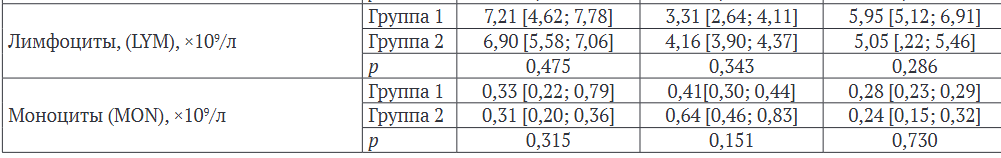
При анализе уровня маркера воспаления С-реактивного белка на дооперационном этапе существенных различий между группами не обнаружили (рис. 2). Однако через четыре недели после операции у животных в группе 1 уровень СРБ был существенно выше, чем в группе 2, что могло быть связано
Теоретические и экспериментальные исследования как с реакцией организма на введение имплантата, так и с техникой выполнения имплантации. Спустя восемь недель после операции различий в уровне маркера воспаления между группами не выявлено.
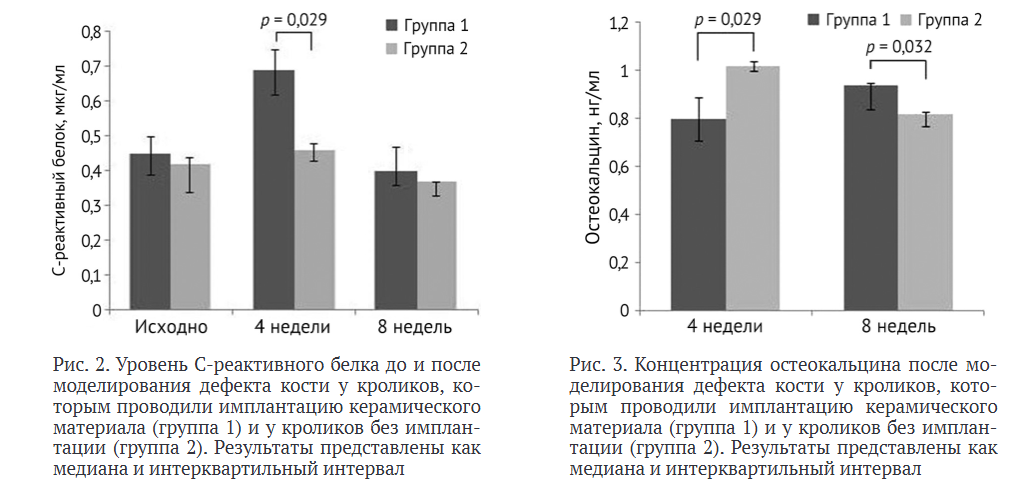
Концентрация маркера остеогенеза остеокальцина через четыре недели после операции была существенно выше в группе 2. Однако через восемь недель значительно более высокий уровень остеокальцина наблюдали в группе 1 (рис. 3). Полученные данные свидетельствуют об изменении динамики остеогенеза у животных, которым проводили имплантацию керамического аугмента в сравнении с животными контрольной группы.
Исходно 4 недели 8 недель
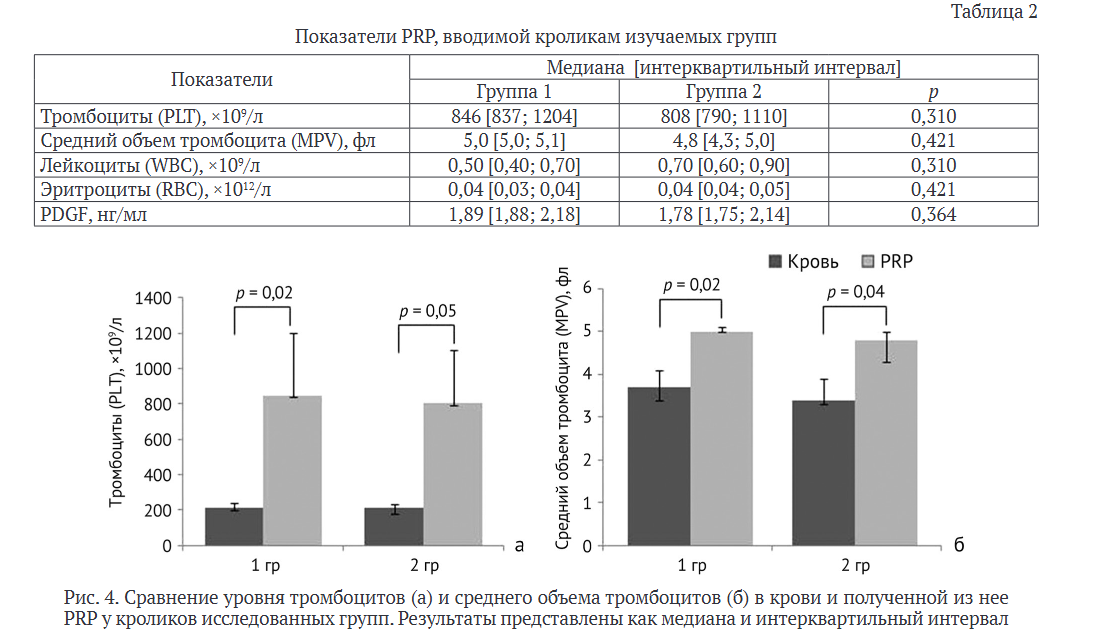
Полученная PRP была охарактеризована с использованием таких параметров как концентрация тромбоцитов, лейкоцитов и эритроцитов (табл. 2). Относительное количество лейкоцитов не превышало 5-8 %, эритроцитов — 1 % от исходного уровня данных клеток в крови. Концентрация PDGF, одного из факторов роста, выделяемых при активации тромбоцитами, также не имела существенных различий между группами 1 и 2. Относительно исходного уровня в крови количество тромбоцитов в PRP было увеличено в четыре раза, средний объем тромбоцитов — в 1,4 раза (рис. 4).
Для оценки влияния PRP на динамику остеогенеза при хирургическом моделировании костного дефекта в области дистального метафиза бедренной кости кроликов проведен сравнительный анализ гистологического строения тканей в области моделирования дефекта кости.
Гистологический анализ показал, что через четыре недели после операции у животных группы 2 (без имплантации) при моделировании дефекта без введения PRP в микропрепаратах встречались крупные фокусы фиброза (рис. 5, а), а также фокусы незавершенного вторичного остеогенеза (рис. 5, б). В случае применения PRP обнаруживали регенерирующие костные балки, что свидетельствовало о более эффективной регенерации при введении тромбоцитарного продукта (рис. 5, в).
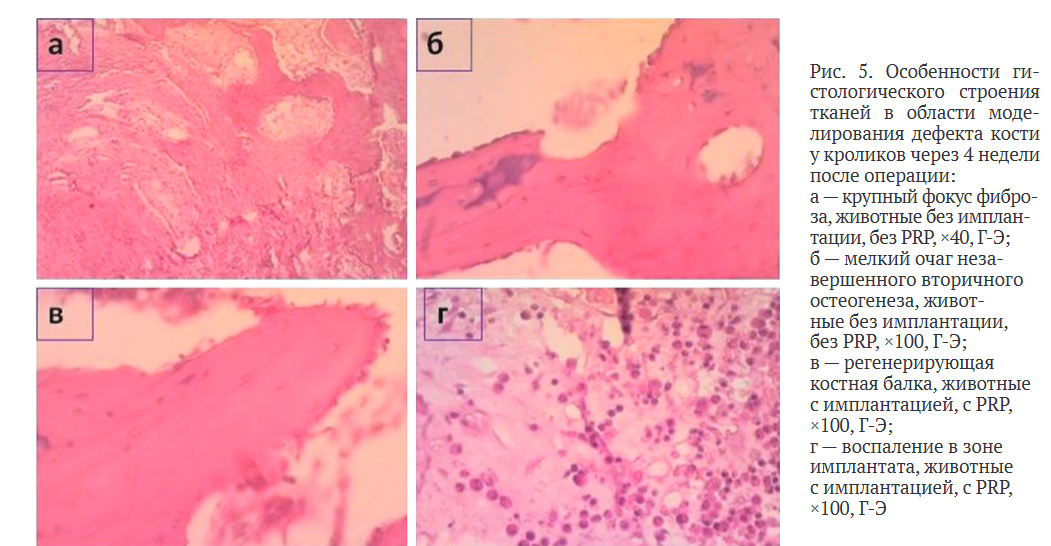
В группе 1 (с имплантацией керамического материала) также наблюдали более активный репарационный процесс при введении в зону дефекта PRP, однако в отличие от группы 2 и вне зависимости от применения PRP в периимплантной зоне обнаруживали воспалительный процесс (рис. 5, г). Выявленное воспаление может быть связано как с реакцией на введение имплантата, так и с техникой выполнения имплантации.
Через восемь недель после операции без введения PRP в микропрепаратах костной ткани животных обеих групп сохранялись признаки незавершенной репаративной регенерации костной ткани в виде вторичного (энхондрального) остеогенеза и участков фиброза. Вместе с тем применение PRP способствовало более эффективной репаративной регенерации как в группе, где не проводили аугментацию костного дефекта, так и в группе, где применяли имплантат. В обеих группах выявлены регенерирующие костные балки. В таблице 3 приведены результаты сравнения в отношении применения PRP в группах 1 и 2.
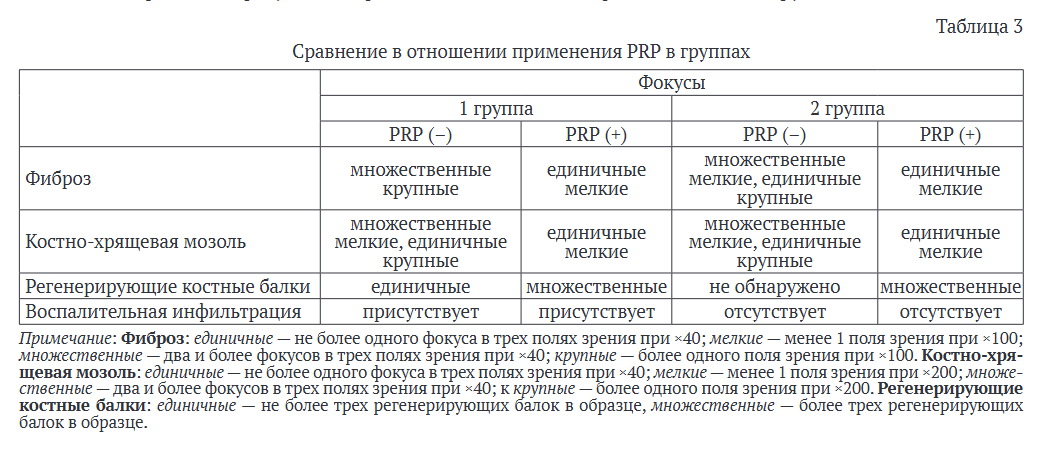
Таким образом, применение PRP увеличивало количество регенерирующих костных балок как в группе 1, так и в группе 2. Использование тромбоцитарного продукта приводило также к снижению количества и размера фокусов фиброза и костно-хрящевой мозоли в обеих группах. Наличие признаков воспаления в гистологических образцах, по-видимому, связано с реакцией организма на введение искусственного имплантата, не исключено также влияние техники выполнения имплантации. Вместе с тем необходимо отметить, что к восьмой послеоперационной неделе уровень биохимического маркера воспаления С-реактивного белка в группе животных, которым проводили имплантацию, не имел существенных различий с группой животных, которым имплантацию не проводили.
ОБСУЖДЕНИЕ
Стремление к поиску оптимальных стратегий лечения пациентов с костной травмой привело к изучению возможности использования PRP для ускорения заживления переломов [17], поскольку обогащенная тромбоцитами плазма является экономически эффективным аутологичным препаратом, содержащими широкий спектр факторов роста, цитокинов, молекул адгезии [18].
Введение PRP непосредственно в травмированный участок обеспечивает высокую концентрацию факторов роста непосредственно в месте повреждения, что способствует восстановлению тканей, уменьшению воспаления, ускорению регенеративного процесса [19]. Использование обогащенной тромбоцитами плазмы при хирургических процедурах может сочетаться с использованием костных трансплантатов, этот подход направлен на оптимизацию интеграции остеозамещающих материалов и повышение эффективности репаративной регенерации [19]. В настоящее время эффективность и безопасность PRP продемонстрирована в большом числе медицинских исследований [20]. Тем не менее, регенеративные эффекты PRP при использовании искусственных, в частности керамических, имплантатов до сих пор полностью не выяснены [21].
Известно, что эффективность использования PRP зависит от состояния здоровья донора [22]. Отражением общего состояния организма может служить клинический анализ крови. Наше исследование показало, что введение имплантатов из диоксида циркония включенным в исследование животным не оказывало существенного влияния на показатели эритроцитов, лейкоцитов и тромбоцитов в динамике послеоперационного периода.
Биокерамика на основе диоксида циркония, стабилизированного иттрием, кроме исключительных механических свойств демонстрирует также биосовместимость, не вызывает цитотоксических эффектов или аллергических реакций в окружающих тканях [23, 24]. В нашем исследовании при высокочувствительном анализе концентрации С-реактивного белка обнаружено, что введение кроликам имплантата повышало уровень данного маркера воспаления относительно животных, которым имплантацию не проводили. Однако, учитывая, что к концу срока наблюдения различий в уровне С-реактивного белка между группами выявлено не было, можно заключить, что данная реакция была связана не с физико-химическими свойствами керамического материала, а с ответом организма на введение имплантата и техникой выполнения хирургического вмешательства.
Ранее нами было показано, что темп пролиферации фибробластов человека в присутствии образцов биокерамики замедлен по сравнению с контролем на начальных этапах роста культуры клеток [25]. В настоящем исследовании для оценки остеогенеза мы использовали остеокальцин, высвобождающийся остеобластами в процессе остеосинтеза и используемый в качестве информативного маркера формирования кости [26]. Мы обнаружили, что введение имплантата несколько замедляет процесс остеогенеза в раннем периоде после операции, что можно объяснить процессами адаптации на введение искусственного остеозамещающего материала.
Полученная в настоящем исследовании PRP была охарактеризована с точки зрения клеточного состава, а также концентрации тромбоцитарного фактора роста, выделяемого при активации из альфа-гранул. Количество тромбоцитов является одним из основных параметров, рутинно оцениваемых при приготовлении PRP, поскольку считается, что он имеет связь с концентрацией биологически активных компонентов в тромбоцитарном продукте. Хотя в настоящее время не поддерживается четкая корреляция между количеством тромбоцитов в PRP и клиническим ответом [27], рекомендуемое количество тромбоцитов в PRP колеблется от 800 х 109 до 1200 * 109/л [21, 28]. В нашей работе количество тромбоцитов в PRP в обеих группах соответствовало данным рекомендациям.
Недавние исследования показали, что средний объем тромбоцитов может быть полезным параметром, — более высокий уровень MPV указывает на более высокую концентрацию биологически активных молекул [29]. Мы обнаружили, что MPV в полученной нами PRP был существенно выше, чем MPV в цельной крови кроликов. Возможно, это связано с техникой приготовления плазмы. Данную особенность мы наблюдали в обеих группах исследованных животных.
Лейкоциты выполняют многочисленные биологические функции, которые, как правило, способствуют воспалению и инициируют его. Уровень лейкоцитов необходимо определять и упоминать при описании получения PRP [30]. Польза от включения лейкоцитов в PRP является спорной, однако высвобождение лейкоцитами полезных цитокинов считается положительным фактором, особенно в случаях, когда необходим первоначальный провоспалительный процесс [31]. В то же время присутствие эритроцитов в PRP считается нежелательным [32]. В нашем исследовании в PRP сохранялось небольшое количество лейкоцитов (4-7 % от исходного уровня), остаточное количество эритроцитов не превышало 1 % от их исходного содержания в крови.
Альфа-гранулы тромбоцитов при активации высвобождают множество факторов роста, включая тромбоцитарный фактор роста (PDGF), фактор роста эндотелия сосудов (VEGF), фактор роста фибробластов (FGF), эпидермальный фактор роста (EGF) и инсулиноподобные факторы роста (IGF-1 и IGF-2). Эти факторы управляют основными биологическими процессами, включая индукцию ангиогенеза, разрешение воспаления и регенерацию тканей [33]. Уровень ростовых факторов в PRP и, соответственно, её качество можно определять после процедуры замораживания-оттаивания [34]. Мы применили данный метод с последующим определением PDGF, — уровень тромбоцитарного фактора роста имел близкие значения в PRP изучаемых групп. В работе S. Pulcini et al. обнаружена прямая корреляция количества тромбоцитов с изоформой PDGF-AA, но не с изоформами -BB и -AB. Мы не выявили корреляцию между количеством тромбоцитов и PDGF [21]. Это можно объяснить тем, что мы проводили определение субъединицы А, которая присутствует и в изоформе PDGF-AA, и в изоформе PDGF-AB.
Применение PRP для улучшения регенерации костной ткани при восстановлении костного дефекта разнообразно. В частности, использование аутологичной PRP является простым и эффективным способом обеспечения остеоиндукции и улучшения регенерации кости при применении костного трансплантата и тканеинженерных реконструкций кости [35, 36].
Наше исследование было направлено на изучение того, усиливает ли обогащенная тромбоцитами плазма остеогенный потенциал керамических имплантатов из диоксида циркония при возмещении дефектов костной ткани. Гистологическую оценку эффективности использования PRP для коррекции остеогенеза при хирургическом моделировании костного дефекта в области дистального ме- тафиза бедренной кости кроликов проводили через четыре и восемь недель после операции. Ранее D. Saginova et al. показали, что комплекс PRP-костный трансплантат улучшает восстановление костной ткани в костном дефекте на начальных этапах регенерации кости [37]. B. Okta§ et al. также обнаружили, что применение PRP может играть роль в ускорении заживления переломов и уменьшении несращения на очень ранних сроках при восстановлении костных дефектов [38]. Наши данные согласуются с этими исследованиями, мы также показали, что через четыре недели после имплантации керамического материала более активный репарационный процесс наблюдается при введении в зону дефекта PRP. В более отдаленном периоде, спустя восемь недель после операции, мы обнаружили, что применение PRP не только увеличивает количество регенерирующих костных балок, но и снижает количество и размер фокусов фиброза и костно-хрящевой мозоли.
Известно, что концентраты тромбоцитов обладают способностью контролировать воспалительную среду благодаря своим противовоспалительным свойствам [39]. В нашем исследовании при анализе гистологических образцов, тем не менее, не обнаружено выраженного снижения воспалительной инфильтрации в периимплантной ткани в условиях введения PRP.
Обогащенная тромбоцитами плазма — полезный вспомогательный инструмент в контексте репаративной регенерации костной ткани, учитывая преимущества, которые включают в себя стимуляцию клеточных реакций, ускоренное восстановление тканей и потенциальную ускоренную реабилитацию. Вместе с тем для интеграции методов, использующих PRP, в доказательную медицинскую практику, необходимы дальнейшие тщательные клинические исследования, которые позволят углубить понимание места PRP в области регенеративной медицины и будут способствовать эффективному лечению пациентов с травмой и заболеваниями опорно-двигательного аппарата.
ЗАКЛЮЧЕНИЕ
Применение обогащенной тромбоцитами плазмы эффективно при возмещении дефектов костной ткани с использованием керамических имплантатов из диоксида циркония, допированного оксидом иттрия.
СПИСОК ИСТОЧНИКОВ
Global status report on road safety 2018. Geneva: World Health Organization; 2018.
Schade AT, Mbowuwa F, Chidothi P, et al. Epidemiology of fractures and their treatment in Malawi: Results of a multicentre prospective registry study to guide orthopaedic care planning. PLoS One. 2021;16(8):e0255052. doi: 10.1371/journal.pone.0255052.
Файн А.М., Ваза А.Ю., Гнетецкий С.Ф. и др. Доступные способы повышения регенераторного потенциала пластического материала в неотложной травматологии. Часть 1. Использование аутологичной богатой тромбоцитами плазмы крови. Трансплантология. 2022;14(1):79-97. doi: 10.23873/2074-0506-2022-14-1-79-97.
Parikh SN. Bone graft substitutes: past, present, future. J Postgrad Med. 2002;48(2):142-148.
Oryan A, Alidadi S, Moshiri A, Maffulli N. Bone regenerative medicine: classic options, novel strategies, and future directions. JOrthop SurgRes. 2014;9(1):18. doi: 10.1186/1749-799X-9-18.
Vaiani L, Boccaccio A, Uva AE, et al. Ceramic Materials for Biomedical Applications: An Overview on Properties and Fabrication Processes. JFunctBiomater. 2023;14(3):146. doi: 10.3390/jfb14030146.
Gahlert M, Roehling S, Sprecher CM, et al. In vivo performance of zirconia and titanium implants: a histomorphometric study in mini pig maxillae. Clin Oral Implants Res. 2012;23(3):281-286. doi: 10.nn/j.1600-0501.2011.02157.x.
Han JM, Hong G, Lin H, et al. Biomechanical and histological evaluation of the osseointegration capacity of two types of zirconia implant. Int J Nanomedicine. 2016;11:6507-6516. doi: 10.2147/IJN.S119519.
Кирилова И.А., Садовой М.А., Подорожная В.Т. Сравнительная характеристика материалов для костной пластики: состав и свойства. Хирургия позвоночника. 2012;(3):72-83. doi: 10.14531/ss2012.3.72-83.
Bin Shahri N, Chong AKS, Karjalainen T. The role of orthobiologics in bone healing and joint and tendon degeneration in the upper limb. J Hand Surg Eur Vol. 2025;50(6):728-737. doi: 10.1177/17531934251327034.
Khandan-Nasab N, Torkamanzadeh B, Abbasi B, et al. Application of Platelet-Rich Plasma-Based Scaffolds in Soft and Hard Tissue Regeneration. Tissue Eng Part B Rev. 2025. doi: 10.1089/ten.teb.2024.0285.
Mishra A, Tummala P, King A, et al. Buffered platelet-rich plasma enhances mesenchymal stem cell proliferation and chondrogenic differentiation. Tissue Eng Part C Methods. 2009;15(3):431-435. doi: 10.1089/ten.tec.2008.0534.
Becerra-Bayona SM, Solarte VA, Alviar Rueda JD, et al. Effect of biomolecules derived from human platelet-rich plasma on the ex vivo expansion of human adipose-derived mesenchymal stem cells for clinical applications. Biologicals. 2022;75:37-48. doi: 10.1016/j. biologicals.2021.11.001.
Teotia AK, Oayoom I, Kumar A. Endogenous Platelet-Rich Plasma Supplements/Augments Growth Factors Delivered via Porous Collagen-Nanohydroxyapatite Bone Substitute for Enhanced Bone Formation. ACS Biomater Sci Eng. 2019;5(1):56-69. doi: 10.1021/ acsbiomaterials.8b00227.
Lyu J, Ma T, Huang X, et al. Core decompression with p-tri-calcium phosphate grafts in combination with platelet-rich plasma for the treatment of avascular necrosis of femoral head. BMCMusculoskelet Disord. 2023;24(1):40. doi: 10.1186/s12891-022-06120-z.
Борзунов Д.Ю., Гильманов Р.Т. Перспективные костно-пластические материалы и хирургические технологии при реконструктивно-восстановительном лечении больных с псевдоартрозами и дефектами костной ткани. Гений ортопедии. 2024;30(2):263- 272. doi: 10.18019/1028-4427-2024-30-2-263-272.
Kale P, Shrivastava S, Balusani P, Pundkar A. Therapeutic Potential of Platelet-Rich Plasma in Fracture Healing: A Comprehensive Review. Cureus. 2024;16(6):e62271. doi: 10.7759/cureus.62271.
Zhang N, Wu YP, Oian SJ, et al. Research progress in the mechanism of effect of PRP in bone deficiency healing. ScientificWorldJournal. 2013;2013:134582. doi: 10.1155/2013/134582.
Bacevich BM, Smith RDJ, Reihl AM, et al. Advances with Platelet-Rich Plasma for Bone Healing. Biologics. 2024;18:29-1859. doi: 10.2147/BTT.S290341
Gupta S, Paliczak A, Delgado D. Evidence-based indications of platelet-rich plasma therapy. Expert Rev Hematol. 2021;14(1):97-108. doi: 10.1080/17474086.2021.1860002.
Pulcini S, Merolle L, Marraccini C, et al. Apheresis Platelet Rich-Plasma for Regenerative Medicine: An In Vitro Study on Osteogenic Potential. Int J Mol Sci. 2021;22(16):8764. doi: 10.3390/ijms22168764.
O'Donnell C, Migliore E, Grandi FC, et al. Platelet-Rich Plasma (PRP) From Older Males With Knee Osteoarthritis Depresses Chondrocyte Metabolism and Upregulates Inflammation. J Orthop Res. 2019;37(8):1760-1770. doi: 10.1002/jor.24322
Yin L, Nakanishi Y, Alao AR, et al. A review of engineered zirconia surfaces in biomedical applications. Procedia CIRP. 2017;65:284- 290. doi: 10.1016/j.procir.2017.04.057
Ульянов Ю.А., Зарипова Э.М., Мингазова Э.Н. К вопросу о биосовместимости керамических имплантатов при оказании ортопедической помощи. Менеджер здравоохранения. 2023;(9):18-22. doi: 10.21045/1811-0185-2023-9-18-22.
Ulitko M, Antonets Y, Antropova I, et al. Ceramic materials based on lanthanum zirconate for the bone augmentation purposes: cytocompatibility in a cell culture model. Chimica Techno Acta. 2023;10(4):202310402. doi: 10.15826/chimtech.2023.10.4.02.
Дружинина Т.В., Хлусов И.А., Карлов А.В., Ростовцев А.В. Маркеры остеогенеза в периферической крови как патогенетические факторы и предикторы системных эффектов имплантатов для остеосинтеза. Гений ортопедии. 2007;4:83-88.
Laver L, Filardo G, Sanchez M, et al. ESSKA-ORBIT Group. The use of injectable orthobiologics for knee osteoarthritis: A European ESSKA-ORBIT consensus. Part 1-Blood-derived products (platelet-rich plasma). Knee Surg Sports Traumatol Arthrosc. 2024;32(4):783- 797. doi: 10.1002/ksa.12077.
Aprili G, Gandini G, Guaschino R, et al. SIMTI Working Group. SIMTI recommendations on blood components for non-transfusional use. Blood Transfus. 2013;11(4):611-622. doi: 10.2450/2013.0118-13
Ozer K, Kankaya Y, ^olak O. An important and overlooked parameter in platelet rich plasma preparation: The mean platelet volume. JCosmetDermatol. 2019;18(2):474-482. doi: 10.1111/jocd.12682.
Ragni E, Taiana MM, Cengic T, et al. PRP or not PRP: Is the debate surrounding platelets-based blood-derived products evolving? Knee Surg Sports Traumatol Arthrosc. 2025;33(5):1920-1924. doi: 10.1002/ksa.12655.
Tischer T, Bode G, Buhs M, et al. Platelet-rich plasma (PRP) as therapy for cartilage, tendon and muscle damage - German working group position statement. J Exp Orthop. 2020;7(1):64. doi: 10.1186/s40634-020-00282-2.
Zhou JY, Wong JH, Berman ZT, et al. Bleeding with iron deposition and vascular remodelling in subchondral cysts: A newly discovered feature unique to haemophilic arthropathy. Haemophilia. 2021;27(6):e730-e738. doi: 10.1111/hae.14417.
Kale P, Shrivastava S, Balusani P, Pundkar A. Therapeutic Potential of Platelet-Rich Plasma in Fracture Healing: A Comprehensive Review. Cureus. 2024;16(6):e62271. doi: 10.7759/cureus.62271.
Tang S, Wang L, Zhang Y, Zhang F. A Biomimetic Platelet-Rich Plasma-Based Interpenetrating Network Printable Hydrogel for Bone Regeneration. FrontBioengBiotechnol. 2022;10:887454. doi: 10.3389/fbioe.2022.887454.
Корыткин А.А., Зыкин А.А., Захарова Д.В., Новикова Я.С. Применение обогащенной тромбоцитами плазмы при замещении очага аваскулярного некроза головки бедренной кости аллотрансплантатами. Травматология и ортопедия России. 2018;24(1):115-122. doi: 10.21823/2311-2905-2018-24-1-115-122
Guo Y, Yang Y, Peng B, Xing G. Repair of Vertebral Bone Defects with Injectable Calcium Phosphate Bone Cement Reinforced with Autologous Platelet-rich Plasma in Goats. Tissue Eng Part C Methods. 2025;31(6):211-220. doi: 10.1089/ten.tec.2025.0021.
Saginova D, Tashmetov E, Tuleubaev B, Kamyshanskiy Y. Effect of autologous platelet-rich plasma on new bone formation and viability of a Marburg bone graft. Open Life Sci. 2023;18(1):20220761. doi: 10.1515/biol-2022-0761.
Okta§ B, ^lrpar M, §anli E, et al. The effect of the platelet-rich plasma on osteogenic potential of the periosteum in an animal bone defect model. JtDis Relat Surg. 2021;32(3):668-675. doi: 10.52312/jdrs.2021.199.
Salem M, Rizk A, Mosbah E, et al. Reinforcement of osteochondoral defects repair with leukocyte platelet-rich fibrin and bone marrow-derived mononuclear cells in a rabbit model. BMCMusculoskeletDisord. 2025;26(1):707. doi: 10.1186/s12891-025-08952-x.
Информация об авторах:
Ирина Петровна Антропова — доктор биологический наук, ведущий научный сотрудник
Елена Александровна Волокитина — доктор медицинских наук, профессор, заведующий кафедрой, ведущий научный сотрудник
Кирилл Андреевич Тимофеев — аспирант кафедры, врач — травматолог-ортопед
Роман Андреевич Труфаненко — ассистент кафедры
Сергей Михайлович Кутепов — член-корр. РАН, профессор, доктор медицинских наук, руководитель института травматологии ЦНИЛ
Лариса Георгиевна Полушина — кандидат медицинских наук, старший научный сотрудник
Теги: имплантат
234567 Описание для анонса:
234567 Начало активности (дата): 01.05.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: возмещение дефектов костной ткани, имплантат, циркониевая керамика, обогащенная тромбоцитами плазма, остеоинтеграция, эксперимент
12354567899
Похожие статьи
Роль рентгенологической навигации при трансапикальной имплантации митральных неохорд при значимой митральной регургитации на работающем сердцеРентген на дому 8 495 22 555 6 8
Применение индивидуального 3D -имплантата в сочетании с индуцированной мембраной при лечении огнестрельного диафизарного дефекта костей голени
Факторы риска нестабильности имплантатов после спондилэктомии у пациентов с опухолями позвоночника
Отдаленный результат лечения перелома заднего края вертлужной впадины с вывихом бедра после остеосинтеза и разгрузки сустава имплантируемым устройством



