 02.10.2025
02.10.2025
“Нелегкая” легкая бронхиальная астма
Бронхиальная астма (БА) представляет собой клиническую форму, которая контролируется объемом фармакологической терапии ступени 1 или 2, т.е. предпочтительные варианты лечения включают применение низких доз ингаляционного глюкокортикостероида (ИГКС) + формотерол по потребности или низких доз ИГКС ежедневно.
Введение
Бронхиальная астма (БА) - это гетерогенное хроническое респираторное заболевание, которое независимо от степени тяжести характеризуется воспалением дыхательных путей, наличием респираторных симптомов и вариабельной обструкции дыхательных путей [1]. У большинства пациентов (50-75%) заболевание характеризуется легким течением [2, 3]. Подавляющее количество проводимых исследований сосредоточено на изучении аспектов течения тяжелых форм БА из-за трудностей в достижении контролируемого состояния и высокого уровня смертности. Однако не следует игнорировать легкую форму БА, которая из-за не слишком яркой клинической картины сопровождается низким уровнем диагностики, неадекватным медикаментозным лечением. Наличие легких симптомов в повседневной жизни не обязательно указывает на то, что пациенты будут испытывать только легкие обострения заболевания. А длительное бессимптомное течение и нормальные показатели функции дыхания не гарантируют отсутствия риска тяжелых и опасных для жизни обострений [4-6]. Таким образом, легкая форма БА не обязательно является “легкой” для самого больного и его лечащего врача, и крайне важно улучшать понимание всех рисков и подобрать максимально эффективный вариант терапии.
Проблемы контроля легкой БА
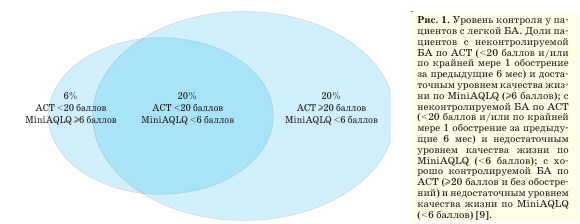
Глобальная инициатива по ведению БА (Global Initiative for Asthma, GINA) определяет легкую степень заболевания как клиническую форму, которая хорошо контролируется объемом фармакологической терапии на уровне ступени 1 или 2, т.е. предпочтительные варианты стратегии лечения включают применение низких доз ингаляционного глюкокортикостероида (ИГКС) + формотерол по потребности или низких доз ИГКС ежедневно с короткодействующими Р2-агонистами (КДБА) по потребности [1]. Необходимо помнить о том, что термин “легкая БА” далеко не всегда указывает на отсутствие у пациента симптомов и обострений, снижающих качество жизни. Легкая БА - это гетерогенное заболевание с широким спектром причин и проявлений, в основе которого лежит персистирующее эндобронхиальное воспаление. По данным эпидемиологических исследований, недооценка воспалительного процесса в бронхах приводит к тому, что об отсутствии контроля заболевания (по результатам теста по контролю БА (Asthma Control Test, ACT)) сообщают до 52,4% пациентов с интермиттирующей БА и до 42,3% пациентов с легкой персистирующей БА [7, 8]. При комбинированной оценке с использованием АСТ и мини-опросника по качеству жизни при БА (Mini Asthma Quality of Life Questionnaire, MiniAQLQ) у 298 пациентов в возрасте 18-75 лет с диагнозом БА легкой степени тяжести, не получавших регулярного лечения, недостаточно контролируемое состояние было зафиксировано у 46% участников исследования (рис. 1) [9].
Обострения, пусть и не столь частые, также являются характерной чертой легкой БА. По данным различных исследований, у 19-36% пациентов с легкой БА обострения, в том числе тяжелые (требующие приема системных глюкокортикостероидов (СГКС) в течение >3 дней или госпитализации), развиваются каждый год [8, 10-14].
Объем назначаемой противовоспалительной и бронхолитической терапии с учетом текущего клинического статуса и истории обострений является определяющим принципом медикаментозного лечения БА, позволяющим достигнуть контролируемого состояния. Однако далекий от оптимального уровень контроля БА в большинстве стран мира свидетельствует о том, что на пути к достижению главной цели необходимо не только учитывать фенотип заболевания, но и принимать во внимание множество других факторов, таких как влияние сопутствующих заболеваний, продолжающееся воздействие триггеров воспаления, низкий уровень приверженности пациента к назначенному лечению, неправильная техника ингаляции.
Клинические особенности неконтролируемой БА и мелкие дыхательные пути
Длительное изучение проблемы мелких дыхательных путей (МДП) у пациентов с различной бронхолегочной патологией (эмфиземой, БА, хронической обструктивной болезнью легких) позволило экспертам сделать вывод о том, что МДП имеют большую площадь поперечного сечения и вносят значительный вклад в увеличение бронхиального сопротивления даже при минимальной бронхиальной обструкции [15-18].
Дальнейшие исследования определили клиническую роль МДП в течении БА любой степени тяжести, включая легкую, поскольку именно дисфункция МДП может коррелировать со специфическими клиническими особенностями и более низким уровнем контроля заболевания (рис. 2).
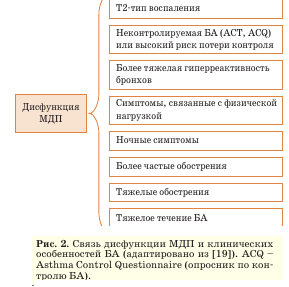
По данным, полученным с использованием различных методов исследования (спирометрия, бодиплетизмография, форсированная импульсная осциллометрия, тест вымывания азота, компьютерная томография, оценка оксида азота в выдыхаемом воздухе и др.), эксперты оценивают вовлеченность МДП у пациентов с БА на уровне не менее 50-60% [20-22]. При этом изменения в МДП происходят независимо от тяжести течения БА, как показано на основании результатов импульсной осциллометрии, проведенной в когорте из 400 пациентов, находившихся на различных ступенях терапии согласно GINA: патология МДП была выявлена у 58,3% пациентов на ступени 2, у 60,9% - на ступени 3, у 63,3% - на ступени 4 и у 78,6% - на Т2-тип воспаления ступени 5 [23]. В известном исследовании ATLANTIS с помощью различных доступных методов оценки было убедительно продемонстрировано, что МДП вовлечены в воспалительный процесс у 90,7% больных БА любой степени тяжести [24].
Возможности основных стратегий терапии легкой БА
Одной из наиболее устоявшихся стратегий терапии для большинства взрослых и подростков, страдающих легкой персистирующей БА, эксперты считают регулярное применение ИГКС в низких дозах в качестве поддерживающей терапии для уменьшения воспаления дыхательных путей, снижения симптомов и риска обострений [1, 25]. В качестве второй равноправной опции, особенно при нечастых клинических проявлениях, выступает использование фиксированных комбинаций быстродействующих Р2-агонистов (прежде всего формотерола) и ИГКС, принимаемых только при возникновении симптомов. Обоснование такого выбора учитывает необходимость супрессии воспаления в дыхательных путях, с одной стороны, и снижения потребности в КДБА, с другой стороны. Это представляется весьма важным, поскольку КДБА не влияют на воспалительный процесс и не защищают от обострений, напротив, более широкое применение КДБА связано с более высоким риском обострений [26, 27].
Во многом актуальные возможности терапии легкой БА определены результатами контролируемых исследований, подтвердивших эффективность основных терапевтических опций.
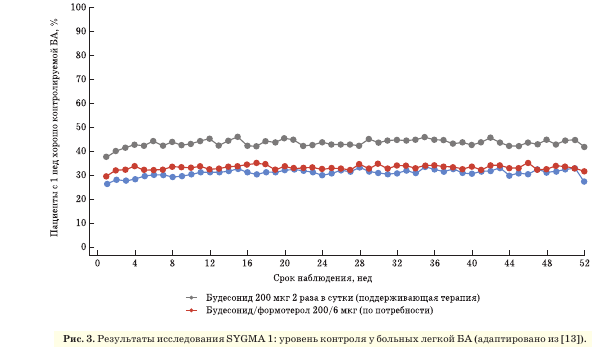
В исследовании III фазы SYGMA 1 длительностью 52 нед (популяция полного анализа составила 3836 пациентов) изучались эффективность и безопасность комбинации будесонид/формотерол (200/6 мкг) в режиме по потребности у пациентов с легкой БА в сравнении с регулярной терапией будесонидом (200 мкг 2 раза в сутки) и тер- буталином (0,5 мг) по потребности или с монотерапией тербуталином (0,5 мг) по потребности. Первичные конечные точки включали контроль симптомов БА и частоту среднетяжелых и тяжелых обострений в течение 1 года [13]. Будесо- нид/формотерол в режиме по потребности показал превосходство над тербуталином по потребности по доле недель с хорошим контролем симптомов БА в среднем на 1 пациента (34,4 против 31,1%; отношение шансов 0,64; 95% доверительный интервал (ДИ) 0,57-0,73), но уступал регулярной терапии будесонидом (44,4%) (рис. 3). Частота среднетяжелых (ухудшение симптомов, потребовавшее дополнительного назначения будесонида 200 мкг 2 раза в сутки с целью предотвращения тяжелого обострения) и тяжелых (ухудшение симптомов, потребовавшее приема СГКС >3 сут и/или госпитализации) обострений в группе будесонида/формотерола оказалась ниже, чем в группе тербуталина, и сопоставима с таковой в группе регулярной терапии будесонидом (отношение рисков 0,90; 95% ДИ 0,65-1,24) (рис. 4).
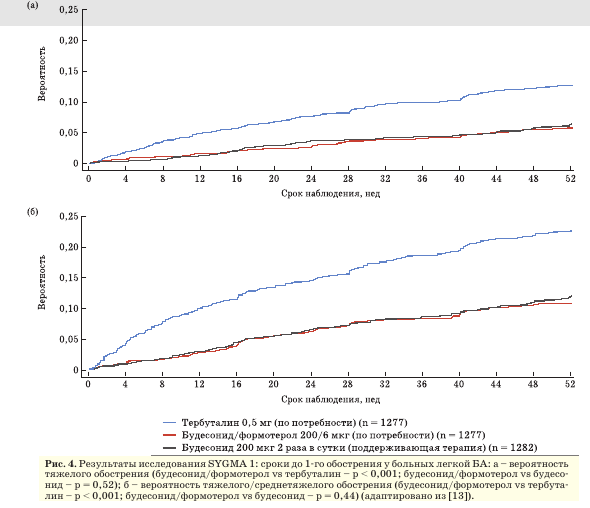
Таким образом, каждый из предлагаемых актуальными клиническими рекомендациями вариантов терапии способен решить основные задачи ведения пациентов с легкой БА. Какие же факторы будут решающими при выборе режима приема ИГКС-содержащих препаратов для достижения оптимального контроля заболевания? В этой связи интересными представляются результаты исследования, проведенного по так называемому модифицированному дельфийскому методу [28]. Метод заключается в поэтапном (3 опроса и виртуальный научный семинар) и анонимном сборе независимых экспертных мнений и выработке консенсуса по поставленной проблеме. Для участия во всех этапах процесса были приглашены 20 экспертов в области респираторной медицины, обладающих знаниями и опытом ведения пациентов с БА, представляющих 10 стран (Аргентина, Индонезия, Япония, Мексика, Малайзия, Филиппины, Испания, Таиланд, Турция и Вьетнам). На 1-м этапе эксперты утвердили и ранжировали наиболее важные факторы, определяющие выбор метода лечения БА легкой степени тяжести.
Для оценки преимуществ и недостатков ежедневного применения ИГКС по сравнению с комбинацией ИГКС/формотерол, назначаемой по потребности, наибольшим весом, по мнению экспертов, обладают доказательства эффективности (с этим согласились 100% участников), особенности статуса пациента (психологические и социальные), данные о безопасности терапии, предпочтения пациента, международные и локальные рекомендации по лечению БА (рис. 5).
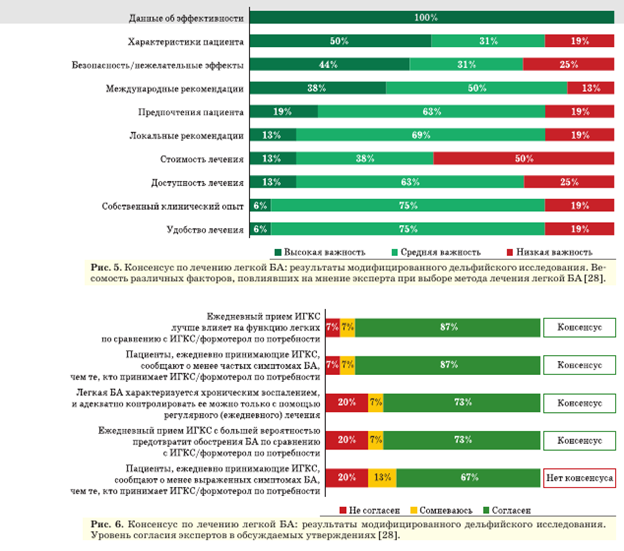
После проведения научного семинара и завершения 2-го опроса был сделан ряд согласованных заявлений: 87% экспертов согласились с тем, что ежедневная поддерживающая терапия ИГКС эффективнее улучшает функцию легких и снижает частоту симптомов; 73% экспертов согласились с тем, что хроническое воспаление при легкой БА надежнее контролировать с помощью регулярного приема ИГКС; 73% экспертов согласились с тем, что ежедневный прием ИГКС с большей вероятностью предотвратит обострения по сравнению с режимом по потребности (рис. 6).
Участники исследования пришли к единому мнению (80% были согласны частично или полностью), что они как правило или всегда рекомендовали бы регулярный прием ИГКС пациентам с легкой БА. При этом основным недостатком такого режима они назвали недостаточную приверженность лечению (56%), а основными преимуществами симптоматического применения комбинации ИГКС/формотерол - удобство (25%) и более высокую приверженность лечению (25%). Эксперты частично или полностью согласились с тем, что при всех режимах может наблюдаться низкая приверженность лечению (87%), что пациенты с меньшей вероятностью будут придерживаться лечения, если они чувствуют себя хорошо (100% согласие) или если препарат необходимо применять каждый день. Вот почему регулярное применение ИГКС должно сопровождаться постоянным обучением пациентов и контролем приверженности лечению (с этим согласились 100% участников).
Экстрамелкий размер частиц имеет значение. Эффективность циклесонида в лечении легкой БА
Важным фактором клинической успешности ингаляционной терапии БА является создание более высокой депозиции действующего вещества (в первую очередь ИГКС) в легких, а также во всех крупных дыхательных путях и МДП.
Для улучшения депозиции в МДП созданы ингаляторы нового поколения, генерирующие лекарственный аэрозоль с экстрамелкими частицами (масс-медианный аэродинамический размер частиц <2 мкм), с меньшей скоростью и большей продолжительностью распыления, с более высокими показателями легочной депозиции и более эффективным проникновением аэрозоля в МДП (рис. 7) [29-32].
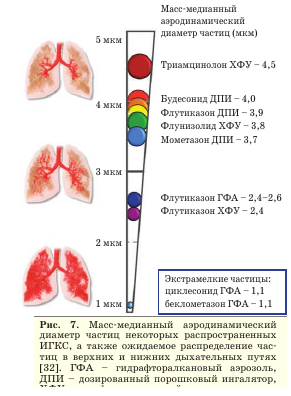
ИГКС (например, беклометазона дипропионат, циклесонид), длительнодействующие Р2-агонис- ты (ДДБА) (например, формотерол) и комбинации ИГКС/ДДБА в фиксированных дозах (например, беклометазона дипропионат/формоте- рол). Относительно недавно были разработаны многодозовый порошковый ингалятор, который доставляет комбинацию ИГКС/ДДБА с экстрамелкими частицами (беклометазона дипропио- нат/формотерол), и ингалятор с “мягким” аэрозолем (soft mist), который доставляет аэрозоли бронхолитиков длительного действия (тиотро- пия бромид и олодатерол). В настоящее время в клинической практике уже применяются фиксированные тройные комбинации действующих веществ в устройствах с экстрамелкими частицами, такие как беклометазона дипропионат/фор- мотерол/гликопирроний.
Внушительный клинический опыт, а также данные проведенных контролируемых клинических исследований позволили выявить некоторые преимущества в лечении пациентов с БА, в том числе легкого течения, при использовании экстрамелкодисперсных (ЭМД) форм ИГКС в сравнении с противовоспалительными препаратами, содержащими частицы стандартного размера (с масс-медианным аэродинамическим размером частиц 2-4 мкм). Рандомизированные контролируемые исследования, в которых сравнивалась краткосрочная эффективность ЭМД беклометазона дипропионата и циклесонида с ИГКС с частицами стандартного размера, показали, что ЭМД-формы обеспечивают эквивалентную клиническую эффективность (в том числе по влиянию на симптомы БА и качество жизни) при назначении в дозе, равной половине дозы стандартных ИГКС [33-36]. В наблюдательных исследованиях по изучению БА во всех возрастных группах сообщалось о сопоставимой или более высокой эффективности (при значительно меньших дозах) ЭМД беклометазона дипропионата и циклесонида в качестве монотерапии или в составе комбинированной терапии с ДДБА по сравнению с ИГКС с более крупными частицами [37-42]. Метаанализ 7 исследований, включавших 33 453 больных БА в возрасте 5-80 лет, показал, что ЭМД беклометазона дипропионат и циклесонид ассоциировались с большей вероятностью достижения контроля БА в сравнении с ИГКС со стандартными частицами (отношение шансов 1,34; 95% ДИ 1,22-1,46) [43]. По результатам когортного исследования, включавшего 1244 пациента с БА, противовоспалительная терапия с применением циклесонида была связана с лучшими исходами БА в течение 1 года наблюдения, меньшей вероятностью модификации базисной терапии из-за ее неэффективности в течение этого года в сравнении с немелкодисперсными ИГКС (флутиказона пропионат и бекломета- зона дипропионат). В исследование включались курящие и некурящие, пациенты с хорошей и плохой техникой ингаляции, со стабильной и нестабильной БА, а также с хорошей и плохой приверженностью терапии. Медиана (межквар- тильный диапазон) предписанных доз циклесо- нида и неэкстрамелкодисперсных ИГКС составила 160 (160-160) и 500 (250-500) мкг/сут соответственно (р < 0,001). В течение 1 года наблюдения у пациентов, получавших циклесонид, отмечалась более низкая частота тяжелых обострений (скорректированный коэффициент частоты 0,69; 95% ДИ 0,53-0,89) и более высокие показатели контроля БА (скорректированный коэффициент частоты 2,08; 95% ДИ 1,68-2,57), чем у тех, кто принимал ИГКС с более крупными частицами. Вероятность смены терапии на фоне приема циклесонида оказалась ниже и составила 0,70 (95% ДИ 0,59-0,83) [44].
При лечении пациентов с нетяжелым обострением БА ЭМД циклесонидом в высоких дозах (1280 мкг/сут) отмечалось более быстрое клиническое улучшение в сравнении с использованием высоких доз ИГКС со стандартным размером частиц (1000 мкг флутиказона пропионата или 1280 мкг будесонида). Назначение циклесонида в этом исследовании позволило снизить риск эскалации противовоспалительной терапии с применением СГКС, а также назначения антибактериальной терапии [45].
Дополнительным клиническим преимуществом ЭМД ИГКС, требующим, впрочем, дальнейшего уточнения, может быть меньший риск развития обструктивного апноэ во сне, как показано в масштабном ретроспективном когортном исследовании. Проанализировав электронные истории болезни 29 816 пациентов с БА старше 12 лет, исследователи выявили взаимосвязь размера частиц ингалируемого аэрозоля с частотой нарушений дыхания во сне и предположили, что ЭМД ИГКС могут иметь преимущество у лиц с высоким риском обструктивного апноэ (в том числе у мужчин и у лиц с ожирением) [32].
В различных исследованиях лечение ЭМД ИГКС ассоциировалось с низкой частотой нежелательных эффектов, прежде всего за счет орофарингеальных проявлений, таких как канди- доз, дисфония, фарингит, которые характерны для ИГКС и связаны с депозицией активного лекарственного вещества в верхних дыхательных путях. В исследованиях у взрослых и подростков было выявлено отсутствие достоверной разницы в частоте развития орофарингеальных нежелательных эффектов на фоне лечения ЭМД циклесонидом независимо от дозы (от 80 до 640 мкг/сут) в сравнении с плацебо [46-48]. При сравнении с другими ИГКС циклесонид также демонстрировал лучшую переносимость. Так, в систематическом обзоре целого ряда исследований, включавшем 6846 пациентов, авторы установили, что частота орофарингеальных нежелательных эффектов на фоне терапии циклесони- дом была достоверно ниже в сравнении с другими ИГКС [48].
В декабре 2022 г. в России был зарегистрирован первый отечественный ЭМД циклесонид (Асмалиб Эйр, компания “ПСК Фарма”). Клиническую эффективность и безопасность препарата Асмалиб Эйр еще предстоит оценить после накопления опыта его применения в широкой практике. По результатам исследования аэродинамического распределения частиц in vitro, а также сопоставимости состава препаратов (действующих и вспомогательных веществ), лекарственных форм и схожих по принципу действия ингаляционных устройств были получены данные о фармацевтической эквивалентности воспроизведенного лекарственного препарата Асмалиб Эйр аэрозоль для ингаляций дозированный, 40, 80 и 160 мкг/доза, и референтного лекарственного препарата Альвеско в тех же дозах [49]. В открытом рандомизированном исследовании у 132 пациентов в возрасте от 18 до 70 лет с частично контролируемой БА Асмалиб Эйр в дозе 320 мкг/сут продемонстрировал не меньшую клиническую эффективность в сравнении с Альвеско в отношении динамики показателей функции внешнего дыхания, уровня контроля. В результате сравнительного анализа нежелательных эффектов по частоте и выраженности не было выявлено различий между лечебными группами [50].
В настоящее время известны предварительные результаты еще одного открытого проспективного исследования по оценке эффективности и безопасности препарата Асмалиб Эйр (циклесо- нид ДАИ 160 мкг) в качестве средства базисной терапии недостаточно контролируемой БА легкого течения [51]. На данном этапе в исследование включено 100 взрослых пациентов (мужчины и женщины, средний возраст 38 и 45 лет соответственно) с легкой недостаточно контролируемой БА (средний балл по АСТ составлял 15). На момент включения в исследование все пациенты получали монотерапию ИГКС в эквивалентных низких дозах: будесонид (200-400 мкг/сут) - 52%, беклометазон (100-250 мкг/сут) - 42%, флутиказона пропионат (100-250 мкг/сут) - 6%. Среди наиболее значимых сопутствующих заболеваний, которые при опросе были зафиксированы у 56% пациентов, отмечались следующие: аллергический ринит (26%), артериальная гипертония (15%), гастроэзофагеальная рефлюксная болезнь (11%), сахарный диабет 2-го типа (2%), псориаз (1%), гипотиреоз (1%). Об истории курения сообщили 15% пациентов.
После включения в исследование все пациенты переводились на терапию циклесонидом (Асмалиб Эйр) 160 мкг 1 раз в сутки, контроль за симптомами БА осуществлялся в ходе 4 визитов на протяжении 12 нед (рис. 8). Предварительные данные исследования подтверждают гипотезу об эффективности циклесонида в виде ЭМД-аэрозоля с режимом дозирования 1 раз в сутки по сравнению со стандартной сопоставимой монотерапией. При переводе на терапию циклесонидом к 12-й неделе лечения хороший контроль БА (>20 баллов по АСТ) был достигнут у подавляющего числа пациентов (97%). При этом полного контроля симптомов удалось достичь в 26% случаев. Циклесонид продемонстрировал также высокий профиль орофарингеальной безопасности: зафиксирован 1 случай (1%) развития дисфонии. Серьезных нежелательных явлений не зарегистрировано.
Заключение
Бронхиальная астма многолика и характеризуется широким спектром причин и проявлений. Несмотря на то что у пациентов с БА легкой степени риск обострений относительно низкий, симптомы могут быть значительно выраженными и даже тяжелыми. Вот почему лечение этой формы заболевания необходимо индивидуализировать и проводить с таким же вниманием, какое обычно уделяется при более тяжелом течении БА. Назначение противовоспалительных препаратов, оценка текущих симптомов и будущих рисков - обязательные составляющие такого подхода. Даже симптоматическое применение препаратов, содержащих ИГКС, приносит пользу пациентам, при этом, без сомнения, назначения КДБА в качестве единственного средства лечения следует избегать. Выбор оптимального режима терапии (ежедневно или по потребности) определяется особенностями клинической ситуации, в том числе частотой симптомов, ожидаемой приверженностью лечению, предпочтениями пациента, доступностью и стоимостью препаратов, наличием сопутствующих заболеваний. Нельзя также забывать, что ингаляционное устройство и заключенное в нем действующее вещество являются полноправными “участниками” процесса терапии, а индивидуальные характеристики аэрозоля или порошка могут значительным образом повлиять на исходы лечения БА.
Список литературы
Global Initiative for Asthma. Global strategy for asthma management and prevention. Updated 2024.
Dusser D, Montani D, Chanez P, de Blic J, Delacourt C, De- schildre A, Devillier P, Didier A, Leroyer C, Marguet C, Marti- nat Y, Piquet J, Raherison C, Serrier P, Tillie-Leblond I, Ton- nel AB, Tunon de Lara M, Humbert M. Mild asthma: an expert review on epidemiology, clinical characteristics and treatment recommendations. Allergy 2007 Jun;62(6):591-604.
Rabe KF, Adachi M, Lai CK, Soriano JB, Vermeire PA, Weiss KB, Weiss ST. Worldwide severity and control of asthma in children and adults: the global asthma insights and reality surveys. The Journal of Allergy and Clinical Immunology 2004 Jul;114(1):40-7.
FitzGerald JM, Barnes PJ, Chipps BE, Jenkins CR, O’Byrne PM, Pavord ID, Reddel HK. The burden of exacerbations in mild asthma: a systematic review. ERJ Open Research 2020 Aug;6(3):00359-2019.
Mulgirigama A, Barnes N, Fletcher M, Pedersen S, Pizzichi- ni E, Tsiligianni I. A review of the burden and management of mild asthma in adults - implications for clinical practice. Respiratory Medicine 2019 Jun;152:97-104.
Tang W, Sun L, Fizgerald JM. A paradigm shift in the treatment of mild asthma? Journal of Thoracic Disease 2018 Oct;10(10):5655-8.
Olaguibel JM, Quirce S, Julia B, Fernandez C, Fortuna AM, Molina J, Plaza V; MAGIC Study Group. Measurement of asthma control according to Global Initiative for Asthma guidelines: a comparison with the Asthma Control Questionnaire. Respiratory Research 2012 Jun;1(13):50.
Price D, Fletcher M, van der Molen T. Asthma control and management in 8,000 Europe an patients: the REcognise Asthma and LInkto Symptoms and Experience (REALISE) survey. NPJ. Primary Care Respiratory Medicine 2014 Jun;24:14009.
Eriksson S, Giezeman M, Hasselgren M, Janson C, Kisiel MA, Montgomery S, Nager A, Sandelowsky H, Stallberg B, Sundh J, Lisspers K. Risk factors associated with asthma control and quality of life in patients with mild asthma without preventer treatment, a cross-sectional study. Journal of Asthma and Allergy 2024 Jul;17:621-32.
O’Byrne PM, Barnes PJ, Rodriguez-Roisin R, Runnerstrom E, Sandstrom T, Svensson K, Tattersfield A. Low dose inhaled budesonide and formoterol in mild persistent asthma: the OPTIMA randomized trial. American Journal of Respiratory and Critical Care Medicine 2001 Oct;164(8 Pt 1):1392-7.
Ding B, Small M. Disease burden of mild asthma: findings from a cross-sectional real-world survey. Advances in Therapy 2017 May;34(5):1109-27.
Bloom CI, Nissen F, Douglas IJ, Smeeth L, Cullinan P, Quint JK. Exacerbation risk and characterisation of the UK’s asthma population from infants to old age. Thorax 2018 Apr;73(4):313-20.
O’Byrne PM, FitzGerald JM, Bateman ED, Barnes PJ, Zhong N, Keen C, Jorup C, Lamarca R, Ivanov S, Reddel HK. Inhaled combined budesonide-formoterol as needed in mild asthma. The New England Journal of Medicine 2018 May 17;378(20):1865-76.
Bateman ED, Reddel HK, O’Byrne PM, Barnes PJ, Zhong N, Keen C, Jorup C, Lamarca R, Siwek-Posluszna A, FitzGerald JM. As-needed budesonide-formoterol versus maintenance budesonide in mild asthma. The New England Journal of Medicine 2018 May;378(20):1877-87.
Green M. How big are the bronchioles? St. Thomas Hospital Gazette 1965;63:136-9.
Macklem PT, Mead J. Resistance of central and peripheral airways measured by a retrograde catheter. Journal of Applied Physiology 1967;22(3):395-401.
Hogg JC, Macklem PT, Thurlbeck WM. Site and nature of airway obstruction in chronic obstructive lung disease. The New England Journal of Medicine 1968 Jun;278(25):1355-60.
Hogg JC, Pare PD, Hackett TL. The contribution of small airway obstruction to the pathogenesis of chronic obstructive pulmonary disease. Physiological Reviews 2017 Apr;97(2):529-52.
Cottini M, Lombardi C, Passalacqua G, Bagnasco D, Berti A, Comberiati P, Imeri G, Landi M, Heffler E. Small airways: the “silent zone” of 2021 GINA report? Frontiers in Medicine 2022;9:884679.
Cottini M, Licini A, Lombardi C, Berti A. Clinical characterization and predictors of IOS-defined small-airway dysfunction in asthma. The Journal of Allergy and Clinical Immunology. In Practice 2020 Mar;8(3):997-1004.e2.
Abdo M, Trinkmann F, Kirsten AM, Pedersen F, Herzmann C, von Mutius E, Kopp MV, Hansen G, Waschki B, Rabe KF, Watz H, Bahmer T; Study Group. Small airway dysfunction links asthma severity with physical activity and symptom control. Journal of Allergy and Clinical Immunology. In Practice 2021 Sep;9(9):3359-68.e1.
Usmani OS, Singh D, Spinola M, Bizzi A, Barnes PJ. The prevalence of small airways disease in adult asthma: a systematic literature review. Respiratory Medicine 2016 Jul;116:19-27.
Cottini M, Licini A, Lombardi C, Berti A. Prevalence and features of IOS-defined small airway disease across asthma severities. Respiratory Medicine 2021 Jan;176:106243.
Postma DS, Brightling C, Baldi S, Van den Berge M, Fab- bri LM, Gagnatelli A, Papi A, Van der Molen T, Rabe KF, Siddiqui S, Singh D, Nicolini G, Kraft M; ATLANTIS study group. Exploring the relevance and extent of small airways dysfunction in asthma (ATLANTIS): baseline data from a prospective cohort study. The Lancet. Respiratory Medicine 2019 May;7(5):402-16.
Shahidi N, Fitzgerald JM. Current recommendations for the treatment of mild asthma. Journal of Asthma and Allergy 2010 Dec;3:169-76.
O’Byrne PM, Jenkins C, Bateman ED. The paradoxes of asthma management: time for a new approach? The European Respiratory Journal 2017 Sep;50(3):1701103.
Stanford RH, Shah MB, D’Souza AO, Dhamane AD, Schatz M. Short-acting b-agonist use and its ability to predict future asthma-related outcomes. Annals of Allergy, Asthma & Immunology 2012 Dec;109(6):403-7.
Domingo C, Garcia G, Gemicioglu B, Van GV, Larenas-Linne- mann D, Neffen H, Poachanukoon O, Sagara H, Berend N, Piz- zichini E, Irusen E, Aggarwal B, Eken V, Levy G. Consensus on mild asthma management: results of a modified Delphi study. The Journal of Asthma 2023 Jan;60(1):145-57.
Woolcock AJ. Effect of drugs on small airways. American Journal of Respiratory and Critical Care Medicine 1998 May;157(5 Pt 2):S203-7.
Leach C, Colice GL, Luskin A. Particle size of inhaled corticosteroids: does it matter? The Journal of Allergy and Clinical Immunology 2009;124(6 Suppl):S88-93.
Leach CL, Davidson PJ, Hasselquist BE, Boudreau RJ. Lung deposition of hydrofluoroalkane-134a beclomethasone is greater than that of chlorofluorocarbon fluticasone and chlorofluorocarbon beclomethasone: a cross-over study in healthy volunteers. Chest 2002 Aug;122(2):510-6.
Henao MP, Kraschnewski JL, Bolton MD, Ishmael F, Craig T. Effects of inhaled corticosteroids and particle size on risk of obstructive sleep apnea: a large retrospective cohort study. International Journal of Environmental Research and Public Health 2020 Oct;17(19):7287.
Davies RJ, Stampone P, O’Connor BJ. Hydrofluoroal- kane-134a beclomethasone dipropionate extrafine aerosol provides equivalent asthma control to chlorofluorocarbon bec- lomethasone dipropionate at approximately half the total daily dose. Respiratory Medicine 1998 Jun;92(Suppl A):23-31.
Gross G, Thompson PJ, Chervinsky P, Vanden Burgt J. Hydro- fluoroalkane-134a beclomethasone dipropionate, 400 microg, is as effective as chlorofluorocarbon beclomethasone dipropionate, 800 microg, for the treatment of moderate asthma. Chest 1999 Feb;115(2):343-51.
Vermeulen JH, Gyurkovits K, Rauer H, Engelstatter R. Randomized comparison of the efficacy and safety of ciclesonide and budesonide in adolescents with severe asthma. Respiratory Medicine 2007 Oct;101(10):2182-91.
von Berg A, Engelstatter R, Minic P, Sreckovic M, Garcia Garcia ML, Latos T, Vermeulen JH, Leichtl S, Hellbardt S, Beth- ke TD. Comparison of the efficacy and safety of ciclesonide 160 microg once daily vs. budesonide 400 microg once daily in children with asthma. Pediatric Allergy and Immunology 2007 Aug;18(5):391-400.
Barnes N, Price D, Colice G, Chisholm A, Dorinsky P, Hilly- er EV, Burden A, Lee AJ, Martin RJ, Roche N, von Ziegen- weidt J, Israel E. Asthma control with extrafine-particle hydrofluoroalkane-beclometasone vs. large-particle chloro- fluorocarbon-beclometasone: a real-world observational study. Clinical and Experimental Allergy 2011 Nov;41(11):1521-32.
Martin RJ, Price D, Roche N, Israel E, van Aalderen WM, Grigg J, Postma DS, Guilbert TW, Hillyer EV, Burden A, von Ziegenweidt J, Colice G. Cost-effectiveness of initiating extrafine- or standard size-particle inhaled corticosteroid for asthma in two health-care systems: a retrospective matched cohort study. NPJ. Primary Care Respiratory Medicine 2014 Oct;24:14081.
Postma DS, Roche N, Colice G, Israel E, Martin RJ, van Aalderen WM, Grigg J, Burden A, Hillyer EV, von Ziegenweidt J, Gopalan G, Price D. Comparing the effectiveness of small-particle versus large-particle inhaled corticosteroid in COPD. International Journal of Chronic Obstructive Pulmonary Disease 2014 Oct;9:1163-86.
Roche N, Postma DS, Colice G, Burden A, Guilbert TW, Israel E, Martin RJ, van Aalderen WM, Grigg J, Hillyer EV, von Ziegenweidt J, Price DB. Differential effects of inhaled corticosteroids in smokers/ex-smokers and nonsmokers with asthma. American Journal of Respiratory and Critical Care Medicine 2015 Apr;191(8):960-4.
van der Molen T, Postma DS, Martin RJ, Herings RM, Over- beek JA, Thomas V, Miglio C, Dekhuijzen R, Roche N, Guil- bert T, Israel E, van Aalderen W, Hillyer EV, van Rysewyk S, Price DB. Effectiveness of initiating extrafine-particle versus
fine-particle inhaled corticosteroids as asthma therapy in the Netherlands. BMC Pulmonary Medicine 2016 May;16(1):80.
Allegra L, Cremonesi G, Girbino G, Ingrassia E, Marsico S, Nicolini G, Terzano C; PRISMA (PRospectIve Study on asthMA control) Study Group. Real-life prospective study on asthma control in Italy: cross-sectional phase results. Respiratory Medicine 2012 Feb;106(2):205-14.
Sonnappa S, McQueen B, Postma DS, Martin RJ, Roche N, Grigg J, Guilbert T, Gouder C, Pizzichini E, Niimi A, Phi- patanakul W, Chisholm A, Dandurand RJ, Kaplan A, Israel E, Papi A, van Aalderen WMC, Usmani OS, Price D. Extrafine versus fine inhaled corticosteroids in relation to asthma control: a systematic review and meta-analysis of observational real-life studies. Journal of Allergy and Clinical Immunology. In Practice 2018 May-Jun;6(3):907-15.e7.
Postma DS, Dekhuijzen R, van der Molen T, Martin RJ, van Aalderen W, Roche N, Guilbert TW, Israel E, van Eick- els D, Khalid JM, Herings RM, Overbeek JA, Miglio C, Thomas V, Hutton C, Hillyer EV, Price DB. Asthma-related outcomes in patients initiating extrafine ciclesonide or fine-particle inhaled corticosteroids. Allergy, Asthma & Immunology Research 2017 Mar;9(2):116-25.
Zietkowski Z, Lukaszyk M, Skiepko R, Budny W, Skiepko U, Jozwik A, Bodzenta-Lukaszyk A. Efficacy of ciclesonide in the treatment of patients with asthma exacerbation. Post^py Der- matologii i Alergologii 2019 Apr;36(2):217-22.
Langdon CG, Adler M, Mehra S, Alexander M, Drollmann A. Once-daily ciclesonide 80 or 320 microg for 12 weeks is safe and effective in patients with persistent asthma. Respiratory Medicine 2005 Oct;99(10):1275-85.
Busse W, Kaliner MA, Berstein D, Nayak A, Kundu S, Williams J, Fish J, Banerji D. The novel inhaled corticosteroid ciclesonide is efficacious and has a favourable safety profile in adults and adolescents with severe persistent asthma. Journal of Allergy and Clinical Immunology 2005;115(2):213.
Engelstaetter R, Banerji D, Steinijans V, Wurst W. Low incidence of oropharyngeal adverse events in asthma patients treated with ciclesonide: results from a pooled analysis. American Journal of Respiratory and Critical Care Medicine 2004;169(7):72.
Авторы:
А.И. Синопальников, Ю.Г. Белоцерковская
Теги: легкая бронхиальная астма
234567 Начало активности (дата): 02.10.2025
234567 Кем создан (ID): 989
234567 Ключевые слова: легкая бронхиальная астма, мелкие дыхательные пути, фармакотерапия бронхиальной астмы, экстрамелкодисперсный аэрозоль, циклесонид, Асмалиб Эйр
12354567899
Похожие статьи
Роль ультразвука в диагностике внебольничной пневмонииРентген на дому 8 495 22 555 6 8
Влияние хронической обструктивной болезни легких на выживаемость пациентов после хирургического лечения по поводу рака легкого
Внебольничная пневмония у взрослых
Особенности влияния туберкулеза легких на тяжесть сопутствующей хроническкой обструктивной болезни легких



