 09.03.2025
09.03.2025
Прямой боковой спондилодез с непрямой декомпрессией корешков спинного мозга у пациентов с дегенеративным поясничным спинальным стенозом
Дегенеративные заболевания позвоночника занимают лидирующие позиции в структуре заболеваемости населения, ими страдают до 80 % трудоспособного населения.
ВВЕДЕНИЕ
Дегенеративные заболевания позвоночника занимают лидирующие позиции в структуре заболеваемости населения. Болевой синдром на фоне дегенеративных изменений позвоночника является основной причиной нетрудоспособности населения в развитых странах. По данным ВОЗ (Всемирная Организация Здравоохранения), ими страдают до 80 % трудоспособного населения. С каждым годом в мире увеличивается количество пациентов с дегенеративными заболеваниями поясничного отдела позвоночника примерно на 266 млн. (3,63 % населения всего мира) [1].
Увеличение среднего возраста населения и высокие требования к качеству жизни являются основаниями для дальнейшего развития методов хирургического лечения пациентов с дегенеративными заболеваниями позвоночника [2]. Современное диагностическое оборудование, инновационные технические решения в области малоинвазивной хирургии позвоночника, а также возможности анестезиологического пособия уже позволяют оказывать хирургическую помощь пациентам, которым ранее хирургия позвоночника была недоступна в связи с высокими рисками осложнений [3]. В хирургических сообществах активно поднимается вопрос о снижении травматичности хирургических вмешательств [4].
Цель работы — на основании данных литературы определить перспективы выполнения LLIF как самостоятельного декомпрессивно-стабилизирующего хирургического вмешательства.
Декомпрессивные малоинвазивные вмешательства с сохранением опорных структур позвоночника наименее травматичны в сравнении с декомпрессивно-стабилизирующими операциями, но в некоторых случаях невозможно обойтись без фиксации позвоночно-двигательного сегментаДекомпрессивно-стабилизирующие хирургические вмешательства выполняются из вентральных (ALIF/OLIF), задних (PLIF/TLIF) и бокового (LLIF) доступов. В настоящее время каждый из этих доступов может быть выполнен по технологии MIS. При выполнении LLIF исключается ряд осложнений, встречающихся при PLIF/TLIF и OLIF/ALIF, а возможность непрямой декомпрессии у некоторых категорий пациентов после установки межтелового имплантата и отсутствие необходимости в дополнительной фиксации ПДС позволяют рассматривать LLIF как малоинвазивное самостоятельное декомпрессивно-стабилизирующее хирургическое вмешательство.
МАТЕРИАЛЫ И МЕТОДЫ
В данной статье представлены обобщенные сведения отечественных и зарубежных публикаций о прямом боковом спондилодезе с непрямой декомпрессией корешков спинного мозга в поясничном отделе позвоночника, описаны исторические факты развития метода, его возможности в лечении пациентов с дегенеративными заболеваниями позвоночника, отличия от иных доступов к поясничному отделу позвоночника.
Отбор научных источников проведен в информационных системах PubMed, Scopus, eLibrary с использованием следующих поисковых слов и словосочетаний: прямой боковой спондилодез (direct lumbar interbody fusion, lateral lumbar interbody fusion, extreme lumbar interbody fusion), непрямая декомпрессия корешков спинного мозга (indirect decompression), предикторы непрямой декомпрессии (predictors of indirect decompression). В обзор включено 60 статей, опубликованных с 1998 по 2023 год включительно.
Критерии включения научных публикаций в исследование:
полнотекстовые научные статьи, тезисы научно-практических конференций и диссертации, в которых представлены сведения о методах хирургического лечения пациентов с дегенеративным спинальным стенозом;
полнотекстовые научные работы о прямом боковом спондилодезе и его возможностях в достижении непрямой декомпрессии корешков спинного мозга, сравнении прямого бокового спондилодеза с другими методами спондилодеза;
полнотекстовые научные публикации, в которых изложены характер и частота осложнений после LLIF, в том числе в сравнении с другими методами спондилодеза.
Критерии невключения: научные статьи, в которых отсутствует информация о лечении пациентов с дегенеративными заболеваниями позвоночника.
В общей сложности для написания обзора литературы отобрано 60 научных работ, из них отечественных источников — 6 (10 %), иностранных — 54 (90 %).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
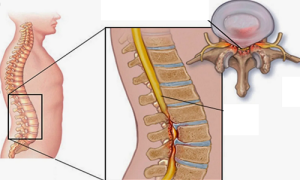
Дегенеративный спинальный стеноз является следствием прогрессирующих патологических изменений в позвоночнике, которые приводят к уменьшению резервных пространств для нервно-сосудистых образований в позвоночном канале и межпозвонковых отверстиях, и может вызывать компрессию корешков спинного мозга, проявляющуюся в виде нейрогенной перемежающей хромоты и (или) корешкового синдрома [5].
Патоморфологическими субстратами компрессии корешков спинного мозга выступают гипертрофированные дугоотростчатые суставы, гипертрофированные желтые связки, остеофиты и интраканальные синовиальные кисты дугоотростчатых суставов. Дегенеративный спинальный стеноз может быть локализован в позвоночном канале, латеральных карманах и межпозвонковых отверстиях.
Хирургическое лечение дегенеративного спинального стеноза
Дегенеративные заболевания являются причиной хирургических вмешательств в 59,9-71,4 % в структуре хирургии позвоночника [6]. В лечении пациентов с дегенеративным спинальным стенозом выполняют декомпрессивные, декомпрессивно-стабилизирующие, декомпрессивно-корригирующие и декомпрессивно-пластические хирургические вмешательства с использованием открытой хирургической техники и малоинвазивно. На сегодняшний день в арсенале хирурга есть возможность выполнить хирургические вмешательства на поясничном отделе позвоночника из разных доступов: LLIF, ALIF, OLIF, PLIF, TLIF. Технические решения в области хирургической визуализации и силовое оборудование позволяют максимально сохранить опорные структуры позвоночника при декомпрессиях корешков спинного мозга и в ряде случаев могут исключить необходимость в спондилодезе [4].
Существует отдельная группа пациентов с нестабильностью позвоночно-двигательного сегмента позвоночника, которым требуется выполнение спондилодеза, а в сочетании с дегенеративным спинальным стенозом — и декомпрессия корешков спинного мозга. При выполнении таким пациентам спондилодеза из вентральных доступов может произойти непрямая декомпрессия корешков спинного мозга, особенно в случаях их динамической компрессии [7]. Такие хирургические вмешательства являются малоинвазивными и могут обеспечить длительное сохранение результата лечения.
В настоящее время подбор метода хирургического вмешательства зависит от решения хирурга, так как не существует строгих стандартов в выборе способа фиксации позвоночно-двигательного сегмента, хирургического доступа и декомпрессии корешков спинного мозга [8].
Метод прямого бокового спондилодеза
В 2006 г. B.M. Ozgur et al. опубликовали технику спондилодеза, позволяющую без эндоскопического оборудования и тракции кзади поясничной мышцы выполнить доступ к межпозвонковым дискам поясничного отдела позвоночника [9]. Метод является модернизацией забрюшинного доступа к поясничному отделу позвоночника кпереди от поясничной мышцы, описанного P.C. McAfee et al. в 1998 г., и доступа через поясничную мышцу с использованием эндоскопического оборудования, опубликованного L. Pimenta в 2001 г. [10, 11]. Прямой боковой спондилодез в современной литературе имеет несколько вариантов названия: LLIF (англ.: lateral lumbar interbody fusion), DLIF (англ.: direct lumbar interbody fusion), XLIF\ELIF (англ.: extreme lateral lumbar interbody fusion). Метод прямого бокового спондилодеза с каждым годом становится более популярным, что подтверждается увеличением научных публикаций на данную тему в динамике [12]. Прямой боковой спондилодез чаще выполняют на уровнях L2-L3, L3-L4 и реже — на L1-L2, L4-L5. Сегмент L4-L5 может быть недоступен в связи с высоким расположением гребней подвздошных костей, а нижние ребра могут затруднить доступ к межпозвонковому диску L1-L2.
Осложнения в виде ретроградной эякуляции, повреждения крупных сосудов, мочеточника, брюшины, кишечника, венозной или артериальной тромбоэмболии при LLIF значительно меньше в сравнении с ALIF\OLIF, а сохранённые передняя и задняя продольные связки не позволяют мигрировать имплантату в переднем и заднем направлениях [13, 14, 15].
LLIF может быть наиболее подходящим методом хирургического вмешательства для пациентов с избыточной массой тела, так как не является фактором, повышающим риск осложнений при выполнении прямого бокового спондилодеза [16], и не усложняет ход операции. Перенесенные хирургические вмешательства в поясничном отделе позвоночника из вентральных или задних доступов также являются ключевыми причинами выбора LLIF для лечения смежного уровня [17, 18], так как позволяют избежать работы с рубцовой тканью и не продлевают транспедикулярную систему [19]. При непрямой декомпрессии корешков спинного мозга не требуется микрохирургическая декомпрессия корешков спинного мозга, следовательно, сокращается время хирургического вмешательства, резко снижается риск повреждения твердой мозговой оболочки и корешков спинного мозга. К преимуществам вентральных доступов относятся параметры межтеловых имплантатов, имеющие площадь опорной поверхности больше, чем у имплантатов для PLIF/TLIF [20]. В свою очередь, имплантаты при LLIF шире, чем для OLIF\ALIF, за счет чего задействованы кортикальные края замыкательных пластинок позвонков, являющиеся наиболее стойкими зонами к проседаниям межтеловых имплантатов [21-24], тем самым риск проседания имплантата при LLIF не повышается без дополнительной транспедикулярной фиксации [25, 26].
Непрямая декомпрессия
Непрямая декомпрессия корешков спинного мозга при выполнении спондилодезов из вентральных доступов часто упоминается в научной литературе. Непрямую декомпрессию нужно воспринимать как клинический результат в виде регресса компрессионных синдромов корешков спинного мозга после операции, а уже во вторую очередь — как увеличение размеров межпозвонковых отверстий, латерального кармана или позвоночного канала по данным нейровизуализации. Непрямая декомпрессия корешков спинного мозга в межпозвонковых отверстиях после вентральных спондилодезов является не редким результатом [9, 10, 11, 19, 27, 28], а непрямая декомпрессия корешков спинного мозга в позвоночном канале менее предсказуема, особенно при грубых стенозах.
Увеличение размеров межпозвонковых отверстий можно определить на интраоперационных рентгенологических снимках. При дегенеративном стенозе позвоночного канала интраоперационно визуализировать увеличение резервного пространства для корешков спинного мозга затруднительно, следовательно, сделать вывод об успешности выполнения LLIF, как декомпрессионного хирургического вмешательства, можно только при активизации пациента. Это обстоятельство заставляет хирургов сомневаться в LLIF как единственном хирургическом вмешательстве с целью декомпрессии корешков спинного мозга в позвоночном канале и стабилизации ПДС. LLIF активно используют в качестве первого этапа хирургии для стабилизации и/или коррекции баланса позвоночника. Вторым этапом выполняют микрохирургическую декомпрессию корешков спинного мозга и траспедикулярную фиксацию позвоночно-двигательного сегмента. Непрямая декомпрессия корешков спинного мозга вызывает большой интерес у нейрохирургов, так как её эффект аналогичен микрохирургической декомпрессии, но отсутствует контакт с твердой мозговой оболочкой, что резко снижает возможность ее повреждения, особенно при повторных хирургических вмешательствах [29].
Механизм непрямой декомпрессии корешков спинного мозга основан на восстановлении высоты межпозвонкового диска, увеличении высоты межпозвонковых отверстий и растяжении задней продольной и желтой связок [30-41]. К тому же после LLIF до двух лет наблюдается увеличение резервного пространства для корешков спинного мозга в позвоночном канале за счет гипотрофии желтой связки в условиях ригидной фиксации позвоночно-двигательного сегмента [42-44].
Максимальное сохранение анатомической целостности позвоночно-двигательного сегмента при выполнении LLIF, в сравнении с ALIF/OLIF, а именно сохранение передней и задней продольных связок, большей части фиброзного кольца положительно влияет на стабильность сегмента и создает условия, при которых невозможна миграция кейджа в переднем и заднем направлениях [45]. Но это является и основной причиной необходимости более строго отбора пациентов для планирования непрямой декомпрессии корешков спинного мозга в позвоночном канале после LLIF в сравнении с ALIF/OLIF, ведь ограничение в возможности установки более высокого межтелового имплантата может привести к недостаточному увеличению объема позвоночного канала.
Говоря о возможностях непрямой декомпрессии корешков спинного мозга в позвоночном канале, следует отметить, что стеноз позвоночного канала grade D по SAizas считается наименее перспективным для непрямой декомпрессии при выполнении прямого бокового спондилодеза, однако существуют результаты хирургических вмешательств, после которых отсутствует необходимость выполнения прямой декомпрессии [46], что позволяет резко снизить объем хирургического вмешательства.
В современных научных публикациях основное внимание уделено непрямой декомпрессии корешков спинного мозга в межпозвонковых отверстиях [12, 47, 48]. Исследования, в которых основное внимание уделено непрямой декомпрессии корешков спинного мозга в позвоночном канале и выявлению её предикторов, имеют низкую достоверность [49, 50, 51]. Прочие исследования практически не имеют группы пациентов с исключительно дегенеративным стенозом позвоночного канала и оценкой эффективности непрямой декомпрессии корешков спинного мозга у таких пациентов [52-54]. Встречаются публикации, где из исследования исключены пациенты со стенозом позвоночного канала с grade C и D по Schizas [55]. Также опубликованы работы по оценке эффективности непрямой декомпрессии из разных хирургических доступов (LLIF, OLIF, ALIF) [29]. Все это затрудняет сделать однозначные выводы о выборе модели пациента с дегенеративным стенозом позвоночного столба, у которого можно прогнозировать клинически эффективную непрямую декомпрессию после LLIF.
Пациенты с 3 типом сагиттального профиля позвоночника по Roussouly определены как наиболее подходящие для непрямой декомпрессии [56], а стеноз позвоночного канала, обусловленный оссифицированными задней продольной и жёлтой связками, является абсолютно не подходящим к выполнению LLIF с целью непрямой декомпрессии корешков спинного мозга [45].
Непрямую декомпрессию корешков спинного мозга при выполнении ALIF и OLIF в большинстве случаев можно спрогнозировать до операции благодаря изученности возможностей данных методов.
При необходимости в прямой декомпрессии эти доступы позволяют выполнить микрохирургическую декомпрессию корешков спинного мозга через межтеловое пространство после тотальной дискэктомии, тем самым осуществив весь объем хирургического вмешательства в один этап.
В научных публикациях встречается понятие IDF (англ.: indirect decompression failure after lateral lumbar interbody fusion), что означает отсутствие непрямой декомпрессии при планировании ее на дооперационном этапе, преимущественно в позвоночном канале после прямого бокового межтелового спондилодеза [57]. Такой исход хирургического вмешательства является следствием недостаточной изученности непрямой декомпрессии корешков спинного мозга в позвоночном канале при выполнении прямого бокового спондилодеза.
MIS LLIF позволяет получить непрямую декомпрессию корешков спинного мозга в межпозвонковых отверстиях, эквивалентную MIS TLIF и ALIF [46]. При отсутствии костного блока на заинтересованном позвоночно-двигательном сегменте имеется высокая вероятность увеличения высоты диска за счет установки межтелового имплантата, что неизбежно приводит к увеличению высоты и площади межпозвонковых отверстий, причем практически равномерно с обеих сторон, вне зависимости от выбора стороны хирургического доступа [45]. Эффективность непрямой декомпрессии корешков спинного мозга в межпозвонковых отверстиях после LLIF не зависит от положения межтелового имплантата, тогда как в позвоночном канале вероятность непрямой декомпрессии корешков спинного мозга выше при дорзальном положении имплантата [46]. Это является усложняющим фактором в планировании непрямой декомпрессии корешков спинного мозга в позвоночном канале с коррекцией сагиттального баланса, так как для восстановления сагиттального профиля положение межтелового имплантата предпочтительнее в передней трети межтелового промежутка. Проседание межтелового имплантата в меньшей степени влияет на потерю эффекта непрямой декомпрессии в межпозвонковых отверстиях, чем в позвоночном канале [12].
Несмотря на формирование грубого стеноза позвоночного канала, запас компенсаторных возможностей организма позволяет многим пациентам длительное время не обращаться за медицинской помощью в связи с отсутствием клинических проявлений заболевания [58]. Из этого следует, что непрямая декомпрессия корешков спинного мозга при незначительном увеличении объема позвоночного канала на уровне дегенеративного стеноза по данным нейровизуализации может быть эффективной в виде купирования клинических проявлений компрессии корешков спинного мозга.
Осложнения после LLIF
Ятрогенная травма поясничного сплетения является ведущим осложнением в раннем послеоперационном периоде после LLIF [59]. Она проявляется в виде слабости сгибателей бедра в 24 % случаев, снижения чувствительности по передней поверхности бедра — в 38 %, пареза мышцы живота — в 1,8 %. Другие осложнения после LLIF представлены в виде повреждения сосудов (0,1 %), повреждения кишечника (0,08 %), проседания межтелового имплантата (14 %) [60].
Распространенными последствиями, связанными с хирургическим доступом через поясничную мышцу, являются слабость поясничной мышцы, боль или снижение чувствительности по передней поверхности бедра со стороны хирургического доступа, которые купируются от двух недель до одного года на фоне консервативного лечения [12].
При дегенеративном стенозе позвоночного канала и необходимости стабилизировать позвоночнодвигательный сегмент для некоторых категорий пациентов наиболее предпочтительным методом лечения может являться LLIF с непрямой декомпрессией корешков спинного мозга и транскутанной транспедикулярной фиксацией (или без таковой).
Для выполнения LLIF, как единственного декомпрессивно-стабилизирующего хирургического вмешательства, требуется уверенность в том, что он будет эффективен в устранении компрессии корешков спинного мозга в позвоночном канале. Для этого необходимо определить предикторы непрямой декомпрессии корешков спинного мозга в позвоночном канале при его дегенеративном стенозе для LLIF. В поиске предикторов непрямой декомпрессии и возможностей LLIF в ее достижении нельзя исключать из исследований пациентов со стенозом позвоночного канала grade D по S^zas. Возможно, даже незначительного увеличения объёма позвоночного канала будет достаточно для купирования клинических проявлений компрессии корешков спинного мозга.
В условиях ригидной фиксации позвоночно-двигательного сегмента происходит уменьшение толщины гипертрофированной желтой связки. Следовательно, возможно рассмотреть выполнение LLIF как единственного декомпрессивно-стабилизирующего хирургического вмешательства с непрямой декомпрессией корешков спинного мозга, а с течением времени наблюдать увеличение объёма позвоночного канала по данным МРТ и МСКТ поясничного отдела позвоночника.
Такой подход может повысить эффективность хирургического лечения пациентов с дегенеративным стенозом позвоночного канала в поясничном отделе позвоночника, чаще использовать в практике метод LLIF как единственное декомперссивно-стабилизирующее малоинвазивное хирургическое вмешательство отдельной группе пациентов, тем самым сократить количество хирургических этапов лечения, снизить продолжительность операций, уменьшить кровопотерю и травматичность общего объёма хирургического пособия.
ЗАКЛЮЧЕНИЕ
LLIF является методом хирургического вмешательства на поясничном отделе позвоночника, который зарекомендовал себя как эффективное малоинвазивное хирургическое вмешательство с целью стабилизации и коррекции деформации в позвоночно-двигательном сегменте, а также для достижения непрямой декомпрессии корешков спинного мозга в межпозвонковых отверстиях.
Прямой боковой спондилодез редко выполняют как единственное хирургическое вмешательство на позвоночно-двигательном сегменте с целью декомпрессии и стабилизации ввиду малой изученности возможностей метода в достижении непрямой декомпрессии корешков спинного мозга в позвоночном канале при его дегенеративном стенозе.
Выявление предикторов непрямой декомпрессии корешков спинного мозга в позвоночном канале позволит повысить эффективность хирургического лечения пациентов методом LLIF.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
СПИСОК ИСТОЧНИКОВ
Ravindra VM, Senglaub SS, Rattani A, et al. Degenerative Lumbar Spine Disease: Estimating Global Incidence and Worldwide Volume. Global Spine J. 2018;8(8):784-794. doi: 10.1177/2192568218770769
Ruetten S, Komp M. Endoscopic Lumbar Decompression. Neurosurg Clin N Am. 2020;31(1):25-32. doi: 10.1016/j. nec.2019.08.003
Бывальцев В.А., Калинин А.А., Шепелев В.В. Сравнение результатов и экономической эффективности минимально инвазивного и открытого трансфораминального поясничного межтелового спондилодеза: метаанализ проспективных когортных исследований. Вестник РАМН. 2019;74(2):125-135. doi: 10.15690/vramn1093
Karlsson T, Forsth P, Skorpil M, et al. Decompression alone or decompression with fusion for lumbar spinal stenosis: a randomized clinical trial with two-year MRI follow-up. Bone Joint J. 2022;104-B(12):1343-1351. doi: 10.1302/0301-620X.104B12.BJJ-2022-0340.R1
Gagliardi MJ, Guiroy AJ, Camino-Willhuber G, et al. Is Indirect Decompression and Fusion More Effective than Direct Decompression and Fusion for Treating Degenerative Lumbar Spinal Stenosis With Instability? A Systematic Review and meta-Analysis. Global Spine J. 2023;13(2):499-511. doi: 10.1177/21925682221098362
Лопарев Е.А., Климов В.С., Евсюков А.В. Повторные оперативные вмешательства у пациентов с дегенеративно-дистрофическим заболеванием поясничного отдела позвоночника после удаления грыж дисков. Хирургия позвоночника. 2017;14(1):51-59. doi: 10.14531/ss2017.1.51-59
Боков А.Е. Хирургическая тактика при дегенеративном и посттраматическом стенозе позвоночного канала у ациентов с нарушением плотности костной ткани: дис.... д-ра. мед наук. М.; 2023:258.
Гуща А.О. Теоретические и практические аспекты применения декомпрессивно-стабилизирующих операций дегенеративных стенозах пояснично-крестцового при отдела позвоночника. Алгоритм выбора хирургического вмешательства. В кн.: Хирургия дегенеративных поражений позвоночника. Под ред. А.О. Гущи, Н.А. Коновалова, А.А. Гриня. М.: ГЭОТАР-Медиа; 2019:358-381.
Ozgur BM, Aryan HE, Pimenta L, Taylor WR. Extreme Lateral Interbody Fusion (XLIF): a novel surgical technique for anterior lumbar interbody fusion. Spine J. 2006;6(4):435-443. doi: 10.1016/j.spinee.2005.08.012
McAfee PC, Regan JJ, Geis WP, Fedder IL. Minimally invasive anterior retroperitoneal approach to the lumbar spine. Emphasis on the lateral BAK. Spine (Phila Pa 1976). 1998;23(13):1476-1484. doi: 10.1097/00007632-199807010-00009
Pimenta L. Lateral endoscopic transpsoas retroperitoneal approach for lumbar spine surgery. In: Paper presented at the VIII Brazilian Spine Society Meeting. May 2001. Belo Horizonte, Minas Gerais, Brazil.
Nikaido T, Konno SI. Usefulness of Lateral Lumbar Interbody Fusion Combined with Indirect Decompression for Degenerative Lumbar Spondylolisthesis: A Systematic Review. Medicina (Kaunas). 2022;58(4):492. doi: 10.3390/ medicina58040492
Phan K, Thayaparan GK, Mobbs RJ. Anterior lumbar interbody fusion versus transforaminal lumbar interbody fusion-systematic review and meta-analysis. Br J Neurosurg. 2015;29(5):705-711. doi: 10.3109/02688697.2015.1036838
Malham GM, Parker RM, Ellis NJ, et al. Anterior lumbar interbody fusion using recombinant human bone morphogenetic protein-2: a prospective study of complications. J Neurosurg Spine. 2014;21(6):851-860. doi: 10.3171/2014.8.SPINE13524
Mobbs RJ, Phan K, Daly D, et al. Approach-Related Complications of Anterior Lumbar Interbody Fusion: Results of a Combined Spine and Vascular Surgical Team. Global Spine J. 2016;6(2):147-154. doi: 10.1055/s-0035-1557141
Rodgers WB, Cox CS, Gerber EJ. Early complications of extreme lateral interbody fusion in the obese. J Spinal Disord Tech. 2010;23(6):393-397. doi: 10.1097/BSD.0b013e3181b31729
Jain D, Verma K, Mulvihill J, et al. Comparison of Stand-Alone, Transpsoas Lateral Interbody Fusion at L3-4 and Cranial vs Transforaminal Interbody Fusion at L3-4 and L4-5 for the Treatment of Lumbar Adjacent Segment Disease. Int J Spine Surg. 2018;12(4):469-474. doi: 10.14444/5056
Nakano M, Futakawa H, Nogami S, et al. A Comparative Clinical Study of Lateral Lumbar Interbody Fusion between Patients with Multiply Operated Back and Patients with First-Time Surgery. Medicina (Kaunas). 2023;59(2):342. doi: 10.3390/medicina59020342
Wang MY, Vasudevan R, Mindea SA. Minimally invasive lateral interbody fusion for the treatment of rostral adjacent- segment lumbar degenerative stenosis without supplemental pedicle screw fixation. JNeurosurg Spine. 2014;21(6):861- 866. doi: 10.3171/2014.8.SPINE13841
Yuan W, Kaliya-Perumal AK, Chou SM, Oh JY. Does Lumbar Interbody Cage Size Influence Subsidence? A Biomechanical Study. Spine (Phila Pa 1976). 2020;45(2):88-95. doi: 10.1097/BRS.0000000000003194
Palejwala SK, Sheen WA, Walter CM, et al. Minimally invasive lateral transpsoas interbody fusion using a stand-alone construct for the treatment of adjacent segment disease of the lumbar spine: review of the literature and report of three cases. Clin Neurol Neurosurg. 2014;124:90-96. doi: 10.1016/j.clineuro.2014.06.031
Alkalay RN, Adamson R, Groff MW. The effect of interbody fusion cage design on the stability of the instrumented spine in response to cyclic loading: an experimental study. Spine J. 2018;18(10):1867-1876. doi: 10.1016/j.spinee.2018.03.003
Wewel JT, Hartman C, Uribe JS. Timing of Lateral Lumbar Interbody Subsidence: Review of Exclusive Intraoperative Subsidence. World Neurosurg. 2020;137:e208-e212. doi: 10.1016/j.wneu.2020.01.134
Taba HA, Williams SK. Lateral Lumbar Interbody Fusion. Neurosurg Clin N Am. 2020;31(1):33-42. doi: 10.1016/j. nec.2019.08.004
Manzur MK, Steinhaus ME, Virk SS, et al. Fusion rate for stand-alone lateral lumbar interbody fusion: a systematic review. Spine J. 2020;20(11):1816-1825. doi: 10.1016/j.spinee.2020.06.006
Chen E, Xu J, Yang S, et al. Cage Subsidence and Fusion Rate in Extreme Lateral Interbody Fusion with and without Fixation. World Neurosurg. 2019;122:e969-e977. doi: 10.1016/j.wneu.2018.10.182
Mobbs RJ, Phan K, Malham G, et al. Lumbar interbody fusion: techniques, indications and comparison of interbody fusion options including PLIF, TLIF, MI-TLIF, OLIF/ATP, LLIF and ALIF. J Spine Surg. 2015;1(1):2-18. doi: 10.3978/j. issn.2414-469X.2015.10.05
Lee DH, Lee DG, HwangJS, et al. Clinical and radiological results ofindirect decompression after anterior lumbar interbody fusion in central spinal canal stenosis. J Neurosurg Spine. 2021;34(4):564-572. doi: 10.3171/2020.7.SPINE191335
Gagliardi MJ, Guiroy AJ, Camino-Willhuber G, et al. Is Indirect Decompression and Fusion More Effective than Direct Decompression and Fusion for Treating Degenerative Lumbar Spinal Stenosis With Instability? A Systematic Review and meta-Analysis. Global Spine J. 2023;13(2):499-511. doi: 10.1177/21925682221098362
Ahmadian A, Bach K, Bolinger B, et al. Stand-alone minimally invasive lateral lumbar interbody fusion: multicenter clinical outcomes. J Clin Neurosci. 2015;22(4):740-746. doi: 10.1016/j.jocn.2014.08.036
Alimi M, Hofstetter CP, Tsiouris AJ, et al. Extreme lateral interbody fusion for unilateral symptomatic vertical foraminal stenosis. Eur Spine J. 2015;24 Suppl 3:346-352. doi: 10.1007/s00586-015-3940-z
Campbell PG, Nunley PD, Cavanaugh D, et al. Short-term outcomes of lateral lumbar interbody fusion without decompression for the treatment of symptomatic degenerative spondylolisthesis at L4-5. Neurosurg Focus. 2018;44(1):E6. doi: 10.3171/2017.10.FOCUS17566
Castellvi AE, Nienke TW, Marulanda GA, et al. Indirect decompression of lumbar stenosis with transpsoas interbody cages and percutaneous posterior instrumentation. Clin Orthop Relat Res. 2014;472(6):1784-1791. doi: 10.1007/ s11999-014-3464-6
Dominguez I, Luque R, Noriega M, et al. Extreme lateral lumbar interbody fusion. Surgical technique, outcomes and complications after a minimum of one year follow-up. RevEsp Cir Ortop Traumatol. 2017;61(1):8-18. doi: 10.1016/j. recot.2016.09.001
Formica M, Berjano P, Cavagnaro L, et al. Extreme lateral approach to the spine in degenerative and post traumatic lumbar diseases: selection process, results and complications. Eur Spine J. 2014;23 Suppl 6:684-692. doi: 10.1007/ s00586-014-3545-y
Kepler CK, Sharma AK, Huang RC, et al. Indirect foraminal decompression after lateral transpsoas interbody fusion. J Neurosurg Spine. 2012;16(4):329-333. doi: 10.3171/2012.1.SPINE11528
Marchi L, Abdala N, Oliveira L, et al. Radiographic and clinical evaluation of cage subsidence after stand-alone lateral interbody fusion. J Neurosurg Spine. 2013;19(1):110-118. doi: 10.3171/2013.4.SPINE12319
Navarro-Ramirez R, Berlin C, Lang G, et al. A New Volumetric Radiologic Method to Assess Indirect Decompression After Extreme Lateral Interbody Fusion Using High-Resolution Intraoperative Computed Tomography. World Neurosurg. 2018;109:59-1067. doi: 10.1016/j.wneu.2017.07.155
Pereira EA, Farwana M, Lam KS. Extreme lateral interbody fusion relieves symptoms of spinal stenosis and low- grade spondylolisthesis by indirect decompression in complex patients. J Clin Neurosci. 2017;35:56-61. doi: 10.1016/j. jocn.2016.09.010
Tessitore E, Molliqaj G, Schaller K, Gautschi OP. Extreme lateral interbody fusion (XLIF): A single-center clinical and radiological follow-up study of 20 patients. J Clin Neurosci. 2017;36:76-79. doi: 10.1016/j.jocn.2016.10.001
Tohmeh AG, Khorsand D, Watson B, Zielinski X. Radiographical and clinical evaluation of extreme lateral interbody fusion: effects of cage size and instrumentation type with a minimum of 1-year follow-up. Spine (Phila Pa 1976). 2014;39(26):E1582-E1591. doi: 10.1097/BRS.0000000000000645
Nakashima H, Kanemura T, Satake K, et al. Indirect Decompression on MRI Chronologically Progresses After Immediate Postlateral Lumbar Interbody Fusion: The Results From a Minimum of 2 Years Follow-Up. Spine (Phila Pa 1976). 2019;44(24):E1411-E1418. doi: 10.1097/BRS.0000000000003180
Ohtori S, Orita S, Yamauchi K, et al. Change of Lumbar Ligamentum Flavum after Indirect Decompression Using Anterior Lumbar Interbody Fusion. Asian Spine J. 2017;11(1):105-112. doi: 10.4184/asj.2017.11.1.105
Dangelmajer S, Zadnik PL, Rodriguez ST, et al. Minimally invasive spine surgery for adult degenerative lumbar scoliosis. Neurosurg Focus. 2014;36(5):E7. doi: 10.3171/2014.3.FOCUS144
Sharma AK, Kepler CK, Girardi FP, et al. Lateral lumbar interbody fusion: clinical and radiographic outcomes at 1 year: a preliminary report. J Spinal Disord Tech. 2011;24(4):242-250. doi: 10.1097/BSD.0b013e3181ecf995
Li J, Li H, Zhang N, et al. Radiographic and clinical outcome of lateral lumbar interbody fusion for extreme lumbar spinal stenosis of Schizas grade D: a retrospective study. BMC Musculoskelet Disord. 2020;21(1):259. doi: 10.1186/ s12891-020-03282-6
Formica M, Quarto E, Zanirato A, et al. Lateral Lumbar Interbody Fusion: What Is the Evidence of Indirect Neural Decompression? A Systematic Review of the Literature. HSSJ. 2020;16(2):143-154. doi: 10.1007/s11420-019-09734-7
Lang G, Perrech M, Navarro-Ramirez R, et al. Potential and Limitations of Neural Decompression in Extreme Lateral Interbody Fusion-A Systematic Review. WorldNeurosurg. 2017;101:99-113. doi: 10.1016/j.wneu.2017.01.080
Shimizu T, Fujibayashi S, Otsuki B, et al. Indirect decompression with lateral interbody fusion for severe degenerative lumbar spinal stenosis: minimum 1-year MRI follow-up. J Neurosurg Spine. 2020;33(1):27-34. doi: 10.3171/2020.1.SPINE191412
Elowitz EH, Yanni DS, Chwajol M, et al. Evaluation of indirect decompression of the lumbar spinal canal following minimally invasive lateral transpsoas interbody fusion: radiographic and outcome analysis. Minim Invasive Neurosurg. 2011;54(5-6):201-6. doi: 10.1055/s-0031-1286334
Walker CT, Xu DS, Cole TS, et al. Predictors of indirect neural decompression in minimally invasive transpsoas lateral lumbar interbody fusion. J Neurosurg Spine. 2021;35(1):80-90. doi: 10.3171/2020.8.SPINE20676
Angel Roldan M, Atalay B, Navarro-Ramirez R, et al. Excessive Fluid in the Lumbar Facet Joint as a Predictor ofRadiological Outcomes After Lateral Lumbar Interbody Fusion. Cureus. 2022;14(10):e30217. doi: 10.7759/cureus.30217
Oliveira L, Marchi L, Coutinho E, Pimenta L. A radiographic assessment of the ability of the extreme lateral interbody fusion procedure to indirectly decompress the neural elements. Spine (Phila Pa 1976). 2010;35(26 Suppl):S331-S337. doi: 10.1097/BRS.0b013e3182022db0
Manzur MK, Samuel AM, Morse KW, et al. Indirect Lumbar Decompression Combined With or Without Additional Direct Posterior Decompression: A Systematic Review. Global Spine J. 2022;12(5):980-989. doi: 10.1177/21925682211013011
Василенко И.И., Евсюков А.В., Рябых С.О. и др. Лечение пациентов с дегенеративными деформациями поясничного отдела позвоночника с использованием MIS-технологий: анализ 5-летних результатов. Хирургия позвоночника. 2022;19(4):52-59. doi: 10.14531/ss2022.4.52-59
Hiyama A, Katoh H, Sakai D, et al. The Analysis of Preoperative Roussouly Classification on Pain Scores and Radiological Data in Lateral Lumbar Interbody Fusion for Patients with Lumbar Degenerative Disease. World Neurosurg. 2023;175:e380-e390. doi: 10.1016/j.wneu.2023.03.102
Kirnaz S, Navarro-Ramirez R, Gu J, et al. Indirect Decompression Failure After Lateral Lumbar Interbody Fusion-Reported Failures and Predictive Factors: Systematic Review. Global Spine J. 2020;10(2 Suppl):8S-16S. doi: 10.1177/2192568219876244
Spirig JM, Farshad M. CME: Lumbar spinal stenosis.Praxis (Bern 1994). 2018;107(1):7-15. (In German) doi: 10.1024/1661- 8157/a002863
Epstein NE. Review of Risks and Complications of Extreme Lateral Interbody Fusion (XLIF). Surg Neurol Int. 2019;10:237. doi: 10.25259/SNI_559_2019
Hlubek RJ, Eastlack RK, Mundis GM Jr. Transpsoas Approach Nuances. Neurosurg Clin N Am. 2018;29(3):407-417. doi: 10.1016/j.nec.2018.02.002
Статья поступила 10.06.2024; одобрена после рецензирования 09.07.2024; принята к публикации 21.10.2024.
The article was submitted 10.06.2024; approved after reviewing 09.07.2024; accepted for publication 21.10.2024.
Информация об авторах:
Илья Дмитриевич Исаков — младший научный сотрудник
Абдугафур Джабборович Сангинов — научный сотрудник
Шамиль Альфирович Ахметьянов — научный сотрудник
Евгений Андреевич Мушкачев — младший научный сотрудник
Артем Николаевич Сорокин — научный сотрудник
Алексей Владимирович Пелеганчук — старший научный сотрудник
Теги: дегенеративный стеноз позвоночного канала
234567 Начало активности (дата): 09.03.2025
234567 Кем создан (ID): 989
234567 Ключевые слова: дегенеративный стеноз позвоночного канала, прямой боковой спондилодез, непрямая декомпрессия, предикторы непрямой декомпрессии
12354567899
Похожие статьи
Результаты хирургического лечения дегенеративного стеноза позвоночного канала у пожилых пациентовРентген на дому 8 495 22 555 6 8
Оценка качества работы искусственного интеллекта в выявлении дегенеративных заболеваний пояснично-крестцового отдела позвоночника
Оценка качества работы искусственного интеллекта в выявлении дегенеративных заболеваний пояснично-крестцового отдела позвоночника
Использование диффузионнотензорной магнитнорезонансной эндоскопическом удалении грыжи шейного отдела позвоночника. Клинические наблюдения



