 02.09.2023
02.09.2023
Малигнизация при хроническом остеомилите бедра:клинический случай
Хронический остеомиелит - широко распространенное заболевание, но малигнизация является редким и поздним его осложнением
ВВЕДЕНИЕ
Хронический остеомиелит является одним из тяжелейших посттравматических осложнений при лечении переломов длинных костей. Больные нередко подвергаются многократным оперативным вмешательствам, оставаясь неизлеченными десятки лет. Процент инва- лидизации больных хроническим остеомиелитом остается высоким и составляет от 50 до 90 % [1]. По данным разных авторов, в структуре переломов всех костей скелета на долю бедренной кости приходится от 15 до 45 % случаев [2, 3]. Среди инвалидов с гнойной патологией костей и суставов больные с посттравматическим остеомиелитом бедренной кости составляют до 18,7 % [4].
Злокачественные опухоли, возникающие при хроническом остеомиелите, являются редким и слабо изученным поздним осложнением. Наиболее частым злокачественным новообразованием является плоскоклеточный рак, развивающийся спустя десятилетия после постановки диагноза хронического остеомиелита. Проведенные ранее исследования показали, что длительность течения остеомиелита находится в прямой зависимости от количества выявленных случаев малигнизации, период манифестации, по данным разных авторов, составил от 24,5 до 49,2 года от начала заболевания [5-8].
Причины малигнизации при хроническом остеомиелите малоизучены, точный механизм злокачественной трансформации остается неизвестным. Известно, что воспаление и/или инфекция способствуют инициации процесса канцерогенеза. В случае развития хронического воспаления риск образования опухолевых клеток увеличивается [9].
Злокачественная трансформация начинается в коже или эпителии свищевых ходов и инфильтрирует прилежащие ткани, в том числе кости. Увеличение отделяемого из свищевого хода, а также персистенция, экзофитная форма роста язвы или образования могут быть предвестниками злокачественной трансформации [7, 10].
Ранняя диагностика и своевременное лечение злокачественной трансформации хронического остеомиелита имеют решающее значение для прогноза и конечных результатов лечения.
Цель - представить клинический случай злокачественной трансформации спустя 34 года после постановки диагноза хронического остеомиелита бедра.
МАТЕРИАЛЫ И МЕТОДЫ
Анализ истории болезни и патоморфологическое исследование операционного материала пациента Д. Исследование выполнено в соответствии с этическими нормами Хельсинкской декларации 1975 г., пересмотренными в 2013 г., одобрено этическим комитетом учреждения. Пациент дал добровольное информированное согласие на публикацию результатов исследования без раскрытия личности.
Операционный материал (фрагменты корковой пластинки, свободно лежащей губчатой кости, содержимое костномозговой полости) фиксировали в 10 % растворе нейтрального формалина, частично декальцинировали в смеси соляной и муравьиной кислот. Затем образцы подвергали стандартной гистологической обработке, дегидратировали в спиртах восходящей концентрации, пропитывали уплотняющей смесью и заливали в парафин. На санном микротоме фирмы «Reichert» (Австрия) изготавливали гистологические срезы толщиной 5-7 мкм, которые окрашивали гематоксилином и эозином. Исследование микропрепаратов и микрофотосъемку проводили с использованием стереомикроскопа «AxioScope.A1» с цифровой камерой «AxioCam» с программным обеспечением «Zenblue» (CarlZeissMicroImagingGmbH, Германия).
РЕЗУЛЬТАТЫ
Больной Д., 58 лет, обратился в Клинику костно-суставной инфекции в 2019 году с жалобами на наличие свищевого хода с гнойным отделяемым, боли в левом бедре, нарушение функции левой нижней конечности.
An. morbi. В 1987 году в результате ДТП получил открытый оскольчатый перелом левой бедренной кости, проводилось скелетное вытяжение в течение месяца. Рана зажила. Через 1 месяц открылся свищевой ход. Выполнен дебридмент, интрамедуллярный остеосинтез, установлены серкляжные швы. Через 1 месяц после операции - повышение температуры тела, сопровождающееся болевым синдромом. Потребовалось вскрытие и дренирование, удаление интрамедуллярного стержня, серкляжной проволоки. Через 2 месяца вновь открылся свищевой ход, оперирован через 5 лет после травмы, операция в виде остеонекрэктомии. Эффект не был достигнут, далее пациент получал консервативное лечение. В течение последних 6 месяцев беспокоили боли в вечернее и ночное время в нижней трети левого бедра. Было проведено несколько хирургических вмешательств с забором операционного материала для патоморфологического исследования, при морфологических исследованиях признаки остеомиелита, без малигнизации.
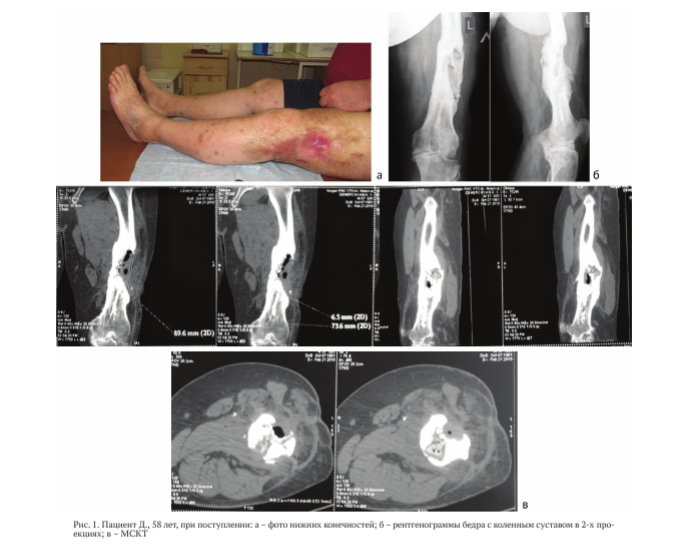
St. localis при поступлении. Ходит при помощи трости, хромает на левую ногу. Свищевой ход на границе средней и нижней трети левого бедра с гнойным отделяемым, идущий в глубину тканей. На уровне свищевого хода по передней поверхности определяется мягкотканное образование (рис. 1, а), при пальпации болезненное.
Отек левого бедра + 5 см. Укорочение левой нижней конечности на 3 см. Движения в левом коленном суставе: качательные с установкой в положении разгибания 180 гр.
На рентгенограммах левого бедра в 2-х проекциях: консолидированный перелом дистального отдела левой бедренной кости, неоднородность, дефект костной ткани по латеральной поверхности диафиза с выраженной периостальной реакцией на данном уровне. Остеопороз (рис. 1, б).
Мультиспиральная компьютерная томография (МСКТ). Полость в средней трети костномозгового канала бедренной кости с неровным внутренним контуром, протяженностью до 9 см, и на этом протяжении дефект кортикальной пластинки по передненаружной поверхности. Плотность кортикала на уровне полости около 1100 ед. Н. В задних отделах кортикала дефект, замещенный пористым субстратом, размером 2 х 2 х 35 см (губчатая кость имплантат). В центральных отделах дистального метадиафиза линейный аваскулярный секвестр размером 0,65 х 7,5 см (рис. 1, в).
Бактериологическое исследование отделяемого свищевого хода: Pseudomonas aeruginosa 5 х 10 х 4 КОЕ/мл.
Пациенту в Кинике костно-суставной инфекции выполнили операцию: ревизия свищевого хода левого бедра. Остеонекрэктомия (дебридмент). Ультразвуковая кавитация, при которой был продлен дефект кортикальной стенки для лучшей визуализации. В костномозговом канале присутствовал неприятный запах, патологическая грануляционная ткань, секвестры, внутренний кортикальный слой был поражен остеомиелитическим процессом. Остеонекрэктомия была выполнена с забором материала на гистологическое (кортекс на уровне полости, содержимое костномозгового канала) и микробиологическое исследование. Аваскулярный дистальный секвестр, ввиду незадействия в воспалительном процессе, не был удален.
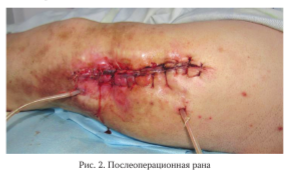
После операции была получена внутриканальная полость объемом 75 мл. Операция закончилась обработкой костномозгового канала пульс-ловажем с раствором ловасепта и установкой двух дренажей навстречу друг другу (рис. 2). Бактериологическое исследование показало отсутствие роста грибов и анаэробной флоры, вновь был выявлен Pseudomonas aeruginosa. Получал антибиотикотерапию согласно чувствительности микроорганизма. На 7-е сутки после операции появился неприятный запах содержимого дренажа. Установка проточно промывной системы не привела к разрешению процесса.
Выполнена повторная МСКТ. Полость в костномозговом канале нижней трети протяженностью до 14 см с дефектом кортикальной пластинки по наружной поверхности. Контур полости четкий, неровный. По внутренней поверхности костномозгового канала формирующиеся мелкие аваскулярные секвестры. В метаэпифизе линейный асептический секвестр до 4,3 см. Была выполнена ревизия раны с остеонекрэктомией. Удалены мелкие крошковидные секвестры, асептический секвестр. Взяты материалы на гистологические и бактериологические исследования. На 21-е сутки после операции был вскрыт гнойный затек. Пациента выписали для наблюдения к травматологу-ортопеду по месту жительства на период отделения аваскулярных секвестров.
В метаэпифизе линейный асептический секвестр до 4,3 см. Была выполнена ревизия раны с остеонекрэктомией. Удалены мелкие крошковидные секвестры, асептический секвестр. Взяты материалы на гистологические и бактериологические исследования. На 21-е сутки после операции был вскрыт гнойный затек. Пациента выписали для наблюдения к травматологу-ортопеду по месту жительства на период отделения аваскулярных секвестров.
Пациенту были выданы предметные стекла и фрагменты операционного материала с рекомендациями обратиться к онкологу.
При дальнейшей госпитализации в 2020 году продолжал функционировать свищевой ход с серозногнойным отделяемым (рис. 4), с неприятным зловонным запахом.
Со слов пациента онколог не подтвердил наличие злокачественного процесса. Заключение: исходя из обследования (КТ, цитологические и гистологические исследования, ПСА) убедительных данных за злокачественное новообразование левой бедренной кости нет.
При оперативном вмешательстве выявлены мелкие отдельно лежащие секвестры, внутренний кортикальный слой остеомиелитической полости был покрыт участками грануляционной ткани и мягкотканными образованиями белесоватого цвета, которые были взяты на гистологическое исследование. Также оперативное лечение не привело к ремиссии остеомиелитического процесса. В условиях центра выполнена МСКТ органов грудной клетки, органов брюшной полости и малого таза без и с контрастированием. Органы грудной клетки без видимой патологии. Жировая инфильтрация печени, поджелудочной железы. Взят ПСА, результат отрицательный.
Через 2 месяца после лечения развился патологический перелом диафиза бедренной кости. Дебридмент и установка антимикробного спейсера с фиксацией ортопедическим тутором не привели к ремиссии (рис. 5). Пациенту дважды была выполнена остеонекрэктомия по типу резекции до 7 см с остеосинтезом аппаратом Илизарова. Консолидация не достигнута (рис. 6).
При патоморфологическом исследовании операционного материала в 2020 году в полости костномозгового канала наблюдали признаки псевдокарци- номатозной гиперплазии, отмечен инвазивный рост эпителиальных тяжей (рис. 7, а), фигуры митотического деления встречались редко (рис. 7, б), избыточная кератинизация сопровождалась образованием «роговых жемчужин» - очагов гиперкератоза округлой формы с признаками незавершенной кератинизации в центре (рис. 7, в, г). Воспалительный инфильтрат лим- фогистиоцитарного типа с содержанием нейтрофилов. В губчатой кости наблюдали выраженную инвазию эпителиальных комплексов, костные микросеквестры и воспалительный инфильтрат (рис. 7, д). Отмечены обширные участки остеонекроза, в межтрабекулярных промежутках скопления чешуек плоского эпителия и воспалительный инфильтрат (рис. 7, е).
Для подтверждения диагноза нами было рекомендовано пациенту повторно обратиться в специализированную онкологическую клинику. В итоге в 2021 году по месту жительства провели ампутацию конечности на уровне верхней трети бедра. Обращает внимание наличие грамотрица- тельной микрофлоры при всех госпитализациях (Pseudomonas aeruginosa).
ОБСУЖДЕНИЕ
Анализ литературы показал, что продолжительность остеомиелитического процесса является основным фактором, связанным с началом канцерогенеза, с минимальным латентным периодом 20 лет и более. Бедренная, большеберцовая кости и кости стопы являются наиболее частыми локализациями гнойно-некротического процесса. Признаки, которые должны насторожить лечащего врача о злокачественной трансформации, включают усиление боли, выделений из свищевого хода, прогрессирующее разрушение и эрозия костей, растущая масса «опухолевого типа» в области раны [6, 7, 8, 11].
По данным N. Jiang et al. (2020), при анализе 167 наблюдений плоскоклеточный рак при хроническом остеомиелите конечности чаще всего возникал у пациентов с посттравматическим остеомиелитом в анамнезе [12].
В представленном клиническом случае после полученного в результате ДТП оскольчатого перелома левой бедренной кости в возрасте 25 лет развился длительно текущий хронический остеомиелит, завершившийся патологическим переломом в возрасте 59 лет, приведший к ампутации конечности. Обращает на себя внимание длительное безрецидивное течение остеомиелита на протяжении 34 лет, появление болевого синдрома в вечернее и ночное время в бедре, наличие грамотрицательной микрофлоры, наличие белесоватых мягкотканных масс на внутренней стенке остеомиелитической полости. При последней госпитализации пациента беспокоили выраженные боли в проекции гнойного очага, купируемые инъекциями раствора трамадола дважды в сутки.
Отмеченные нами структурные изменения костной ткани - некроз, фиброз костного мозга, костные микросеквестры, воспалительный инфильтрат с высоким содержанием нейтрофилов соответствовали морфологическим признакам хронического остеомиелита в стадии обострения. Патоморфологическая картина исследуемого операционного материала характеризовалась наличием псевдокарциноматозной гиперплазии, продолжительное существование которой может явиться причиной возникновения плоскоклеточного рака бедренной кости.
Установить, когда реактивная пролиферация эпидермиса приобретает принципиально иные биологические свойства злокачественной опухоли, клинически и гистологически не представляется возможным [13], что является серьезной проблемой в своевременной постановке диагноза.
Плоскоклеточная карцинома характеризуется внутриэпидермальной пролиферацией атипичных кератиноцитов, при хроническом остеомиелите обычно имеет низкую степень злокачественности [14].
Известно, что у пациентов с иммуносупрессией плоскоклеточный рак встречается чаще и протекает более агрессивно. По данным T. Kurihara, при хроническом остеомиелите инвазия плоскоклеточного рака в кость из мягких тканей и костномозговой полости происходит в 77 % случаев [15].
В 2019 году в операционном материале нами были выявлены комплексы плоскоклеточного инвазивного роста, в 2020 году отмечено массовое появление «роговых жемчужин» и инвазия плоского эпителия костной ткани, при этом клетки плоского эпителия представлялись высокодифференцированными, в межтрабекулярных пространствах массовое скопление эпителиальных чешуек. Усиление признаков агрессивности инвазивного роста плоского эпителия в полости свищей и распространение процесса в костную ткань с формированием «роговых жемчужин» свидетельствовало об озлокачествлении процесса.
В представленном клиническом случае развитие плоскоклеточной неоплазии происходило по высокодифференцированному типу. Опухоль из эпителиальной ткани кожной язвы по костномозговой полости инвазировала костную ткань.
Патогенез малигнизации изучен недостаточно, наиболее широко распространенная теория сосредоточена на хроническом воспалительном состоянии [12, 16]. Микробная инфекция характеризуется горизонтальным переносом генов и последующими латентными мутациями, которые нарушают иммунный ответ. Имеются данные о том, что карциноматозная трансформация может следовать за изменением бактериальной флоры. Грам- положительная флора может быть заменена преобладающей грамотрицательной флорой, которая продуцирует эндотоксины, связанные с канцерогенезом [17].
Для предотвращения местной инвазии и метастатического распространения не следует откладывать лечение. Наиболее эффективным методом лечения в этих случаях является ампутация конечности, широкая резекция показана только у отдельных пациентов [18, 19, 20].
ЗАКЛЮЧЕНИЯ
Представлен редкий клинический случай малигнизации при хроническом остеомиелите бедренной кости через 34 года после первоначального перелома и инфекции. Опухоль из эпителиальной ткани кожной язвы по костномозговой полости инвазировала костную ткань. Тщательная патологоанатомическая оценка материала из участков поражения - язвы, свищевого хода, костномозгового пространства - необходима для раннего выявления злокачественных новообразований, возникающих при остеомиелите. Наличие длительной динамики псев- докарциноматозной гиперплазии требует настороженности в отношении процесса озлокачествления.
СПИСОК ИСТОЧНИКОВ
1. Миронов С.П., Цискарашвили А.В., Горбатюк Д.С. Хронический посттравматический остеомиелит как проблема современной травматологии и ортопедии (обзор литературы). Гений ортопедии. 2019;25(4):610-621. doi 10.18019/1028-4427-2019-25-4-610-621
2. Клевно В.А., Новоселов А.С. Анализ и структура переломов длинных трубчатых костей. Медлайн.ру. 2003;4:71-72.
3. Апагуни А.Э. Ошибки и осложнения оперативного лечения диафизарных переломов бедренной кости. Травматология и ортопедия России. 2005;(1):38-39.
4. Мироманов А.М., Борзунов Д.Ю. Доклиническая диагностика хронического травматического остеомиелита при переломах длинных костей конечностей. Гений ортопедии. 2012;(4):21-23.
5. Altay M, Arikan M, Yildiz Y, Saglik Y. Squamous cell carcinoma arising in chronic osteomyelitis in foot and ankle. Foot Ankle Int. 2004 Nov;25(11):805-809. doi: 10.1177/107110070402501109
6. Alami M, Mahfoud M, El Bardouni A, Berrada MS, El Yaacoubi M. Squamous cell carcinoma arising from chronic osteomyelitis. Acta Orthop Traumatol Turc. 2011;45(3):144-148. doi: 10.3944/AOTT.2011.2537
7. Moura DL, Ferreira R, Garru^o A. Malignant transformation in chronic osteomyelitis. Rev Bras Ortop. 2017 Mar 8;52(2):141-147. doi: 10.1016/j. rboe.2017.03.005
8. Клюшин Н.М., Судницын А.С., Мигалкин Н.С., Ступина Т.А., Суворов Н.Р. Малигнизация при хроническом остеомиелите стопы и голеностопного сустава (серия случаев). Гений ортопедии. 2019;25(4):517-522.
9. Свитич О.А., Филина А.Б., Давыдова Н.В., Ганковская Л.В., Зверев В.В. Роль факторов врожденного иммунитета в процессе опухолеобразования. Медицинская иммунология. 2018;20(2):151-162.
10. Chagou A, Benameur H, Alidrissi N, Chahbouni M, Zine A, Bouabid S, Boussougua M, Jaafar A. Carcinome epidermoide survenant sur une lesion d’osteomyelite chronique: rapport de cas [Squamous cell carcinoma in a patient with chronic osteomyelitic lesion: a case report]. Pan Afr Med J. 2020 Dec 3;37:307. French. doi: 10.11604/pamj.2020.37.307.22388
11. Khaladj M, Mbibong RM, Shah N, Mohiuddin A, Siddiqui A. Invasive squamous cell carcinoma with osteomyelitis of the foot a case report. J Am Podiatr Med Assoc. 2015 Jul;105(4):374-376. doi: 10.7547/14-049.1
12. Jiang N, Li SY, Zhang P, Yu B. Clinical characteristics, treatment, and prognosis of squamous cell carcinoma arising from extremity chronic osteomyelitis: a synthesis analysis of one hundred and seventy six reported cases. Int Orthop. 2020 Nov;44(11):2457-2471.
13. Федотов В.П. Псевдорак кожи (клиническая лекция). Дерматовенерология. Косметология. Сексопатология. 2015;(1-2):45-57.
14. Caruso G, Gerace E, Lorusso V, Cultrera R, Moretti L, Massari L. Squamous cell carcinoma in chronic osteomyelitis: a case report and review of the literature. J Med Case Rep. 2016 Aug 4;10:215. doi: 10.1186/s13256-016-1002-8
15. Kurihara T, Suehara Y, Akaike K, Hayashi T, Okubo T, Kim Y, Takagi T, Kaneko K, Yao T, Saito T. Squamous cell carcinoma arising from chronic osteomyelitis massively expanding into the medullary cavity: A case report. Human Pathology: Case Reports. 2019;16:100289. doi: 10.1016/j. ehpc.2019.01.008
16. Kerr-Valentic MA, Samimi K, Rohlen BH, Agarwal JP, Rockwell WB. Marjolin's ulcer: modern analysis of an ancient problem. Plast Reconstr Surg. 2009 Jan;123(1):184-191. doi: 10.1097/PRS.0b013e3181904d86
17. Zou J, Guo P, Lv N, Huang D. Lipopolysaccharide-induced tumor necrosis factor-а factor enhances inflammation and is associated with cancer (Review). Mol Med Rep. 2015 Nov;12(5):6399-6404. doi: 10.3892/mmr.2015.4243
18. Li Q, Cui H, Dong J, He Y, Zhou D, Zhang P, Liu P. Squamous cell carcinoma resulting from chronic osteomyelitis: a retrospective study of 8 cases.
Int J Clin Exp Pathol. 2015 Sep 1;8(9):10178-84.
19. Panteli M, Giannoudis PV. Chronic osteomyelitis: what the surgeon needs to know. EFORT Open Rev. 2017 Mar 13;1(5):128-135. doi: 10.1302/2058- 5241.1.000017
20. Su YD, Shen PY. Intraosseous squamous cell carcinoma arising from chronic osteomyelitis: a case report and review of the literature. Biomed J Sci & Tech Res, 2019;17(5):13167-13170. doi: 10.26717/BJSTR.2019.17.003077
Информация об авторах:
1. Александр Леонидович Шастов - кандидат медицинских наук
2. Татьяна Анатольевна Ступина - доктор биологических наук
3. Николай Сергеевич Мигалкин
Теги: хронический остеомиелит
234567 Начало активности (дата): 02.09.2023 21:57:00
234567 Кем создан (ID): 989
234567 Ключевые слова: хронический остеомиелит, бедренная кость, псевдокарциноматозная гиперплазия, малигнизация
12354567899
Похожие статьи
Рентген на дому 8 495 22 555 6 8Малигнизация при хроническом остеомилите бедра:клинический случай
Особенности структурных изменений дистального суставного конца бедренной кости при экспериментальном моделировании остеомиелита
Способ моделирования хронического травматического остеомиелита



