 14.05.2022
14.05.2022
Особенности ортопедической патологии у больных нейрофиброматозом I типа
Нейрофиброматоз 1-го типа (НФ1) - наследственный опухолевый синдром, встречающийся с частотой 1:3000 населения в мире. Помимо нейрофибром и пигментных пятен на коже, у 60,0 % больных НФ1 развиваются скелетные аномалии.
ВВЕДЕНИЕ
Нейрофиброматоз 1-го типа (НФ1) является самым распространенным аутосомно-доминантным наследственным опухолевым синдромом. Частота встречаемости НФ1 в среднем по миру составляет 1:3000 населения. Болезнь развивается вследствие наследуемых герминативных гетерозиготных мутаций в онкосупрессорном гене NF1. Около 50,0 % случаев болезни - спорадические, обусловленные мутациями de novo, что говорит о высокой мутабельности гена NF1. Продукт гена, белок нейрофибромин, негативно регулирует активность онкогенов Ras за счет гидролиза их активных ГТФ-связанных форм в неактивные ГДФ-связанные. Соответственно, мутации в гене NF1 приводят к стимуляции Ras и усиленной пролиферации клеток с формированием доброкачественных (нейрофибром, глиом) и злокачественных опухолей [1].
К диагностическим критериям НФ1 относятся:
1) 6 или более пятен цвета кофе-с-молоком (CALM - cafe-au-lait macules) диаметром более 5 мм в допубертате и более 15 мм в постпубертате;
2) веснушчатость в подмышечной или паховой областях;
3) две
или более кожных нейрофибром или одна
плексиформная нейрофиброма; 4) две или
более гамартомы радужки глаза (узелки
Лиша); 5) глиома зрительного нерва;
6)
специфические костные дисплазии;
7) наличие НФ1 у родственников 1 степени родства [2]. Диагноз НФ1 устанавливается при наличии двух из 7 диагностических критериев, к которым относятся также специфические скелетные аномалии [3], такие как дисплазия крыла клиновидной кости, истончение кортикального слоя длинных трубчатых костей, врожденный псевдоартроз большеберцовой кости (ВПБК) [2].
Для больных НФ1 характерны пятна цвета кофе-с-молоком (cafe-au-lait macule - CALM), которые являются опухолеподобными образованиями, развивающимися вследствие инактивации второго аллеля NF1 в меланоцитах. Последние, как и клетки Шванна, происходят от общих предшественников нервного гребня [4]. К опухолевидным образованиям, характерным для НФ1, относятся гамартомы радужной оболочки глаз, которые встречаются у 70,0 % пациентов [5], а также «фиброзные гамартомы» длинных трубчатых костей, вызывающие развитие ВПБК [6]. Клиническая картина НФ1 характеризуется разнообразием проявлений и их распространенностью. У 99,0 % больных НФ1 определяются CALM, у 90,0 % - веснушчатость, у 81,0 % - проблемы с поведением (до 40,0 % - синдром дефицита внимания и гиперактивности) [7], у 5,4 % - эпилепсия [8], у 2,0 % - мальформация Арнольда-Киари [9]. При НФ1 частота встречаемости нейрофибром составляет 40,0-60,0 %, нарушений интеллекта - до 30,0-65,0 %, плексиформных нейрофибром - 30,0-50,0 %, глиом зрительных нервов -15,0-20,0 %, злокачественных опухолей из оболочек периферических нервов (MPNST) - 8,0-13,0 % [5].
У 60,0 % больных НФ1
определяется поражение опорно-двигательной
системы (ОДС), из которых наиболее часто
встречаются деформации позвоночника
и ВПБК. Для лечения тяжелых форм данной
патологии применяются хирургические
методы в связи с неэффективностью
консервативной терапии [10]. ВПБК
диагностируется у 5,0 % пациентов с НФ1
[7].
Черепно-лицевые аномалии развития
определяются у большинства больных,
включая уменьшение нижней челюсти (53,0
%) [11], гипертелоризм (63,5 %) [12], увеличенную
окружность головы (25,0 %), асимметрию лица
(10,0 %). Характерная для болезни дисплазия
крыла клиновидной кости выявляется в
5,0 - 12,0 % случаев НФ1 [13].
О поражении ОДС свидетельствует задержка роста. Дети с НФ1 нормально растут до полового созревания, после чего скорость удлинения тела уменьшается по сравнению со здоровыми сверстниками. Низкий рост определяется у 18,0-30,0 % взрослых пациентов с НФ1, для которых характерна более высокая частота серьезных осложнений, таких как выраженный сколиоз, опухоли ЦНС и плексиформные нейрофибромы [14].
У 50,0 % больных НФ1 развивается остеопороз, что приводит к значительному увеличению частоты переломов [1]. Ситуация осложняется тем, что при НФ1 наблюдается дефицит в выполнении ряда функциональных задач, значительное нарушение баланса, мышечной силы и координации верхних конечностей. Характерны недостаток времени реакции и моторики, умеренный дефицит ловкости рук и равновесия, нарушение походки [3]. Деформация грудной клетки выявляется у 37,6 % [12], позвоночника (сколиоз, кифоз) - от 21,0-49,0 % [7] до 60,0 % больных НФ1 [10]. Прогностически неблагоприятными являются дистрофические аномалии (ротация, клиновидная или зубчатая деформация позвонков, расширение спинномозгового канала, веретенообразные поперечные отростки) так как они приводят к прогрессированию патологии с серьезными искривлениями позвоночника. В связи с этим при данной патологии показано раннее хирургическое лечение. Генетические исследования всех случаев ВПБК в общей популяции показали, что большинство из них (80,0 %) ассоциированы с НФ1 [10].
Целью данной статьи является определение механизмов развития патологии ОДС при НФ1 на молекулярном уровне, выявление возможного влияния особенностей мутаций в гене NF1 и генов-модификаторов на развитие скелетных аномалий.
Новые данные могли бы стать основой для разработки эффективных методов профилактики и лечения болезни с учетом полученных данных молекулярно-генетических исследований.
МАТЕРИАЛЫ И МЕТОДЫ
Использованы статьи, представленные в базах данных PubMed , Scopus, Web of Science преимущественно за последние 5 лет. Проведен поиск по ключевым словам с различными комбинациями «neurofibromatosis type 1» со словами «skeletal abnormalities», «musculoskeletal system», «pseudarthrosis», «scoliosis», «pathogenesis», «deformation», «treatment», «frequency», «prevalence», «genotype-phenotype correlation», «genes modifiers».
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Патогенез скелетных аномалий при нейрофибро-матозе I типа
Точные механизмы развития очаговых костных поражений при НФ1 пока неизвестны, однако нет сомнений, что в их развитии участвуют изменения сигнальных путей, вызванные дефицитом нейрофибромина. В норме NF1 экспрессируется остеобластами, остеокластами, хондроцитами, фибробластами и эндотелиальными клетками сосудов. Находящиеся под негативным регуляторным контролем нейрофибромина белки Ras необходимы для нормального формирования черепнолицевых структур, поскольку челюсти и основание черепа развиваются, главным образом, из нервного гребня [13]. Нейрофибромин играет роль в росте и метаболизме скелетной мускулатуры, поэтому при НФ1 наблюдается сниженная мышечная масса и слабость [3]. Кроме того, деформации костей при НФ1 часто могут быть вторичными вследствие прорастания плексиформных нейрофибром и давления их массой на окружающие ткани [15].
Механизм развития патологии ОДС при НФ1 может быть обусловлен взаимосвязями гена NF1 с различными молекулами, поскольку нейрофибромин содержит несколько функциональных доменов. Основным является GAP-связанный домен (GRD - GAP-related domain), который регулирует пути MAPK и PIK3/AKT/mTOR путем воздействия на их активатор Ras. Однако при дефиците нейрофибромина репрессируется транскрипционный фактор ZNF423 и активируется связанный с эпителиально-мезенхимальным переходом фактор, что говорит о роли NF1 в транскрипционной регуляции [16]. По одну сторону от GRD расположены цистеин-серин-богатый домен (cysteine-serine-rich domain - CSRD) и тубулин-связанный домен (tubulin-binding domain - TBD). Домен CSRD связывается с диметиламиногидролазой диметиларгинина (dimethylarginin dimethylaminohydrolase 1 -DDAH1). TBD взаимодействует с тубулином и LRPPRC (leucine-rich pentatricopeptide motif-containing protein). По другую сторону от GRD расположено несколько доменов: SEC14 (связывается с фосфолипидами и LIM-киназой 2); PH (pleckstrin homology domain - домен гомологии плекстрина - взаимодействует с валозин-содержащим белком и LIM-киназой 2); CTD (carboxy-terminal domain - С-концевой домен - связывается с дигидропиримидиназ-связанным белком 2 (DPYSL2), киназой фокальной адгезии (FAK) и DDAH1); SBD (syndecan-binding domain - синдекан-связанный домен - взаимодействует с синдеканом). Домены SEC14 и РН вызывают ингибирование LIM-киназы 2 с помощью RHO-ассоциированной протеинкиназы, которая модулирует актиновый цитоскелет [17]. Таким образом, комплексная структура нейрофибромина и наличие нескольких доменов, связывающихся с различными молекулами, является причиной сложного патогенеза НФ1 и развития скелетных аномалий, что отражается в выраженном клиническом полиморфизме болезни [18, 19].
Развитие остеопороза у половины больных НФ1 обусловлено дефектным костным метаболизмом остеобластов. Кроме того, играет роль врожденный дефицит нейрофибромина в гематопоэтических клетках и остеокластах, которые становятся нечувствительными к бис-фосфонатам [1]. Исследование клеток ВПБК показало инактивацию второго аллеля NF1 у всех больных, что свидетельствует о роли активации сигнальных путей Ras в развитии данной патологии [20], а также о перспективности применения эффективных методов лечения опухолевого синдрома (с помощью ингибиторов MEK) для терапии ВПБК. Более того, потеря гетерози-готности NF1 выявляется в образцах тканей позвонков, полученных при хирургическом лечении сколиоза при НФ1 [21]. Профилирование транскриптомов показало, что в клетках псевдоартроза при НФ1 происходит повышенная экспрессия EREG (кодирует эпирегулин) и EGFR (рецептор эпидермального фактора роста). Это приводит к ингибированию остеогенной дифференци-ровки. Секвенирование мРНК отдельных остеоцитов позволило определить, что сверхэкспрессия EREG обусловлена мутациями второго аллеля гена NF1 без изменений экспрессии трансформирующего фактора роста бета (TGF01). В экспериментах на мышах было подтверждено данное явление, которое является консервативным для животных. Однако блокирование функции эпирегулина с помощью AG-1478 или EGFR с помощью позиотиниба не восстанавливало нормальной дифференцировки клеток, что свидетельствовало о необходимости поиска других путей воздействия на данную патологию [22]. Наиболее перспективно использование ингибиторов MEK, которые показали свою эффективность не только в лечении остеопороза при НФ1 [1], но и опухолевого синдрома [23].
Роль генов-модификаторов в развитии проявлений нейрофиброматоза I типа
Хотя клинические
проявления НФ1 характеризуются
значительной вариабельностью, не
доказано ассоциации специфических
симптомов болезни с определенным типом
мутации.
Более того, идентичная мутация
в гене NF1 может вызывать стертое течение
болезни у одних больных и тяжелые
проявления у других, даже у членов одной
семьи [18, 19]. В связи со сложной структурой
гена NF1 и взаимодействием его белкового
продукта с различными молекулами [17]
предполагается роль генов-модификаторов
в патогенезе НФ1.
Данное предположение
было высказано еще в 1993 году Easton et al. на
основании анализа корреляции симптомов
НФ1 у монозиготных близнецов и других
родственников [24].
Идентификация генов-модификаторов может послужить ключом для разработки эффективных методов терапии НФ1. Для решения данной задачи проводится как исследование специфических генов, так и секвенирование всего генома с учетом особенностей белок-кодирующих генов и некодирующих РНК [19]. Так, в качестве модификаторов туморогенеза при НФ1 определены специфические микроРНК miR-34a, miR-10b [25], miR-24 [26], miR-107 [27]. Экспрессия miR-204 снижена в тканях спорадических MPNST и у больных НФ1. В эксперименте на клеточных линиях MPNST in vitro и на мышах in vivo было показано, что восстановление уровней miR-204 значительно снижает пролиферацию, миграцию и инвазию опухолевых клеток. Данная микроРНК ингибирует Ras-сингалинг и является биомаркером для диагностики MPNST, а также кандидатной мишенью для разработки таргетной терапии данных опухолей [28]. В клетках MPNST, по сравнению с нейрофибромами, определено значительное повышение экспрессии miR-21, мишенью которой является белок запрограммированной гибели клеток PDCD4. Трансфекция ингибитора miR-21 в клеточные линии MPNST значительно повышала активность каспазы и подавляла рост клеток со стимуляцией экспрессии PDCD4. В результате индуцировался апоптоз, что позволяет рассматривать miR-21 в качестве мишени для таргетной терапии MPNST [29].
В тканях нейрофибром у больных НФ1 было определено значительное повышение экспрессии хемоки-нов CXCR4 в 120 раз и CXCL12 в 512 раз. Это говорит о значении генов CXCR4 и CXCR12 в развитии опухолей при НФ1 [30]. В результате проведенного сравнительного полногеномного поиска ассоциаций (GWAS) у больных НФ1 с разным количеством CALM было обнаружено влияние аллельного варианта гена RPS6KA2 (rs12190451) на развитие CALM. Ген RPS6KA2 фос-форилируется и активируется киназами ERK1/2 по сигнальным путям RAS-MAPK. В связи с этим предполагается, что RPS6KA2 служит в качестве гена-модификатора развития CALM при НФ1 [4]. Эксперименты на мышах показали роль гена ATM в инициации образования нейрофибром [31]. Мета-анализ результатов GWAS при НФ1 с использованием стратегий прямой и обратной генетики позволил сконструировать сети бе-лок-белковых взаимодействий для поиска потенциальных генов, вовлеченных в патогенез НФ1. В результате были определены 10 потенциальных генов-модификаторов в развитии НФ1: AKT1 (кодирует белок-гомолог вирусного онкогена V-Akt тимомы мышей), BRAF (кодирует серин-треониновую киназу B-Raf), EGFR (эпидермальный фактор роста), LIMK1 (содержащая LIM-мотив протеинкиназа), PAK1 (Р21-активируемая киназа 1), PTEN (Phosphatase and TENsin homolog), RAF1 (серин-треониновая киназа Raf-1), SDC2 (синде-кан), SMARCA4 (SWI/SNF Related, Matrix Associated, Actin Dependent Regulator Of Chromatin, Subfamly A, Member 4) и VCP (валозин-содержащий белок) [18].
О роли генов-модификаторов
в развитии НФ1 свидетельствуют особенности
«НФ1-микроделеционного синдрома», когда
теряется не только NF1, но и соседние
гены, проявления болезни более тяжелые
с врожденными пороками сердца, ранней
манифестацией и большим количеством
кожных нейрофибром, выраженной умственной
отсталостью [32]. В область ми-кроделеции
хромосомы 17q11.2 вовлечен ген HCA66, белковый
продукт которого взаимодействует с
онкосупрессором Apaf-1 (apoptic protease activating
factor-1).
Соответственно, при инактивации HCA66 клетки становятся менее восприимчивыми к апоптозу [19]. Другими кандидатными генами-модификаторами, расположенными в области микроделеции, могут служить CENTA2 (кодирует белок Arf-GAP с двойным фосфатным доменом), RAB11FIP4 (кодирует белок, взаимодействующий с семейством Rab11), C17orf79 (открытая рамка считывания хромосомы 17), UTP6 (кодирует малую субъединицу ядрышка) [32].
Влияние генов-модификаторов на специфические проявления НФ1 отражается в ассоциации патологии ОДС с другими признаками болезни. Так, у детей с плексиформными нейрофибромами определена комор-бидность с тяжелыми скелетными аномалиями. Преклинические исследования на мышах показали, что дефицит NF1 в клетках костных предшественниках нарушает гомеостаз пирофосфата MEK-зависимым образом, что изменяет минерализацию костей. Была выявлена повышенная экспрессия ANKH, наряду с Enpp1, в нейрофибромах мыши и человека. Ген ANKH кодирует трансмембранный белок, экспрессирующийся в суставах и играющий роль в развитии остеобластов и остеокластов [15]. В NF1 -дефицитных стромальных клетках костного мозга мышей (mBMSC) было отмечено снижение экспрессии гена щелочной фосфатазы ALPL [22]. В тканях нейрофибром выявлена низкая экспрессия гена коллагена COL14A1 [31]. У больных НФ1 с низким ростом чаще развиваются тяжелые осложнения, такие как опухоли головного мозга, крупные плексиформные нейрофибромы и тяжелый сколиоз. При этом наблюдается взаимосвязь наличия глиом зрительных нервов в сочетании с патологией ОДС с развитием данных осложнений [14]. Мутации в гене NF1 выявляются в среднем в 10,0 % всех спорадических злокачественных новообразований у людей, не страдающих НФ1. Более того, эти мутации могут быть драйверами канцерогенеза и инициировать резистентность опухоли к химиотерапии. В связи с этим, поскольку ген NF1 обладает повышенной мутабельностью [17], можно предположить, что соматические мутации в нем могут быть причиной развития патологии ОДС в общей популяции. Для подтверждения данного предположения необходимы молекулярно-генетические исследования клеток образцов тканей, взятых у пациентов во время хирургического лечения таких патологий, как псевдоартроз, фиброзная дисплазия, сколиоз, поскольку при НФ1 в подобных случаях выявляется биаллельная инактивация NF1 [20, 21].
Современное лечение скелетных аномалий при ней-рофиброматозе I типаНа заседании Международного
консорциума костных аномалий, спонсируемого
Детским фондом опухолей, в 2011 году были
разработаны концепции лечения ВПБК.
Хирургический подход заключается в
санации «фиброзной гамартомы» и
надкостницы до здоровой кости, жесткой
стабилизации врожденного псевдоартроза
и костной пластике аутогенным гребнем
подвздошной кости. У детей предпочтительно
применение аппарата Илизарова для
обеспечения последующего удлинения
кости [6]. В экспериментах на мышах с НФ1
было показано эффективное лечение ВПБК
с помощью комбинации ингибиторов MEK и
местного введения костного морфогенетического
белка (BMP2) в область псевдоартроза.
Планируется внедрение данного метода в клинику [33]. При тяжелой степени сколиоза с углом Кобба более 45° при НФ1 эффективно проведение хирургической коррекции задним доступом с использованием металлоконструкций высокой плотности третьего поколения [34]. При использовании стандартных методов хирургической коррекции сколиоза у больных НФ1 к редким осложнениям относятся случаи поломок стержня и винтов, проксимального перехода кифоза, феномен adding-on, смещение ствола и прогрессирование искривления [35].
Поскольку в патогенезе
скелетных аномалий при НФ1 участвуют
те же механизмы, что и при развитии
опухолевого синдрома (дефицит
нейрофибромина [1, 13], и присутствует
потеря гетерозиготности гена NF1 [20, 21]),
для лечения патологии ОДС могут быть
использованы те же подходы, что в терапии
неоплазм при НФ1. Наиболее перспективен
подход, направленный на ингибирование
сигнальных путей RAS с использованием
наиболее избирательных агентов, так
как некоторые препараты не показали
значимого эффекта в клинике. Например,
типифарниб, ингибитор фарнезилтрансферазы,
блокирующий RAS, при клиническом
исследовании на 62 больных НФ1 не оказал
влияния на прогрессирование плексиформных
нейрофибром по сравнению с плацебо
[36]. Однако выраженную эффективность
показали ингибиторы MEK в лечении как
плексиформных нейрофибром, так и
низкодифференцированных глиом. Первым
препаратом из этой группы, одобренным
FDA, стал селуметиниб [23], который
представляет собой небольшую молекулу,
действующую как АТФ-независимый ингибитор
митоген-активируемой протеинкиназы
(MEK-киназы 1 и 2), являющейся ключевым
медиатором активации пути RAS/RAF/MER/ERK
(усиленном при НФ1) [37]. В 2016 году опубликованы
данные Dombi et al. о результатах лечения 24
детей с НФ1 с помощью селуметиниба.
Наиболее распространенными токсическими
эффектами были угревая сыпь, бессимптомное
повышение креатинкиназы, поражение
желудочно-кишечного тракта. Пероральный
прием лекарства в дозе 25.0 мг на 1,0 м2 площади
тела проведен 28-дневными циклами. В
результате у 71,0 % детей определялось
снижение объема нейрофибром. Сходные
данные получены в экспериментах
(уменьшение размеров нейрофибром у 67,0
% мышей) [38]. Кроме того, на линии клеток
MPNST (NF1-/-) была показана эффективность
селуметиниба в комплексной терапии с
LDN-193189 (ингибитор рецептора BMP2 первого
типа), в то время как изолированное
применение LDN-193189 не давало должного
антипролиферативного эффекта.
Полученные результаты предполагают применение селу-метиниба в комплексной химиотерапии MPNST [39]. В 2020 году Baldo et al. исследовали 17 детей с ПН в течение 12 месяцев приема селуметиниба и оценили уменьшение размеров (более 20,0 % объема) опухолей у 16 из 17 больных НФ1 [37]. У 2 детей в последующем было отмечено необычное осложнение в виде одностороннего отека нижней конечности без изменений лимфооттока и кровообращения [40]. В 2020 году Santo et al. описали эффективность селуметиниба в лечении ПН у 18 из 19 больных НФ1 (95,0 %) в первые 60-90 дней [41]. В 2020 году в исследовании Gross et al. во второй фазе открытого клинического исследования детей с НФ1 применения селуметиниба по непрерывному графику (28-дневные циклы) описали стойкое уменьшение размеров неоперабельных нейрофибром у 70.0 % пациентов (35 из 44) [42].
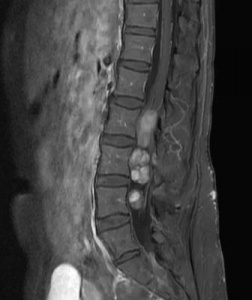
Селуметиниб показал свою эффективность при опухолях головного мозга у больных НФ1. Проведено лечение 6 групп пациентов в возрасте от 3 до 21 лет с использованием селуметиниба в дозе 25 мг/м2 дважды в день - 26 курсов по 28 дней. У 36,0 % (9 из 25) пациентов с пилоцитарной астроцитомой 1 степени, у 40,0 % (10 из 25) больных с глиомой низкой степени злокачественности показан стойкий клинический эффект. Соответственно, в среднем, у 38,0 % больных НФ1 показана эффективность препарата в лечении опухолей головного мозга [43]. Спинальные нейрофибромы при НФ1 вызывают прогрессирующую компрессию спинного мозга и неврологическую дисфункцию. Лечение с помощью селуметинаба (12 циклов) 24 больных НФ1 в возрасте от 6 до 60 лет со спинальными нейрофибромами (у 20 пациентов отмечалась деформация спинного мозга) показало свою клиническую эффективность у 18 исследованных индивидов (75,0 %) [44]. Попытки применения других групп препаратов для лечения НФ1 показали значительно меньшую результативность, хотя и отличающуюся от плацебо. Например, уменьшение объема плексиформных нейрофибром у больных с НФ1 при использовании иматиниба мези-лата (ингибитор киназ) было достигнуто в 17,0 % случаев [45], при применении пэг-интерферона альфа - в 5,0 % [46]. Противовоспалительный и антифиброзиру-ющий препарат пирфенидона (разработан для борьбы с идиопатическим легочным фиброзом) подавлял рост ПН у 15,0 % взрослых больных НФ1 [47], но не влиял на данный тип опухолей у детей с НФ1 [48].
Поскольку остеокласты
при НФ1 нечувствительны к бисфосфонатам,
для лечения остеопороза необходим
персонализированный подход с применением
ингибиторов MEK.
Неэффективно также длительное применение витамина D и кальция. Однако NF1+/- предшественники остеокластов проявляют значительную гиперчувствительность к M-CSF, который связывается с их c-Fms рецепторами и усиливает их миграцию, адгезию и костнорезорбтивную способность [1]. Введение PLX3397, фармакологического ингибитора c-Fms рецепторов, снижает активность остеокластов. Соответственно, PLX3397 может быть перспективным препаратом для лечения остеопороза у больных НФ1 [49]. Показана также эффективность ингибиторов MEK в усилении заживления перелома большеберцовой кости [50] и лечении псевдоартроза на моделях мышей с НФ1 (в комбинации с рекобинантным белком костного морфогенеза человека - rhBMP-2) [51]. Потенциальным ингибитором минерализации костей является повышенное накопление пирофосфатов в ответ на активацию ERK в хондроцитах больных НФ1. В экспериментах на мышах с НФ1 выявлена эффективность асфотазы альфа для лечения остеопороза, поскольку данный фермент снижает концентрацию пирофосфата в костях [52].
Перспективным направлением является этиотропное лечение НФ1 без редактирования генома с использованием рекомбинантного аденоассоциированного вируса (rAAV), содержащего кассету экспрессии для замены мутантных аллелей и восстановления функции нейрофибромина. Однако, вследствие больших размеров кДНК гена NF1 (8500 п.н.), использование стандартных векторных систем доставки не представляется возможным. Поэтому, в качестве альтернативы, могут применяться усеченные варианты гена NF1, сохраняющие функциональные домены [53]. В 2019 году на клеточных линиях MPNST и клеток Шванна человека была показана эффективность восстановления Ras-ГТФазной активности за счет экспрессии GRD с использованием панели векторов аденоассоциированного вируса (AAV). В результате происходило выраженное подавление Ras специфичным для NF1 путем [54]. Путем трансфекции изолированных доменов GRD, CSRD, LRD, CTD белка нейрофибромина в эксперименте на линии клеток нейрофибромы была частично восстановлена их нормальная функция. Более того, последовательности рекомбинантного трансгена могут быть сконструированы для кодирования усеченных функциональных белков, которые легко упаковываются в вирусные векторы [55]. Можно надеяться, что полученные результаты станут основой для внедрения в клинику генотерапии НФ1, поскольку для ряда моногенных болезней данный способ лечения показал свою эффективность. Разрабатываются также альтернативные способы генотерапии НФ1. В частотности, при нонсенс-мутациях, которые составляют до 20,0 % причин развития НФ1 [40], используются подходы по подавлению терминации трансляции преждевременных стоп-кодонов (PTC - premature termination codons) в рамке считывания. Для этого используют псевдоуриди-лирование РТС, ингибирование нонсенс-опосредован-ного распада мРНК и суперссорные тРНК. Наиболее простым способом является применение аминоглико-зидов, которые способствуют трансляции белка нормальной длины до 35 % от нормы за счет неправильного спаривания аминоацил-тРНК с преждевременным стоп-кодоном. К другим антибиотикам, подавляющим РТС, относятся негамицин (связывается с малой субъединицей рибосомы), спирамицин, джозамицин и ти-лозин. Подавление РТС в клетках млекопитающих без воздействия на терминацию трансляции в нормальных стоп-кодонах вызывает РТС124, известный как аталу-рен. Данный агент показал свою эффективность в отношении восстановления трансляции нормальных белков на моделях различных моногенных болезней [56].
Исследование роли
генов-модификаторов в патогенезе НФ1
может стать основой для разработки
таргетной терапии болезни, в том числе
в лечении скелетных аномалий.
Наиболее
перспективно применение в качестве
объектов молекул микроРНК, роль которых
в качестве генов-модификаторов при НФ1
описана ранее [25-29]. При НФ1 в кожных
нейрофибромах и в клеточных линиях
MPNST определяются повышенные уровни
miR-27a-3p и miR-27b-3p, которые способствуют
пролиферации, миграции и инвазивной
способности опухолевых клеток. Обе
микроРНК непосредственно воздействуют
на мРНК гена NF1 [57]. Показана способность
miR-641 ингибировать экспрессию NF1. Уровни
данной микроРНК повышены при
немелкоклеточном раке легкого, что
вызывает резистентность к химитерапии,
нацеленной на EGFR (рецепторы эпидермального
фактора роста).
Соответственно, таргетным воздействием на данную микроРНК можно регулировать экспрессию NF1 [58]. Сходным образом miR-103a-3p вызывает химиорезистентность к цисплатину при немелкоклеточном раке легкого путем воздействия на NF1 [59]. Повышенные уровни miR-27a-3p в глиомах способствуют резистентности к темозоломиду за счет целевого ингибирующего воздействия на NF1 [60]. Анализ с люциферазным репортером показал, что ген NF1 является прямой мишенью для miR-514a, усиленная выработка которой в клеточных линиях меланомы ингибирует экспрессию NF1 , что коррелирует с повышенной выживаемостью клеток. MiR-514a относится к кластеру микроРНК, вовлеченных в трансформацию меланоцитов и способствующих развитию меланомы. MiR-514a экспрессируется в 69,0 % всех линий клеток меланомы и лишь в 3,0 % других ЗНО [61]. Для рака желудка характерна повышенная экспрессия miR-107, которая ингибирует мРНК гена NF1 за счет связывания с областью внутри 3’-UTR. Данная микроРНК вызывает прогрессирование рака желудка, а ее уровни коррелируют с размером опухоли и глубиной инвазии [27]. Ген NF1 является также прямой мишенью miR-125a-3p, которая способствует дифференцировке и апоптозу клеток линии клеток моноцитарного лейкоза человека [62]. В плоскоклеточном раке легкого фибробласты стимулируют развитие опухоли и проявляют повышенную экспрессию miR-369, которая оказывает целевое воздействие на мРНК гена NF1 . За счет этого потенцируется миграция и инвазия раковых клеток, так как активируются MAPK сигнальные пути [63]. Полученные данные о роли различных микроРНК в управлении экспрессии гена NF1 могут стать основой как для таргетной терапии специфических ЗНО, так и для лечения НФ1 путем стимуляции экспрессии нормального аллеля НФ1 [53].
ЗАКЛЮЧЕНИЕ
Скелетные аномалии развиваются у большинства больных НФ1 и являются специфическими признаками болезни. Это свидетельствует о роли гена NF1 и взаимодействующих с его белковым продуктом молекул в регуляции развития опорно-двигательной системы. В клетках псевдоартроза и деформированных позвонков при сколиозе выявляется биаллельная инактивация гена NF1 . Поскольку ген NF1 обладает повышенной мутабельностью, можно предположить, что в общей популяции соматическая инактивация NF1 может служить причиной патологии ОДС. Данное предположение связано с тем, что соматические мутации в гене NF1 у пациентов, не страдающих НФ1, выявляются в среднем в 10 % спорадических злокачественных новообразований и являются драйверами канцерогенеза. Кроме того, в лечении скелетных аномалий при НФ1 показали свою эффективность те же препараты (ингибиторы MEK), которые успешно используются в терапии опухолевого синдрома при данной болезни. Поскольку НФ1 характеризуется выраженным клиническим полиморфизмом даже у пациентов с идентичной мутацией и членов одной семьи, вероятно влияние генов-модификаторов на развитие признаков болезни. Об этом свидетельствуют результаты работ ряда авторов. Выявление влияния специфических генов на развитие НФ1 может стать основой для разработки новых способов лечения как опухолевого синдрома, так и скелетных аномалий. В настоящее время для лечения ортопедической патологии при НФ1 используется комплексный подход: при врожденном псевдоартрозе большеберцовой кости и тяжелой степени сколиоза -хирургическое лечение с фармакотерапией. В лечении остеопороза при НФ1 предполагается также применение асфотазы альфа, ингибитора c-Fms рецепторов (PLX3397). Перспективно использование ингибиторов MEK с местным введением rhBMP-2 в область псево-дартроза, а также внедрение в клинику генотерапии НФ1.
СПИСОК ИСТОЧНИКОВ
1. Rhodes S.D., Yang
F.C. Aberrant Myeloid Differentiation Contributes to the Development
of Osteoporosis in Neurofibromatosis Type 1 // Curr. Osteoporos. Rep.
2016. Vol. 14, No 1. P. 10-15.
2. Neurofibromatosis
type 1 / D.H. Gutmann, R.E. Ferner, R.H. Listernick, B.R. Korf, P.L.
Wolters, K.J. Johnson // Nat. Rev. Dis. Primers. 2017. Vol. 3. P.
17004.
3. Skeletal muscle and motor deficits in Neurofibromatosis Type 1 / M.A. Summers, K.G. Quinlan, J.M. Payne, D.G. Little, K.N. North, A. Schindeler // J. Musculoskelet. Neuronal Interact. 2015. Vol. 15, No 2. P. 161-170.
4. Genome-wide association study of cafe-au-lait macule number in neurofibromatosis type 1 / H. Sung, P.L. Hyland, A. Pemov, J.A. Sabourin, A.M. Baldwin, S. Bass, K. Teshome, W. Luo; Frederick National Laboratory for Cancer Research; B.C. Widemann, D.R. Stewart, A.F. Wilson // Mol. Genet. Genomic Med. 2020. Vol. 8, No 10. P. e1400. DOI: 10.1002/mgg3.1400.
5. Anderson J.L., Gutmann D.H. Neurofibromatosis type 1 // Handb. Clin. Neurol. 2015. Vol. 132. P. 75-86. DOI: 10.1016/B978-0-444-62702-5.00004-4.
6. Approaches to treating NF1 tibial pseudarthrosis: consensus from the Children’s Tumor Foundation NF1 Bone Abnormalities Consortium / D.A. Stevenson, D. Little, L. Armstrong, A.H. Crawford, D. Eastwood, J.M. Friedman, T. Greggi, G. Gutierrez, K. Hunter-Schaedle, D.L. Kendler, M. Kolanczyk, F. Monsell, M. Oetgen, B.S. Richards, A. Schindeler, E.K. Schorry, D. Wilkes, D.H. Viskochil, F.C. Yang, F. Elefteriou // J. Pediatr. Orthop. 2013. Vol. 33, No 3. P. 269-275. DOI: 10.1097/BPO.0b013e31828121b8.
7. Ly K.I., Blakeley J.O. The Diagnosis and Management of Neurofibromatosis Type 1 // Med. Clin. North Am. 2019. Vol. 103, No 6. P. 1035-1054. DOI: 10.1016/j.mcna.2019.07.004.
8. Bernardo P., Cinalli G., Santoro C. Epilepsy in NF1: a systematic review of the literature // Childs Nerv. Syst. 2020. Vol. 36, No 10. P. 2333-2350. DOI: 10.1007/s00381-020-04710-7.
9. Chiari type 1 malformation in Neurofibromatosis type 1: experience of a center and review of the literature / E. Miraglia, G. Fabbrini, C. Di Biasi, C. Iacovino, G. Ferrazzano, G. Gualdi, S. Calvieri, S. Giustini // Clin. Ter. 2016. Vol. 167, No 1. P. e6-e10. DOI: 10.7417/T.2016.1912.
10. Management of spinal deformities and tibial pseudarthrosis in children with neurofibromatosis type 1 (NF-1) / K.V. Mladenov, A.S. Spiro,K. L. Krajewski, R. Stucker, P. Kunkel // Childs Nerv. Syst. 2020. Vol. 36, No 10. P. 2409-2425. DOI: 10.1007/s00381-020-04775-4.
11. Craniomaxillofacial morphology alterations in children, adolescents and adults with neurofibromatosis 1: A cone beam computed tomography analysis of a Brazilaian sample / E.B. Luna, M.E. Janini, F. Lima, R.R. Pontes, F.R. Guedes, M. Geller, L.E. da Silva, A.T. Motta, K. Cunha // Med. Oral Patol. Oral Cir. Bucal. 2018. Vol. 23, No 2. P. e168-e179. DOI: 10.4317/medoral.22155.
12. Minor disease features in neurofibromatosis type 1 (NF1) and their possible value in diagnosis of NF1 in children < or = 6 years and clinically suspected of having NF1. Neurofibromatosis team of Sophia Children’s Hospital / M.H. Cnossen, K.G. Moons, M.P. Garssen, N.M. Pasmans, A. de Goede-Bolder, M.F. Niermeijer, D.E. Grobbee // J. Med. Genet. 1998. Vol. 35, No 8. P. 624-627. DOI: 10.1136/jmg.35.8.624.
13. Craniofacial bone alterations in patients with neurofibromatosis type 1 / J. Chauvel-Picard, L. Lion-Francois, P.A. Beuriat, C. Paulus, A. Szathmari, C. Mottolese, A. Gleizal, F. Di Rocco // Childs Nerv. Syst. 2020. Vol. 36, No 10. P. 2391-2399. DOI: 10.1007/s00381-020-04749-6.
14. Growth and
pubertal disorders in neurofibromatosis type 1 / R. Virdis, M.E.
Street, M.A. Bandello, C. Tripodi, A. Donadio, A.R. Villani, L.
Cagozzi,L. Garavelli, S.
Bernasconi // J. Pediatr. Endocrinol. Metab. 2003. Vol. 16, No Suppl.
2. P. 289-292.
15. A molecular basis for neurofibroma-associated skeletal manifestations in NF1 / Y. Ma, A.M. Gross, E. Dombi, A. Pemov, K. Choi, K. Chaney, S.D. Rhodes, S.P. Angus, N. Sciaky, D.W. Clapp, N. Ratner, B.C. Widemann, J.J. Rios, F. Elefteriou // Genet. Med. 2020. Vol. 22, No 11. P. 17861793. DOI: 10.1038/s41436-020-0885-3.
16. NF1 regulates apoptosis in ovarian cancer cells by targeting MCL1 via miR-142-5p / J. Su, S. Ruan, S. Dai, J. Mi, W. Chen, S. Jiang // Pharmacogenomics. 2019. Vol. 20, No 3. P. 155-165. DOI: 10.2217/pgs-2018-0161.
17. Ratner N.A., Miller S.J. RASopathy gene commonly mutated in cancer: the neurofibromatosis type 1 tumour suppressor // Nat. Rev. Cancer. 2015. Vol. 15, No 5. P. 290-301. DOI: 10.1038/nrc3911.
18. Systems Biology Approaches Reveal Potential Phenotype-Modifier Genes in Neurofibromatosis Type 1 / T.W. Kowalski, L.B. Reis, T.F. Andreis, P. Ashton-Prolla, C. Rosset // Cancers (Basel). 2020. Vol. 12, No 9. P. 2416. DOI: 10.3390/cancers12092416.
19. Sharafi P., Ayter S. Possible modifier genes in the variation of neurofibromatosis type 1 clinical phenotypes // J. Neurogenet. 2018. Vol. 32, No 2. P. 65-77. DOI: 10.1080/01677063.2018.1456538.
20. Neurofibromatosis type 1-related pseudarthrosis: Beyond the pseudarthrosis site / C. Brekelmans, S. Hollants, C. de Groote, N. Sohier, M. Marechal, L. Geris, F.P. Luyten, L. Ginckels, R. Sciot, T. de Ravel, L. de Smet, J. Lammens, E. Legius, H. Brems // Hum. Mutat. 2019. Vol. 40, No 10. P. 17601767. DOI: 10.1002/humu.23783.
21. NF1 Somatic Mutation in Dystrophic Scoliosis / R.L. Margraf, C. van Sant-Webb, R. Mao, D.H. Viskochil, J. Carey, H. Hanson, J. D'Astous, A. Grossmann, D.A. Stevenson // J. Mol. Neurosci. 2019. Vol. 68, No 1. P. 11-18. DOI: 10.1007/s12031-019-01277-0.
22. The reduced osteogenic potential of Nf1-deificient osteoprogenitors is EGFR-independent / S.E. Tahaei, G. Couasnay, Y. Ma, N. Paria, J. Gu,B. F. Lemoine, X. Wang, J.J. Rios, F. Elefteriou // Bone. 2018. Vol. 106. P. 103-111. DOI: 10.1016/j.bone.2017.10.012.
23. Neurofibromatosis in the Era of Precision Medicine: Development of MEK Inhibitors and Recent Successes with Selumetinib / R. Galvin, A. L. Watson, D.A. Largaespada, N. Ratner, S. Osum, C.L. Moertel // Curr. Oncol. Rep. 2021. Vol. 23, No 4. P. 45. DOI: 10.1007/s11912-021-01032-y.
24. An analysis of variation in expression of neurofibromatosis (NF) type 1 (NF1): evidence for modifying genes / D.F. Easton, M.A. Ponder, S.M. Huson, B. A. Ponder // Am. J. Hum. Genet. 1993. Vol. 53, No 2. P. 305-313.
25. Genome-wide transcriptome analyses reveal p53 inactivation mediated loss of miR-34a expression in malignant peripheral nerve sheath tumours / S. Subramanian, V. Thayanithy, R.B. West, C.H. Lee, A.H. Beck, S. Zhu, E. Downs-Kelly, K. Montgomery, J.R. Goldblum, P.C. Hogendoorn, C. L. Corless, A.M. Oliveira, S.M. Dry, T.O. Nielsen, B.P. Rubin, J.A. Fletcher, C.D. Fletcher, M. van de Rijn // J. Pathol. 2010. Vol. 220, No 1. P. 58-70. DOI: 10.1002/path.2633.
26. Identification of serum microRNAs in genome-wide serum microRNA expression profiles as novel noninvasive biomarkers for malignant peripheral nerve sheath tumor diagnosis / Y. Weng, Y. Chen, J. Chen, Y. Liu, T. Bao // Med. Oncol. 2013. Vol. 30, No 2. P. 531. DOI: 10.1007/s12032-013-0531-x.
27. miR-107 regulates tumor progression by targeting NF1 in gastric cancer / S. Wang, G. Ma, H. Zhu, C. Lv, H. Chu, N. Tong, D. Wu, F. Qiang, W. Gong, Q. Zhao, G. Tao, J. Zhou, Z. Zhang, M. Wang // Sci. Rep. 2016. Vol. 6. P. 36531. DOI: 10.1038/srep36531.
28. MicroRNA-204 critically regulates carcinogenesis in malignant peripheral nerve sheath tumors / M. Gong, J. Ma, M. Li, M. Zhou, J.M. Hock, X. Yu // Neuro Oncol. 2012. Vol. 14, No 8. P. 1007-1017. DOI: 10.1093/neuonc/nos124.
29. MicroRNA-21 correlates with tumorigenesis in malignant peripheral nerve sheath tumor (MPNST) via programmed cell death protein 4 (PDCD4) / S. Itani, T. Kunisada, Y. Morimoto, A. Yoshida, T. Sasaki, S. Ito, M. Ouchida, S. Sugihara, K. Shimizu, T. Ozaki // J. Cancer Res. Clin. Oncol. 2012. Vol. 138, No 9. P. 1501-1509. DOI: 10.1007/s00432-012-1223-1.
30. Heightened CXCR4 and CXCL12 expression in NF1-associated neurofibromas / B. Karaosmanoglu, ^.Y. Kocaefe, F. Soylemezoglu, B. Anlar, A. Varan, i. Vargel, S. Ayter // Childs Nerv. Syst. 2018. Vol. 34, No 5. P. 877-882. DOI: 10.1007/s00381-018-3745-6.
31. NF1 patient missense variants predict a role for ATM in modifying neurofibroma initiation / Y. Yu, K. Choi, J. Wu, P.R. Andreassen, PJ. Dexheimer, M. Keddache, H. Brems, R.J. Spinner, J.A. Cancelas, L.J. Martin, M.R. Wallace, E. Legius, K.S. Vogel, N. Ratner // Acta Neuropathol. 2020. Vol. 139, No 1. P. 157-174. DOI: 10.1007/s00401-019-02086-w.
32. Expression analysis of genes lying in the NF1 microdeletion interval points to four candidate modifiers for neurofibroma formation / B. Bartelt-Kirbach, M. Wuepping, M. Dodrimont-Lattke, D. Kaufmann // Neurogentics. 2009. Vol. 10, No 1. P. 79-85. DOI: 10.1007/s10048-008-0154-0.
33. Combined MEK inhibition and BMP2 treatment promotes osteoblast differentiation and bone healing in Qsx-/-mice / J. Ndong de la Croix, D. M. Stevens, G. Vignaux, S. Uppuganti, D.S. Perrien, X. Yang, J.S. Nyman, E. Harth, F. Elefteriou // J. Bone Miner. Res. 2015. Vol. 30, No 1. P. 55-63. DOI: 10.1002/jbmr.2316.
34. Surgical treatment of scoliosis in neurofibromatosis type I: A retrospective study on posterior-only correction with third-generation instrumentation / P. Cinnella, S. Amico, A. Rava, M. Cravino, G. Gargiulo, M. Girardo // J. Craniovertebr. Junction Spine. 2020. Vol. 11, No 2. P. 104-110. DOI: 10.4103/jcvjs.JCVJS_50_20.
35. Surgical Treatment of Dystrophic Scoliosis in Neurofibromatosis Type 1: Outcomes and Complications / Z. Yao, D. Guo, H. Li, Y. Bai, B. Sun, X. Zhang, C. Li, X. Qi // Clin. Spine Surg. 2019. Vol. 32, No 1. P. E50-E55. DOI: 10.1097/BSD.0000000000000716.36. Phase 2 randomized, flexible crossover, double-blinded, placebo-controlled trial of the farnesyltransferase inhibitor tipifarnib in children and young adults with neurofibromatosis type 1 and progressive plexiform neurofibromas / B.C. Widemann, E. Dombi, A. Gillespie, P.L. Wolters, J. Belasco, S. Goldman, B.R. Korf, J. Solomon, S. Martin, W. Salzer, E. Fox, N. Patronas, M.W. Kieran, J.P. Perentesis, A. Reddy, J.J. Wright, A. Kim, S.M. Steinberg, F.M. Balis // Neuro Oncol. 2014. Vol. 16, No 5. P. 707-718. DOI: 10.1093/neuonc/nou004.
37. Selumetinib in the Treatment of Symptomatic Intractable Plexiform Neurofibromas in Neurofibromatosis Type 1: A Prospective Case Series with Emphasis on Side Effects / F. Baldo, A.G. Grasso, L.C. Wiel, A. Maestro, M.P. Trojniak, F.M. Murru, L. Basso, A. Magnolato, I. Bruno, E. Barbi // Paediatr. Drugs. 2020. Vol. 22, No 4. P. 417-423. DOI: 10.1007/s40272-020-00399-y.
38. Activity of Selumetinib in Neurofibromatosis Type 1-Related Plexiform Neurofibromas / E. Dombi, A. Baldwin, L.J. Marcus, M.J. Fisher, B. Weiss, A. Kim, P. Whitcomb, S. Martin, L.E. Aschbacher-Smith, T.A. Rizvi, J. Wu, R. Ershler, P. Wolters, J. Therrien, J. Glod, J.B. Belasco, E. Schorry, A. Brofferio, A.J. Starosta, A. Gillespie, A.L. Doyle, N. Ratner, B.C. Widemann // N. Engl. J. Med. 2016. Vol. 375, No 26. P. 2550-2560. DOI: 10.1056/NEJMoa1605943.
41. Selumetinib for plexiform neurofibromas in neurofibromatosis type 1: a single-institution experience / V.E. Santo, J. Passos, H. Nzwalo, I. Carvalho, F. Santos, C. Martins, L. Salgado, C.E. Silva, S. Vinhais, M. Vilares, D. Salgado, S. Nunes // J. Neurooncol. 2020. Vol. 147, No 2. P. 459-463. DOI: 10.1007/s11060-020-03443-6.
42. Selumetinib in Children with Inoperable Plexiform Neurofibromas / A.M. Gross, P.L. Wolters, E. Dombi, A. Baldwin, P. Whitcomb, M.J. Fisher, B. Weiss, A. Kim, M. Bornhorst, A.C. Shah, S. Martin, M.C. Roderick, D.C. Pichard, A. Carbonell, S.M. Paul, J. Therrien, O. Kapustina, K. Heisey,D. W. Clapp, C. Zhang, C.J. Peer, W.D. Figg, M. Smith, J. Glod, J.O. Blakeley, S.M. Steinberg, D.J. Venzon, L.A. Doyle, B.C. Widemann // N. Engl. J. Med. 2020. Vol. 382, No 15. P. 1430-1442. DOI: 10.1056/NEJMoa1912735.
43. Selumetinib in paediatric patients with BRAF-aberrant or neurofibromatosis type 1-associated recurrent, refractory, or progressive low-grade glioma: a multicentre, phase 2 trial / J. Fangusaro, A. Onar-Thomas, T.Y. Poussaint, S. Wu, A.H. Ligon, N. Lindeman, A. Banerjee, R.J. Packer, L. B. Kilburn, S. Goldman, I.F. Pollack, I. Qaddoumi, R.I. Jakacki, P.G. Fisher, G. Dhall, P. Baxter, S.G. Kreissman, C.F. Stewart, D.T.W. Jones, S.M. Pfister, G. Vezina, J.S. Stern, A. Panigrahy, Z. Patay, B. Tamrazi, J.Y. Jones, S.S. Haque, D.S. Enterline, S. Cha, M.J. Fisher, L.A. Doyle, M. Smith, I.J. Dunkel, M. Fouladi // Lancet Oncol. 2019. Vol. 20, No 7. P. 1011-1022. DOI: 10.1016/S1470-2045(19)30277-3.
44. The MEK inhibitor selumetinib reduces spinal neurofibroma burden in patients with NF1 and plexiform neurofibromas / S. Jackson, E.H. Baker,A. M. Gross, P. Whitcomb, A. Baldwin, J. Derdak, C. Tibery, J. Desanto, A. Carbonell, K. Yohay, G. O'Sullivan, A.P. Chen, B.C. Widemann, E. Dombi // Neurooncol. Adv. 2020. Vol. 2, No 1. P. vdaa095. DOI: 10.1093/noajnl/vdaa095.
45. Imatinib mesylate for plexiform neurofibromas in patients with neurofibromatosis type 1: a phase 2 trial / K.A. Robertson, G. Nalepa, F.C. Yang, D.C. Bowers, C.Y. Ho, G.D. Hutchins, J.M. Croop, T.A. Vik, S.C. Denne, L.F. Parada, C.M. Hingtgen, L.E. Walsh, M. Yu, K.R. Pradhan, M. K. Edwards-Brown, M.D. Cohen, J.W. Fletcher, J.B. Travers, K.W. Staser, M.W. Lee, M.R. Sherman, C.J. Davis, L.C. Miller, D.A. Ingram,D. W. Clapp // Lancet Oncol. 2012. Vol. 13, No 12. P. 1218-1224. DOI: 10.1016/S1470-2045(12)70414-X.
46. Phase II trial of pegylated interferon alfa-2b in young patients with neurofibromatosis type 1 and unresectable plexiform neurofibromas / R.I. Jakacki, E. Dombi, S.M. Steinberg, S. Goldman, M.W. Kieran, N.J. Ullrich, I.F. Pollack, A. Goodwin, P.E. Manley, J. Fangusaro, R. Allen, B.C. Widemann // Neuro Oncol. 2017. Vol. 19, No 2. P. 289-297. DOI: 10.1093/neuonc/now158.
47. Phase II trial of pirfenidone in adults with neurofibromatosis type 1 / D. Babovic-Vuksanovic, K. Ballman, V. Michels, P. McGrann, N. Lindor, B. King, J. Camp, V. Micic, N. Babovic, X. Carrero, R. Spinner, B. O'Neill // Neurology. 2006. Vol. 67, No 10. P. 1860-1862. DOI: 10.1212/01. wnl.0000243231.12248.67.
48. Phase II trial of pirfenidone in children and young adults with neurofibromatosis type 1 and progressive plexiform neurofibromas / B.C. Widemann, D. Babovic-Vuksanovic, E. Dombi, P.L. Wolters, S. Goldman, S. Martin, A. Goodwin, W. Goodspeed, M.W. Kieran, B. Cohen, S.M. Blaney, A. King, J. Solomon, N. Patronas, F.M. Balis, E. Fox, S.M. Steinberg, R.J. Packer // Pediatr. Blood Cancer. 2014. Vol. 61, No 9. P. 1598-1602. DOI: 10.1002/pbc.25041.
49. c-Fms signaling mediates neurofibromatosis Type-1 osteoclast gain-in-functions / Y. He, S.D. Rhodes, S. Chen, X. Wu, J. Yuan, X. Yang, L. Jiang, X. Li, N. Takahashi, M. Xu, K.S. Mohammad, T.A. Guise, F.C. Yang // PLoS One. 2012. Vol. 7, No 11. P. e46900. DOI: 10.1371/journal. pone.0046900.
50. Hyperactive Ras/MAPK signaling is critical for tibial nonunion fracture in neurofibromin-deficient mice / R. Sharma, X. Wu, S.D. Rhodes, S. Chen,Y. He, J. Yuan, J. Li, X. Yang, X. Li, L. Jiang, E.T. Kim, D.A. Stevenson, D. Viskochil, M. Xu, F.C. Yang // Hum. Mol. Genet. 2013. Vol. 22, No 23. P. 4818-4828. DOI: 10.1093/hmg/ddt333.
51. A Combination of rhBMP-2 (Recombinant Human Bone Morphogenetic Protein-2) and MEK (MAP Kinase/ERK Kinase) Inhibitor PD0325901 Increases Bone Formation in a Murine Model of Neurofibromatosis Type I Pseudarthrosis / J. El-Hoss, T. Cheng, E.C. Carpenter, K. Sullivan, N. Deo, K. Mikulec, D.G. Little, A. Schindeler // J. Bone Joint Surg. Am. 2014. Vol. 96, No 14. P. e117. DOI: 10.2106/JBJS.M.00862.
52. Corrigendum: Asfotase-a improves bone growth, mineralization and strength in mouse models of neurofibromatosis type-1 / J. Ndong de la Croix, A.J. Makowski, S. Uppuganti, G. Vignaux, K. Ono, D.S. Perrien, S. Joubert, S.R. Baglio, D. Granchi, D.A. Stevenson, J.J. Rios, J.S. Nyman, F. Elefteriou // Nat. Med. 2015. Vol. 21, No 4. P. 414. DOI: 10.1038/nm0415-414c.
53. Walker J.A., Upadhyaya M. Emerging therapeutic targets for neurofibromatosis type 1 // Expert Opin. Ther. Targets. 2018. Vol. 22, No 5. P. 419-437. DOI: 10.1080/14728222.2018.1465931.
54. Feasibility of using NF1-GRD and AAV for gene replacement therapy in NFl-associated tumors / R.Y. Bai, D. Esposito, A.J. Tam, F. McCormick, G.J. Riggins, D.W. Clapp, V. Staedtke // Gene Ther. 2019. Vol. 26, No 6. P. 277-286. DOI: 10.1038/s41434-019-0080-9.
55. NF1, Neurofibromin and Gene Therapy: Prospects of Next-Generation Therapy / X.W. Cui, J.Y. Ren, Y.H. Gu, Q.F. Li, Z.C. Wang // Curr. Gene Ther. 2020. Vol. 20, No 2. P. 100-108. DOI: 10.2174/1566523220666200806111451.
56. Therapeutics based on stop codon readthrough / K.M. Keeling, X. Xue, G. Gunn, D.M. Bedwell // Annu. Rev. Genomics. Hum. Genet. 2014. Vol. 15. P. 371-394. DOI: 10.1146/annurev-genom-091212-153527.
57. Lu H., Liu P., Pang Q. MiR-27a-3p/miR-27b-3p Promotes Neurofibromatosis Type 1 via Targeting of NF1 // J. Mol. Neurosci. 2021. Vol. 71, No 11. Р. 2353-2363. DOI: ~10.1007/s12031-020-01779-2.
58. Increased expression of miR-641 contributes to erlotinib resistance in non-small-cell lung cancer cells by targeting NF1 / J. Chen, J.D. Cui, X.T. Guo, X. Cao, Q. Li // Cancer Med. 2018. Vol. 7, No 4. P. 1394-1403. DOI: 10.1002/cam4.1326.
59. Zhu H., Yang J., Yang S. MicroRNA-103a-3p potentiates chemoresistance to cisplatin in non-small cell lung carcinoma by targeting neurofibromatosis 1 // Exp. Ther. Med. 2020. Vol. 19, No 3. P. 1797-1805. DOI: 10.3892/etm.2020.8418.
60. MiRNA-27a-3p induces temozolomide resistance in glioma by inhibiting NF1 level / S. Li, W. Li, G. Chen, J. Huang, W. Li // Am. J. Transl. Res. 2020. Vol. 12, No 8. P. 4749-4756.
61. miR-514a regulates the tumour suppressor NF1 and modulates BRAFi sensitivity in melanoma / M.S. Stark, V.F. Bonazzi, G.M. Boyle, J.M. Palmer, J. Symmons, C.M. Lanagan, C.W. Schmidt, A.C. Herington, R. Ballotti, P.M. Pollock, N.K. Hayward // Oncotarget. 2015. Vol. 6, No 19. P. 1775317763. DOI: 10.18632/oncotarget.3924.
62. LukS-PV-Regulated MicroRNA-125a-3p Promotes THP-1 Macrophages Differentiation and Apoptosis by Down-Regulating NF1 and Bcl-2 / X.X. Sun, S.S. Zhang, C.Y. Dai, J. Peng, Q. Pan, L.F. Xu, X.L.Ma // Cell Physiol. Biochem. 2017. Vol. 44, No 3. P. 1093-1105. DOI: 10.1159/000485415.
63. Fibroblast-derived exosomal microRNA-369 potentiates migration and invasion of lung squamous cell carcinoma cells via NF1-mediated MAPK signaling pathway / L. Guo, B. Li, J. Yang, J. Shen, J. Ji, M. Miao // Int. J. Mol. Med. 2020. Vol. 46, No 2. P. 595-608. DOI: 10.3892/ijmm.2020.4614.
Информация об авторе:
Рустам Наилевич Мустафин - кандидат биологических наук
Теги: нейрофиброматоз
234567 Начало активности (дата): 14.05.2022 22:46:00
234567 Кем создан (ID): 989
234567 Ключевые слова: гены-модификаторы, деформация грудной клетки, нейрофиброматоз 1-го типа, псевдоартроз, сколиоз
12354567899
Похожие статьи
Применение методов ядерной медицины в диагностике нейроэндокринных опухолейЛевый коленный сустав
Рентген на дому 8 495 22 555 6 8
Вариант восстановительного лечения пациента с врожденным ложным суставом костей голени (случай из практики)
Пороки развития стопы и кисти при синдроме Горлина-Гольтца (описание двух клинических случаев)



