 19.02.2021
19.02.2021
Результаты оперативного лечения пациентов с синдромом запястного канала в зависимости от степени выраженности заболевания
Несмотря на то, что при лечении пациентов с синдромом запястного казана (СЗК) хирургический метод признан высокоэффективным, его результаты не у всех являются одинаково положительными. Это предопределено исходной выраженностью клинических проявлений заболевания, объективизированной данными инструментальных методов обследования.
ВВЕДЕНИЕ
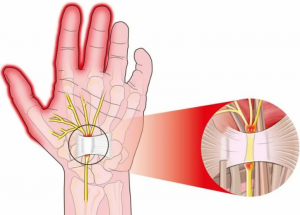
Синдром запястного канала (СЗК) - одна из наиболее частых клинических форм компрессионно-ишемической невропатии верхней конечности. Она проявляется болью, чувством онемения и покалывания в области первого-третьего пальцев кисти, слабостью мышц тенара, нарушениями функции кисти. Заболевание диагностируют на основании анамнестических и клинических данных, а также результатов инструментальных методов обследования, наиболее значимыми из которых являются электронейромиография (ЭНМГ) и ультразвуковое исследование (УЗИ) [1, 2].
При лечении пациентов с СЗК первоначально отдают предпочтение консервативной терапии, включающей лечебную иммобилизацию, физиотерапию, пероральный прием НПВП, местные инъекции кортикостероидов [3]. Однако при отсутствии улучшения, нарастании функциональных расстройств и появлении патологических симптомов становится очевидной необходимость оперативного лечения [4, 5].
Несмотря на то, что хирургический метод признан высокоэффективным, его результаты далеко не у всех являются положительными, что во многом предопределено исходной выраженностью морфологических изменений в области запястного канала [6-8].
По данным ряда исследователей, для инструментальной диагностики СЗК более весомой, по сравнению с УЗИ, является ЭНМГ - благодаря ее более высокой специфичности и чувствительности [9-10].
Это позволило использовать показатели ЭНМГ в качестве основы для разработки классификаций по выраженности СЗК. Благодаря такому подходу в руках хирургов появился удобный инструмент, дающий возможность сопоставлять данные, полученные в ходе лечения, с исходными показателями и, таким образом, объективно оценивать его результаты.
Однако число научных публикаций, глубоко отражающих этот вопрос, невелико [11-15].
Цель - дать клиническую оценку результатам оперативного лечения пациентов с СЗК с использованием опросников и показателей ЭНМГ в сопоставлении с исходной степенью выраженности заболевания.
МАТЕРИАЛЫ И МЕТОДЫ
Основу настоящего исследования составили 230 пациентов, страдающих идиопатическим СЗК, которым в период 2014-2019 гг. выполнили хирургические вмешательства одинакового содержания по купированию заболевания. Из исследования исключили 69 пациентов с хронической почечной недостаточностью, ревматоидным артритом, сопутствующим синдромом кубитального канала, последствиями переломов костей кисти и кистевого сустава, отказавшихся от проведения исследования и выбывших до его окончания по другим причинам.
В итоге, результаты лечения изучили у 161 пациента (151 женщина и 10 мужчин) в возрасте от 34 до 81 года (в среднем 56,3 ± 8,4 года) в сроки полутора, 3, 6 и 12 месяцев после хирургического вмешательства.
Из общего числа пациентов операцию только на одной кисти выполнили у 133 человек (правая - 88, левая - 45). У остальных 28 человек - на обеих кистях, но по отдельности с интервалом не менее трех месяцев. В итоге, проанализировали результаты лечения 161 пациента, которым произвели вмешательства на 189 кистях. Операцию на одной кисти считали одним клиническим наблюдением.
В соответствии с классификацией, предложенной Beck J.D. et al. (2013) [12], всех пациентов, в зависимости от величины дистальной латентности моторных волокон срединного нерва (ДМЛ), разделили на три клинические группы (табл. 1).
При постановке диагноза учитывали наличие положительных симптомов Фалена, Тинеля, «стряхивания» кисти («flick maneuver»), «scratch test».
Для оценки результатов лечения применяли опросник Boston Carpal Tunnel Questionnaire, состоящий из двух составных частей: шкалы тяжести симптомов (BCTQs) и шкалы функциональных нарушений (BCTQf), с градацией признаков от 1 (наилучший результат) до 5 баллов (наихудший результат) [16-17].
Запись ЭНМГ осуществляли на электронейромиографе Viking Quest (Nicolet Biomedical) с четырехканальным усилителем (ПО VikingQuest), с использованием накожных серебряных электродов SE-2, располагаемых друг от друга на расстоянии 2 см.
В ходе ЭНМГ-исследования изучали динамику четырех показателей: амплитуда М-ответа короткой мышцы, отводящей большой палец (A), дистальная латентность моторных волокон срединного нерва (ДМЛ), скорость проведения импульса по моторным (MC) и сенсорным волокнам срединного нерва (CC).
Статистический анализ проводили в среде пакета SPSS 25 (IBM SPSS Statistics, США). Сравнение данных выполняли посредством дисперсионного анализа Краскелла-Уоллиса с последующими межгрупповыми сравнениями по критерию Манна-Уитни-Вилкоксона с поправкой Бонферрони, а сравнения в динамике наблюдения - по парному критерию Вилкоксона. Для определения характера восстановления скорости проведения нервных импульсов по сенсорным волокнам срединного нерва применили метод Каплана-Мейера.
В ходе исследования использовали средние величины и стандартные отклонения (M ± SD), на графиках типа «усатый ящик» -медианы и квартили. Тесноту взаимосвязей оценивали по коэффициенту корреляции Спирмена. Результаты считали статистически значимыми при р < 0,05.
Хирургическая техника. Операцию открытой декомпрессии срединного нерва проводили в положении больного лежа на спине с отведенной и супинированной верхней конечностью. С целью обескровливания на плечо накладывали пневматическую манжету. Для обезболивания применяли сочетание внутривенной седации и местной анестезии.
Во всех клинических наблюдениях выполняли слегка дугообразный или Z-образный разрез длиной 25 мм («miniopen incision») параллельно складке возвышения большого пальца, не выходя за пределы проекции крючка крючковидной кости и дистальной складки запястья (рис. 1, а).
При этом учитывали местоположение ладонной ветви срединного нерва. Дугообразным продольным разрезом рассекали ладонный апоневроз. Удерживатель сгибателей рассекали по его ладонно-локтевой поверхности, чтобы избежать повреждения моторной ветви срединного нерва (рис. 1, б).
Фасцию предплечья рассекали в проксимальном направлении, как минимум до уровня дистальной складки запястья. Послойно ушивали ладонный апоневроз и кожу. Запястье фиксировали съемной лонгетой на 3 недели. Со второго послеоперационного дня разрешали движения в суставах пальцев и запястье, исключая сгибание кисти. В дальнейшем при тяжелых нагрузках рекомендовали применять ортез для кистевого сустава.
РЕЗУЛЬТАТЫ
В обобщенном виде результаты лечения всех пациентов представлены в таблице 2. В ней отражена динамика шести показателей (BCTOs, BCTOf, А, ДМЛ, МС, СС) в трех клинических группах с временным промежутком 12 месяцев.
На основании данных таблицы можно заключить, что в соответствии с характером изменений большинства показателей у пациентов первой и второй групп наступило существенное клиническое улучшение, достигшее показателей нормы. Так, по динамике четырех показателей, таких как BCTOs, BCTOf, ДМЛ и СС, достоверность различий между периодом до операции и через 12 месяцев была весомой (р < 0,001).
У пациентов третьей группы статистически достоверное улучшение наступило в соответствии с годичной динамикой всех шести показателей. Однако ни по одному из них усредненно не было достигнуто значений нормы.
Наряду с этим интерес представляет изменение показателей не только через 12 месяцев после операции, но и в более ранние сроки, а также сравнение показателей между группами в эти же сроки. Так, по результатам анкеты BCTOs достоверный регресс клинических симптомов наблюдали во все временные периоды, по сравнению с периодом до операции, и во всех группах (рис. 2). В наибольшей степени, практически «скачкообразно», эти изменения произошли через 1,5 месяца. В первой группе полуторамесячные показатели BCTOs улучшились на 47 %, во второй - на 42 %, в третьей группе - на 31 %. При этом достоверные различия зарегистрировали между первой и третьей, второй и третьей группами. Во все последующие временные промежутки - через 3, 6 и 12 месяцев - показатели между группами практически не различались.
Наряду с анкетными данными, показатели ЭНМГ также претерпели ряд изменений, свидетельствующих о постепенном улучшении функционального статуса кисти и кистевого сустава. Как представлено на рисунке 4, величина амплитуды М-ответа короткой мышцы, отводящей большой палец, во всех группах постепенно увеличивалась. Но ее рост происходил медленно и не всегда значимо по сравнению с периодом до операции. Так, через 1,5 месяца у пациентов всех трех групп амплитуда оставалась такой же, как и до операции. Через 3 месяца после хирургического вмешательства значение данного показателя достоверно увеличилось только в третьей группе, максимально приблизившись к первой и второй группам, а затем начала «отставать» от них.
Показатель дистальной моторной латентности срединного нерва на всех этапах исследования и во всех группах также имел положительную динамику. Особо наглядно эта закономерность проявилась через 12 месяцев после операции (рис. 5). Так, усредненная величина показателя дистальной моторной латентности в первой группе уменьшилась с 4,65 ± 0,44 мс до 3,80 ± 0,29 мс (р < 0,001), во второй - с 6,29 ± 0,54 мс до 4,22 ± 0,44 мс (р < 0,001) и в третьей группе - с 9,03 ± 1,72 мс до 5,26 ± 1,13 мс (р < 0,001), при величине нормы < 4,2 мс. При межгрупповом сравнении в каждом периоде имелись достоверные различия между первой и третьей, между второй и третьей группами.
Скорость проведения импульса по моторным волокнам срединного нерва также постепенно нарастала (рис. 6), но с «запаздыванием» в третьей группе. Через 12 месяцев в первой и второй группах она стала соответствовать значению нормы, составив соответственно, 55,19 ± 3,86 м/с и 53,91 ± 3,62 м/с. В то же время в третьей группе продолжала оставаться низкой - 46,81 ± 9,56 м/с, при величине нормы > 50 м/с. В каждом периоде наблюдения сохранялись достоверные различия между первой и третьей, между второй и третьей группами.
Следует отметить, что в 63 (37,3 %) клинических наблюдениях сенсорная скорость до операции не определялась, т.е. имела нулевые значения. Из всех таких клинических наблюдений 54 (85,7 %) - это наблюдения из третьей группы, при максимальной выраженности СЗК.
С целью выяснения сроков восстановления сенсорной скорости и категорий пациентов, у которых это происходило наиболее значимо, использовали статистический подход для работы с цензурированными данными, широко применяемый в анализе выживаемости, - построение кривых Каплана-Мейера.
Анализ кривых Каплана-Мейера показал (рис. 8), что, начиная с 1,5 месяцев после операции, у пациентов с исходной нулевой сенсорной скоростью восстановление ее шло быстрее в первой и второй группах, рассмотренных совокупно, чем у пациентов третьей группы.
Таким образом, на фоне в целом положительной динамики, сведения из анкет и величины ЭНМГ-показателей свидетельствуют о своеобразном «запаздывающем» восстановлении функциональных возможностей верхних конечностей у пациентов третьей группы, по сравнению с пациентами первой и второй групп, не достигающем значений нормы даже через 12 месяцев после операции. При этом нельзя отрицать положительного влияния операции на течение СЗК у пациентов третьей группы. Это проявилось своеобразным «скачком» функционального восстановления, наиболее ярко проявившимся, по большинству изученных показателей, через 1,5-3 месяца после операции.
Клинический пример. Пациентка К., 52 лет, швея, обратилась с жалобами на нарушение чувствительности и боль в 1-2-3 пальцах левой кисти, усиливающиеся в утренние часы. В течение года лечилась консервативно с незначительным улучшением. Боль постепенно нарастала, стала беспокоить преимущественно в ночное время. Кроме этого, по утрам начал возникать отек кисти, движения пальцами становились затрудненными. Профессиональная и бытовая деятельность заметно снизились.
Внешний вид левой кисти не изменен, соответствует правой кисти. Объем движений в суставах пальцев полный. Отмечается болезненность в проекции запястного канала, с иррадиацией в 1-2-3 пальцы. Тесты Тинеля и Фалена «положительные». Интенсивность боли ночью по визуальной аналоговой шкале (ВАШ) -7,5 балла. От ночной боли пациентка просыпается 5 раз и более. Результаты опросников BCTOs и BCTOf составили соответственно 4,46 и 3,13 баллов. Отмечается выраженная слабость в руке.
Повседневная активность резко снижена из-за боли и нарушения чувствительности в пальцах. При ЭМГ выявлены признаки СЗК: А -2,8 мВ; МС - 48 м/с; ДМЛ - 5,0 мс; СС - 36 м/с.
В августе 2019 года выполнили операцию: открытую из мини-разреза декомпрессию срединного нерва на левом запястье. Невропатическая боль исчезла сразу же после хирургического вмешательства. Послеоперационный период протекал без осложнений. Рана зажила первичным натяжением. Пациентка все рекомендации по лечению выполняла аккуратно.
При осмотре через 6 месяцев: жалоб не предъявляет, трудоспособность по прежней профессии сохранена. Чувствительность в пальцах оперированной кисти не изменена - чувства онемения и покалывания нет. Боль в покое отсутствует, но после нагрузки ее уровень повышается до 1,8 балла. Объем активных движений в пальцах кисти - полный (рис. 9).
Сохраняется легкая слабость в кисти при физической нагрузке. По результатам анкетирования отмечается положительная динамика: BCTOs - 1,36 балла, а BCTOf - 2,0 балла. На контрольной ЭМГ - также положительная динамика: А - 6,1 мВ; МС - 53 м/с; ДМЛ - 3,6 мс; СС - 54 м/с (рис. 10). Пациентка вполне удовлетворена результатами лечения.
ОБСУЖДЕНИЕ
В современных условиях оперативную декомпрессию срединного нерва в запястном канале выполняют посредством мини-доступа, стандартного доступа, а также эндоскопически. Так, J. Iida и соавт. (2008) отмечают, что после операций из мини-доступа 94 % пациентов полностью перестают беспокоить нарушения чувствительности в ночное и дневное время, а у 4 % они существенно уменьшаются. H. Aslani и соавт. (2012) [19] указывают на лучшие ранние результаты (через 4 месяца) у 105 пациентов при использовании мини-доступа и эндоскопической техники, в сравнении со стандартным доступом.
Вместе с этим, D. Louie и соавт. (2013) [20] сообщают о 88 % удовлетворительных результатах, достигнутых у 113 пациентов через 13 лет после операций, выполненных из стандартного доступа. M. Larsen и соавт. (2013) [21] сравнивают в 90 клинических наблюдениях стандартный доступ, мини-доступ и эндоскопическую технику и не выявляют значимых различий в результатах через 6 месяцев после операции.
Мини-доступ, примененный нами, практически всегда позволял полноценно и атравматично рассекать удерживатель сгибателей и проводить ревизию срединного нерва. Во всех 189 клинических наблюдениях нам удалось избежать повреждения ладонной чувствительной ветви срединного нерва и двигательной ветви тенара, развития инфекции и комплексного регионального болевого синдрома. Через 3 месяца после операции в четырех клинических наблюдениях (2,1 %) пациенты отмечали повышенную чувствительность в области послеоперационного рубца, и в семи клинических наблюдениях (3,7 %) - умеренную болезненность в области тенара и гипотенара. У всех пациентов эти симптомы были купированы консервативными мероприятиями.
Результаты лечения, полученные нами зависимо от исходной степени выраженности СЗК, отчасти соответствуют литературным данным. Так, J. Iida и соавт. (2008), разделяя клинические наблюдения по степени выраженности СЗК на 4 группы, отмечают 100 % выздоровления только в «ранней» группе, 99 % - в «средней», 94 % - в «умеренной» и 50 % выздоровления - в «выраженной» группе. У таких пациентов показатели ЭНМГ не достигают нормы даже через 12 месяцев после операции. Исходя из этого, авторы рекомендуют прибегать к раннему оперативному лечению, когда клинические проявления СЗК еще не уравнялись с «выраженной» группой.
M. Mondelli и соавт. (2000) [22] констатируют первое значимое улучшение через 1 месяц и второе улучшение - через 6 месяцев после операции, диагностированные по результатам опросника BCTO и измерения сенсорной и двигательной скорости. Авторы, однако, ничего не говорят о возможной корреляции данных опросника и величин ЭНМГ-скоростей. Мы такую зависимость выявили в период 1,5 месяцев после хирургического вмешательства. Отчетливо это проявилось при сравнении результатов опросников с уровнем амплитуды М-ответа (р = 0,003), величиной ДМЛ (р = 0,006) и со значением сенсорной скорости (p = 0,002). Кроме этого, в период 12 месяцев после операции мы отметили достоверную связь между критериями опросника BCTOf и снижением значений ДМЛ (р = 0,030).
J. Iida и соавт. (2008) указывают на успешное купирование ночной и дневной дизестезии у 94 % пациентов, подвергнутых открытой декомпрессии из мини-доступа. Авторы обращают внимание на то, что, независимо от степени выраженности заболевания, удовлетворительные результаты можно получить только тогда, когда скорость проведения импульса по сенсорным волокнам до операции сохраняется на минимальном уровне. Если она не идентифицируется (находится на нулевом уровне), то рассчитывать на успех оперативного лечения нет оснований. По нашим данным, абсолютное большинство пациентов, у которых до операции не удавалось определить сенсорную скорость, относились к третьей группе - с выраженной степенью СЗК.
S. Kronlage и M. Menendez (2015) [23] констатируют, что через 12 месяцев после операции и позже удается достичь более благоприятных результатов у пациентов с умеренными проявлениями заболевания по сравнению с выраженными. Симптомы заболевания остаются неустраненными у 2 % пациентов с умеренной и у 19 % - с выраженной степенью СЗК.
Несмотря на то, что в обеих категориях в целом имеется положительная клиническая динамика, у пациентов с выраженной симптоматикой восстановление чувствительности через 12 месяцев происходит не в полном объеме. В исследовании, проведенном нами, мы, аналогично, не наблюдали быстрого восстановления скорости проведения импульса по сенсорным волокнам у пациентов третьей группы с выраженной степенью СЗК. Через 12 месяцев после операции эта скорость у них также не достигла нормы.
K. Pedersen и соавт. (2017) [24] свидетельствуют, что через 1,5 месяца после операций, выполненных из стандартного доступа, характерным является уменьшение ДМЛ, но зависимо от его первоначального уровня. Так, в группе пациентов, у которых исходная ДМЛ была > 4,2 ms, ее показатели после хирургического вмешательства снижаются линейно.
Напротив, в группе, где исходная величина ДМЛ была 4,2 ms, ее значения остаются неизменными. По данным нашего исследования, величина ДМЛ у пациентов третьей группы в каждом периоде наблюдения изменялась в наименьшей степени, в сравнении с пациентами первой и второй групп.
S. Cha и соавт. (2016) отмечают, что у пациентов, давших согласие оперативное лечения сразу после консультации кистевым хирургом, клинические результаты являются значимо лучше, чем у лиц, отказавшихся от операции и лечившихся в течение последующих 6 месяцев консервативно. В настоящем исследовании мы такого сравнения не проводили.
J. Fowler и соавт. (2016) [25] констатируют, что начальная степень клинических проявлений СЗК, диагностированная по данным ЭНМГ и дискриминационного теста, является своеобразным предиктором успешного лечения. При выраженной степени симптомы заболевания удавалось устранять менее значимо и менее быстро, чем при легкой и умеренной степенях (р = 0,008). При этом между группами пациентов с легкой и умеренной степенями СЗК значимых различий в разрешении симптомов не выявлено (р = 0,4).
Существенное различие в купировании проявлений СЗК мы наблюдали через 1,5 и 3 месяца после операции - между первой и третьей группами и между второй и третьей группами. Наряду с этим, через 12 месяцев во всех клинических наблюдениях отмечали улучшение клинической картины, но практически без достоверных различий между группами.
ВЫВОДЫ
1. Открытая декомпрессия срединного нерва, выполненная у пациентов с СЗК из мини-доступа, позволяет во всех клинических наблюдениях достигнуть через 12 месяцев после операции существенного клинического и функционального улучшения.
2. У пациентов с «легкой» и «умеренной» степенью СЗК клиническое и функциональное улучшение наступает раньше - через 1,5 месяца после операции - по сравнению с пациентами с «выраженной» степенью СЗК.
3. Показатель дистальной моторной латентности, являющийся ведущим ЭНМГ-критерием в диагностике степени тяжести СЗК, через 12 месяцев приходит к норме у большинства пациентов с «легкой» и «умеренной» степенью заболевания. У пациентов с «выраженной» степенью СЗК величина данного критерия к этому сроку среднестатистической нормы не достигает.
4. Показатель дистальной моторной латентности, наряду с клиническими тестами, можно считать основополагающим критерием в принятии решения об оперативном лечении, особенно у пациентов с «легкой» и «умеренной» степенью выраженности СЗК.
ЛИТЕРАТУРА
1. Новиков А.В., Щедрина М.А., Мотякина О.П. Современные представления об этиологии и механизмах патогенеза компрессионно-ишемических невропатий верхней конечности (обзор литературы) // Вопросы травматологии и ортопедии. 2012. № 3. С. 35-39.
2. Синдром запястного (карпального) канала / А.А. Богов (мл.), Р.Ф. Масгутов, И.Г. Ханнанова, А.Р. Галямов, Р.И. Муллин, В.Г. Топыркин, И.Ф. Ахтямов, А.А. Богов // Практическая медицина. 2014. № 4-2: Инновационные технологии в медицине. С. 35-40.
3. Science of Variation Group. Carpal tunnel syndrome: Assessment of surgeon and patient preferences and priorities for decision-making / M.G. Hageman, A. Kinaci, K. Ju, T.G. Guitton, C.S. Mudgal, D. Ring // J. Hand Surg. Am. 2014. Vol. 39, No 9. P. 1799-1804.e1.
4. Differences in the postoperative outcomes according to the primary treatment options chosen by patients with carpal tunnel syndrome: conservative versus operative treatment / S.M. Cha, H.D. Shin, J.S. Ahn, J.W. Beom, D.Y. Kim // Ann. Plast. Surg. 2016. Vol. 77, No 1. P. 80-84. DOI: 10.1097/ SAP.0000000000000598
5. Wright A.R., Atkinson R.E. Carpal Tunnel Syndrome: An Update for the Primary Care Physician // Hawaii J. Health Soc. Welf. 2019. Vol. 78, No.11 Suppl. 2. P. 6-10.
6. Bland J.D. Treatment of carpal tunnel syndrome // Muscle Nerve. 2007. Vol. 36, No 2. P. 167-171. [PMID: 17534984]. DOI: 10.1002/mus.20802
7. Surgical versus non-surgical treatment for carpal tunnel syndrome / R.J. Verdugo, R.A. Salinas, J.L. Castillo, J.G. Cea // Cochrane Database Syst. Rev. 2008. Vol. 2008, No 4. P. CD001552. DOI: 10.1002/14651858.CD001552.pub2
8. Surgery versus non-surgical therapy for carpal tunnel syndrome: a randomized parallel-group trial / J.G. Jarvik, B.A. Comstock, M. Kliot, J.A. Turner, L. Chan, PJ. Heagerty, W. Hollingworth, C.L. Kerrigan, R.A. Deyo // Lancet. 2009. Vol. 374, No 9695. P. 1074-1081. DOI: 10.1016/ S0140-6736(09)61517-8
9. Kwon B.C., Jung K.I., Baek G.H. Comparison of sonography and electrodiagnostic testing in the diagnosis of carpal tunnel syndrome // J. Hand Surg. Am. 2008. Vol. 33, No 1. P.65-71. DOI: 10.1016/j.jhsa.2007.10.014
10. A comparison of the benefits of sonography and electrophysiologic measurements as predictors of symptom severity and functional status in patients with carpal tunnel syndrome / B. Kaymak, L. Oz^akar, A. Cetin, M. Candan Cetin, A. Akinci, Z. Has^elik // Arch. Phys. Med. Rehabil. 2008. Vol. 89, No 4. P. 743-748. DOI: 10.1016/j.apmr.2007.09.041
11. Carpal tunnel syndrome: electrophysiological grading and surgical results by minimum incision open carpal tunnel release / J. Iida, H. Hirabayashi, H. Nakase, T. Sakaki // Neurol. Med. Chir. (Tokyo). 2008. Vol. 48, No 12. P. 554-559. DOI: 10.2176/nmc.48.554
12. Clinical outcomes of endoscopic carpal tunnel release in patients 65 and over / J.D. Beck, N.C. Wingert, M.R. Rutter, K.S. Irgit, X. Tang, J.C. Klena // J. Hand Surg. Am. 2013. Vol. 38, No 8. P. 1524-1529. DOI: 10.1016/j.jhsa.2013.05.016
13. Zyluk A., Walaszek I., Szlosser Z. No correlation between sonographic and electrophysiological parameters in carpal tunnel syndrome // J. Hand Surg. Eur. Vol. 2014. Vol. 39, No. 2. P. 161-166. DOI: 10.1177/1753193413489046
14. The role of electrophysiological severity scales for decision-making with regard to surgery in idiopathic carpal tunnel syndrome / T. Kanatani, I. Nagura, Y. Harada, M. Sumi // Kobe J. Med. Sci. 2017. Vol. 63, No 3. P. E68-E72.
15. Гиннятулина Р.И. Международные подходы к управлению качеством медицинской помощи (обзор литературы) // Наука и инновации в медицине. 2019. Т. 4, № 4. С. 38-43.
17. A self-administered questionnaire for the assessment of severity of symptoms and functional status in carpal tunnel syndrome / D.W. Levine, B.P. Simmons, M.J. Koris, L.H. Daltroy, G.G. Hohl, A.H. Fossel, J.N. Katz // J. Bone Joint Surg. 1993. Vol. 75, No 11. P. 1585-1592. DOI: 10.2106/00004623-199311000-00002
18. Прогнозирование вероятности ревизионного эндопротезирования тазобедренного сустава с заменой вертлужного компонента в зависимости от вида его цементной фиксации / С.Н. Измалков, А.Н. Братийчук, А.К. Усов, Ф.Ш. Галеев, С.А. Литвинов // Гений ортопедии. 2019. Т. 25, № 4. С. 474-480.
19. Comparison of carpal tunnel release with three different techniques / H.R. Aslani, K. Alizadeh, A. Eajazi, A. Karimi, M.H. Karimi, Z. Zaferani, S.M. Hosseini Khameneh // Clin. Neurol. Neurosurg. 2012. Vol. 114, No 7. P. 965-968. DOI: 10.1016/j.clineuro.2012.02.017
20. Outcomes of open carpal tunnel release at a minimum of ten years / D.L. Louie, B.E. Earp, J.E. Collins, E. Losina, J.N. Katz, E.M. Black, B.P. Simmons, P.E. Blazar // J. Bone Joint Surg. Am. 2013. Vol. 95, No 12. P. 1067-1073. DOI: 10.2106/JBJS.L.00903
21. Carpal tunnel release: a randomized comparison of three surgical methods / M.B. Larsen, A.I. S0rensen, K.L. Crone, T. Weis, M.E. Boeckstyns // J. Hand Surg. Eur. Vol. 2013. Vol. 38 (E), No 6. P. 646-650. DOI: 10.1177/1753193412475247
22. Relationship between the self-administered Boston Questionnaire and electrophysiological findings in follow-up of surgically treated carpal tunnel syndrome / M. Mondelli, F. Reale, F. Sicurelli, L. Padua // J. Hand Surg. Br. 2000. Vol. 25, No. 2. P. 128-134. DOI: 10.1054/jhsb.2000.0361
23. Kronlage S.C., Menendez M.E. The benefit of carpal tunnel release in patients with electrophysiologically moderate and severe disease // J. Hand Surg. Am. 2015. Vol. 40, No 3. P. 438-444.e1. DOI: 10.1016/j.jhsa.2014.12.012
24. Evolution of clinical, electrophysiological, and radiological aspects of the carpal tunnel syndrome before and after surgery / K. Pedersen, V. Duez, B. Stallenberg, N. Mavroudakis // Acta Neurol. Belg. 2017. Vol. 117, No 4. P. 903-908. DOI: 10.1007/s13760-017-0837-0
25. Pre-operative electrodiagnostic testing predicts time to resolution of symptoms after carpal tunnel release / J.R. Fowler, M. Munsch, Y. Huang, W.C. Hagberg, J.E. Imbriglia // J. Hand Surg. Eur. Vol. 2016. Vol. 41, No 2. P. 137-142
Сведения об авторах:
1. Семенкин Олег Михайлович, к. м. н., ГБУЗ СО «Самарская областная клиническая больница им. В.Д. Середавина», г. Самара, Россия, ФГБОУ ВО СамГМУ Минздрава России, г. Самара, Россия
2. Измалков Сергей Николаевич, д. м. н., профессор, ФГБОУ ВО СамГМУ Минздрава России, г. Самара, Россия
3. Братийчук Александр Николаевич, д. м. н., профессор, ФГБОУ ВО «СамГМУ» Минздрава России, г. Самара, Россия
4. Солопихина Эля Борисовна, ГБУЗ СО «Самарская областная клиническая больница им. В.Д. Середавина», г. Самара, Россия
5. Балаклеец Светлана Владимировна, ГБУЗ СО «Самарская областная клиническая больница им. В.Д. Середавина», г. Самара, Россия
6. Богданова Мария Александровна, ГБУЗ СО «Самарская областная клиническая больница им. В.Д. Середавина», г. Самара, Россия
7. Князев Никита Алексеевич, ФГБОУ ВО «СамГМУ» Минздрава России, г. Самара, Россия
Теги: запястье
234567 Начало активности (дата): 19.02.2021 15:59:00
234567 Кем создан (ID): 989
234567 Ключевые слова: синдром запястного канала, оперативное лечение
12354567899
Похожие статьи
Определение костного возраста у детей с использованием ультразвукового метода исследованияРентген на дому 8 495 22 555 6 8
Поллицизация как метод восстановления двухстороннего схвата кисти при врожденной и приобретенной патологии верхней конечности
Пересадка кровоснабжаемых костных трансплантатов для лечения ложных суставов и дефектов костей
Восстановительные операции на культях кисти



