 30.04.2026
30.04.2026
Сравнительная оценка коммерческих наборов бактериофагов и перспективы их применения для лечения пациентов с ортопедической MRSA-инфекцией
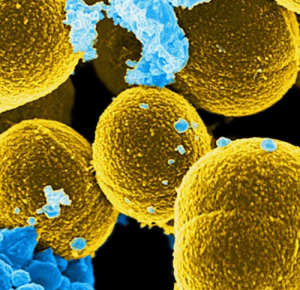
Стафилококки являются ведущими этиотропными агентами имплантат-ассоциированной инфекции, при этом 15 % штаммов S. aureus являются метициллин-резистентными (MRSA).
ВВЕДЕНИЕ
Антибиотики с момента их открытия в начале XX века произвели революцию в медицинской практике, позволили взять под контроль и вылечить многие инфекционные заболевания [1]. Широкое применение антибактериальных препаратов стимулировало развитие адаптивных механизмов устойчивости среди бактерий [2-4]. Всемирная организация здравоохранения признала устойчивость бактерий к антибиотикам одной из десяти главных угроз общественному здравоохранению [5]. Необходимость поиска альтернативных методов лечения, которые могут эффективно бороться с бактериальными инфекциями, является одним из приоритетов современной системы здравоохранения [6].
Возрастающее количество ортопедических операций, сопровождающихся установкой различных металлоконструкций, приводит к соответствующему увеличению числа инфекционных осложнений, связанных с имплантатами.
Частота инфекций, связанных с ортопедическими имплантатами, достигает 0,3-5,0 % при всех видах операций (погружной остеосинтез, эндопротезирование суставов) [7].
Золотым стандартом лечения пациентов с перипротезной инфекцией считается хирургическое удаление инфицированных имплантатов и длительное лечение антибиотиками, активными в отношении выделенных возбудителей.
Однако проблемы, связанные с устойчивостью патогенов к антибиотикам и сохранением биопленок на поверхности имплантатов, часто приводят к рецидивирующим или трудно поддающимся лечению инфекциям, что создает серьезную угрозу здоровью и жизни пациентов [8].
Лечение с использованием бактериофагов представляет собой многообещающий подход к решению проблемы антибиотикорезистентности бактерий [9-11]. Активность фагов определяется возможностью реализации всех стадий их жизненного цикла, включая адсорбцию, проникновение генетического материала в клетку, репликацию генетического материала, сборку фаговых частиц и лизис бактерии [12]. В отличие от антибиотиков широкого спектра действия, которые могут воздействовать на значительный спектр бактерий, фаги высокоспецифичны, обычно нацелены только на один вид или даже на определенный штамм бактерий [12]. Специфичность фагов представляет как сильные стороны, так и проблемы в их терапевтическом применении [13, 14]. Преимуществом является конкретное нацеливание на патогенные бактерии с сохранением полезной микробиоты человека. Однако такая специфичность требует точного микробиологического заключения для выбора активного фага, что делает назначение более сложным в сравнении с антибиотиками широкого спектра действия [15].
Цель работы — сравнительная оценка активности коммерческих наборов бактериофагов в отношении метициллин-резистентных Staphylococcus aureus, выделенных от пациентов с ортопедической инфекцией.
В настоящее время на фармацевтическом рынке РФ присутствуют разнообразные препараты бактериофагов, в том числе для местного и/или системного применения. Концентрация активных в отношении инфекционного агента бактериофагов в препарате напрямую влияет на его эффективность [16] и более широкие спектры активности, позволяющие снизить разнообразие фагов в коктейлях с сохранением суммарного диапазона действия, для терапевтических бактериофагов это является предпочтительным свойством [17, 18]. Особый интерес представляет сравнительный анализ литической активности отечественных препаратов бактериофагов в отношении штаммов стафилококков, выделенных от пациентов с ортопедической инфекцией.
МАТЕРИАЛЫ И МЕТОДЫ
Выделение культур S. aureus выполняли проспективно в 2025 г. из биоматериала пациентов с перипро- тезной инфекцией и/или остеомиелитом в соответствии с международными стандартами микробиологических исследований. Видовую идентификацию выполняли методом MALDI-TOF MS с использованием системы FlexContral и программного обеспечения MBT Compass 4.1, Score > 2,0. Чувствительность клинических изолятов к антибактериальным препаратам изучали в соответствии с требованиями EUCAST v.15.
По заключению локального комитета по этической экспертизе клинических и экспериментальных исследований данная работа основана на микробиологическом анализе свойств восприимчивости патогенов, что не является предметом рассмотрения в этическом комитете.
В исследовании оценена чувствительность MRSA (п = 25) к пяти отечественным препаратам бактериофагов (ПБФ):
ПБФ 1 — Пиофаг® (Микроген, Нижний Новгород, ИМП РУ ЛП-№ (002513)-(Pr-RU) МЗ РФ),
ПБФ 2 — Пиобактериофаг® (Микроген, Уфа, ИМП РУ № ЛС-002031 МЗ РФ),
ПБФ 3 — Секстафаг® (Микроген, Пермь, ИМП РУ № ЛС-001049 МЗ РФ),
ПБФ 4 — Стафилофаг® (Микроген, Нижний Новгород, ИМП РУ № Р N001973-01 МЗ РФ);
ПБФ 5 — Стафилофаг® (Микроген, Пермь, ИМП РУ № Р N001973-01 МЗ РФ).
Оценку литических свойств ПБФ выполняли на мясо-пептонном агаре (МПА). Для этого бактериальную взвесь (0,5 по МсF) ватным тампоном наносили на МПА и через 10 минут на поверхность агара дозатором наносили 10 мкл ПБФ в дубликатах. Чашки инкубировали при 37 °С. Через 24 часа оценивали активность ПБФ по пятибалльной шкале в соответствии с методическими рекомендациями «Рациональное применение бактериофагов в лечебной и противоэпидемической практике» (2023 г.) и в зависимости от полученных результатов определяли степень чувствительности штамма к действию определенного препарата: чувствителен, слабо чувствителен и устойчив.
Статистический анализ различий данных в исследуемых группах восприимчивости и коммерческих препаратов выполняли с помощью непараметрического параметра критерия Краскела - Уоллиса в программе IBM SPSS Statistics Version 26. В случае выявления статистически значимых различий при анализе активности трех препаратов бактериофагов для попарного сравнения групп (post-hoc анализ) применяли критерий Данна (Dunn's test) с поправкой на множественные сравнения. С учетом множественных сравнений использовали меньший критический уровень значимости, который рассчитывался по формуле: p = 1 - 0,951/n, где n — количество производимых сравнений. Для данного исследования статистически значимыми считали значения p < 0,017.
РЕЗУЛЬТАТЫ
Все включенные в исследование штаммы S. aureus (n = 25) характеризовались устойчивостью к це- фокситину (MRSA). Тестируемые препараты бактериофагов были активны в отношении большинства клинических изолятов MRSA, выделенных от пациентов с ортопедической инфекцией, однако при сравнении ПБФ были выявлены различия (табл. 1, рис. 1).
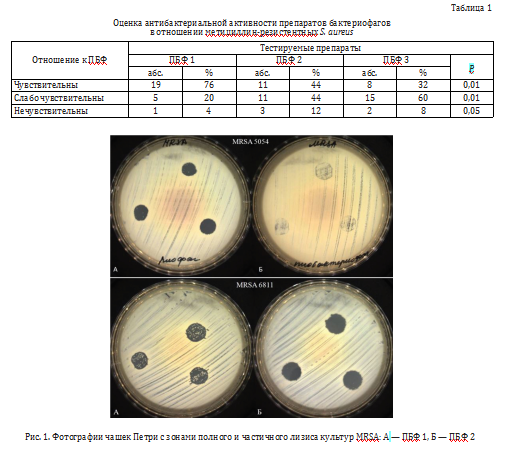
Из протестированных штаммов MRSA наибольшее количество (76 %) были чувствительны к препарату ПБФ 1 (р = 0,004 — попарное сравнение с ПБФ 2). Для остальных градаций чувствительности зарегистрирована обратная тенденция, — большее количество штаммов (60 %) были отнесены к группе «слабо чувствительны» к ПБФ 3 (р = 0,003 — попарное сравнение с ПБФ 1, р = 0,009 — общее). Доли «нечувствительных» культур отличались меньше, при этом только один штамм демонстрировал устойчивость ко всем трем тестируемым препаратам бактериофагов.
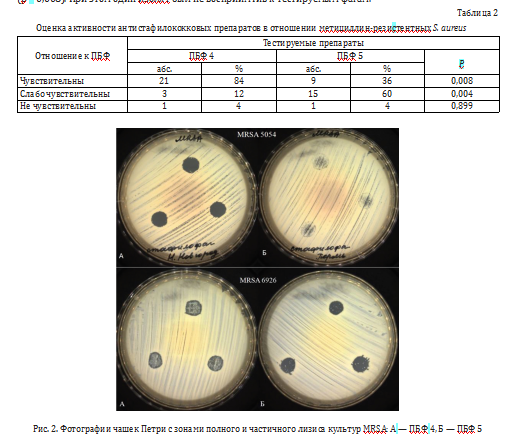
Сравнительный анализ антистафилококковых препаратов различного производства также показал отличия в их активности против клинических изолятов MRSA, выделенных от пациентов в нашем Центре (табл. 2, рис. 2).
Доля изолятов, чувствительных к препарату ПБФ 4, составила 84 %, а к ПБФ 5 — 36 % (р = 0,008). При этом один изолят был не восприимчив к тестируемым фагам.
ОБСУЖДЕНИЕ
Наличие механизмов резистентности к антибиотикам у возбудителей инфекционных заболеваний ухудшает прогноз исхода заболевания, удлиняет сроки лечения и значимо увеличивает расходы системы здравоохранения [1]. В нашем исследовании 2024 г. показано, что в течение 12-летнего периода в 33 % случаев возбудителями ортопедической инфекции были S. aureus, из них доля метициллин-резистентных штаммов S. aureus не снижалась ниже 15 % на протяжении всего изученного периода [19]. В работах А.В. Цискарашвили с соавт. [20] и А.В. Соколовского с соавт. [21] также было установлено, что наиболее частыми возбудителями перипротезной инфекции были S. aureus, — 32 % и 38 % соответственно.
Способность S. aureus противостоять широкому спектру антибактериальных препаратов делает его идеальным объектом для исследований с использованием бактериофагов. В последние годы подходы к отбору, производству и доставке фагов значительно расширились, а усовершенствование технологий их получения позволяет проводить персонализированную фаговую терапию.
В травматологии и ортопедии в ряде клинических случаев показан многообещающий потенциал фагов против MRSA [22]. Е.А. Фёдоров с соавт. продемонстрировали, что добавление раствора коммерческого стафилококкового бактериофага (6 мл на 40,0 г сухого вещества полиметилметакрилата) с дальнейшим введением его по дренажу или пункционно в перипротезную область в течение 10 дней увеличивает эффективность одноэтапного лечения стафилококковой перипротезной инфекции тазобедренного сустава с 69 % до 96 % [23]. T. Ferry et al. регистрировали улучшение состояние трех пациентов с хронической перипротезной инфекцией после использования фагового коктейля в сочетании с антибиотиками [24]. Аналогичные результаты представлены в работе C. Ramirez-Sanchez et al., в которой авторы описали успешное лечение пациентов с MRSA-инфекцией коленного сустава путем внутрисуставного введения фагового коктейля [25]. Разнообразие методов использования свидетельствует о безопасности применения бактериофагов, что являются их значимым преимуществом в сравнении с антибиотиками. Однако для успешной фаготерапии необходимо четкое определение чувствительности конкретного возбудителя к определенному препарату бактериофагов (к конкретной партии коммерческого набора), что обеспечит элиминацию патогена и профилактику развития резистентности бактерий к бактериофагу.
В нашем Центре чувствительность к фагам определяют для всех выделенных штаммов MRSA, используя различные коммерческие препараты. При лечении пациентов с перипротезной инфекцией, вызванной возбудителем чувствительным к имеющимся фагам, после завершения операции устанавливают дренаж из полости сустава. По дренажу в перипротезную область в течение трех-пяти дней ежедневно вводят по 20 мл препарата бактериофагов, затем дренаж перекрывают для увеличения времени экспозиции фагов. После завершения фаготерапии дренаж удаляют. В соответствии с клиническими рекомендациями, все пациенты с перипротезной инфекцией также получают высокодозную, этиотропную антибактериальную терапию, так как бактериофаготерапия не отменяет назначение антибиотиков, а осуществляется совместно в составе комплексного лечения. В обзоре 2023 г. [26] описаны результаты исследований совместного применения литических бактериофагов и антибиотиков в отношении инфекций, вызванных резистентными штаммами S. aureus. Авторы подчеркивают, что во многих случаях комбинированное введение фага и антибиотика приводит к значительному снижению роста численности бактерий, в то время как обратный антагонистический эффект встречается значительно реже [26]. На результаты лечения может влиять последовательность введения терапевтических агентов, наилучшие результаты регистрируют в случаях, когда фаготерапия предшествует антибиотикам [27]. Также установлено, что применение бактериофагов может менять профиль чувствительности бактерий к антибактериальным препаратам и, как следствие, ведет к включению препарата в схему лечения [28].
Кроме того, понимание фармакокинетики (ФК) и фармакодинамики (ФД) фагов имеет решающее значение для оптимизации терапевтической эффективности в клинических условиях [29]. Однако достижение всестороннего понимания ФК/ФД для фаговой терапии представляет собой сложную задачу из-за наличия трехсторонних взаимодействий между фагами, бактериями и человеком. Поскольку практически каждая комбинация фаг - бактерия - пациент может демонстрировать уникальный профиль ФК/ФД, разработка стандартизированных моделей, применимых в различных клинических ситуациях, остается сложной задачей. До настоящего времени не существует валидированного подхода к клиническому использованию фаговой терапии, что требует проведения сравнительных клинических исследований или накопления и анализа данных реальной клинической практики использования бактериофагов при лечении пациентов с ортопедической инфекцией.
Выполненное нами сравнительное исследование активности коммерческих наборов бактериофагов в отношении клинических штаммов MRSA, выделенных от пациентов с ортопедической инфекцией, показало высокий уровень литических свойств входящих в состав препаратов фагов. Особенно важно отметить различный уровень антибактериального действиях наборов, произведенных на разных территориальных производствах. В работе И.М. Пчелина с соавт. отмечено, что поиск активных бактериофагов, планируемых для использования в качестве противомикробных средств, вероятно, следует проводить в местообитаниях, географически приближенных к популяциям патогенных бактерий [30]. По-видимому, различия в активности коммерческих наборов могут быть связаны с составом полученных препаратов, обладающих меньшей тропностью к штаммам, выделенным от пациентов другого региона. Однако поиск активных фагов, скорее, необходим при назначении персонализированной фаготерапии с подбором конкретного бактериофага против определенного штамма возбудителя. С учетом широкой географии проживания пациентов с ортопедической инфекцией, госпитализируемых в Федеральные Центры, возможность выбирать бактериофаги из широкой линейки представленных на рынке коммерческих наборов увеличивает вероятность успешного их применения.
ЗАКЛЮЧЕНИЕ
Представленные на рынке отечественные коммерческие препараты бактериофагов характеризовались различной литической активностью в отношении метициллин-резистентных S. aureus, выделенных от пациентов с ортопедической инфекцией. Пиофаг® и Стафилофаг® (Н. Новгород) показали высокую эффективность в сравнении с другими протестированными препаратами. В травматологии и ортопедии применение фаготерапии следует рассматривать как один из перспективных методов борьбы с инфекциями, вызванными резистентными к антибиотикам возбудителями, совместно с принятыми методами лечения после обязательного исследования восприимчивости патогена к препаратам бактериофагов.
СПИСОК ИСТОЧНИКОВ
Akinwotu ST, Fapohunda O. War against antimicrobial resistance. J Microbiol Exp. 2020;8(4):148-154. doi: 10.15406/jmen.2020.08.00300.
Sinha S, Upadhyay LSB. Understanding antimicrobial resistance (AMR) mechanisms and advancements in AMR diagnostics. Diagn Microbiol Infect Dis. 2025;113(2):П6949. doi: 10.1016/j.diagmicrobio.2025.116949.
Muteeb G, Kazi RNA, Aatif M, et al. Antimicrobial resistance: Linking molecular mechanisms to public health impact. SLAS Discov. 2025;33:100232. doi: 10.1016/j.slasd.2025.100232.
Behera B, Singh R, Sharma K, et al. A comprehensive review of advanced strategies to combat antimicrobial resistance. Arch Microbiol. 2025;207(11):281. doi: 10.1007/s00203-025-04464-3.
FAO, OIE, WHO, UNEP. Antimicrobial resistance and the United Nations Sustainable Development Cooperation Framework: Guidance for United Nations country teams. Paris, FAO, OIE and WHO; 2021.
Kelly JB, Nolan AC, Zeden MS. How can we escape the ESKAPEs: Antimicrobial resistance mechanisms and what lies ahead? PLoSPathog. 2024;20(6):e1012270. doi: 10.1371/journal.ppat.1012270.
Grammatopoulos G, Kendrick B, McNally M, et al. Outcome Following Debridement, Antibiotics, and Implant Retention in Hip Periprosthetic Joint Infection-An 18-Year Experience. J Arthroplasty. 2017;32(7):2248-2255. doi: 10.1016/j.arth.2017.02.066.
Mayorga-Ramos A, Carrera-Pacheco SE, Barba-Ostria C, Guaman LP. Bacteriophage-mediated approaches for biofilm control. Front Cell Infect Microbiol. 2024;14:1428637. doi: 10.3389/fcimb.2024.1428637.
Olawade DB, Fapohunda O, Egbon E, et al. Phage therapy: A targeted approach to overcoming antibiotic resistance. Microb Pathog. 2024;197:107088. doi: 10.1016/j.micpath.2024.107088.
Ibrahim R, Aranjani JM, Kalikot Valappil V, Nair G. Unveiling the potential bacteriophage therapy: a systematic review. Future Sci OA. 2025;11(1):2468114. doi: 10.1080/20565623.2025.2468114.
Kushwaha SO, Sahu SK, Yadav VK, et al. Bacteriophages as a potential substitute for antibiotics: A comprehensive review. CellBiochem Funct. 2024;42(3):e4022. doi: 10.1002/cbf.4022.
Hatfull GF, Dedrick RM, Schooley RT. Phage Therapy for Antibiotic-Resistant Bacterial Infections. Annu Rev Med. 2022;73:197-211. doi: 10.1146/annurev-med-080219-122208.
D^browska K. Phage therapy: What factors shape phage pharmacokinetics and bioavailability? Systematic and critical review. Med Res Rev. 2019;39(5):2000-2025. doi: 10.1002/med.21572.
Palma M, Oi B. Advancing Phage Therapy: A Comprehensive Review of the Safety, Efficacy, and Future Prospects for the Targeted Treatment of Bacterial Infections. Infect Dis Rep. 2024;16(6):1127-1181. doi: 10.3390/idr16060092.
Akinwotu ST, Fapohunda O. War against antimicrobial resistance. J Microbiol Exp. 2020;8(4):148-154. doi: 10.15406/ jmen.2020.08.00300.
Ryan EM, Gorman SP, Donnelly RF, Gilmore BF. Recent advances in bacteriophage therapy: how delivery routes, formulation, concentration and timing influence the success of phage therapy. J Pharm Pharmacol. 2011;63(10):1253-1264. doi: 10.1111/j.2042- 7158.2011.01324.x.
Ross A, Ward S, Hyman P. More Is Better: Selecting for Broad Host Range Bacteriophages. Front Microbiol. 2016;7:1352. doi: 10.3389/ fmicb.2016.01352.
Casey E, van Sinderen D, Mahony J. In Vitro Characteristics of Phages to Guide 'Real Life' Phage Therapy Suitability. Viruses. 2018;10(4):163. doi: 10.3390/v10040163.
Касимова А.Р., Туфанова О.С., Гордина Е.М. и др. Двенадцатилетняя динамика спектра ведущих возбудителей ортопедической инфекции: ретроспективное исследование. Травматология и ортопедия России. 2024;30(1):66-75. doi: 10.17816/2311- 2905-16720.
Цискарашвили А.В., Меликова Р.Э., Новожилова Е.А. Анализ шестилетнего мониторинга основных возбудителей перипротез- ной инфекции крупных суставов и их тенденция к резистентности. Гений ортопедии. 2022;28(2): 179-188. doi: 10.18019/1028- 4427-2022-28-2-179-188.
Соколовский А.В., Соколовский В.А., Мачак Г.Н. и др. Отдалённые результаты профилактики и лечения перипротезной инфекции в онкоортопедии. Вестник травматологии и ортопедии им. Н.Н. Приорова. 2023;30(2):143-159. doi: 10.17816/vto322787.
Шералиев Т.У., Самохин А.Г., Таштанов Б.Р., и др. Возможности фаготерапии при лечении перипротезной инфекции, вызванной полирезистентными возбудителями: обзор литературы. Травматология и ортопедия России. 2024;30(4):180-191. doi: 10.17816/2311-2905-17563.
Фёдоров Е.А., Кретьен С.О., Самохин А.Г. и др. Ближайшие результаты лечения стафилококковой перипротезной инфекции тазобедренного сустава с использованием комбинированной терапии антибиотиками и бактериофагами. Acta Biomedica Scientifica. 2021;6(4):50-63. doi: 10.29413/ABS.2021-6.4.5.
Ferry T, Kolenda C, Batailler C, et al. Phage Therapy as Adjuvant to Conservative Surgery and Antibiotics to Salvage Patients With Relapsing S. aureus Prosthetic Knee Infection. Front Med (Lausanne). 2020;7:570572. doi: 10.3389/fmed.2020.570572.
Ramirez-Sanchez C, Gonzales F, Buckley M, et al. Successful Treatment of Staphylococcus aureus Prosthetic Joint Infection with Bacteriophage Therapy. Viruses. 2021;13(6):1182. doi: 10.3390/v13061182.
Абдраймова Н.К., Шитиков Е.А., Городничев Р.Б., Корниенко М.А. Комбинация бактериофагов и антибиотиков как наиболее эффективный подход борьбы со Staphylococcus aureus. Медицина экстремальных ситуаций. 2023;25(4):39-47. doi: 10.47183/ mes.2023.058.
Gordillo Altamirano FL, Barr JJ. Phage Therapy in the Postantibiotic Era. Clin Microbiol Rev. 2019;32(2):e00066-18. doi: 10.1128/ CMR.00066-18.
Chaudhry WN, Concepcion-Acevedo J, Park T, et al. Synergy and Order Effects of Antibiotics and Phages in Killing Pseudomonas aeruginosa Biofilms. PLoSOne. 2017;12(1):e0168615. doi: 10.1371/journal.pone.0168615.
Kim MK, Suh GA, Cullen GD, et al. Bacteriophage therapy for multidrug-resistant infections: current technologies and therapeutic approaches. J Clin Invest. 2025;135(5):e187996. doi: 10.1172/JCI187996.
Пчелин И.М., Гончаров А.Е., Асланов Б.И., Азаров Д.В. Спектры литической активности бактериофагов. Антибиотики и хими- отер. 2023; 68 (11-12): 59-66. doi: 10.37489/0235-2990-2023-68-11-12-59-66.
Статья поступила 18.12.2025; одобрена после рецензирования 19.12.2025; принята к публикации 09.02.2026.
The article was submitted 18.12.2025; approved after reviewing 19.12.2025; accepted for publication 09.02.2026.
Информация об авторах:
Екатерина Михайловна Гордина — кандидат медицинских наук, старший научный сотрудник
Алина Рашидовна Касимова — кандидат медицинских наук, доцент, доцент кафедры, врач — клинический фармаколог
Светлана Анатольевна Божкова — доктор медицинских наук, профессор, заведующая научным отделением
Лариса Николаевна Смирнова — лаборант
Теги: ортопедическая инфекция
234567 Начало активности (дата): 30.04.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: бактериофаги, ортопедическая инфекция, S. aureus, MRSA
12354567899
Похожие статьи
Как снять пластиковый гипс?Рентген на дому 8 495 22 555 6 8
Эндопротезирование суставов
Заболевания кисти при специфических хирургических инфекциях
Инфекция протезированного тазобедренного сустава



