 14.02.2026
14.02.2026
Лечение ВИЧ-инфицированных пациентов с инфекционным неспецифическим кокситом с использованием антимикробного спейсера тазобедренного сустава
. Борьба с неспецифической инфекцией на фоне иммунодефицита у ВИЧ-инфицированных больных представляет собой сложную задачу
ВВЕДЕНИЕ
Заболеваемость инфекционными кокситами в мире составляет от 4 до 10 на 100 000 человек [1]. Проблема оказания медицинской помощи пациентам с инфекционными кокситами сохраняет свою актуальность в связи с отсутствием эффективных протоколов лечения [2, 3, 4]. При несвоевременном лечении инфекционный процесс приводит к деструктивным изменениям костных структур суставных образований, значительному снижению качества жизни пациента, а иногда к развитию сепсиса и летальному исходу [5].
Особенно сложной задачей является лечение пациентов с инфекционным кокситом, ассоциированным с ВИЧ-инфекцией. Распространенность воспалительных заболеваний суставов среди пациентов с ВИЧ-инфекцией варьирует от 3 до 71 % [6, 7]. В то же время статистически значимых данных о результатах лечения этой когорты пациентов в доступной литературе практически нет. В публикациях со ссылкой на незначительное число наблюдений авторы отмечают высокий процент неудовлетворительных результатов [8].
Авторы исследований приводят данные об эффективности двухэтапного эндопротезирования тазобедренного сустава при инфекционных кокситах как технологии, позволяющей добиться эрадикации инфекционного процесса и восстановления утраченной функции сустава [9, 10, 11, 12]. Логично предположить, что данная методика может являться технологией выбора и при ВИЧ-ассоциированном коксите. Преимуществом применения на первом этапе насыщенного антимикробными препаратами цементного спейсера является возможность сохранить анатомические взаимоотношения между резецированными суставными концами, обеспечить функциональную активность и удовлетворительное качество жизни пациента до установки постоянного импланта, создать депо антимикробных препаратов, осуществляя локальное воздействие на патогенную микрофлору в области сустава [13, 14, 15, 16]. Создание локальной бактерицидной концентрации является одной из основных функций спейсера и позволяет сократить продолжительность и увеличить эффективность системной антибактериальной терапии [13, 14, 15, 16].
Цель работы — на двух клинических примерах продемонстрировать возможность применения оригинальной конструкции антимикробного двухслойного артикулирующего спейсера, ранее разработанной для лечения пациентов с деструктивными формами туберкулезного коксита, в оперативном лечении больных неспецифическим инфекционным кокситом с ВИЧ-инфекцией.
Вместе с тем, в ряде исследований доказано, что при создании высоких концентраций нагруженной препаратами цементной смеси при изготовлении спейсера отмечается значительное снижение прочностных характеристик конструкций [17, 18, 19]. Известно, что максимальный выход антибиотика происходит с поверхности спейсера, а антимикробные препараты из внутренних отделов спейсера за счет плотности структуры костного цемента практически не элюируют в окружающую среду [20, 21, 22]. Таким образом, депонирующую функцию несет не весь спейсер, а только его поверхностный слой. В связи с этим насыщение антимикробными препаратами всего объема цемента для изготовления спейсера является нецелесообразным. Насыщение антимикробными препаратами только поверхностных слоев спейсера не отражается на прочностных характеристиках и повышает его медикаментозную эффективность, что позволяет добиться высокой локальной антимикробной концентрации даже таких препаратов как рифампицин, известный своим ингибирующим действием на процесс полимеризации костного цемента [23].
МАТЕРИАЛЫ И МЕТОДЫ
Ретроспективно оценены результаты лечения двух больных инфекционным кокситом, страдающих ВИЧ-инфекцией, у которых на первом этапе лечения использована оригинальная двухслойная конструкция цементного спейсера, насыщенного антимикробными препаратами в зависимости от индивидуальной чувствительности микробного агента.
Для достижения поставленной цели конструктивным решением стало создание спейсера тазобедренного сустава с двухкомпонентной головкой, внутренний компонент которой изготавливается из обычного цемента с известными прочностными характеристиками, а наружный компонент выполняется из цементной мантии, содержащей антимикробные препараты в необходимых, в т.ч. и высоких, концентрациях в зависимости от индивидуальной чувствительности микробного агента. На устройство получен патент РФ «Антимикробный спейсер тазобедренного сустава» RU 212287 U1 [24].
Техника оперативного вмешательства
После стандартного доступа к тазобедренному суставу вывихивают головку бедренной кости, резецируют ее, удаляют капсулу сустава, гнойное содержимое, некротические ткани. Штангенциркулем измеряют диаметр головки бедренной кости. Производят механическую и антисептическую обработку полости резецированного сустава. В бедренной кости рашпилем минимального размера формируют ложе для установки спейсера. Далее на отдельном столике изготавливают спейсер. Первым этапом, методом литья из костного цемента, изготавливают ножку спейсера в стерильной пластиковой пресс-форме, а по оси ножки располагают металлическую арматуру, обеспечивающую его прочность на сгибание.
В верхней части ножки проксимальный конец металлической арматуры длиной 40 мм на первом этапе остается временно непокрытым цементной мантией до изгиба. Размер пластиковой пресс-формы и соответственно ножки соответствует нулевому размеру рашпиля системы «ЭСИ» по аналогии с методикой установки эндопротеза. Вторым этапом изготавливают головку спейсера. Первый (внутренний) компонент головки полушаровидной формы изготавливают целиком из костного цемента путем погружения проксимального конца металлической арматуры ножки в специальную пластиковую форму нескольких типоразмеров (диаметром 44 мм, 46 мм, 48 мм, 50 мм, 52 мм, 54 мм, 56 мм и 58 мм), заполненную жидким цементом на стадии полимеризации. Размер внутреннего компонента головки подбирают на 2 мм меньше размеров удаленной головки бедренной кости и вертлужной впадины.
После частичного затвердевания первого компонента через 4-6 минут после начала полимеризации его извлекают из пластиковой формы. Затем изготавливают второй (наружный) компонент головки. Изначально в порошкообразный полимер костного цемента добавляют порошковые формы антимикробных препаратов в необходимой концентрации и перемешивают механическим путем. Далее в порошковидную смесь полимера с антимикробным препаратом добавляют жидкий мономер, смесь помещают в пластиковую форму размером на 2 мм больше внутреннего компонента. Внутренний компонент головки погружают в заполненную цементно-антимикробным составом форму до затвердевания на 8-10 минутах после смешивания, затем образец извлекают из пластиковой формы.
Таким образом, головка спейсера, изготовленного по данной технологии, состоит из двух компонентов: первый (внутренний) выполнен из цемента, соответственно обладает необходимыми прочностными характеристиками и может нести функциональную нагрузку; второй (наружный) толщиной 2 мм выполнен из смеси цемента с антимикробным препаратом и обладает антимикробным эффектом.
Соответственно, кроме опорно-двигательной функции изготовленный спейсер выполняет роль депо с постепенным высвобождением антимикробного препарата. Изготовленный спейсер вводят в канал бедренной кости. Головку спейсера вправляют в вертлужную впадину. Рану ушивают послойно. Дозированную ходьбу разрешают через 2-4 дня после операции.
Для исследования эффективности метода использовали результаты динамической оценки выраженности болевого синдрома по шкале ВАШ, функционального состояния поражённого сустава с помощью шкал HSS (англ.: Harris Hip Score), WOMAC (англ.: Western Ontario and McMaster Universities osteoarthritisIndex) и лучевые данные пациентов в раннем послеоперационном периоде и через 12 мес. наблюдения.
Первый клинический случай
У пациента Ш. 42 лет с левосторонним кокситом инфекционистами установлен сопутствующий диагноз: ВИЧ-инфекция 3 ст., субклиническая на фоне приема антиретровирусных препаратов (АРТ), выявленная в 2021 г., путь заражения со слов пациента — половой. В анамнезе: операция по поводу варикоцеле слева в 1994 г.
Боли в тазобедренном суставе — с ноября 2021 г. В июле 2022 г. получил курс внутрисуставных инъекций препаратов гиалуроной кислоты с непродолжительным положительным эффектом. С декабря 2022 г. боль резко усилилась, стал передвигаться при помощи костылей.
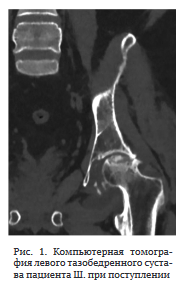
Антибактериальную терапию на амбулаторном этапе не получал. Поступил в НМИЦ ФПИ с жалобами на боль в левом тазобедренном суставе, передвигался при помощи костылей. Функциональные показатели сустава по шкале HHS — 35, по шкале WOMAC — 79, выраженность болевого синдрома по шкале ВАШ — 7 баллов. На КТ левого тазобедренного сустава определена деструкция верхнего фрагмента головки левой бедренной кости без признаков контактной деструкции вертлужной впадины, сужение суставной щели (рис. 1).
Иммунологические исследования: CD-4 = 551 кл/мкл, ВН в крови < 20 копий/мл. Лабораторные исследования: отклонение от рееференсных значений: СОЭ — 36 мм в час, лейкоциты — 2,41*109, С-реактивный белок — 4,5 мг/л. 07.03.2023 под лучевым контролем выполнена трепанобиопсия области очага костной деструкции в головке бедренной кости.
Микробиологическое исследование биоматериала: получена культура Acinetobacter baumanii (чувствительность к гентамицину), Staphylococcus capitis (чувствительный ко всему спектру антибиотиков). Патогистологическое заключение: признаки хронического неспецифического коксита. Пациенту установлен диагноз: неспецифический коксит слева, ассоциированный с ВИЧ-инфекцией.
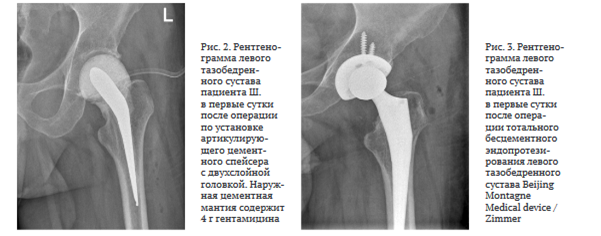
Перед оперативным лечением по назначению клинического фармаколога проведен курс комбинированной антибактериальной терапии: меропенем 2000 мг 3 раза в сут. в/в, амикацин 1000 мг 1 раз в сут. в/в в течение 15 дней. 27.03.2023 проведена резекция головки левой бедренной кости, установка артикулирующего двухслойного спейсера с гентамицином (4 г) (рис. 2). ПЦР операционного материала от 28.03.2023: ДНК микробактерии туберкулеза (МБТ) не обнаружена. Послеоперационный период протекал без осложнений.
При повторной госпитализации через семь месяцев в НМИЦ ФПИ выполнена трехкратная пункция пери- имплантного пространства левого тазобедренного сустава. Роста микроорганизмов не выявлено. Перед вторым этапом эндопротезирования функциональные показатели сустава по шкале HHS — 64, по шкале WOMAC — 32, выраженность болевого синдрома по шкале ВАШ — 2 балла. 17.11.2023 произведен второй этап эндопротезирования в объеме удаления артикулирующего спейсера, тотального бесцементного эндопротезирования левого тазобедренного сустава Beijing Montagne Medical device / Zimmer (рис. 3).
Второй клинический случай
Пациент К. 47 лет с правосторонним кокситом в анамнезе на догоспитальном этапе перенес двухсторонний эксудативный плеврит, туберкулёзный спондилит Th8-Th10.
Заключение инфекциониста: ВИЧ 4В, фаза ремиссии на фоне АРТ. Хронический гепатит С вне биохимической активности. ВИЧ выявлен в 2020 г. Путь заражения — половой. АРТ с 2020 г. по схеме: тенфовир, ламивудин, долутегра- вир. При поступлении заключение фтизиатра: клиническое излечение двухстороннего экссудативного плеврита, туберкулёзного спондилита Th8-Th10. В 2021 г. проведено лечение по режиму 3 противотуберкулезной химиотерапии, получено 324 дозы
Со слов пациента, считает себя больным с июня 2022 г., когда возникла боль и припухлость в области правого тазобедренного сустава. В стационаре по месту жительства в течение трех недель получал антибактериальную терапию линкомицином с временным положительным эффектом. В августе 2022 г. начал ходить с дополнительной опорой на костыли с дозированной нагрузкой на правую нижнюю конечность. На фоне нагрузки боль снова усилилась, повторно в течение двух недель проводили курс антибактериальной терапии (линкомицин) с положительным эффектом.
Пациент поступил в клинику НМИЦ ФПИ с жалобами на боль и резкое ограничение движений в правом тазобедренном суставе. Функциональные показатели сустава по шкале HHS — 25, по шкале WOMAC — 84, выраженность болевого синдрома по шкале ВАШ — 6 баллов.
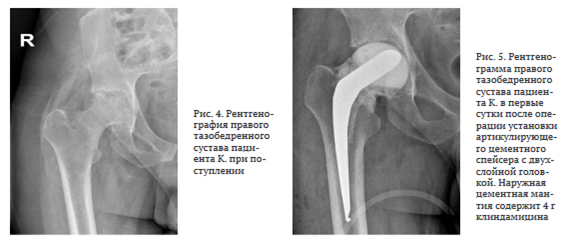
На рентгенограмме правого тазобедренного сустава визуализировали контактную деструкцию суставных концов, сужение суставной щели (рис. 4).
Под лучевым контролем выполнена трепанационная биопсия головки правой бедренной кости.
Исследование биологического материала: ДНК МБТ не обнаружена. При определении РНК вируса иммунодефицита человека методом ПЦР-РВ (HIV) в биоптате обнаружено 6,7*104 коп/мл. Микроскопия операционного материала: отрицательно. Микробиологическое исследование операционного материала: роста микроорганизмов не выявлено. Гистологическое исследование: признаки неспецифического коксита. Иммунологическое исследование крови: СД4 — 19 % — 654 кл/мкл, РНК ВИЧ — 120 коп/мл. Учитывая данные анамнеза и гистологического исследования, установлен диагноз: правосторонний неспецифический коксит.
07.03.23 произведена операция в объеме резекции головки бедренной кости, установки артикулирующего спейсера из костного цемента с клиндамицином (4,5 г) (рис. 5). Выбор клиндомицина обусловлен близким к линкомицину механизмом действия и антимикробным спектром (в анамнестических данных пациента есть указания на положительный эффект применения линкомицина), а также высокой элюционной способностью препарата [25].
Микробиологическое исследование тканей, взятых интрао- перационно, возбудителя не выявило.
Послеоперационных осложнений не отмечено, больной приступил к ходьбе с дополнительной опорой на вторые сутки после операции. Выписан под наблюдение травматолога-ортопеда и инфекциониста.
Повторно госпитализирован через шесть месяцев. Местный статус: укорочения правой нижней конечности нет. Послеоперационный рубец — без признаков воспаления.
Функциональные показатели сустава по шкале HHS — 77, по шкале WOMAC — 24, выраженность болевого синдрома по шкале ВАШ — 2 балла. При пальпации обнаружена незначительная локальная болезненность в проекции правого тазобедренного сустава (2 балла по шкале ВАШ).
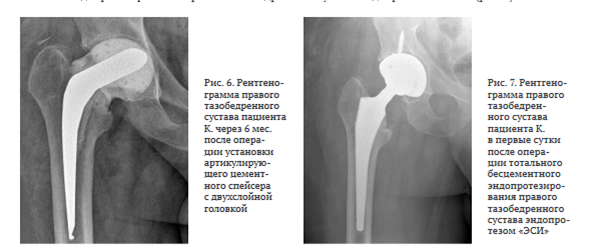
Рентгенограмма представлена на рис. 6.
Выполнена пункция периимплантного пространства из трех точек. При микробиологическом исследовании операционного материала роста микрофлоры не выявлено.
10.10.2023 произведена операция в объеме: удаление артикулирующего спейсера, тотальное бесцементное эндопротезирование правого тазобедренного сустава эндопротезом «ЭСИ» (рис. 7).
Через 12 мес. после второго этапа эндопротезирования в объеме удаления артикулирующего спейсера, тотального бесцементного эндопротезирования левого тазобедренного сустава Beijing Montagne Medical device / Zimmer функциональные показатели сустава пациента по шкале HHS — 89, по шкале WOMAC — 14, выраженность болевого синдрома по шкале ВАШ — 1 балл. Рентгенограмма представлена на рис. 8.
Через 12 мес. после операции тотального бесцементного эндопротезирования правого тазобедренного сустава эндопротезом "ЭСИ" функциональные показатели сустава по шкале HHS — 91, по шкале WOMAC — 11, выраженность болевого синдрома по шкале ВАШ — 0 баллов. Рентгенограмма представлена на рис. 9.
ОБСУЖДЕНИЕ
В литературе не приводятся результаты лечения больных инфекционным кокситом, ассоциированным с ВИЧ-инфекцией. Отдельные авторы публикуют данные о примерно одинаковой частоте неудовлетворительных результатов у пациентов с нормальным и сниженным иммунодефицитом при эндопротезировании дегенеративных заболеваний суставов [25]. Другие авторы отмечают значительное снижение эффективности двухэтапного лечения, даже с применением антибактериального спейсера, при наличии имплантат-ас- социированной инфекции [26]. Первичные гнойные артриты на фоне ВИЧ-инфекции представляют крайне сложную клиническую группу. Наш опыт клинических наблюдений этой когорты пациентов показывает высокую частоту неудовлетворительных результатов, выражающихся в реактивации инфекции.
Техническим результатом применения разработанной технологии является возможность создания длительной высокой локальной концентрации используемых антимикробных препаратов, добавляемых к костному цементу, что повышает эффективность лечения [27, 28, 29, 30] и позволяет сохранить прочностные характеристики спейсера. Известные модели спейсеров обладают удовлетворительными механическими характеристиками, однако не позволяют создать необходимую ингибирующую антимикробную концентрацию при использовании препаратов, влияющих на прочностные функции костного цемента, таких как рифампицин.
Предложенная нами конструкция спейсера изначально создана для применения в хирургии туберкулезного коксита, являющегося частым сопутствующим заболеванием у больных ВИЧ-инфекцией. Данная конструкция показала свою эффективность и у пациентов с неспецифическими процессами. Значительное повышение функционального состояния оперированного сустава отмечено уже после выполнения первого этапа оперативного лечения. При контрольных обследованиях через 12 мес. пациенты выражают удовлетворение результатами лечения. На наш взгляд, разработанная оригинальная конструкция может стать эффективной альтернативой традиционным методам лечения.
ЗАКЛЮЧЕНИЕ
Применение оригинальной конструкции антимикробного двухслойного артикулирующего спейсера в оперативном лечении двух пациентов с инфекционным неспецифическим кокситом привело к эра- дикации инфекции, уменьшению болевого синдрома, восстановлению функциональности тазобедренного сустава.
СПИСОК ИСТОЧНИКОВ
D'Angelo F, Monestier L, Zagra L. Active septic arthritis of the hip in adults: what's new in the treatment? A systematic review. EFORT Open Rev. 2021;6(3):164-172. doi: 10.1302/2058-5241.6.200082.
Астахов Д.И., Артюх В.А. Патогенез и современные методы лечения пациентов с инфекционным артритом тазобедренного сустава: обзор литературы. Травматология и ортопедия России. 2024;30(2):192-205. doi: 10.17816/2311-2905-17497.
Balato G, de Matteo V, Ascione T, et ak. Management of septic arthritis of the hip joint in adults. A systematic review of the literature. BMCMusculoskeletDisord. 2021;22(Suppl 2):1006. doi: 10.1186/s12891-021-04843-z.
Anagnostakos K, Duchow L, Koch K. Two-stage protocol and spacer implantation in the treatment of destructive septic arthritis of the hip joint. Arch Orthop Trauma Surg. 2016;136(7):899-906. doi: 10.1007/s00402-016-2455-3.
Mathews CJ, Weston VC, Jones A, et al. Bacterial septic arthritis in adults. Lancet. 2010;375(9717):846-855. doi: 10.1016/S0140- 6736(09)61595-6.
Biviji AA, Paiement GD, Steinbach LS. Musculoskeletal manifestations of human immunodeficiency virus infection. J Am Acad Orthop Surg. 2002;10(5):312-320. doi: 10.5435/00124635-200209000-00003.
Буханова Д.В., Белов Б.С. Поражение суставов при ВИЧ-инфекции. Медицинский совет. 2018;(9):82-87. doi: 10.21518/2079- 701X-2018-9-82-87.
Зубиков В.С. Перецманас Е.О., Герасимов И.А. Опыт хирургического лечения туберкулезного и неспецифического артрита методом двухэтапной артропластики с использованием артикулирующих цементных спейсеров, насыщенных антибиотиками. Туберкулез и болезни легких. 2019;97(11):25-32. doi: 10.21292/2075-1230-2019-97-11-25-32.
Николаев Н.С., Карпухин А.С., Максимов А.Л. и др. Опыт лечения больных с неспецифическим кокситом методом двухэтапного эндопротезирования. Кафедра травматологии и ортопедии. 2020;4(42):5-13. doi: 10.17238/issn2226-2016.2020.4.5-13.
Luo H, He C, Zhao Y, et al. Outcomes of single- vs two-stage primary joint arthroplasty for septic arthritis: a systematic review and meta-analysis. EFORT Open Rev. 2023;8(9):672-679. doi: 10.1530/EOR-22-0142.
Russo A, Migliorini F, Giustra F, et al. Two-stage total joint replacement for hip or knee septic arthritis: post-traumatic etiology and difficult-to-treat infections predict poor outcomes. Arch Orthop Trauma Surg. 2024;144(12):5111-5119. doi: 10.1007/s00402-024- 05249-x.
Chen CY, Lin CP, Tsai CH, et al. Medullary-Sparing Antibiotic Cement Articulating Spacer Reduces the Rate of Mechanical Complications in Advanced Septic Hip Arthritis: A Retrospective Cohort Study. JPers Med. 2024;14(2):162. doi: 10.3390/jpm14020162.
D'Angelo F, Monestier L, Zagra L. Active septic arthritis of the hip in adults: what's new in the treatment? A systematic review. EFFORT Open Rev. 2021;6(3):164-172. doi: 10.1302/2058-5241.6.200082.
Dudareva M, Kumin M, Vach W, et al. Short or Long Antibiotic Regimes in Orthopaedics (SOLARIO): a randomised controlled open- label non-inferiority trial of duration of systemic antibiotics in adults with orthopaedic infection treated operatively with local antibiotic therapy. Trials. 2019;20(1):693. doi: 10.1186/s13063-019-3832-3.
Lin TL, Tsai CH, Fong YC, et al. Posterior-Stabilized Antibiotic Cement Articulating Spacer With Endoskeleton-Reinforced Cam Reduces Rate of Post-Cam Mechanical Complications in Prosthetic Knee Infection: A Preliminary Study. J Arthroplasty. 2022;37(6):1180-1188. e2. doi: 10.1016/j.arth.2022.01.094.
Ayre WN, Birchall JC, Evans SL, Denyer SP. A novel liposomal drug delivery system for PMMA bone cements. J Biomed Mater ResB ApplBiomater. 2016;104(8):1510-1524. doi: 10.1002/jbm.b.33488.
Galvez-Lopez R, Pena-Monje A, Antelo-Lorenzo R, et al. Elution kinetics, antimicrobial activity, and mechanical properties of 11 different antibiotic loaded acrylic bone cement. Diagn Microbiol Infect Dis. 2014;78(1):70-74. doi: 10.1016/j. diagmicrobio.2013.09.014.
Paz E, Sanz-Ruiz P, Abenojar J, et al. Evaluation of Elution and Mechanical Properties of High-Dose Antibiotic-Loaded Bone Cement: Comparative "In Vitro" Study of the Influence of Vancomycin and Cefazolin. J Arthroplasty. 2015;30(8):1423-1429. doi: 10.1016/j. arth.2015.02.040.
Pithankuakul K, Samranvedhya W, Visutipol B, Rojviroj S. The effects of different mixing speeds on the elution and strength of high-dose antibiotic-loaded bone cement created with the hand-mixed technique. J Arthroplasty. 2015;30(5):858-863. doi: 10.1016/j. arth.2014.12.003.
Bistolfi A, Massazza G, Verne E, et al. Antibiotic-loaded cement in orthopedic surgery: a review. ISRN Orthop. 2011;2011:290851. doi: 10.5402/2011/290851.
Anagnostakos K, Meyer C. Antibiotic Elution from Hip and Knee Acrylic Bone Cement Spacers: A Systematic Review. Biomed Res Int. 2017;2017:4657874. doi: 10.1155/2017/4657874.
Athans V, Veve MP, Davis SL. Trowels and Tribulations: Review of Antimicrobial-Impregnated Bone Cements in Prosthetic Joint Surgery. Pharmacotherapy. 2017;37(12):1565-1577. doi: 10.1002/phar.2040.
Перецманас Е.О., Артюхов А.А., Штильман М.И. и др. Исследование элюционных характеристик противотуберкулезных препаратов, смешанных с костным цементом. Туберкулез и болезни легких. 2021;99(4):30-35. doi: 10.21292/2075-1230-2021-99-4-3.
Перецманас Е.О., Тюлькова Т.Е., Зубиков В.С. и др. Антимикробный спейсер тазобедренного сустава. Патент РФ на полезную модель № 212287. 14.07.22. Бюл. № 20.
Zhao CS, Li X, Zhang Q, et al Early Outcomes of Primary Total Hip Arthroplasty for Osteonecrosis of the Femoral Head in Patients with Human Immunodeficiency Virus in China. Chin Med J (Engl). 2015;128(15):2059-64. doi: 10.4103/0366-6999.161364.
Тряпичников А.С., Ермаков А.М., Клюшин Н.М. и др. Результаты лечения перипротезной инфекции крупных суставов у ВИч- позитивных больных. Травматология и ортопедия России. 2019;25(4):117-125. doi: 10.21823/2311-2905-2019-25-4-117-125.
Кильметов Т.А., Ахтямов И.Ф., Гильмутдинов И.Ш. и др. Локальная антибиотикотерапия при инфекции области эндопротеза сустава. Казанский медицинский журнал. 2014;95(3):405-411. doi: 10.17816/KMJ1526.
Шевченко Ю.Л., Стойко Ю.М., Грицюк А.А. и др. Локальная антибиотикопрофилактика при эндопротезировании крупных суставов (литературный обзор). Вестник Национального медико-хирургического Центра им. Н.И. Пирогова. 2010;5(3):44-56.
Masri BA, Duncan CP, Beauchamp CP. Long-term elution of antibiotics from bone-cement: an in vivo study using the prosthesis of antibiotic-loaded acrylic cement (PROSTALAC) system. J Arthroplasty. 1998;13(3):331-338. doi: 10.1016/s0883-5403(98)90179-6.
Wall V, Nguyen TH, Nguyen N, Tran PA. Controlling Antibiotic Release from Polymethylmethacrylate Bone Cement. Biomedicines. 2021;9(1):26. doi: 10.3390/biomedicines9010026.
Информация об авторах:
Евгений Оркович Перецманас — доктор медицинских наук, руководитель отдела
Владимир Сергеевич Зубиков — доктор медицинских наук, профессор, ведущий научный сотрудник
Илья Александрович Герасимов — врач — травматолог-ортопед
Ярослав Алексеевич Рукин — доктор медицинских наук, профессор, ведущий научный сотрудник
Теги: ВИЧ-инфекция
234567 Начало активности (дата): 14.02.2026
234567 Кем создан (ID): 989
234567 Ключевые слова: инфекционный коксит, ВИЧ-инфекция, двухэтапное эндопротезирование, спейсер, антимикробные препараты
12354567899
Похожие статьи
ГЛАВА 15 ТУБЕРКУЛЕЗ И ВИЧ-ИНФЕКЦИЯРентген на дому 8 495 22 555 6 8
Периимплантная инфекция у пациентов с ревматоидным артритом на примере серии случаев
Ротавирусная инфекция в вопросах и ответах
Раны и раневая инфекция



