 04.08.2024
04.08.2024
Новые технологии реконструкции пальцев кисти с применением 3D-печати
Применение 3D-технологии при реконструкции пальцев обеспечивает прецизионность вмешательства, минимизацию донорского изъяна, оптимизацию внешнего вида и функции пальца.
ВВЕДЕНИЕ
За последнее десятилетие технология трехмерной печати получила развитие в медицине, она открывает новые перспективы в научных исследованиях, обучении персонала и в индивидуальном подходе к лечению, позволяя повысить его эффективность [1-3]. По мнению специалистов, в хирургии трехмерную печать можно использовать для создания геометрически сложных и высокодетализированных персонализированных конструкций и их одноразового изготовления, для предоперационного планирования, проектирования ортопедических изделий и протезирования в соответствии с конкретными требованиями хирурга и пациента [3-6], для создания вспомогательных средств, адаптированных для конкретного пациента, для интраоперационного использования, создания аппаратных средств и индивидуальных устройств, протезов для имплантации, быстрого создания прототипов хирургически имплантируемых изделий, а также приложений для обучения стажеров [7-10]. Преимуществом технологии является то, что индивидуальные имплантаты и слепки могут быть изготовлены в соответствии с анатомией конкретного человека [9, 11]. Вместе с тем, применению этой технологии в хирургии кисти посвящено небольшое количество исследований. В литературе имеются немногочисленные публикации о применении технологии при пересадке пальцев стопы и замещении донорского дефекта лоскутами на микрососудистых анастомозах.
Это позволило сократить время работы за счет предоставления цифровых и точных схем для выполнения операции. Авторами создана модель большого пальца и второго пальца стопы, чтобы понять размеры заимствования тканей из донорской области. Эта модель также применена для устранения дефекта донорского участка путем использования соответствующих кожно-костных лоскутов подвздошной кости на поверхностных огибающих подвздошную кость артериях [9].
Сообщается о предоперационном планировании реконструкций большого пальца с пересадкой второго пальца стопы с использованием 3D-печати. Компьютерная ангиография (КТ-ангиография) использована для картирования сосудистой сети донорского участка, тогда как данные КТ — для создания трехмерных моделей мягких тканей и скелета поврежденных и неповрежденных рук. На основе переформатированной модели (зеркало неповрежденной руки) с помощью 3D-принтера созданы модели мягких тканей и скелета пальцев. Модель пальца использована также для определения уровня остеотомии на донорской стопе. Это позволило оптимизировать функцию и внешний вид реконструированного большого пальца, минимизируя повреждение донорского участка [12, 13]. Метод позволяет точно рассчитать размеры кожи и костей донорского участка в качестве эталона для хирургической операции и выполнить операцию в соответствии с моделью [14]. Технологию применяют также с целью моделирования размеров кожно-жирового лоскута для замещения дефектов мягких тканей пальца в экстренных случаях [15], при трансплантации кисти [16]. Вместе с тем, в настоящее время не изучены возможности и перспективы применения 3D-технологии при других методах реконструкции пальцев. Нуждаются в изучении различные аспекты пред- и интраоперационного использования 3D-технологии при кожно-костной реконструкции пальцев кисти и дистракционном удлинении культей пальцев и пястных костей, направленные на оптимизацию планирования лечения и прецизионности вмешательства, на улучшение результатов, уменьшение донорского изъяна и частоты развития осложнений.
Цель работы — продемонстрировать новые способы предоперационного планирования и реконструкции пальцев, улучшающие результаты оперативного лечения.
МАТЕРИАЛЫ И МЕТОДЫ
Ретроспективно мы оценили результаты кожно-костной реконструкции лучевым лоскутом первого пальца у двух больных, дистракционного удлинения культей первой и второй пястных костей у двух больных, перемещения культи третьего пальца у одного больного по разработанным технологиям. У обоих больных планирование реконструкции первого пальца выполнено с применением разработанного устройства.
Техническое исполнение
Патент РФ 211603 «Устройство для предоперационного планирования реконструкции первого пальца кисти» [17].
Устройство для предоперационного планирования пальца кисти создано с помощью гибридного параметрического моделирования, топологической оптимизации и аддитивных технологий 3D-печати. Оно снабжено ложементом для культи пальца, зафиксированным на кисти лентой Велкро или лейкопластырем, дистальная часть ложемента соединена с помощью шарового шарнира с возможностью фиксации в определенном положении с втулкой, соединенной с поршнем с возможностью выдвижения и фиксации достигнутого положения резьбовым стержнем с последующим измерением длины восстанавливаемого пальца и углов его фиксации к культе I пальца (рис. 1, а, б).
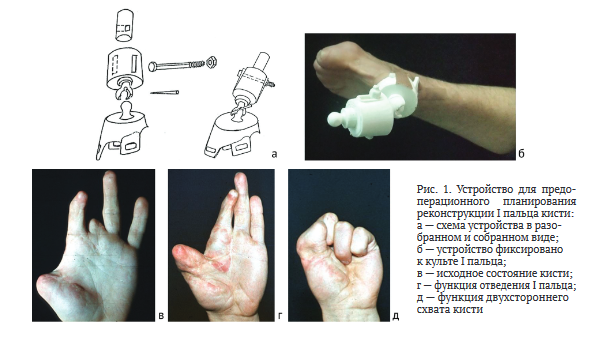
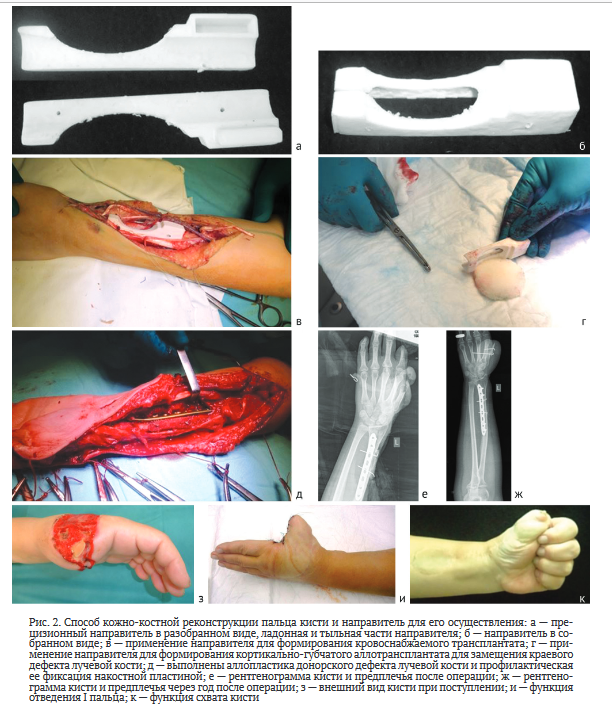
Предварительно по данным компьютерной томографии создавали индивидуальную модель лучевой кости, а затем с помощью этой модели — направитель для забора трансплантата на донорском участке кости (рис. 2).
Направитель для реализации способа кожно-костной реконструкции пальца кисти содержит паз для установки лезвия пилы и центральное осевое отверстие, изготавливается индивидуально по данным компьютерной томографии с помощью ЗБ-печати в зависимости от планируемых размеров и формы трансплантата. Направитель по длине у дистального конца больше планируемого трансплантата не менее чем на 1 см, по длине у проксимального конца — не менее чем на 2,5 см. Устройство состоит из двух равных частей — ладонной и тыльной. Осевое отверстие прецизионно соответствует внешней поверхности лучевой кости в области формирования планируемого трансплантата. Паз для полотна пилы — ладьевидной формы, посередине в области дистального конца на- правителя выполнена сплошная прорезь шириной 2 мм для размещения межмышечной перегородки и содержащихся в ней сосудов. В его проксимальном конце выполнен соединительный элемент по типу «выступ-паз» и два отверстия для спиц (рис. 2, а, б).
Патент РФ 2796438 «Способ дистракционного удлинения культи пястной кости» [19].
На этапе предоперационного планирования после компьютерной томографии кисти определена область остеотомии и необходимые размеры дистрагируемого дистального фрагмента пястной кости и его поперечного сечения на уровне остеотомии. Затем с помощью гибридного параметрического моделирования сформирован макет спейсера полой цилиндрической формы (рис. 3). Длина и внутренний диаметр спейсера определены в зависимости от планируемой дистракции. Внутреннее поперечное сечение спейсера соответствует поперечному сечению дистрагируемой пястной кости на расстоянии 0,5 см от места планируемой поперечной остеотомии. Стенка спейсера имеет толщину 1 мм.
Спейсер имеет полуоткрытый сквозной продольный прямоугольный паз шириной 2 мм. Торцевой край паза заканчивается на расстоянии 0,5 см от противоположного края спейсера длиной 1,5 см. Концы спейсера должны надеваться на глубину 0,5 см на концы проксимального и дистального костных фрагментов и с учетом диастаза костных фрагментов на 0,5 см. На основе изготовленного спейсера из полимерного материала PLA создана матрица с помощью технологии ЗБ-печати. Во время операции матрицу заполняют костным цементом, содержащим гентамицин. После затвердевания костного цемента спейсер извлекают. С помощью осцилляторной пилы выполняют поперечную остеотомию пястной кости в области ее средней трети. Изготовленный спейсер из костного цемента надет сплошным концом на проксимальный конец дистального фрагмента пястной кости. Через дистальный фрагмент пястной кости и осевое отверстие спейсера проведена интрамедуллярно спица Киршнера. Проксимальный конец спицы изогнут П-образно, короткая бранша спицы заведена в паз спейсера до упора областью изгиба в торцевой край закрытой части паза и проксимальный конец дистального фрагмента.
Дистальный конец спицы выведен наружу. Второй конец спейсера с пазом надет на проксимальный фрагмент пястной кости.
Выполнен монтаж аппарата Илизарова с базовым кольцом на предплечье и выносными винтовыми тягами. К винтовым тягам аппарата фиксирован дистальный конец интрамедуллярной спицы. Ушита послеоперационная рана.
Через 5 дней после операции осуществлена постепенная дистракция дистального фрагмента вместе с цементным спейсером по 1 мм в день.
После завершения дистракции дистального фрагмента пястной кости выполнен второй этап операции. При этом образовавшаяся остеогенная мембрана рассечена вдоль на всем протяжении дистракционного дефекта и концов фрагментов пястной кости. Удалена интрамедуллярная спица и спейсер с сохранением дистракционного регенерата.
Выполнена пластика дистракционного дефекта кортикально-губчатым аллотрансплантатом, поперечные размеры которого не превышали наружный диаметр спейсера. При этом сохранены образовавшиеся дистракционные регенераты в области дистального и проксимального фрагментов пястной кости.
Выполнен остеосинтез костных фрагментов и трансплантата спицами. Ушита образовавшаяся остеогенная капсула узловыми рассасывающимися швами над всей поверхностью трансплантата и областью его контактов с фрагментами пястных костей. Послойно ушита подкожная клетчатка и кожа над остеогенной капсулой.
РЕЗУЛЬТАТЫ
Клинические примеры
Больной Ч., 45 лет, находился в клинике ПИМУ после тяжелой механической травмы по поводу культи I пальца на уровне головки пястной кости, приводящей контрактуры первой пястной кости тяжелой степени, культи III и деформации IV пальцев, сгибательных контрактур II пальца в межфаланговых суставах, внутрисуставного многооскольчатого перелома головки основной фаланги, локтевой девиации средней фаланги IV пальца правой кисти (рис. 1, в). Пациент желал восстановить щипковый схват I с сохранившимся II пальцем.
При поступлении функциональные возможности кисти резко ограничены, схват кисти отсутствует, движения в пястно-фаланговом, межфаланговом суставах II пальца, запястно-пястном суставе культи первой пястной кости возможны в объеме 15-20°. Длина культи первого пальца составляет 5,5 см. В связи с отсутствием функции схвата кисти решено восстановить I палец методом перемещения культи III пальца, так как больной отказался от пересадки пальца стопы и кожно-костной реконструкции пальца с использованием лучевого лоскута. Ограничение функции II пальца и отсутствие перспектив на ее улучшение, наличие приводящей контрактуры первой пястной кости обусловило необходимость определения адекватной длины и положения формируемого I пальца. Перед операцией после установки клинико-рентгенологического диагноза выполнена компьютерная томография поврежденной кисти. Затем с помощью гибридного параметрического моделирования, топологической оптимизации и аддитивных технологий SD-печати сформировано индивидуальное устройство для определения величины и положения формируемого пальца в зависимости от величины культи III пальца. Устройство позволило определить длину формируемого пальца и его положение в трех плоскостях. Втулка устройства по размерам соответствовала размерам перемещаемой культи III пальца.
Устройство фиксировано к культе I пальца с помощью клейкой ленты Велкро, проведенной через ушки ложемента. Пациенту проведено функциональное тестирование кисти с захватом предметов маленькой, средней и большой величины с использованием фиксированного к культе I пальца устройства.
Путем постепенного выдвижения и фиксации поршня с помощью гайки резьбового стержня, а также изменения положения втулки вместе с поршнем в трех плоскостях с фиксацией шарнира стопором эмпирически определены положение и длина формируемого пальца, обеспечивающие возможность выполнения щипкового схвата с деформированным пальцем. При этом учитывали также и профессиональные требования пациента к восстанавливаемой функции схвата. Произведено измерение длины I пальца, его положения во фронтальной, сагиттальной и горизонтальной плоскостях. Длину пальца измеряли от основания втулки до дистального конца поршня, она составила 6,5 см. Измеряли с помощью угломера угол лучевого, ладонного отведения, ротации втулки вместе с поршнем. Величина ладонного отведения составила 45°, лучевого отведения 35°, ротации втулки с поршнем — 90°. Эти параметры соответствовали положению и длине перемещенной в позицию I пальца культи III пальца. Согласно измерениям, длина формируемого пальца вместе с пястной костью должна была составить 11,5 см (на здоровой кисти длина I пальца вместе с пястной костью составляла 10 см). Полученные размеры и углы фиксации перемещенной культи использованы во время операции перемещения культи III пальца и фиксации ее к культе первой пястной кости. В результате достигнут щипковый схват сформированного I пальца с культей средней фаланги II пальца, а также с IV, V пальцами.
Необходимости в выполнении корригирующих операций по изменению положения I пальца после операции не возникло. Пациент быстро приспособился к восстановленному схвату кисти, удерживал предметы малой и средней величины с помощью I и II пальцев, большой величины — с использованием I и сохранившихся IV, V пальцев, активно использовал сформированный I палец в бытовой и производственной деятельности. Расстояние между I и II пальцами при максимальным отведении I пальца и разгибании II пальца составило 7 см (на здоровой кисти — 12 см), восстановлена функция отведения I пальца и приведения его к II (рис. 1, в, г, д).
Больная С., 25 лет, находилась в клинике ПИМУ по поводу культи I пальца левой кисти на уровне основания основной фаланги, дефекта мягких тканей лучевого края кисти (рис. 2, з). Пациентка пострадала на производстве 07.06.19, когда ее левая кисть попала под валки обрабатывающего станка. При поступлении больной сформированы мягкие ткани I пальца и замещен дефект мягких тканей на кисти за счет пластики несвободным паховым осевым кожно-жировым лоскутом (13.06.19).
Следующим этапом 10.02.20 выполнена кожно-костная реконструкция I пальца левой кисти за счет перемещения кожно-костного лучевого лоскута на периферической сосудистой ножке. Перед операцией определены необходимые размеры костного остова восстанавливаемого пальца, размеры и форма трансплантата лучевой кости, длина его сосудистой ножки, выполнена компьютерная томография костей предплечья.
После этого с помощью гибридного параметрического моделирования, топологической оптимизации и аддитивных технологий SD-печати изготовлен персонифицированный направитель для остеотомии лучевой кости. Во время операции мобилизована лучевая артерия с кожно-жировым лоскутом с сохранением межмышечной перегородки с септальными и надкостничными сосудами в области забора трансплантата. Две части направителя приложены к области остеотомии и соединены между собой. Затем направитель единым блоком временно фиксирован к области забора трансплантата лучевой кости спицами (рис. 2, в). При этом межмышечная перегородка с септальными сосудами уложена в сплошную прорезь направите- ля с целью профилактики их повреждения, лучевая артерия расположена на боковой его поверхности. Выполнена краевая ладьевидная остеотомия лучевой кости с использованием направителя. При этом при ведении пилы ее полотно прижимали к пазу направителя. В результате сохранена целостность септальных и надкостничных сосудов, отходящих от лучевой артерии, и адекватное кровоснабжение трансплантата, получена ровная плоскость опила. С использованием этого же направителя выпилен бессосудистый кортикально-губчатый аллотрансплантат (рис. 2, г), прецизионно соответствующий по длине, толщине и форме образовавшемуся краевому дефекту лучевой кости и сформированному кровоснабжаемому трансплантату, но превышающий его по ширине на 0,5 см. Бессосудистый аллотрансплантат уложен в дефект лучевой кости и фиксирован двумя спицами, выполнена профилактическая фиксация лучевой кости накостной пластиной (рис. 2, д, е).
Краевой бессосудистый костный трансплантат лучевой кости полностью конгруэнтен дефекту и плотно прилегает к нему. Кровоснабжаемый трансплантат лучевой кости вместе с кожным лоскутом перемещен на культю первой пястной кости и сформирован I палец. Послеоперационное течение гладкое. Раны зажили первичным натяжением. Кожный лоскут прижился полностью, что свидетельствует о сохранении и функционировании септальных сосудов. Через два месяца после операции определены отчетливые признаки консолидации трансплантата из лучевой кости, что свидетельствует о сохранении надкостничных сосудов и его кровоснабжения. В отдаленном послеоперационном периоде не выявлено патологического перелома лучевой кости, достигнуты полная консолидация и перестройка аллотрансплантата с полным устранением краевого дефекта (рис. 2, ж).
Больная осмотрена через два года после операции. Длина восстановленного пальца составила 55 мм, что соответствует послеоперационным данным и длине интактного I пальца другой кисти. Сформированный палец занимает функционально-выгодное положение. Восстановлен двухсторонний схват кисти. Расстояние между концами V пальца и восстановленного I пальца при его максимальном отведении составляет 19,5 см, как и на здоровой кисти. Определялась болевая и температурная чувствительность восстановленного I пальца. Рубец донорской раны на предплечье нормотрофический, незначительный, беспокойства больной не причинял.
Восстановлена функция противопоставления первого пальца: тест Капанжи показал результат 9 баллов. На контрольных рентгенограммах левой кисти отмечена полная консолидация первой пястной кости и кровоснабжаемого трансплантата лучевой кости. Восстановлены функция I пальца и схвата кисти (рис. 2, и, к). Признаков резорбции сформированного костного остова I пальца левой кисти нет. Также на контрольных рентгенограммах предплечья через два года после операции отмечены полная консолидация и замещение донорского дефекта лучевой кости аллотрансплантатом, что имеет решающее значение в профилактике патологического перелома в донорской области.
Больная А., 22 лет, поступила в клинику ПИМУ по поводу культей I, II, III, IV пальцев на уровне проксимальных третей основных фаланг, культи V пальца на уровне дистальной трети основной фаланги левой кисти (рис. 3, а). Пациентка пострадала на производстве 19.10.21 в результате того, что кисть попала во вращающийся механизм станка. По поводу размозжения I-V пальцев в экстренном порядке выполнена первичная хирургическая обработка ран, сформированы культи всех пальцев кисти. В послеоперационном периоде отмечали некрозы кожных лоскутов на торцах культей пальцев. После выполнения некрэктомий сформировались дефекты мягких тканей размерами 2 см на 6 см.
При поступлении в клинику на торцах культей пальцев имеются тонкие, изъязвляющиеся рубцы, спаянные с подлежащими костями, схват кисти отсутствует (рис. 3, а). Предварительно выполнено замещение дефектов на торцевой поверхности культей II—IV пальцев и I пальца за счет пластики стеблем Филатова с образованием петли (06.04.22 и 17.05.22) (рис. 3, б). При повторном поступлении 14.09.22 выполнен первый этап дистракционного удлинения культей первой и второй пястных костей с целью восстановления функции двухстороннего схвата кисти по разработанной технологии (рис. 3). Перед операцией определены необходимые размеры поперечного сечения первой и второй пястных костей на уровне их середины и с отступом на 0,5 см от середины. Они оказались равными 10 мм. После этого с помощью гибридного параметрического моделирования, топологической оптимизации смоделированы матрица и спейсер полой цилиндрической формы так, что его поперечное сечение соответствовало поперечному сечению дистрагируемой пястной кости на расстоянии 0,5 см от места поперечной остеотомии. Длина спейсера — 1,5 см, толщина стенки спейсера — 1 мм. Спейсер имел полуоткрытый сквозной продольный прямоугольный паз шириной 2 мм и длиной 1 см. С помощью аддитивных технологий 3Б-печати выполнена матрица из PLA (рис. 3, в).
Во время операции проведены поперечные остеотомии I и II пястных костей на уровне их середины. Матрица наполнена костным цементом, после затвердения которого сформирован спейсер в виде полого цилиндра. Изготовленный спейсер надет сплошным концом на проксимальный конец дистального фрагмента второй пястной кости (рис. 3, г). Через дистальный фрагмент пястной кости и осевое отверстие спейсера интрамедуллярно проведена спица Киршнера. Проксимальный конец спицы изогнут П-образно, короткая бранша спицы заведена в паз спейсера до упора областью изгиба в торцевой край закрытой части паза и проксимальный конец дистального фрагмента. Дистальный конец спицы выведен наружу. Второй конец спицы надет на проксимальный фрагмент пястной кости. На первой пястной кости проведена аналогичная дистрагирующая спица без применения спейсера. К винтовым тягам базового кольца аппарата Илизарова фиксированы дистальные концы интрамедуллярных спиц.
После операции проведена постепенная дистракция фрагментов пястных костей по 1 мм в день (рис. 3, д). Достигнуто разведение костных фрагментов на 35 мм. 15.11.22 выполнен второй этап дистракционного удлинения, при этом снят аппарат внешней фиксации, выполнен разрез по послеоперационному рубцу. Отмечено, что образовалась хорошо выраженная гиперваскулярная индуцированная капсула на всем протяжении дистракционного дефекта с захождением ее на концы костных фрагментов на 0,5 см. Капсула на всем своем протяжении имела одинаковую равномерную толщину стенки, равную 2 мм. Образовавшаяся капсула рассечена продольно на всем протяжении дистракционного дефекта и концов фрагментов пястной кости. Удалены интрамедуллярные спицы и спейсер (рис. 3, ж). В области проксимального конца дистального фрагмента сформирован эндостально расположенный костный регенерат длиной 1,5 см. В области торца проксимального фрагмента определялись краевые пластинчатые костные регенераты длиной 1 см и зрелый регенерат в виде шипа, имевший костную структуру. Выполнена пластика дистракционного дефекта кортикально-губчатым аллотрансплантатом, поперечные размеры которого не превышали наружный диаметр спейсера (рис. 3, з). При этом сохранены образовавшиеся дистракционные регенераты в области дистального и проксимального фрагментов. Выполнен остеосинтез костных фрагментов и трансплантатов спицами. Ушита образовавшаяся остеогенная капсула узловыми рассасывающимися швами над трансплантатом и областью его контактов с фрагментами пястных костей (рис. 3, и). В результате трансплантат и область его контактов с фрагментами пястной кости полностью укрыты остеогенной капсулой. Послойно ушита подкожная клетчатка и кожа над остеогенной капсулой. Следует отметить, что на первой пястной кости дистракционный регенерат менее выражен. Выполнена также пластика дефекта кортикально-губчатым аллотрансплантатом с фиксацией спицами (рис. 3, к). Кисть иммобилизована гипсовой лонгетой сроком на пять недель. Раны зажили первичным натяжением. После снятия лонгеты отмечается консолидация костных фрагментов с трансплантатами по типу первичного заживления, больше выраженная на второй пястной кости. Через два месяца выполнено разделение петли стебля Филатова, сформированы дистальные отделы I и II пальцев. Больная осмотрена через шесть месяцев после операции. Длина первого луча составляет 8 см, второго — 9 см. Расстояние между торцами культей при отведении первого луча — 4 см (рис. 3, к). В результате проведенного лечения восстановлена функция двухстороннего схвата кисти (рис. 3, л). Удлиненные культи имели адекватное мягкотканное покрытие, без признаков пролабирования дистальных отделов. На R-граммах кисти определяли признаки консолидации и перестройки аллотрансплантатов (рис. 3, м).
ОБСУЖДЕНИЕ
Эффективность реконструктивного вмешательства предопределяется его адекватно проведенным планированием. Предоперационные 3D-модели для планирования реконструкции пальца представляют собой жесткую интегральную конструкцию, не позволяющую изменять размеры и положение отдельных его частей, имитирующих фаланги пальца, в различных плоскостях. Кроме того, известные предоперационные модели применяют при изолированном отсутствии I пальца, когда определения функционального положения суставов относительно остальных поврежденных пальцев не требуется [13, 14]. Это затрудняет выбор оптимальной позиции восстановленного пальца относительно сохранившихся сегментов кисти при ее тяжелой деформации. Известный способ планирования величины удлинения позволяет определить оптимальную длину I пальца при дистракционном удлинении его культи индивидуально в каждом конкретном случае, но лишено возможности определения функционально-выгодного положения формируемого пальца относительно сохранившихся пальцев [20].
При реализации нашего способа создается индивидуальная модель пальца с изменяемыми биомеханическими параметрами, обеспечивается активное участие самого пациента в планировании операции. Разработанная модель имеет регулируемые биомеханические параметры (длина I пальца, положение его фаланг в суставах и относительно продольной оси). Устройство представляет собой индивидуальную разборную конструкцию, компоненты которой в зависимости от характера дефекта кисти и метода реконструкции могут имитировать основную и ногтевую фаланги с возможностью изменения их положения в суставах и ротационного положения, а также изменения длины модели основной фаланги. Устройство позволяет избежать выполнения корригирующих вмешательств на восстановленном пальце по изменению его положения.
Проблема минимизации донорского изъяна при пластике лучевым лоскутом сохраняет актуальность. Наиболее значимой при этом является профилактика патологических переломов в области забора костного трансплантата, так как подобные осложнения являются сдерживающим фактором в широком применении метода. При реконструкции пальца с использованием кожно-костного лучевого лоскута особое значение для профилактики перелома имеет точное определение глубины выреза, не превышающего критических значений. С этой целью применяют различные подходы (скругление углов, стопорные отверстия, проведение спиц-ориентиров под контролем С-дуги, применение триммера Митчелла, измерителя глубины винта, защитной металлической ленты, расположенной в продольном разрезе и т.д.), не обеспечивающие достаточную прецизионность краевой остеотомии лучевой кости [21, 22]. Кроме того, плоскость остеотомии получается недостаточно ровной, особенно при формировании выреза ладьевидной формы из-за возможного соскальзывания полотна пилы с округлой поверхности диафиза кости. При этом существует риск повреждения осевого и септальных сосудов трансплантата лучевой кости. Случайное увеличение глубины выреза может значительно уменьшить прочность кости. Некоторые авторы во время операции используют созданную перед операцией модель краевого дефекта в качестве образца, эталона для подражания при остеотомии. [23]. Этому способу присущи аналогичные недостатки. При кожно-костной реконструкции пальца мы применяем 3D-технологии непосредственно при выполнении самого основного этапа операции — заборе кровоснабжаемого трансплантата и подготовке аллотрансплантата для пластики краевого дефекта лучевой кости.
Создается инструмент одноразового использования для конкретного пациента. Трехмерное печатное приспособление для лучевой кости, предназначенное для конкретного пациента, обеспечивает точное предоперационное планирование. В доступной литературе мы не нашли специального инструментария для подобных вмешательств. При реализации нашего способа для краевой остеотомии мы создаем индивидуальный инструмент методом 3И-печати. Способ позволяет предотвратить подрез (перерез) кости, образуется ровная поверхность опила лучевой кости и трансплантата, что обеспечивает плотный их контакт по всей плоскости остеотомии. В случае вынужденного превышения критической глубины выреза устройство оптимизирует условия костной пластики за счет формирования трансплантата, прецизионно соответствующего величине, поверхности и форме краевого дефекта. Ровные поверхности остеотомии и аллотрансплантата обеспечивают их плотный контакт и оптимальные условия для сращения и перестройки при костной пластике, позволяют получить качественно новый результат, восстановить структуру донорской кости. В зависимости от клинической ситуации, направитель может быть создан для формирования трансплантата ладьевидной, прямоугольной или любой другой формы.
В последнее десятилетие при лечении дефектов костей различной этиологии получает распространение метод Masquelet [24-28]. В то же время некоторые авторы ставят под сомнение эффективность методики [29]. В литературе есть сообщения о преимуществах комбинирования метода дистракции и методики Masquelet при замещении костных дефектов. Так, известен также способ замещения дефекта кости, заключающийся в размещении спейсера из костного цемента в дефекте большеберцовой кости, в выполнении через 6-8 недель второго этапа операции, включающего остеотомию, перемещение с использованием аппарата Илизарова в образовавшуюся остеогенную капсулу кровоснабжаемого костного трансплантата и выполнение его остеосинтеза в зоне сформировавшейся остеоиндуктивной мембраны [30]. Однако возможности такого подхода при реконструкции пальцев кисти не изучены. При использовании интерпозиционного трансплантата всегда имеется опасность его несращения, перелома, пролабирования и инфицирования, особенно при рубцовых изменениях мягких тканей кисти [31, 32].
Необходимость вмешательств на мягкотканном футляре в подобных неблагоприятных условиях применения технологии Masquelet подчеркивается многими авторами [26]. При использовании нашего способа минимизируется опасность таких осложнений. Наш способ основан на разработке и имплантации нестандартного устройства — полого цилиндрического дистрагируемого спей- сера из костного цемента. Способ обеспечивает восстановление адекватного мягкотканного покрытия культей, формирование остеогенной капсулы одновременно с дистракцией культи и образованием регенерата, в результате чего бессосудистый костный интерпозиционный трансплантат окружается на всем протяжении и в области контакта костных фрагментов уже сформированной остеогенной мембраной и кровоснабжаемыми тканями. В подобных случаях улучшаются условия консолидации, перестройки трансплантата, обеспечивается профилактика осложнений, сокращаются сроки лечения.
ЗАКЛЮЧЕНИЕ
Применение технологии 3D-печати при планировании реконструкции пальца различными методами, а также создании индивидуального хирургического инструментария при пластике кожно-костным лучевым лоскутом позволило повысить результаты лечения. Комбинированное применение метода дистракции и метода Masquelet при реконструкции пальцев кисти обеспечило адекватные функциональные результаты, профилактику осложнений в условиях обширного дефекта мягких тканей.
СПИСОК ИСТОЧНИКОВ
Diment LE, Thompson MS, Bergmann JHM. Clinical efficacy and effectiveness of 3D printing: a systematic review. BMJ Open. 2017;7(12):e016891. doi: 10.1136/bmjopen-2017-016891
Matter-Parrat V, Liverneaux P. 3D printing in hand surgery. Hand Surg Rehabil. 2019;38(6):338-347. doi: 10.1016/j. hansur.2019.09.006
Wixted CM, Peterson JR, Kadakia RJ, Adams SB. Three-dimensional Printing in Orthopaedic Surgery: Current Applications and Future Developments. J Am Acad Orthop Surg Glob Res Rev. 2021;5(4):e20.00230-11.
Mohammadi A, Lavranos J, Zhou H, et al. A practical 3D-printed soft robotic prosthetic hand with multi-articulating capabilities. PLoS One. 2020;15(5):e0232766. doi: 10.1371/journal.pone.0232766
Oud TAM, Lazzari E, Gijsbers HjH, et al. Effectiveness of 3D-printed orthoses for traumatic and chronic hand conditions: A scoping review. PLoS One. 2021;16(11):e0260271. doi: 10.1371/journal.pone.0260271
O'Brien L, Cho E, Khara A, et al. 3D-printed custom-designed prostheses for partial hand amputation: Mechanical challenges still exist. J Hand Ther. 2021;34(4):539-542. doi: 10.1016/j.jht.2020.04.005
Bauermeister AJ, Zuriarrain A, Newman MI. Three-Dimensional Printing in Plastic and Reconstructive Surgery: A Systematic Review. AnnPlast Surg. 2016;77(5):569-576. doi: 10.1097/SAP.0000000000000671
Mulford JS, Babazadeh S, Mackay N. Three-dimensional printing in orthopaedic surgery: review of current and future applications. ANZ J Surg. 2016;86(9):648-653. doi: 10.1111/ans.13533
Keller M, Guebeli A, Thieringer F, Honigmann P. Overview of In-Hospital 3D Printing and Practical Applications in Hand Surgery. BiomedRes Int. 2021;2021:4650245. doi: 10.1155/2021/4650245
Zhang D, Bauer AS, Blazar P, Earp BE. Three-Dimensional Printing in Hand Surgery. J Hand Surg Am. 2021;46(11):1016- 1022. doi: 10.1016/j.jhsa.2021.05.028
Eltorai AE, Nguyen E, Daniels AH. Three-Dimensional Printing in Orthopedic Surgery. Orthopedics. 2015;38(11):684- 687. doi: 10.3928/01477447-20151016-05
Tan H, Yang K, Wei P, et al. A Novel Preoperative Planning Technique Using a Combination of CT Angiography and Three-Dimensional Printing for Complex Toe-to-Hand Reconstruction. J Reconstr Microsurg. 2015;31(5):369-77.
Xu L, Tan J, Wei P, et al. Clinical application of 3D printing technology for preoperative planning of thumb reconstruction. Acta OrtopBras. 2021;29(4):211-218. doi: 10.1590/1413-785220212904235492
Lu H, Peng H, Peng Z, et al. The Application of Digital Design Combined with 3D Printing Technology in Skin Flap Transplantation for Fingertip Defects during the COVID-19 Epidemic. Biomed Res Int. 2021;2021:5554500.
Александров Н.М., Вешаев И.Д. Устройство для предоперационного планирования реконструкции первого пальца кисти. Патент РФ на изобретение № 211603. 15.06.22. Бюл. № 17.
Карякин Н.Н., Александров Н.М., Горбатов Р.О., Вешаев И.Д. Способ кожно-костной реконструкции пальца кисти и направитель для его осуществления. Патент РФ на изобретение № 2747694. 12.05.21. Бюл. № 14.
Александров Н.М. Способ дистракционного удлинения культи пястной кости. Патент РФ на изобретение № 2796438. 14.12.22. Бюл. № 15.
Корюков А.А. Устройство для определения величины удлинения культи первого пальца. Патент РФ на изобретение № 84215. 10.07.09. Бюл. № 19.
Avery CM. Review of the radial free flap: still evolving or facing extinction? Part two: osteocutaneous radial free flap. Br J Oral Maxillofac Surg. 2010;48(4):253-260. doi: 10.1016/j.bjoms.2009.09.017
Shnayder Y, Tsue TT, Toby EB, et al. Safe osteocutaneous radial forearm flap harvest with prophylactic internal fixation. Craniomaxillofac Trauma Reconstr. 2011;4(3):129-136. doi: 10.1055/s-0031-1279675
Capito AE, Hansen BK, Schmitt MW, et al. Osteocutaneous Radial Forearm Flap: Harvest Technique and Prophylactic Volar Locked Plating. Plast Reconstr Surg Glob Open. 2023;11(11):e5449. doi: 10.1097/GOX.0000000000005449
Masquelet AC, Begue T. The concept of induced membrane for reconstruction of long bone defects. Orthop Clin North Am. 2010;41(1):27-37. doi: 10.1016/j.ocl.2009.07.011
Lasanianos N Kanakaris N, Giannoudis P. Current management of long bone large segmental defects. Orthopedics and Trauma. 2010;24(2):149-163. doi: 10.1016/j.mporth.2009.10.003
Gupta G, Ahmad S, Mohd Zahid, et al. Management of traumatic tibial diaphyseal bone defect by "induced-membrane technique". Indian J Orthop. 2016;50(3):290-296. doi: 10.4103/0019-5413.181780
Ayouba G, Lemonne F, Kombate NK, et al. Interest of nailing associated with the Masquelet technique in reconstruction of bone defect. J Orthop. 2019;20:228-231. doi: 10.1016/j.jor.2019.12.014
Mi M, Papakostidis C, Wu X, Giannoudis PV. Mixed results with the Masquelet technique: A fact or a myth? Injury. 2020;51(2):132-135. doi: 10.1016/j.injury.2019.12.032
Morris R, Hossain M, Evans A, Pallister I. Induced membrane technique for treating tibial defects gives mixed results. Bone Joint J. 2017;99-B(5):680-685. doi: 10.1302/0301-620X.99B5.BJJ-2016-0694.R2
Борзунов Д.Ю., Моховиков Д.С., Колчин С.Н., Горбач Е.Н. Комбинированное применение несвободной костной пластики по Илизарову и техники Masquelet при реабилитации пациентов с приобретенными костными дефектами и ложными суставами. Гений Ортопедии. 2020;26(4):532-538. doi:10.18019/1028-4427-2020-26-4-532-538
Heo CY, Kwon S, Back GH, Chung MS. Complications of distraction lengthening in the hand. J Hand Surg Eur Vol. 2008;33(5):609-615. doi: 10.1177/1753193408090767
Erdem M, Sen C, Eralp L, et al. Lengthening of short bones by distraction osteogenesis--results and complications. Int Orthop. 2009;33(3):807-813. doi: 10.1007/s00264-007-0491-x
Информация об авторах:
Николай Михайлович Александров — доктор медицинских наук, ведущий научный сотрудник
Теги: метод Илизарова
234567 Начало активности (дата): 04.08.2024 21:12:00
234567 Кем создан (ID): 989
234567 Ключевые слова: метод Илизарова, методика Masquelet, 3D-печать, культя пальца, кожно-костный лучевой лоскут
12354567899
Похожие статьи
Частота, факторы, риска, особенности диафизарных несращений длинных костей нижних конечностейРентген на дому 8 495 22 555 6 8
Операционная политравма-стартовая позиция для удлинения конечночтей и регуляция роста
Перспективные костно-пластические материалы и хирургические технологии при реконструктивно-восстановительном лечении больных с псевдоартрозами и дефектами костной ткани
Применение преваскуляризированных костных скаффолдов in vivo (обзор литературы)



