 30.07.2024
30.07.2024
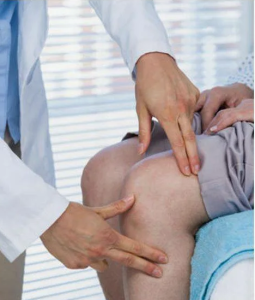
Результаты применения внутритканевой электростимуляции при лечении начальных стадий гонартроза у лиц пожилого и зрелого возраста
Электрометрический анализ выявил более высокую эффективность противоболевой терапии в основной группе по сравнению с контрольной (значения коэффициента асимметрии составили (3,2 ± 0,31) против (1,9 ± 0,4) при p > 0,05).
ВВЕДЕНИЕ
По мнению ряда исследователей, среди множества дегенеративно-дистрофических заболеваний опорно-двигательного аппарата безусловным лидером является гонартроз [1], во всем мире от проявлений данного заболевания страдают свыше 240 млн. человек [2]. От 40 до 70 % случаев заболевания приходится на лиц в возрастном диапазоне 60-70 лет, при этом значимая часть патологии (от 40 до 65 % случаев) связана с генетическим фактором [3]. Несмотря на известные меры профилактики и лечения, количество людей с проявлениями остеоартроза коленного сустава возрастает, при этом отмечается тенденция к снижению возраста больных и увеличению числа лиц молодого, трудоспособного возраста, что негативно сказывается на качестве жизни пациентов [4]. Несмотря на постоянный поиск и совершенствование методик и способов лечения остеоартроза крупных суставов, экономические затраты ряда экономически развитых стран, связанные с лечением и реабилитацией данной категории пациентов, составляют до 2,5 % национального валового продукта [5].
В настоящее время проводится поиск патогенетически обоснованных методов лечения первичного остеоартроза (ОА) коленных суставов, в основе развития которого лежит сложный комплекс биохимических и структурных изменений, охватывающих все суставные компоненты, включая гиалиновый хрящ и субхондральную кость [6-8]. В современной практике с высокой степенью эффективности применяют различные методики лечения болевого и воспалительного компонентов ОА и их комбинации, включающие внутрисуставные инъекции компонентов крови, костного мозга и различные фармакологические и физиотерапевтические пособия. Но проблема лечения болевого синдрома при ОА в настоящее время полностью не решена и, следовательно, является актуальной. Костная ткань богата остеорецепторами, реагирующими на снижение парциального давления кислорода в костных сосудах, обусловленное развитием гипоксии, вызванной венозным застоем в субхондральных отделах кости [9, 10]. Нарушение кровообращения вызывает хронический костно-болевой синдром, характерный для гонартроза. Доказано, что чем хуже кровоснабжение кости, тем интенсивнее боль. Нарушение микроциркуляции в субхондральной кости приводят к резкому снижению диффузии необходимых питательных веществ в матрикс хряща. Снижение внутрикостного давления ликвидирует одно из препятствий для адекватной трофики гиалинового хряща, что подтверждается данными проведенных клинического и биохимического исследований.
Цель работы — оценить результаты использования внутритканевой электростимуляции в качестве варианта монотерапии в курсе консервативного лечения начальных стадий гонартроза на основании данных клинического и биохимического исследованиий.
МАТЕРИАЛЫ И МЕТОДЫ
Объектом исследования являлась когорта пациентов обоего пола в возрасте 45-65 лет (n = 43). Клиническое обследование включало специализированную оценку антропометрических параметров с вычислением индекса массы тела (ИМТ) по известной формуле:
т , I = тт.кг/мА h2
где I — индекс массы тела, m — масса тела в килограммах, h — рост в метрах.
Для определения степени ожирения руководствовались значениями индекса массы тела, выявляли наличие и степень тяжести сопутствующих заболеваний, согласно действующим Клиническим рекомендациям по лечению гонартроза (Утверждены Минздравом РФ 03.09.2021). При помощи «Калькулятора экологической коморбидности» вычисляли числовой показатель - индекс коморбидности (ИК) [11].
Критерии включения в исследование:
наличие в анамнезе установленного диагноза «гонартроз», «артроз коленного сустава» (код М17 согласно МКБ-10);
стадия заболевания I-II (по Kellgen - Lowrence) [12];
односторонний характер заболевания.
Критерии исключения:
системные, аллергические, ревматические и опухолевые поражения суставов, асептический некроз, ожирение выше 1 степени;
отличный от механического фенотип скелетно-мышечной боли;
оперативные вмешательства на коленном суставе;
патология почек;
заболевания опухолевой и эндокринной природы;
количество баллов по результатам теста ходьбы Хаузера менее 5 [13].
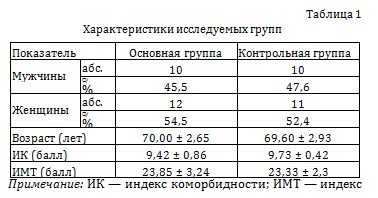
Исходя из методов лечения, исследуемая совокупность пациентов разделена на 2 группы. Контрольную группу (n = 21) составили пациенты, получавшие курс лечения, включавший медикаментозное пособие, курсы физио- и кинезиотерапии, в рамках действующего Приказа Минздрава России от 27.10.2022 № 706 «Об утверждении стандарта медицинской помощи взрослым при гонартрозе (диагностика, лечение и диспансерное наблюдение)». Лица, при лечении которых в качестве монотерапии применяли внутритканевую электростимуляцию по А.А. Герасимову (ВТЭС), отнесены в основную группу (n = 22). Распределение показателей больных дает основание считать, что сравниваемые группы являются сопоставимыми (p < 0,05) (табл. 1).
Р1 х 100 п, х = —р %-
Путем вычитания полученного значения из 100 % вычисляли процент распределения массы тела на другую ногу. Опороспособность конечности считали восстановленной в случае, если показатели пострадавшей конечности достигали значения не менее (80 ± 10) % от здоровой. При отсутствии нарушения и при полном (100 %) восстановлении ОС начисляли 5 баллов, при значениях в 90, 80 и 70 % — по 4, 3 и 2 балла соответственно.
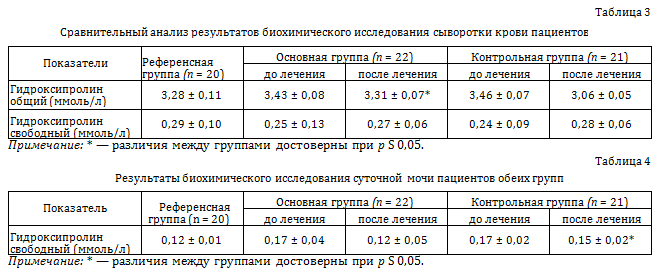
Изучение биологического материала (сыворотки крови и суточной мочи) включало определение ряда показателей — маркеров деградации хрящевой ткани (свободного и общего гидроксипролина). Исследование проводили по методу, предложенному П.Н. Шараевым [16]. Забор биологического материала проводили перед началом курса лечения и через 45 сут. со дня последней процедуры или пребывания в отделении восстановительного лечения. В качестве референсных значений использовали аналогичные показатели здоровых людей в возрастном диапазоне от 45 до 65 лет. Степень удовлетворенности лечением определяли согласно персонифицированной оценке результатов лечения [17], при этом в качестве базовой использовали шкалу WOMAC (англ. Western Ontarioand McMaster University Osteoarthritis Index).
Результаты исследования обработаны непараметрическими методами вариационной статистики для малых выборок. Статистическую значимость различий подтверждали при значении p < 0,05. Показатели проверены на нормальность по критериям Шапиро - Уилка и Титьена - Мура.
РЕЗУЛЬТАТЫ
Анализ стандартных рентгенограмм пациентов обеих групп выявил рентгенологические признаки, характерные для ОА коленных суставов, описанные J. Kallgren и J. Lawrence [12], где нулевое значение свидетельствует об отсутствии изменений, при значении I (сомнительная степень) визуализируются незначительные остеофиты.
Степень II (минимальная) характеризуется наличием чётко выраженных остеофитов. У 11 пациентов отмечены минимальное сужение суставной щели (менее чем на 2/3 по сравнению с нормальными показателями), единичные субхондральные кисты и незначительные краевые костные разрастания. В 32 случаях видимых изменений структуры кости или анатомии сустава выявлено не было (рис. 1).
Основная группа (п = 22) Контрольная группа (п = 21)
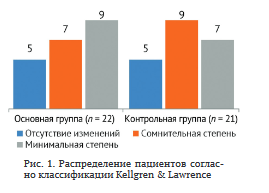
Объективные показатели, характеризующие опороспособность конечности и степень болевого синдрома, перед началом лечения в обеих группах были сопоставимы (табл. 1).
Согласно данным локомоторного тестирования перед началом лечения, нарушение опороспособности выявлено у 70 % пациентов основной и 70 % пациентов контрольной группы. Сравнительный анализ данных показателей в отдаленном периоде выявил статистически подтвержденное различие в полученных значениях (р < 0,05), что указывает на более эффективное восстановление опороспособности конечности в основной группе: (3,59 ± 0,31) против (3,26 ± 1,2).
Путем измерений кожного электропотенциала перед началом курса лечения у большинства обследуемых пациентов установили наличие болевого синдрома различной интенсивности (от умеренной до сильной). Объективное количественное измерение электропотенциала в виде коэффициента асимметрии (КА) стойко коррелировало (г = 0,97) с аналогичными субъективными показателями ВАШ (табл. 2). Клиническое и электрометрическое исследование подтвердило наличие болевого синдрома различной интенсивности у равного числа пациентов, при этом статические и ночные боли также испытывали 55 % (n = 11) пациентов основной и 57 % (n = 11) пациентов контрольной группы. Ликвидации болевого синдрома удалось добиться у всех пациентов основной и у 65 % пациентов контрольной группы. Сравнив числовые значения КА в отдаленном периоде, установили наличие болевого синдрома (от умеренного до незначительного) у 15 пациентов контрольной группы и у 2 человек основной группы. Результат подтвержден данными ВАШ. Выявлено статистически подтвержденное различие (р < 0,05) в показателях, характеризующих наличие и степень интенсивности боли в отдаленном периоде, что указывает на более высокую эффективность противоболевой терапии в основной группе.

Согласно ожиданиям пациентов, проведенное лечение должно купировать болевой синдром, улучшать опороспособность, расширять функциональные возможности и улучшать качество жизни. Высокие показатели степени удовлетворенности лечением зарегистрированы у 95 % пациентов основной группы и у 55 % пациентов контрольной группы. По результатам вводного тестирования каждая из групп была поделена на 2 подгруппы (табл. 5).
Подгруппу «А» составили пациенты, ожидания которых находились в диапазоне «отлично» или у верхней границы диапазона «хорошо» (n = 21). При этом показатель ЖР составил > 85 баллов. В подгруппу «В» вошли пациенты, ожидания которых находились у нижней границы диапазона «хорошо». В данной подгруппе преобладали лица старшей возрастной категории с нарушением опороспособности конечности. Показатель ЖР у этих пациентов составил < 84 баллов. Анализ результатов оценки эффективности лечения выявил различную степень удовлетворенности лечением у пациентов основной и контрольной групп. Установлено, что результатами лечения осталось довольно большинство пациентов основной группы, при этом в 25 % случаев достигнутый результат превзошел ожидаемый. Количество удовлетворенных результатами лечения пациентов в контрольной группе было ниже, чем в основной, выявлено 2 случая с неудовлетворительной результативностью, что, очевидно, являлось результатом низкой эффективности противоболевой и противовоспалительной терапии. Основанием для прекращения процедур внутритканевой электростимуляции (и курса лечения) в основной группе являлись ликвидация болевого синдрома и восстановление параметров опороспособности конечности. Установлено, что длительность сроков лечения пациентов различалась в пользу пациентов основной группы: (13,21 ± 1,2) дня против (18,3 ± 1,2) дня в контрольной.
 .
.
ОБСУЖДЕНИЕ
Известно, что течение ранних стадий остеоартроза характеризуется наличием хронического костно-болевого синдрома различной интенсивности, сопровождается характерными изменениями биомеханических, прочностных свойств кости, обусловленных перестройкой и изменением её качества. Собственные клинические наблюдения, подтвержденные данными литературы, указывают на то, что наиболее интенсивная боль локализуется в брадитрофных зонах костей, образующих коленный сустав (метафизарных отделах голени) [1, 4]. Известно, что результатом применения ВТЭС на ранних стадиях ОА, помимо снятия болевого синдрома, является восстановление локальной микроциркуляции костной и хрящевой тканей [19]. Результаты проведенных ранее полярографических и реографи- ческих исследований показали достоверно значимое ускорение процессов латентного периода доставки и утилизации кислорода в костной ткани после проведения курса электростимуляции. Доказано, что восстановление микроциркуляции и васкуляризации усиливает активность процессов энергетического обмена, что приводит к ликвидации локальных очагов асептического воспаления кости, восстановлению ее пьезоэлектрических и биохимических свойств [19]. В ряде отечественных и зарубежных исследований, посвященных вопросам лабораторной диагностики, показана специфичность маркеров деградации и синтеза хрящевой ткани и субхондральной кости — основных патогенетических звеньев ОА [20], изучена взаимосвязь структурных нарушений гиалинового хряща сустава и параметров системных проявлений воспалительной реакции на различных (в том числе доклинических) стадиях течения заболевания [22, 23]. Известно, что разрушение коллагеновых волокон сопровождается повышением экскреции гидроксипролина и увеличением его содержания в сыворотке крови. По имеющимся в настоящее время данным, гидроксипролин, определяемый в сыворотке крови и моче, является продуктом распада коллагена, причем свободная фракция ГП считается маркером деструкции, а связанная — маркером активности метаболизма соединительной ткани [23-26]. После проведения курса внутритканевой электростимуляции мы отметили уменьшение содержания общего и свободного гидроксипролина в сыворотке крови и суточной моче пациентов преимущественно в основной группе, что косвенно свидетельствовало о более активном торможении процессов распада коллагена и восстановлении активности метаболизма соединительной ткани в этой группе пациентов [27, 29]. Изученные нами биохимические маркеры обладают невысокой специфичностью и высокой диагностической значимостью, поэтому являются косвенным признаком торможения распада коллагена. Однако изменение биохимических маркеров в совокупности с данными клинического и электрометрического исследований позволяют с высокой долей вероятности предполагать хондропротективный эффект от применения внутритканевой электростимуляции.
ЗАКЛЮЧЕНИЕ
Применение ВТЭС на ранних стадиях развития гонартроза ликвидирует болевой синдром, способствует снижению интенсивности процессов деструкции коллагена и восстановлению опороспособности конечности.
Внутритканевая электростимуляция является эффективным, патогенетически обоснованным методом лечения пациентов с остеоартрозом коленных суставов, сопровождающимся хроническим болевым синдромом.
Хело М.Д., Ахтямов И.Ф., Абдуллах А.М., Саид Ф.М. Лечение гонартроза — современные тенденции и проблемные вопросы. Практическая медицина. 2018;16(7 (часть 1)):48-53. doi: 10.32000/2072-1757-2018-16-7-48-53
Katz JN, Arant KR, Loeser RF. Diagnosis and Treatment of Hip and Knee Osteoarthritis: A Review. JAMA.2021;325(6):568- 578. doi: 10.1001/jama.2020.22171
Новаков В.Б., Новакова О.Н., Чурносов М.И. Связь полиморфизма генов LYPLAL1 и TGFA с прогрессированием остеоартроза коленного сустава у жителей Центрального Черноземья России. Травматология и ортопедия России. 2022;28(4):42-53. doi: 10.17816/2311-2905-1979
Алексеева Л.И., Таскина Е.А., Кашеварова Н.Г. Остеоартрит: эпидемиология, классификация, факторы риска и прогрессирования, клиника, диагностика, лечение. Современная ревматология. 2019;13(2):9-21. doi: 10.14412/1996-7012-2019-2-9-21
Повзун А.С., Мазуров В.И., Повзун К.А., Костенко В.А.. Оценка текущей экономической эффективности лечения больных остеоартритом в Санкт-Петербурге и ее перспективы. Вестник Северо-Западного государственного медицинского университета. 2017;9(3)89-9б.
Rizk E, Tajchman S, Fink E, et al. Quality indicators for osteoarthritis pain management in the primary care setting. BMCMusculoskeletDisord. 2023;24<1):538. doi: 10.1186/s12891-023-06637-x
Eymard F, Ornetti P, Maillet J, et al. Intra-articular injections ofplatelet-rich plasma in symptomatic knee osteoarthritis: a consensus statement from French-speaking experts. Knee Surg Sports Traumatol Arthrosc. 2021;29(10):3195-3210. doi: 10.1007/s00167-020-06102-5
Fiz N, Delgado D, Garate A, et al. Intraosseous infiltrations of Platelet-Rich Plasma for severe hip osteoarthritis: A pilot study. J Clin Orthop Trauma. 2020;11(Suppl 4):S585-S590. doi: 10.1016/j.jcot.2019.12.012
Абусева Г.Р., Ковлен Д.В., Пономаренко Г.Н. и др. Физические методы реабилитации пациентов с остеоартрозом: наукометрический анализ доказательных исследований. Травматология и ортопедия России. 2020;26(1):190- 200.
Garvey WT, Garber AJ, Mechanick JI, et al. American association of clinical endocrinologists and american college of endocrinology position statement on the 2014 advanced framework for a new diagnosis of obesity as a chronic disease.
EndocrPract. 2014;20(9):977-989. doi: 10.4158/EP14280.PS
Рагозин О.Н., Малахов Ю.В., Дьячкова Э.Э., Рагозин Р.О. Калькулятор экологической коморбидности. Свидетельство о гос. рег. программы для ЭВМ № 2017663878. 13.12.2017.
Kellgren JH, Jeffrey M, Ball J. Atlas of standard radiographs. Vol 2. Oxford: Blackwell Scientific; 1963.
Коваленко А.П., Камаева О.В., Мисиков В.К. и др. Шкалы и тесты для оценки эффективности лечебно-реабилитационных мероприятий у пациентов со спастичностью нижней конечности. Журнал неврологии и психиатрии им. С.С.
Корсакова. 2018;118(5):120-128. doi: 10.17116/jnevro201811851120
Герасимов А.А. Способ объективной диагностики болевых синдромов. Российский журнал боли. 2013;1(36):76-77.
Бурматов Н.А., Сергеев К.С., Копылов С.А. и др. Способ расчёта объективных показателей опороспособности нижней конечности (SUPPORTTEST). Свидетельство РФ о государственной регистрации программы для ЭВМ № 2023616226. 23.03.2023.
Гаркави Д., Гаркави А., Лычагин А. Универсальный способ персонифицированной оценки результатов лечения у пациентов ортопедо-травматологического профиля. Врач. 2014;(7):31-34.
Иржанский А.А., Куляба Т.А., Корнилов Н.Н. Валидация и культурная адаптация шкал оценки исходов заболеваний, повреждений и результатов лечения коленного сустава WOMAC, KSS и FJS-12. Травматология и ортопедия России. 2018;24(2):70-79. doi: 10.21823/2311-2905-2018-24-2-70-79
Герасимов А.А. Лечение больных с дистрофическими заболеваниями суставов и позвоночника способом внутритканевой электростимуляции: автореф. дис. ... д-ра мед. наук. Санкт-Петербург; 1995;27.
Белова С.В., Гладкова Е.В., Ульянов В.Ю., Блинникова В.В. Метаболические сдвиги у лиц с потенциальным риском развития первичного остеоартроза. Саратовский научно-медицинский журнал. 2018;14(3):511-514.
Гладкова Е.В., Иванов А.Н. Взаимосвязь структурных нарушений суставного гиалинового хряща и параметров системных проявлений воспалительной реакции в патогенезе ранних стадий первичного остеоартроза. Саратовский научно-медицинский журнал. 2018;14(3):518-523.
Галашина Е.А., Бондаренко А.С., Ульянов В.Ю., Климов С.С. Роль маркеров ремоделирования скелетной ткани в патогенезе имплантат-ассоциированного воспаления после первичной артропластики коленного сустава. Саратовский научно-медицинский журнал. 2018;14(3):515-518.
Носивец Д.С. Биохимические маркеры при патологии хрящевой и костной ткани. Материалы научно-практической конференции с международным участием, посвященной 90-летию со дня рождения профессора Н.П. Деми- чева «Современные аспекты травматологии, ортопедии и реконструктивной хирургии», Астрахань, 22-23 марта 2019. Астрахань: Изд-во Астраханского государственного медицинского университета; 2019:90-92.
Русланова Н.М., Поспелова К.И., Бахтин В.М. и др. Клиническое значение гидроксипролина в диагностике соединительнотканной дисплазии. Материалы VI Международной научно-практической конференции молодых учёных и студентов, посвященной году науки и технологий «Актуальные вопросы современной медицинской науки и здравоохранения», Екатеринбург, 8-9 апреля 2021. Екатеринбург: Изд-во УГМУ; 2021:369-374.
Kurd MF, Kreitz T, Schroeder G, Vaccaro AR. The Role of Multimodal Analgesia in Spine Surgery. J Am Acad Orthop Surg. 2017;25(4):260-268. doi: 10.5435/JAAOS-D-16-00049
Рассказов Н.И., Колокольцев В.В., Рассказов Д.Н. Перспективы изучения аутоантител к коллагенам. Вестник дерматологии и венерологии. 1994;(3):12-15.
Лунева С.Н., Сазонова Н.В., Мальцева Л.В., Матвеева Е.Л. Оценка эффективности препарата Терафлек в лечении начальных стадий остеоартрита и его влияния на структуру и метаболизм хрящевой ткани. Consilium Medicum. 2018;20(9):63-70. doi: 10.26442/2075-1753_2018.9.63-70
Parry DDA, Squire JM. Fibrous proteins: new structural and functional aspects revealed. In: Advances in protein chemistry. Elsevier Publ.; 2005:1-10.
. Информация об авторах:
Никита Александрович Бурматов — кандидат медицинских наук, врач травматолог-ортопед, ассистент кафедры
Константин Сергеевич Сергеев — доктор медицинских наук, профессор, заведующий кафедрой
Светлана Николаевна Лунева — доктор биологических наук, профессор, ведущий научный сотрудник
Андрей Александрович Герасимов — доктор медицинских наук, профессор, профессор кафедры
Семен Александрович Копылов — студент 5 курса
Наталия Александровна Спиридонова — кандидат физико-математических наук
Теги: заболевания суставов
234567 Начало активности (дата): 30.07.2024 18:05:00
234567 Кем создан (ID): 989
234567 Ключевые слова: остеоартрит, заболевания суставов, внутритканевая электростимуляция, восстановительное лечение, гонартроз
12354567899



