 18.05.2017
18.05.2017
Параартикулярные ткани: варианты поражения и их лечение
Статья посвящена проблеме поражения параартикулярных тканей суставов
Параартикулярные ткани: варианты поражения и их лечение
Для цитирования: Хитров Н.А. Параартикулярные ткани: варианты поражения и их лечение // РМЖ. 2017. №3. С. 177-184
Статья посвящена проблеме поражения параартикулярных тканей суставов
Ревматизм – это любая боль в миле от сустава!
Philip Hench, лауреат Нобелевской премии 1950 г.
Большую долю заболеваний локомоторного аппарата составляют периартриты – поражения параартикулярных тканей (ППАТ) суставов. ППАТ занимают одно из первых мест среди заболеваний опорно-двигательного аппарата у взрослого населения. Обращения по поводу ППАТ могут составлять до 59% первичных визитов к ревматологу [1].
Параартикулярные ткани представляют совокупность околосуставных структур и отдаленных от суставов тканей. Околосуставные ткани включают: сухожилия мышц и их влагалища, сумки, связки, фасции, апоневрозы. Отдаленные от суставов структуры составляют мышцы, нервно-сосудистые образования, подкожно-жировая клетчатка.
Распознаванию поражения околосуставных тканей успешно способствуют особенности топической диагностики данных структур:
1) поверхностное, часто подкожное, расположение;
2) близость анатомических костных ориентиров;
3) визуализация поражения: припухлость, гиперемия и т. д.;
4) легко выполнимая пальпация;
5) возможность построения рисунка боли, включающего триггерные точки, зоны распространения боли и т. п.;
6) оценка объемов нарушения движений (контрактуры механические, болевые, спастические и т. п.);
7) оценка боли в покое и при движении;
8) оценка активных и пассивных движений;
9) использование провокационных проб (Тинеля, Фалена и др.).
Диагностика ППАТ основывается на наличии локальных изменений: болезненности, уплотнения, отека, гипертермии, гиперемии. При опросе часто выявляется связь возникновения боли с травмой или повторяющимся нагрузочным движением. Обычно боль провоцируется движениями в данном суставе и стихает в покое. Пассивные движения в суставе больного, выполняемые врачом, менее болезненны, чем активные – движения, которые совершает сам пациент [2].
В последние годы среди различных вариантов ППАТ все большее место занимают энтезопатии – патология энтезисов. Термином «энтезис» обозначают место прикрепления сухожилий, связок, апоневрозов или суставных капсул к кости. Термин «энтезопатия» используется в медицинской литературе с 1960-х годов, первоначально его применяли для характеристики первично дегенеративных изолированных изменений, возникающих в энтезисе вследствие перегрузки. Именно область энтезиса становится «слабым звеном» в аппарате околосуставных тканей, где при чрезмерной нагрузке возникают микро- и макроскопические повреждения, приводящие в последующем к локальному воспалению [3, 4]. Клиника энтезопатии характеризуется спонтанной болью, болью при определенных движениях, болезненностью при пальпации, возможной припухлостью в области поражения.
ППАТ характеризуются локальной слабой или сильной болью, порой с иррадиацией по ходу вовлеченных сухожильно-связочных, мышечных и нервных структур. Нейропатическая боль более разнообразна, она эмоционально окрашена (жгучая, колющая, холодящая, беганье мурашек и т. п.) и отличается распространением по ходу иннервируемых областей вовлеченных нервных путей. Дифференциальная диагностика и клинические признаки при различных поражениях опорно-двигательного аппарата представлены в таблице 1.
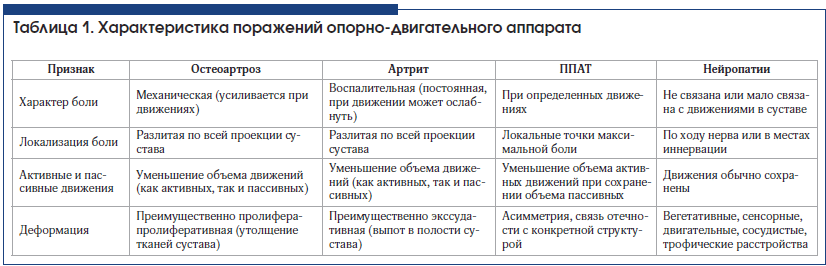
Таблица 1. Характеристика поражений опорно-двигательного аппарата
В отличие от поражения самих суставов для ППАТ характерны:
1) несоответствие между активными и пассивными движениями (обычно ограничены активные движения при нормальном объеме пассивных);
2) усиление боли при строго определенных движениях;
3) отсутствие припухлости сустава или локальная припухлость в проекции пораженного сухожилия;
4) несмотря на стойкий болевой синдром и нарушение функции, лабораторные и рентгенологические изменения недостаточно показательны [2], хотя могут выявляться кальцификация, костное ремоделирование, эрозии костей в местах прикрепления сухожилий и связок. При УЗИ и МРТ хорошо дифференцируются повреждения мягких околосуставных структур, наличие в них включений и жидкости.
Причины ППАТ можно разделить на первичные и вторичные. К первичным причинам ППАТ относятся острая травма, хроническая травматизация, хроническая механическая перегрузка, часто повторяющиеся стереотипные движения в суставе. Вторично ППАТ возникают на фоне различных заболеваний: патологии опорно-двигательного аппарата (ортопедические аномалии развития, артрозы, артриты, спондилоартриты, синдром дисплазии соединительной ткани, гипермобильности суставов), эндокринно-обменных нарушениий (сахарный диабет, нарушения жирового, кальциевого обмена, гипотиреоз, гиповитаминоз), нейротрофических нарушений, сосудистых расстройств, гипериммунных реакциий, беременности и т. п. [5].
В данной публикации остановимся подробно на поражениях параартикулярных тканей верхних конечностей и спины.
Плечо
ППАТ описано S. Duplay в 1872 г. «Меткое во времена Duplay наименование «периартрит» в дальнейшем стало тормозом в изучении болевого синдрома в области плечевого сустава. Врач, вынося диагноз «плечелопаточный периартрит», освобождает себя от поисков клинических симптомов, позволяющих углубить и детализировать те или иные проявления заболевания в этой области. Под этим названием начали скрывать незнание причин боли, и диагноз «периартрит плечевого сустава» стал, по образному выражению J.N. Pender (1959), «waste-basket» – корзиной для ненужных бумаг для многих врачей» – писал Р.А. Зулкарнеев в 1979 г. [6].
Разнообразие форм ППАТ плеча связано с особенностями развитого параартикулярного аппарата плечевого сустава, осуществляющего самые различные движения: сгибание, разгибание, отведение, приведение, вращение и круговое движение. Из-за сложного параартикулярного аппарата и частоты ППАТ плечевой сустав называется «периартритическим органом» [7].
Большую часть ППАТ составляют теномиозиты мышц, образующих так называемую манжету ротаторов плеча. Ротационная манжета формируется из 4-х мышц: надостной, подостной, малой круглой и подлопаточной. Чаще всего поражаются энтезисы – дистальные отделы надостной и подлопаточной мышц в местах их прикрепления соответственно к большому и малому бугоркам плечевой кости.
Энтезопатии – повреждения с реактивным воспалительным компонентом энтезисов надостной и подлопаточной мышц, часто встречающиеся формы ППАТ. Они имеют четкую клиническую картину, включающую в себя затруднение движений, за которые отвечает данная мышца, и болезненность, усиливающуюся при пальпации энтезиса. При энтезопатии надостной мышцы больному трудно отводить и поднимать руку вверх во фронтальной плоскости. При пальпации плеча отмечается боль в верхнелатеральной части большого бугорка плечевой кости. При энтезопатии подлопаточной мышцы пациенту трудно завести руку за спину, при этом отмечаются боль и локальная болезненность при пальпации в области малого бугорка плечевой кости [8].
Кальцифицирующий тендинит – циклично протекающее заболевание сухожилий мышц, в основе которого лежит формирование депозитов кальция. Выделяют несколько фаз заболевания, каждая из которых может продолжаться несколько месяцев: начальная (прекальцификация), кальцификация и восстановление. Характерными проявлениями болезни являются боль и ограничение движений, достигающие максимума в фазе кальцификации [3, 9]. Конгломераты кальция хорошо видны как при рентгенологическом исследовании, так и при УЗИ и МРТ.
Реже клинику ППАТ определяют бурситы, хорошо визуализируемые при УЗИ и МРТ.
Бурсит плеча. При бурсите больные жалуются на боли при абдукции и сгибании в плече, просыпаются от боли, когда лежат на больной стороне. Движения при одевании, причесывании, умывании затруднительны и болезненны. При осмотре часто видна припухлость переднего отдела плечевого сустава. Боль может иррадиироватъ вниз по руке. Иногда больные вспоминают о перенапряжении, предшествующем появлению симптоматики, но чаще никакой явной причины выявить не удается. Объем движений в плечевом суставе может быть резко ограничен из-за боли. Пальпация переднебоковой поверхности сустава выявляет либо незначительную болезненность, либо резкую боль.
Импинджмент-синдром (impingement shoulder syndrome) – проба Dowborn, или симптом столкновения, в отечественной литературе более известный как тест «болезненной дуги». Импинджмент-синдром – дословно: синдром столкновения или соударения. Механизм патологических изменений и появления боли связан с ущемлением мягкотканных структур (капсулы сустава, связок, сухожилий, параартикулярных мягких тканей) между костными структурами. Импинджмент-синдром возникает как при патологическом сужении костно-связочного пространства (при артрозе, вывихах или переломах костей со смещением и наличием костных отломков), так и при увеличении объема самих мягкотканных структур (при дегенеративных изменениях, гематомах, частичных разрывах, воспалительных изменениях сухожилий связок, мышц и т. д.).
Импинджмент-синдром наглядно демонстрируется пробой Дауборна – тестом «болезненной дуги». Если при подъеме с отведением руки во фронтальной плоскости боль возникает на уровне 60–120°, то скорее всего больной страдает бурситом. Возникновение боли при отведении руки на 160–180° предполагает патологию (чаще всего остеоартроз) акромиально-ключичного сустава, когда сустав сдавливается поднятой вверх плечевой костью. Если боль возникает на протяжении всего отведения руки, от 0 до 180° (особенно если врач оказывает сопротивление отведению), то можно предположить патологию надостной мышцы [11–13].
Сложен в диагностическом плане, лечении и прогнозе капсулит. Он характеризуется изолированным поражением наружной, фиброзной части суставной капсулы, сопровождается избыточным ее утолщением, натяжением, стягиванием (ретракцией), слипанием стенок (адгезией) и уменьшением объема полости сустава. Синовиальная оболочка при этом не изменена, воспалительный компонент не выражен. Уменьшение внутрисуставного пространства, потеря растяжимости капсулы и за счет этого сглаживание ее физиологических заворотов устанавливаются при МРТ, контрастной артрографии и артроскопии плечевого сустава. Заболевание, как правило, одностороннее, возникает чаще у женщин среднего возраста после перенесенных травм, переломов, альгодистрофий, инфарктов миокарда. Боль сопровождается ограничением как активных, так и пассивных движений в суставе во всех направлениях. Данное состояние укладывается в понятие «замороженное плечо» [14, 15]. Выделяют 3 фазы течения капсулита: воспалительно-болевую, фиброзно-гипокинетическую (стадия «окоченения») и фазу разрешения (стадия «оттаивания») [16].
Прогноз заболевания достаточно серьезный, с развитием контрактуры, обездвиженности сустава. Лечение капсулита комплексное, включает лечебную физкультуру, физические факторы, применение нестероидных противовоспалительных препаратов (НПВП) и глюкокортикоидов как локально, так и системно. Возможны оперативные пособия.
Длительность ППАТ плеча зависит от клинических вариантов. Заболевание протекает от нескольких недель до более длительных сроков, вплоть до перехода в хроническое состояние с перманентным или рецидивирующим течением на протяжении многих лет. ППАТ могут начинаться медленно и постепенно прогрессировать в течение нескольких лет. Вместе с тем, заболевание может быстро прогрессировать с ранними нарушениями функции сустава, дистрофией сухожильно-связочного аппарата и гипотрофией мышц. Длительное течение процесса является причиной и следствием частого двустороннего поражения плечевых суставов. Одна из причин поражения второго сустава – его механическая перегрузка при компенсаторном выполнении функций за оба сустава.
Локтевая область
Среди ППАТ локтевого сустава чаще всего встречаются эпикондилиты: наружный эпикондилит – «локоть теннисиста» (Tennis elbow) и внутренний – «локоть игрока в гольф» (Golfers elbow) [17]. Основной симптом эпикондилита – боль в области надмыщелка в покое, усиливающаяся при ротационных движениях в локтевом суставе и движениях в кисти (сгибание и разгибание). Боль усиливается при пальпации, причем эпицентр боли может локализоваться, во-первых, в области надмыщелка плечевой кости – в местах энтезисов мышц предплечья, во-вторых, ниже надмыщелка – в области сухожилий прилегающей группы мышц. В–третьих, возможен эпицентр боли при пальпации в верхней трети предплечья – в местах прохождения самих мышц, что говорит о различной степени вовлечения в патологический процесс энтезисов, сухожилий и мышц у различных больных.
Наружный эпикондилит («локоть теннисиста») встречается чаще внутреннего эпикондилита. Появлению боли предшествует механическая усиленная или необычная нагрузка – работа на садовом участке, занятия спортом после большого перерыва, ремонт и т. д. Пациент точно указывает место наибольшей болезненности, соответствующее наружному надмыщелку плечевой кости – энтезису, где прикрепляются сухожилия разгибателей кисти и пальцев, или проекции сухожилий. Эпицентр боли может располагаться несколько ниже надмыщелка. Боль возникает при сопротивлении активному разгибанию в лучезапястном суставе. Боль возникает по наружной поверхности локтя при вращательных движениях (например, при работе с отверткой и т. п.) В точке максимальной болезненности могут отмечаться отек, покраснение и местное повышение температуры.
Внутренний эпикондилит («локоть игрока в гольф») встречается реже наружного эпикондилита и представляет собой энтезопатию мышц-сгибателей кисти и пальцев, прикрепляющихся в области внутреннего надмыщелка плечевой кости. В этом месте определяется пальпаторная болезненность, боль также воспроизводится при сопротивлении активному сгибанию кисти в лучезапястном суставе.
Часто пациент, страдающий эпикондилитом, сам показывает наиболее болезненные для него движения. При латеральном эпикондилите боли усиливаются при супинации предплечья и разгибании кисти, а при медиальном эпикондилите – возникают и усиливаются при пронации предплечья и сгибании кисти [18].
Бурсит локтевого отростка встречается изолированно, как правило, вследствие хронической травматизации задненижней поверхности локтя или в сочетании с артритами, при подагре и ревматоидном артрите. В области локтевого отростка локтевой кости возникает малоболезненное округлое образование размером не больше куриного яйца, мягкое при пальпации. Оно становится хорошо заметным при разогнутой в локтевом суставе руке. При изолированном бурсите движения в локтевом суставе заметно не страдают. Пальпаторно отмечается «наполненность» и флуктуация сумки. Возможны небольшая болезненность, повышение температуры кожи, гиперемия над областью сумки локтевого отростка и ниже по разгибательной поверхности предплечья [19]. Данные симптомы могут наблюдаться в начале развития бурсита, опережая на несколько дней появление подкожной припухлости.
Кисть
На тыльной поверхности кисти или в области лучезапястного сустава в проекции сухожильных влагалищ разгибателей нередко располагается ганглий (эквивалентом ганглия является гигрома) – безболезненный округлый узелок, величиной с горошину или больше. Он представляет собой грыжевидное кистозное образование, связанное с синовиальным влагалищем сухожилия или с капсулой сустава, в последующем возможно отделение от них. Ганглий представляет из себя кистозную полость с капсулой, чаще однокамерную, иногда многокамерную, неправильных очертаний, с боковыми ответвлениями. В полости ганглия находится синовиальная жидкость, представляющая собой серозное или слизистое, по мере концентрации желатиноподобное содержимое, которое сложно аспирировать.
Возраст пациентов с ганглием – от молодого до старческого, чаще средний. Встречается чаще у мужчин. В анамнезе нередко отмечается травма. Старинное домашнее средство от ганглия – удар по нему тяжелой книгой, что заставляет кисту вправиться во влагалищную полость. В медицине применяется пункция ганглия с удалением содержимого, но чаще, при невозможности пункции из-за густого содержимого – хирургическое иссечение ганглия. После удаления ганглий может рецидивировать, причем иногда возникают и новые узлы.
Синдром де Кервена – заболевание, представляющее собой теносиновиты длинного абдуктора (tendo аbductor pollicis longus) и короткого разгибателя (tendo extensor pollicis brevis) I пальца кисти. Синовиальные влагалища данных сухожилий сдавливаются между шиловидным отростком лучевой кости и связкой – ограничителем разгибателей (retinaculum extensorum).
Ранее болезнь описывалась как профессиональная болезнь прачек. В настоящее время заболевание встречается чаще у женщин в первые месяцы после родов по механизму отечного синдрома, провоцирующего туннельный патогенез синдрома.
Клиника характеризуется болью в области на 1,5–2 см проксимальнее основания I пальца («анатомическая табакерка»). Возможна отечность в этом месте. Диагностический тест – провоцирующий симптом Финкельштейна (Finkelstein), когда возникает резкая боль при натяжении воспаленных сухожилий при приведении I пальца к ладони, фиксации его другими пальцами и пассивном или активном приведении кулака в сторону локтевой кости [3, 20].
Синдром карпального (запястного) канала (СКК) относится к частым туннельным синдромам и характеризуется сдавлением срединного нерва в карпальном канале. Уже при небольшом уменьшении объема канала в результате воспалительно-дистрофических процессов в сухожилиях возникает ишемия срединного нерва с симптоматикой СКК. Это одна из часто встречающихся патологий у женщин в возрасте 40–60 лет. СКК как туннельный синдром проявляется онемением, парестезией кисти чаще в ссостоянии покоя и ночью. Пациенты жалуются на боль от слабой до нестерпимой в I–III пальцах и по лучевой поверхности IV пальца (по ходу иннервации срединного нерва). В поздних стадиях может формироваться атрофия мышц тенара (двигательные волокна срединного нерва иннервируют мышцы возвышения большого пальца).
Существуют несколько провокационных тестов, позволяющих подтвердить диагноз СКК. Симптом Тинеля – поколачивание (сдавление) области карпального канала с ладонной стороны (между основаниями тенара и гипотенара). У больных при этом возникают ощущения, подобные приступу. Симптом Фалена – переразгибание в лучезапястном суставе – также воспроизводит картину приступа. Манжеточный тест состоит в том, что с помощью аппарата для измерения артериального давления прекращается кровообращение в руке. Ишемизированный нерв при этом воспроизводит характерный для СКК рисунок боли [20].
СКК, как правило, первично-хроническое заболевание, хотя в течение 6–12 мес. нередко возникает спонтанное разрешение симптомов. В лечении используются НПВП, локальная инъекционная стероидная терапия, лечение физическими факторами. При их неэффективности применяется хирургическое лечение, которое обычно состоит в рассечении связки карпального канала, что приводит к ремиссии, но нередко дает рецидивы.
Ладонный (пальмарный) фасциит (ПаФ) – относительно редкое заболевание, характеризующееся болезненным уплотнением ладонного апоневроза с формированием сгибательных контрактур пальцев. В отличие от контрактуры Дюпюитрена ПаФ характеризуется болевым синдромом, кроме того, сгибательной контрактурой всех пальцев кисти. При осмотре выявляется умеренное относительно равномерное уплотнение и болезненность ладонного апоневроза. Примерно в половине случаев ПаФ является проявлением паранеопластического синдрома при опухолях женской половой сферы и желудочно-кишечного тракта. В связи с этим все впервые обратившиеся пациенты с ПаФ должны быть обследованы по онкологической программе [21].
Ладонный фасциальный фиброматоз – контрактура Дюпюитрена (КД) – заболевание, характеризующееся стойким неболевым нарушением разгибания пальцев, прежде всего мизинца и безымянного.
КД страдают преимущественно мужчины в соотношении к женщинам 5:1. Заболевание развивается чаще после 40 лет, но встречается и в юношеском возрасте, причем чем моложе больной, тем быстрее прогрессирует болезнь, а у больных до 30 лет стремительное развитие заболевания, характеризующееся быстрым прогрессом и неблагоприятным течением в послеоперационном периоде (келлоидные рубцы, рецидивы в виде стойких контрактур). Отмечен семейный характер КД, в т. ч. у близнецов. Часто КД развивается у больных эпилепсией, злоупотребляющих алкоголем и курением, а также у больных сахарным диабетом 2-го типа, причем в сочетании с подошвенным фиброматозом. КД может быть врожденной, при этом иногда двусторонней.
КД характеризуется прогрессирующим фиброзом ладонного апоневроза с формированием на ранней стадии характерных плотных подкожных узлов соответственно ходу лучей апоневроза, без ограничения функции пальцев. Впоследствии формируются распространенные безболезненные уплотнения, укорочение рубцовых тяжей апоневроза, формирование сгибательных контрактур пальцев, ограничение разгибания в пределах до 90°. В поздней стадии сгибательная контрактура пальцев и ограничение разгибания еще более усиливаются. Основным лечением КД является хирургическая реконструкция апоневроза. Нередко встречаются постоперационные рецидивы болезни.
Нодулярный теносиновит сгибателей пальцев кисти, или «защелкивающий палец» – характеризуется затруднениями движений пальца кисти и защелкиванием их в положении разгибания. Развивается обычно в пожилом возрасте, чаще у женщин. Возможно появление заболевания при хронической профессиональной или бытовой механической перегрузке и травматизации мягких тканей ладони и пальцев кисти.
Клинические проявления характеризуются заклиниванием (затруднением при сгибании и разгибании пальца) и разгибанием со щелчком. Щелчок слышен на расстоянии, ощущается при пальпации ладони в месте заклинивания пальца. Чаще отмечается защелкивание III и IV пальцев кисти. Для разгибания пальцев пациент пользуется другой рукой. Нередко пальпируется плотный, слабо болезненный узелок на ладонной поверхности основания пальца в проекции сухожилия его сгибателя.
Узелки не спаяны с окружающими тканями и сме-щаются при движении сухожилия. Возможно самоизлечение в течение 1–2-х лет или переход заболевания на другие пальцы.
Спина
Среди заболеваний, индуцирующих боли в области спины, патология мягких тканей составляет около 70% [22]. Немаловажное место при этом занимает миофасциальный синдром – вариант соматогенной боли, источником которой являются скелетные мышцы и прилегающие фасции [23].
Главенствующую роль при болях в спине играет рефлекторный болевой спазм паравертебральных мышц – дефанс мышц – «симптом вожжей». Нередкой причиной являются тендиниты и энтезиты спины:
1) место прикрепления m. sacrospinales;
2) переход длинной спинной мышцы в сухожилие;
3) место прикрепления m. gluteus maximus;
4) область перехода m. tensor fasciae latae в ягодичную фасцию;
5) повреждения над- и межостных связок [24].
Нередко боли возникают в местах прикрепления мышц шеи к окципитальному гребню, ромбовидных мышц к внутреннему краю лопатки, косых мышц живота к гребню крыльев подвздошной кости. Данные патологии несложны в диагностике и легко поддаются лечению локальной инъекционной стероидной терапией [25].
Лечение
В лечении ППАТ главенствующее место занимает исключение провоцирующих факторов, прежде всего механических перегрузок. Необходимо ограничение механической нагрузки на структуры, которые вовлечены в конкретное поражение. При выраженном воспалении показан полный покой с использованием ортезов, лонгет на острый период заболевания.
Локальная инъекционная терапия, прежде всего глюкокортикоидами (ГК), занимает одно из ведущих мест в лечении ППАТ. С учетом анатомо-морфологических особенностей ППАТ, показаний, противопоказаний, правильно выбранной дозы ГК, числа и кратности введения можно добиться хороших клинических результатов лечения. Возможно локальное введение анестетиков вместе с ГК и без введения ГК.
Также используются анальгетики, слабые опиоиды, миорелаксанты, седативные препараты. При длительном персистировании боли для профилактики хронизации болевого синдрома используются антидепрессанты, антиконвульсанты. При стихании острого процесса проводится лечение физическими факторами: тепло и криотерапия, магнито-, лазеротерапия, электро- и фонофорез, грязевые аппликации, бальнеолечение. Используется как ударно-волновая терапия, так и методы психической релаксации. В случае возникновения ППАТ на фоне ревматических болезней необходимо направленное лечение основного заболевания.
Важно помнить, что режим, лечебная физкультура, массаж, мануальная терапия должны носить механически щадящий характер в безболевой зоне. Нарушение данного принципа вызовет мышечный и сосудистый спазм, ишемию, болевые контрактуры, перевозбуждение ЦНС и, как следствие, нарушение контроля за состоянием больного.
ППАТ как частный вид скелетно-мышечных болезней, независимо от этиологии во многом обусловлены едиными патогенетическими закономерностями, определяющими их появление и переход в хроническое состояние [26]. Неясность этиологических факторов ППАТ, сложность патоморфологических, нейротрофических и иммуновоспалительных расстройств определяют трудность курации и выбор препаратов для лечения, делают неопределенными сроки терапии.
Противовоспалительная терапия является обязательной и включает, прежде всего, нестероидные противовоспалительные препараты (НПВП) локального (накожного) и системного (орального и перорального) применения.
Простые анальгетики, часто используемые при ППАТ, наименее приемлемы, т. к. не действуют на патогенетические звенья синовита и не имеют эффекта. Кроме того, простые и опиоидные анальгетики вызывают феномен «анальгетической личности», при которой больной, не чувствуя боли, чрезмерно расширяет свою двигательную активность, которая не улучшает, а усугубляет как вторичное воспаление, так и клинику болезни. Назначение миорелаксантов при ППАТ, патогенетически обусловленное, чревато ухудшением координации движений у пожилых больных.
При подходе к лечению ППАТ необходимо помнить следующие положения.
1. Боль при ППАТ, являющаяся ведущим симптомом и причиняющая мучительные страдания, требует скорейшего лечения. Эффективное купирование болевого синдрома – первоочередная задача фармакотерапии ППАТ, поскольку боль определяет тяжесть страданий и качество жизни пациента. Быстроту и стойкость анальгетического эффекта относят к основным критериям оценки адекватности лечения, по крайней мере с точки зрения больного [27, 28].
2. Лечение необходимо проводить в короткие сроки, чтобы активный синовит, утяжеляющий боль, был быстро купирован и не оказал патологического деструктивного воздействия на прилегающие ткани. При ППАТ острый болевой синдром обычно сопровождается выраженной воспалительной реакцией.
3. На сегодняшний день не вызывает сомнения, что назначение НПВП не просто желательно, но определенно показано всем больным с ревматическими заболеваниями, испытывающим боли, связанные с острым или хроническим поражением опорно-двигательного аппарата. Их отличает хорошо доказанная эффективность, предсказуемость фармакологического действия, доступность и удобство применения.
НПВП имеют несомненные преимущества по сравнению с другими классами анальгетиков. По сравнению с опиоидами современные НПВП исключительно редко вызывают серьезные осложнения со стороны центральной нервной системы, к ним не развивается привыкание, а потому они не имеют каких-либо формальных ограничений для назначения и приобретения [27].
4. Длительное или постоянное применение НПВП нецелесообразно ввиду повышения риска развития осложнений. Поэтому данные препараты рекомендуются больному на период острой стадии. Важно, что лечебная эффективность и переносимость различных НПВП у каждого пациента индивидуальны, и при назначении их необходим персональный подход с оценкой как эффективности, так и побочных действий препарата [29, 30].
5. Соматические заболевания сопутствуют ППАТ, что часто встречается у пожилых людей. Терапия не должна иметь побочных действий, чтобы не усугубить клинику сопутствующих болезней. Хорошо известно, что основное фармакологическое действие НПВП связано с блокадой циклооксигеназы-2 (ЦОГ-2), фермента, активно синтезирующегося в очагах повреждения и воспаления клетками воспалительного ответа и отвечающего за синтез важнейших медиаторов боли и воспаления – простагландинов. Осложнения, возникающие при приеме НПВП (прежде всего, со стороны ЖКТ), традиционно связываются с подавлением «физиологической» формы ЦОГ – ЦОГ-1, играющей важную роль в поддержании многих параметров гомеостаза человеческого организма, в т. ч. защитного потенциала слизистой оболочки [31, 32].
Тем не менее «физиологическая» ЦОГ-1 также принимает участие в развитии воспаления, и поэтому подавление ее активности в области повреждения (но не во всем организме!) может рассматриваться как положительный момент. Именно такое свойство имеет мелоксикам, обладающий умеренной селективностью в отношении ЦОГ-2, практически не влияющий на «физиологическую» ЦОГ-1 в слизистой оболочке желудка, но эффективно подавляющий ее в очагах воспаления. Важно то, что помимо основного действия (блокады ЦОГ), мелоксикам имеет ряд иных фармакологических свойств, позволяющих прогнозировать его высокую эффективность при лечении боли и воспаления: влияние на синтез важнейших провоспалительных цитокинов (интерлейкин-6, фактор некроза опухоли альфа), блокада синтеза металлопротеиназ, антигистаминное действие, снижение активности в очагах воспаления агрессивных клеток (макрофагов и нейтрофилов) и другие противовоспалительные механизмы [33–35].
6. Для борьбы с болевым и противовоспалительным синдромом при ППАТ желательно использовать внутримышечный способ введения лекарственного препарата – быстродействующий и оказывающий минимальное побочное воздействие на ЖКТ.
Альтернативой внутримышечным инъекциям НПВП с отрицательным воздействием на ЖКТ является применение их в виде ректальных свечей, хотя при этом также сохраняется риск развития гастропатий, но в меньшей степени. При назначении НПВП нужно оценить анамнез больного, факторы риска развития желудочно-кишечных заболеваний, рекомендовать рациональную диету, назначить медикаменты, защищающие слизистую желудка.
Для противовоспалительного лечения ППАТ желательно использовать Амелотекс (международное непатентованное название – мелоксикам) – нестероидный противовоспалительный препарат, относящийся к классу оксикамов, производных энолиевой кислоты, обладающий анальгетическим, противовоспалительным и жаропонижающим действием. Амелотекс селективно ингибирует ферментативную активность ЦОГ-2, подавляет синтез простагландинов в области воспаления в большей степени, чем в слизистой оболочке желудка или почках. Реже вызывает эрозивно-язвенные поражения ЖКТ по сравнению с другими НПВП.
Амелотекс выпускается в виде раствора для внутримышечного введения, в форме свечей, таблеткок и геля. В 1 ампуле (1,5 мл) содержится 15 мг активного вещества мелоксикама.
В начале лечения ППАТ, в острый период, желательно проведение курса внутримышечных инъекций Амелотекса по 1,5 мл 1 р./сут в течение 10–15 дней или ректальное использование Амелотекса – по 1 свече 1 р./сут на период воспаления и болей в течение 1–2-х недель. Далее, при сохранении клиники, возможен переход на пероральный прием препарата 15 мг в день. На период лечения ППАТ Амелотексом желательно использовать гель Амелотекс – нанесение на область поражения параартикулярных тканей 3–6 р./сут в течение 10–14 дней.
Таким образом, поражение параартикулярных тканей – собирательное понятие, включающее патологию энтезисов, связок, сухожилий мышц, параартикулярных сумок и т. п. В патогенезе развития поражений параартикулярных тканей лежат как травматические и дегенеративно-дистрофические, так и воспалительные механизмы. Комплексное лечение поражений параартикулярных тканей должно включать физические методы, оптимальный двигательный режим без травмирующих факторов, локальную стероидную терапию и терапию нестероидными противовоспалительными препаратами, в т. ч. различными формами Амелотекса. Амелотекс является препаратом выбора при противопоказаниях к приему НПВП, а также при неэффективности других методов лечения.
Главная проблема людей современного общества – это способность вести «независимую жизнь». Заболевания опорно-двигательного аппарата причиняют механические, физические, психологические и эстетические страдания. Сохранность органов движения является медицинской и социальной задачей. Большую долю заболеваний локомоторного аппарата составляют периартриты – поражения параартикулярных тканей (ППАТ) суставов.
Параартикулярные ткани представляют совокупность околосуставных структур и отдаленных от суставов тканей. Околосуставные ткани включают: сухожилия мышц и их влагалища, сумки, связки, фасции, апоневрозы. Отдаленные от суставов структуры составляют: мышцы, нервно-сосудистые образования, подкожно-жировая клетчатка [1].
Среди ППАТ выделяют:
• теносиновит – воспаление сухожильного влагалища;
• тендинит – воспаление сухожилия;
• бурсит – воспаление синовиальной сумки;
• энтезопатию (энтезит) – воспаление энтезиса – места прикрепления сухожилия или связки к кости или суставной капсуле;
• капсулит – поражение капсулы сустава;
• фасциит, апоневрозит – поражение фасций и апоневрозов;
• миофасциальный болевой синдром – изменения в скелетной мышце и прилегающей фасции.
Neipel в 1966 г. впервые использовал термин «энтезопатия», J. Ball в 1971 г. сообщил о высокой частоте энтезопатий при анкилозирующем спондилите. В 1991 г. признано, что энтезопатии являются отличительной патогенетически значимой характеристикой спондилоартропатий. Особенно это касается энтезопатий пяточных областей (энтезиты ахиллова сухожилия, подошвенного апоневроза, ахиллотендинит, бурситы и др.), которые обычно сочетаются с периферическим суставным синдромом, но в ряде случаев являются единственным или доминирующим по тяжести поражением опорно-двигательного аппарата при спондилоартритах.
В энтезисах волокна сухожилия или связки перед тем, как перейти в костную структуру, становятся более компактными, затем хрящевыми, и, наконец, кальцифицированными. Питание энтеза происходит посредством анастомозов через оболочки сухожилий – перитенон, перихондрий или периост. Энтезы являются метаболически активными и имеют хорошо развитую иннервацию.
Именно область энтезиса становится «слабым звеном» в аппарате околосуставных тканей, где при чрезмерной нагрузке возникают микро- и макроскопические повреждения, приводящие в последующем к локальному воспалению [2, 3].
Воспаление приобретает важную роль как при энтезопатиях, так и при других ППАТ, лежит в основе обострения ППАТ, усиливает дегенерацию тканей. Воспаление в энтезисе не ограничивается соединительной тканью (например, тендинит или фиброзит). Отмечается также вовлечение в патологический процесс хряща и кости, что приводит первоначально к возникновению периостита, а в дальнейшем к появлению эрозий кости.
За рубежом ревматические поражения мягких тканей объединяются термином «внесуставной ревматизм» (non-articular rheumatism) или «ревматизм мягких тканей» (soft tissue rheumatism).
Бедро
ППАТ в бедренной области носят разнообразный характер и представлены в основном теномиозитами мышц бедра, которые нередко протекают в безболевой форме и характеризуются щелчками при движении, слышимыми на расстоянии. Болевой синдром присутствует при энтезопатиях большого вертела бедренной кости, воспалительных явлениях в синовиальных сумках пояса нижних конечностей.
Больные разного возраста жалуются на щелчки в области тазобедренного сустава (боль при этом обычно отсутствует). Больной сам показывает движения, при которых возникают щелчки. Данная клиника обусловлена: трением подвздошно-большеберцового тракта о большой вертел, трением сухожилия подвздошно-поясничной мышцы о подвздошно-лобковое возвышение, трением большой ягодичной мышцы о большой вертел, а также нестабильностью тазобедренного сустава. Данный симптом встречается при аномалиях развития, дисплазиях соединительной ткани структур бедра, дегенеративно-дистрофических процессах, травмах и др.
Визуализационные методы исследования (рентген, УЗИ, МРТ), помимо обнаружения дисплазий и других изменений в тазобедренном суставе, редко способствуют постановке диагноза. Уточнению данного вида ППАТ способствуют хорошо собранный анамнез, оценка объема и характера движений в тазобедренном суставе и в поясничной области, тщательная пальпация. Основное лечение состоит в том, чтобы успокоить больного, разъяснить суть заболевания, назначить упражнения для разработки мягкотканных структур, заинтересованных в формировании щелчков, под контролем методиста ЛФК. Возможно физиолечение, использование мягких ортезов на пояснично-бедренную область.
В области бедра встречаются болевые синдромы, вызванные поражением сухожильно-связочных и мышечных структур.
Тендинит подвздошно-поясничной мышцы – характеризуется болью в верхней части бедра, затрудняющей ходьбу. При этом встречается ограничение разгибания из-за боли в паху и спине. Отмечаются болезненность при сгибании бедра, болезненные щелчки во время полного разгибания тазобедренного сустава. Возможна боль в брюшной полости. Часто боль локализуется ниже паха, что соответствует месту прикрепления мышцы к малому вертелу бедра. Пальпаторно через переднюю брюшную стенку могут обнаруживаться болезненно уплотненные мышцы. При данном ППАТ возможно ущемление кожного бедренного нерва – невралгия Бернгардта–Рота, сопряженная с онемением и парестезией по наружной поверхности бедра.
Синдром мышцы, натягивающей широкую фасцию бедра – характеризуется появлением боли и дискомфорта при перекидывании пораженной ноги на здоровую. Спонтанная боль возникает редко (может быть ощущение «вбитого гвоздя» в области крыла подвздошной кости).
При положении пациента на боку, при слегка согнутой в тазобедренном и коленном суставах ноги, находящейся сверху, хорошо пальпируется выступающая сверху область большого вертела бедренной кости. Возникающий болевой синдром при этом расценивается как трохантерит. Варианты трохантеритов обычно включают в себя: энтезит большого вертела и более редко встречающийся бурсит вертельной сумки. Причинами трохантерита являются врожденные или приобретенные нарушения строения таза или ног, большие механические нагрузки, травмы, переохлаждение, излишек веса тела, особенно возникший за короткий срок. Часто причину установить не удается.
Энтезит большого вертела – частая причина болей в области бедра. Это заболевание осложняет течение остеоартроза у женщин 40–60 лет, но может протекать и без коксартроза. Проявляется болями, иррадиирующими по наружной поверхности бедра. Типичная жалоба больного – невозможность лежать, особенно спать на боку поражения. Имеет место отчетливая локальная болезненность области большого вертела, сохранность объема пассивной ротации в тазобедренном суставе и боль при сопротивлении активному отведению бедра. Если боль при этом усиливается при движении, ходьбе, то мы имеем дело с энтезопатией отводящих мышц. Постоянная боль указывает на вертельный бурсит.
В отличие от коксартроза трохантерит имеет характерные болевые точки при пальпации. При трохантерите нет ограничения движений в тазобедренном суставе, как пассивных, так и активных. Данные рентгеновского исследования позволяют дифференцировать признаки коксартроза с проявлениями энтезитов в области большого вертела бедренной кости.
Бурситы бедренной области встречаются реже патологии энтезисов, сухожилий и связок данной области. Чаще всего воспаляются следующие сумки тазовой области: вертельная сумка (вursa trochanterica), подвздошно-гребешковая сумка (вursa iliopectinea) и седалищная сумка (вursa ischiadica) [5].
Вертельный бурсит – развивается чаще, чем другие виды бурситов бедра. Вертельная сумка находится возле большого вертела бедренной кости. Вертельный бурсит развивается чаще у профессиональных спортсменов. Чаще заболевают женщины. Предрасположенность женщин к заболеванию вертельным бурситом объясняют особенностями строения женского таза. Женский таз шире, и большой вертел отстоит дальше от средней линии тела, что способствует более сильному трению мышц об него [6].
Основным симптомом являются боли в области большого вертела (по боковой поверхности бедра). Ходьба, различные движения и лежание на боку поражения усиливают боль. Начало вертельного бурсита может быть внезапным, но чаще носит медленно прогрессирующий характер. Беспокоят боли при сгибании бедра, при вставании со стула и при подъеме по лестнице. Особенно сильно беспокоят ночные боли – когда пациенты переворачиваются или лежат на больной стороне, эти боли будят их.
Если попросить показать участок наибольшей болезненности, больной точно указывает на область большого вертела. Если бы действительно была боль в суставе, больной указывал бы на паховую область.
Наилучшим способом диагностики вертельного бурсита служит пальпация области большого вертела для выявления локальной болезненности. Осмотр проводят в положении больного лежа на здоровом боку, со слегка согнутой в тазобедренном суставе и колене ногой. Надавливание на большой вертел вызывает резкую боль, нередко иррадиирующую по наружной стороне бедра в поясницу.
Подвздошно-гребешковый бурсит – второе по частоте развития заболевание среди воспалений сумок бедра. Подвздошно-гребешковая сумка располагается спереди от пояснично-подвздошной мышцы. При накоплении в ней значительного количества экссудата она может определяться в паху в виде опухолевидного образования. В связи с тем что подвздошно-гребешковая сумка находится очень близко к суставу, картина ее воспаления очень напоминает воспаление самого тазобедренного сустава. Основным симптомом этого вида бурсита является болезненность и отечность передневнутренней части бедра ниже уровня паховой связки, боль усиливается при разгибании бедра. Сдавление растянутой сумкой бедренного нерва может приводить к появлению болей и парестезий в бедре.
Седалищный бурсит (синдром «сидящего портного») – развивается при сидении на твердой поверхности, особенно у худых людей. Седалищная сумка располагается в непосредственной близости к седалищному бугру. Возможна энтезопатия этой области, которая встречается как в рамках какого-либо спондилоартрита (реактивный артрит, болезнь Бехтерева), так и самостоятельно. Седалищный бугор испытывает нагрузку в положении человека сидя, особенно на жестком основании. Типична жалоба больного на боль именно в этом положении, в меньшей степени при ходьбе. Боль при седалищном бурсите, в отличие от подвздошно-гребешкового, усиливается при сгибании бедра.
Колено
В области коленного сустава ППАТ представлены наиболее часто бурситами, энтезопатиями и теносиновитами.
Препателлярный бурсит – бурсит преднадколенниковой сумки («колено паркетчика»). Воспаленная преднадколенниковая сумка расположена поверх надколенника и не связана с полостью коленного сустава. Воспаление ее встречается нечасто, вызывается повторной травмой или нагрузкой при длительном нахождении на коленях. Характеризуется флуктуирующей припухлостью, отеком, невыраженным болевым синдромом, возможным местным повышением температуры, гиперемией кожи. Может инфицироваться, особенно при повреждении кожи.
Рецидивов бурсита можно избежать, исключив этиологический фактор (защита коленного сустава при хронической травме с помощью ортеза). При инфицировании препателлярной сумки, что является следствием острой травмы и нарушения целостности кожных покровов в передней части коленного сустава, отмечается припухлость, резкая, дергающая боль в преднадколенниковой области, усиливающаяся при пальпации. Визуально там же отмечается гиперемия, гипертермия кожных покровов. В этом случае содержимое бурсы включает гной и больной должен лечиться как пациент с гнойным процессом.
Киста Бейкера (КБ) – растянутая жидкостью синовиальная сумка подколенной ямки, расположенная в ее медиальном отделе между внутренней головкой икроножной и полуперепончатой мышц и сообщающаяся с коленным суставом посредством соустья.
Наиболее признан клапанный механизм проникновения суставной жидкости через соустье из полости коленного сустава в КБ, когда обратный ток жидкости из КБ в суставную полость затруднен [7]. В 1877 г. W.M. Baker отметил тесную взаимосвязь наличия внутрисуставных повреждений и заболеваний коленного сустава с развитием подколенных кист.
КБ в большинстве случаев возникает как вторичное заболевание. Причинами ее возникновения являются синовиты сустава (остеоартроз, ревматоидный артрит и др.), посттравматические состояния коленного сустава. КБ при малых размерах обычно протекает безболезненно, она не видна невооруженным глазом, пальпация ее затруднительна. На фоне симптомов поражения коленного сустава клиника КБ отсутствует.
При больших размерах КБ видна визуально и легко пальпируется как плотноэластическое опухолевидное образование продолговато-яйцевидной формы, локализующееся в мягких тканях подколенной области, преимущественно в медиальных отделах подколенной ямки (рис. 1). При значительных размерах КБ может частично препятствовать сгибанию в коленном суставе. Пациенты с крупной КБ ощущают тяжесть по задней поверхности сустава при физических нагрузках, чувство дискомфорта, наличие опухолевидного образования в подколенной ямке. Симптомокомплекс может включать боль в икроножных мышцах или нарушение чувствительности по задней поверхности голени, особенно после длительной ходьбы или во время подъема и спуска по лестнице. Все эти симптомы могут быть изолированными, но чаще сочетаются с клиникой внутрисуставной патологии коленного сустава, присутствующей при этом [8–10].
Возможна резорбция жидкости из КБ с обратным развитием ее до полного исчезновения. Такой доброкачественный исход характерен для кист, образовавшихся недавно, обычно после чрезмерных механических перегрузок коленных суставов в процессе строительных работ, спортивных состязаний, интенсивного труда на дачных участках и т. д. В случае стойкого синовита коленного сустава КБ приобретает хроническое течение. При хроническом течении КБ жидкость подвергается частичной резорбции, что приводит к ее сгущению и затрудняет ее аспирацию из полости кисты. При длительном течении в КБ скапливается фибрин, образуются перемычки, септы, дочерние.
Обычно КБ протекает доброкачественно, лишь психологически пугая больных. Однако при быстром накоплении выпота в подколенной сумке возможен разрыв КБ с распространением суставной жидкости по задним межфасциальным пространствам голени. Клиника острого разрыва КБ напоминает картину тромбоза вен голени (отек голени, распирающие боли). После прорыва выпот из коленного сустава и самой КБ исчезает.
Возможно нагноение КБ, которое клинически напоминает тромбофлебит поверхностных вен голени и характеризуется возникновением на фоне суставного анамнеза выпотом и болью в подколенной ямке, гиперемией, гипертермией данной области, а также ознобом, лихорадкой, изменением формулы крови.
Использование УЗИ и МРТ позволяет установить наличие КБ, ее топографическое расположение в подколенной ямке, визуализировать контуры и содержимое кисты, проследить ее границы и протяженность, определить связь кисты с полостью сустава, выявить признаки разрыва и воспаления стенки, повреждения внутрисуставных структур, остеоартроза, артрита коленного сустава. УЗИ подколенной области необходимо не только для диагностики КБ, но и для выявления часто встречаемых патологических состояний: тромбоза (тромбофлебита) глубоких вен, аневризмы бедренной и подколенной артерии, абсцесса, опухоли, разрыва мышц и др.
Нередко страдает связка надколенника, которая несет большую функциональную нагрузку, являясь связующим звеном между квадрицепсом и голенью, принимая участие в разгибании коленного сустава. Надколенник при этом рассматривается как сесамовидная кость. Повреждение связки надколенника возникает при механических нагрузках и травмах обычно в местах соединения связки (в виде энтезопатии) с нижним краем надколенника («колено прыгуна») и большеберцовой костью («колено футболиста»).
«Колено прыгуна» – «верхний» лигаментит связки надколенника. Причиной заболевания служит механическая перегрузка коленного сустава, которая может быть как внезапной, так и хронической. Наиболее часто лигаментит надколенника развивается в результате неадекватного напряжения квадрицепса. «Колено прыгуна» чаще всего наблюдается у теннисистов, легкоатлетов, футболистов, баскетболистов, волейболистов. Предрасполагающим фактором обычно являются длительные прыжки на твердом покрытии.
Клиническая картина складывается из боли, припухлости и болевого ограничения подвижности. Боль, локализующаяся ниже надколенника, усиливается при пальпации и в положении сидя. Визуально в данном месте определяется небольшая припухлость. Отмечается ограничение подвижности в коленном суставе и ощущение утраты его силы.
Болезнь Осгуда–Шлаттера (Osgood–Schlatter’s disease) – можно рассматривать в узком смысле как «нижний» лигаментит связки надколенника, представляющий из себя энтезопатию. Обычно и традиционно болезнь Осгуда–Шлаттера рассматривается как хондропатия – периостит и воспаление бугристости большеберцовой кости. Причинами «колена футболиста» могут быть периодические незначительные травмы этого участка, часто возникающие у мальчиков в подростковом возрасте при физической активности.
Клиника болезни Осгуда–Шлаттера типична: наиболее часто она начинается с нерезких болей в области бугристости большеберцовой кости, которые появляются только при значительной физической нагрузке. С прогрессированием заболевания боли возникают уже при меньших нагрузках. В редких случаях боль появляется и в покое. Отличительным признаком болей при болезни Осгуда–Шлаттера является их усиление в области бугристости большеберцовой кости при напряжении четырехглавой мышцы бедра и при стоянии больного на коленях. Патогномоничным симптомом выступает локальная болезненность, от незначительной до сильной, при пальпации и/или перкуссии области бугристости большеберцовой кости. Пальпация других прилегающих областей, как правило, безболезненна. Амплитуда движений в коленном суставе не изменяется. Рентгенологически при хроническом течении болезни Осгуда–Шлаттера отмечается костная перестройка с кистовидной перестройкой и фрагментацией бугристости большеберцовой кости. При недолгом (остром) течении процесса в виде энтезопатии рентгенологически патологию можно не выявить [11].
Энтезопатия и теномиозит «гусиной лапки» – нередкий вариант ППАТ области коленного сустава. «Гусиная лапка» (pes anserinus) представляет собой место прикрепления к большеберцовой кости сухожилий портняжной (m. sartorius), тонкой (m. gracilis) и полусухожильной (m. semitendinosus) мышц. Анатомически находится на 3–4 см ниже проекции щели коленного сустава по медиальной его поверхности. Данное ППАТ часто осложняет течение гонартроза, в иных случаях наблюдается при здоровом коленном суставе. Заболевание развивается часто у людей, которые много времени проводят на ногах, например у спортсменов-бегунов.
Типичны жалобы больного на боль при ходьбе. Больной указывает пальцем болезненную точку. Отмечается усиление боли при сгибании и разгибании коленного сустава. При осмотре определяется резкая пальпаторная болезненность площадью 3–4 кв. см. Часто симптомы энтезопатии беспокоят пациента значительно больше, чем проявления собственно гонартроза.
Анзериновый бурсит – встречается реже теномиозита «гусиной лапки», наблюдается у женщин старше 55—60 лет, страдающих гонартрозом. У большинства из них отмечаются избыточная масса тела, деформация коленных суставов. Как правило, у этих больных, помимо жалоб, характерных для гонартроза (боли в суставах, усиливающиеся при нагрузке и к концу дня), присутствуют также жалобы на боли, возникающие ночью при давлении одного колена на другое и вынуждающие менять положение ног. У всех этих больных имеется выраженная локальная болезненность в анзериновой области при пальпации. Возможна визуально заметная деформация – припухлость данной области. При УЗИ бурсит «гусиной лапки» легко диагностируется в виде анэхогенного скопления жидкости.
Стопа
Сложное строение стопы и голеностопного сустава обеспечивает удержание тела человека в вертикальном положении. Имея сводчатое строение, стопа выполняет опорную и рессорную функции. Свод стопы фиксируется продольными и поперечными стяжками, а также подошвенным апоневрозом. Многочисленные мышцы стопы относятся к активным стяжкам, которые прикрепляются на разных уровнях стопы. Сухожилия служат «мостиками» между костями и мышцами стопы, которые плотно к ним крепятся. В тех случаях, когда мышечно-скелетная система ног подвергается значительным нагрузкам, связки стопы травмируются.
Среди причин, которые могут вызвать развитие тендинитов стопы, выделяют: чрезмерные физические нагрузки на стопу, механическое повреждение и травму, патологию строения скелета, плоскостопие, неправильную осанку, систематическое ношение обуви с высоким каблуком, привычный подвывих стопы, возрастные отклонения, дегенеративно-дистрофические нарушения в тканях стопы, заболевания суставов (ревматоидный артрит, подагра и др.), нарушение обмена веществ. По причине высокой частоты встречаемости тендинитов и энтезитов стопу называют «энтезитным органом».
Ахиллодиния, или тендинит ахиллова сухожилия – состояние, часто встречающееся при спондилоартритах. Грубое поражение ахиллова сухожилия можно увидеть у больных с синдромом гипермобильности суставов с выраженным плоскостопием, как правило, в возрасте старше 30 лет. При ахиллодинии возникают отечность и боли при нагрузке в области дистальной части сухожилия и/или в месте прикрепления сухожилия к пяточной кости. В последнем случае боли могут быть связаны с бурситом заднетаранной сумки, которая здесь располагается. Боли наиболее выражены при ходьбе и длительном стоянии.
Сгибание и разгибание стопы усиливает боль. Область наибольшей болезненности находится в месте соединения сухожилия с пяточной костью и на 2–3 см проксимальнее. Сухожилие в указанной области отечно и утолщено. Может случиться спонтанный разрыв сухожилия, который характеризуется внезапным возникновением сильной боли по задней поверхности стопы, особенно во время дорсального сгибания.
Тендинит задней большеберцовой мышцы – воспаление сухожилия задней большеберцовой мышцы и его влагалища. Место наибольшей болезненности при этом располагается на медиальной поверхности голеностопного сустава. Боль и отек отмечаются по ходу сухожилия. Боль усиливается при подворачивании стопы внутрь, при пальпации и перкуссии области медиальной лодыжки. Данное ППАТ часто сочетается с туннельным синдромом большеберцового нерва, расцениваемым, как синдром тарзального канала. Под медиальной лодыжкой вместе с сухожилиями задней большеберцовой мышцы и мышц-сгибателей пальцев проходит большеберцовый нерв. Теносиновит указанных мышц с сопутствующим расширением сухожилий приводит к механическим симптомам сдавления и ишемии большеберцового нерва, что проявляется болями, парестезиями и онемением, распространяющимися по медиальной части стопы. При диагностике используют симптом Тинеля и манжеточный тест [12].
Тендинит малоберцовых мышц – под латеральной лодыжкой наблюдается (как изолированно, так и при сопутствующих воспалительных артропатиях) утолщение колбасовидной формы по ходу сухожильного влагалища перонеальных мышц. При ходьбе и пальпации этой области возникает боль.
Подошвенный (плантарный) фасциит (ПлФ) – заболевание, обусловленное воспалительно-дегенеративными изменениями подошвенной фасции. Клиническим признаком ПлФ является боль в подошве, и особенно в пятке. Боли в пяточной области обычно возникают и/или усиливаются при нагрузке. Болевые ощущения более выражены в утренние часы. При выраженном процессе боли распространяются по всей подошвенной поверхности стопы, усиливаются при давлении на низ стопы (при ходьбе, беге, пальпации). Боль ощущается сильнее при первых шагах, после вставания с постели. Постоянная микротравматизация фасции может послужить причиной хронического асептического воспаления с болевым синдромом. Диагностике ПлФ способствуют анализ жалоб пациента, физикальный осмотр, рентгенография, УЗИ, МРТ.
На фоне ПлФ, в качестве компенсаторной реакции, возможно образование краевых костных разрастаний (остеофитов), получивших название «пяточных шпор» (ПШ). ПШ представляют собой депозиты кальция на нижней части пяточной кости. ПШ нередко ассоциированы с ПлФ. ПШ на задней части пяточного бугра нередко ассоциированы с воспалением ахиллова сухожилия (тендинитом) и могут быть причиной болезненности и болей в задней части пятки, усиливающихся при сгибании стопы.
ПШ анатомически располагаются в месте энтезиса – по ходу прикрепления подошвенной фасции или ахиллова сухожилия к пяточной кости.
Важно отметить, что ПШ могут не вызывать никаких симптомов вообще и случайно обнаруживаются во время рентгенологического обследования. ПШ преимущественно страдают люди старше 40 лет, причем больше к этому заболеванию предрасположены женщины. ПШ часто наблюдаются у пожилых людей, т. к. инволюционные изменения в тканях приводят к снижению эластичности подошвенной фасции. Другие факторы развития ПШ: избыточный вес, ожирение, длительное нахождение на ногах, плоскостопие или, наоборот, высокий свод стопы, плохо подобранная или изношенная обувь, метаболические нарушения.
В большинстве случаев пациенты жалуются на интенсивную, очень резкую боль в пятке во время ходьбы. Характерным симптомом ПШ являются так называемые «стартовые» боли – возникающие в утренние часы или после длительного сидения. Причиной боли служит травмирование мягких тканей шпорой.
Рентгенологически выявляется наличие костного выроста по подошвенной или задней поверхности пяточной кости. Этот вырост имеет вид шипа и может сопровождаться периоститом, эрозиями пяточной кости. На ранних стадиях возможно рентгенологическое отсутствие костного шипа. В этом случае причиной болей выступают воспалительные изменения (плантарный фасциит или подпяточный бурсит). Рентгенологическое обнаружение и размер ПШ не всегда коррелируют с выраженностью болевого синдрома. Крупные ПШ могут существовать безболезненно ввиду адаптации перифокальных тканей к болевым раздражителям.
Отсутствие пяточной шпоры в совокупности с пяточной болью требует дифференциального диагноза, в первую очередь с системными воспалительными заболеваниями (ревматоидный артрит, синдром Рейтера и др.), которые также могут дебютировать пяточной болью.
Подошвенный фасциальный фиброматоз, или синдром Леддерхозе (СЛ) – фиброматоз невоспалительного характера. СЛ аналогичен и нередко сочетается с контрактурой Дюпюитрена. Данное ППАТ проявляется локальными утолщениями подошвенной фасции. Вначале заболевание не доставляет страданий, однако в конечных стадиях подошвенная фасция утолщается, стягивается, приводя к сгибательной контрактуре пальцев. Ходьба при этом становится болезненной. У части пациентов симптомы возникают на обеих стопах.
Пальпаторно плотные, безболезненные, округлые и в виде жгутов узлы при СЛ наиболее часто присутствуют около самой высокой точки поперечного свода стопы. Узелки обычно безболезненны, и боль возникает лишь при трении их об обувь или пол. При УЗИ и МРТ выявляется инфильтрирующая масса в апоневрозе рядом с подошвенными мышцами, позволяющая выявить степень повреждения.
Относительно факторов риска СЛ следует отметить, что заболевание нередко носит семейный характер, чаще встречается у мужчин, сочетается с ладонным фиброматозом, болезнью Пейрони, эпилепсией, сахарным диабетом. Обсуждается связь с алкоголизмом, курением, заболеваниями печени, щитовидной железы, напряженной работой с нагрузкой на ноги.
На ранних стадиях лечения рекомендуется избегать прямого давления на узелки, применять мягкие стельки, супинаторы в обуви. На поздних стадиях СЛ используются хирургические методы лечения со сложным прогнозом, т. к. очень близко расположены сухожилия, нервы и мышцы. Так же как и при контрактуре Дюпюитрена, часто развиваются рецидивы болезни. Стопа испытывает нагрузку всего тела, что приводит к нередким постоперационным осложнениям.
Лечение
В лечении ППАТ главенствующим условием является исключение провоцирующих факторов, прежде всего механических перегрузок. Необходимо ограничение механической нагрузки на структуры, которые вовлечены в конкретное поражение. При выраженном воспалении их показан полный покой с использованием ортезов, лангет в острый период заболевания. Двигательный режим, лечебная физкультура, массаж, мануальная терапия должны носить механически щадящий характер и осуществляться в безболевой зоне.
Локальная инъекционная терапия, прежде всего глюкокортикоидами (ГК) с учетом анатомо-морфологических особенностей ППАТ, показаний, противопоказаний, правильно выбранной дозы ГК, числа и кратности введения, позволяет добиться хороших клинических результатов в лечении ППАТ.
Также используются анальгетики, слабые опиоиды, миорелаксанты, седативные препараты. При стихании острого процесса используются физические методы: тепло и криотерапия, магнито-, лазеротерапия, электро- и фонофорез, грязевые аппликации, бальнеолечение. Применяются ударно-волновая терапия и методы психической релаксации. В случае возникновения ППАТ на фоне ревматических болезней необходимо лечение основного заболевания.
ППАТ как частный вид скелетно-мышечных болезней независимо от этиологии во многом обусловлены едиными патогенетическими закономерностями, определяющими появление и переход заболевания в хроническое состояние. Эффективное купирование болевого синдрома – первоочередная задача фармакотерапии ППАТ, т. к. боль представляет наиболее тягостное ощущение, определяющее тяжесть страданий и снижение качества жизни пациента [13].
Противовоспалительные средства являются непременным условием терапии ППАТ, включая прежде всего нестероидные противовоспалительные препараты (НПВП) локального (накожного) и системного (перорального, ректального и внутримышечного) применения. Лечебная эффективность и переносимость различных НПВП у каждого пациента индивидуальны, и при назначении НПВП необходим строго персональный подход с оценкой эффективности и побочных действий применяемого препарата [14, 15].
Для противовоспалительного и обезболивающего действия желательно использовать Амелотекс (международное непатентованное название – мелоксикам) – НПВП, относящийся к классу оксикамов, производных энолиевой кислоты, обладающий анальгетическим, противовоспалительным и жаропонижающим действием. Мелоксикам преимущественно ингибирует ферментативную активность ЦОГ-2, подавляет синтез простагландинов в области воспаления в большей степени, чем в слизистой оболочке желудка или почках, реже вызывает эрозивно-язвенные поражения ЖКТ по сравнению с другими НПВП. Мелоксикам имеет ряд иных фармакологических свойств, позволяющих прогнозировать его высокую эффективность при лечении боли и воспаления: влияние на синтез важнейших провоспалительных цитокинов (интерлейкин–6, фактор некроза опухоли α), блокада синтеза металлопротеиназ, антигистаминное действие, снижение активности агрессивных клеток (макрофагов и нейтрофилов) в очагах воспаления и др. [16–18].
Амелотекс выпускается в виде раствора для внутримышечного введения, свечей, таблеток и геля. Одна ампула (1,5 мл) содержит в качестве активного вещества 15 мг мелоксикама.
Для купирования болевого и воспалительного синдрома при ППАТ желательно использовать внутримышечный способ введения лекарственного препарата ввиду быстрого лечебного эффекта и минимального побочного воздействия на ЖКТ. При невозможности внутримышечных инъекций, во избежание отрицательного воздействия на ЖКТ возможно альтернативное назначение НПВП в виде ректальных свечей (при этом снижается риск развития гастропатий).
В начале лечения, в острый период, желательно проведение курса внутримышечных инъекций Амелотекса по 1,5 мл 1 р./сут 10–15 дней или ректальное использование Амелотекса по 1 свече 1 р./сут на протяжении 1–2-х недель. Далее при сохранении клиники возможен переход на пероральное применение – 15 мг/сут. На период лечения ППАТ Амелотексом желательно использовать гелевую форму препарата: наносить на область поражения параартикулярных тканей 3–6 р./сут в течение 10–14 дней.
Таким образом, к лечению ППАТ необходим дифференцированный подход, т. к. данные заболевания носят собирательный характер и включают патологию энтезисов, связок, сухожилий мышц, параартикулярных сумок и т. п. В патогенезе развития ППАТ лежат различные травматические, воспалительные и дегенеративно-дистрофические механизмы. Лечение ППАТ должно проводиться комплексно, с исключением травмирующих факторов, упорядоченным двигательным режимом, с физическими методами, локальной инъекционной стероидной терапией, а также НПВП, включая различные формы Амелотекса. Амелотекс является препаратом выбора при наличии относительных противопоказаний к приему НПВП, а также при неэффективности других методов лечения.
О дифференциальной диагностике суставного синдрома можно почитать тут.
Теги: Лечение заболеваний суставов
234567 Начало активности (дата): 18.05.2017 12:46:00
234567 Кем создан (ID): 982
234567



