 21.01.2016
21.01.2016
Радионуклидная оценка остеогенеза при замещении дефектов костей нижней конечности у больных с гигантоклеточной опухолью
В настоящее время для замещения дефектов после удаления гигантоклеточной опухоли используется метод чрескостного
остеосинтеза, так как он позволяет управлять перемещением костных фрагментов и их фиксацией, надежно восстанавливать анатомо-функциональные параметры конечности с учетом предполагаемых нагрузок.
В настоящее время для замещения дефектов после удаления гигантоклеточной опухоли используется метод чрескостного
остеосинтеза, так как он позволяет управлять перемещением костных фрагментов и их фиксацией, надежно восстанавливать анатомо-функциональные параметры конечности с учетом предполагаемых нагрузок. Решение
этого вопроса представляет собой большую социальную проблему в связи с чем мы решили поделиться своими результатами по использованию радионуклидных методов исследования для диагностики состояния и оценки активности
репаративного остеогенеза.
Данные исследования впервые проведены нами у 14 больных в возрасте от 10 до 56 лет.
Среди них с опухолью бедренной кости – 8, большеберцовой – 6. У 8 пациентов опухоль локализовалась в области дистального суставного конца бедренной кости .
Всем больным выполнена сегментарная резекция пораженного участка кости с соблюдением принципов онкологического радикализма.Замещение дефекта производили с использованием методик чрескостного остеосинтеза. В удлиняемом
отломке формировали один или два дистракционных регенерата. Протяженность их составила от 6 до 10 см, а суммарная величина замещенного дефекта – 6-14 см.
Для оценки протяженности поражения кости,объема оперативного вмешательства и активности репаративного костеобразования в процессе замещения дефекта костной ткани у больных с гигантоклеточной опухолью нами использован метод остеосцинтиграфии; ее проводили на компьютерном томографе.
В процессе исследования выделяли две фазы: сосудистую и костную. В сосудистую –регистрировали время поступления меченого технефора и наличие гиперваскулярных зон. В костную строили профильные кривые, позволяющие определять накопление препарата в области формирования регенерата и в остальных участках кости.
Для оценки содержания минеральных веществ в регенерате и, следовательно, прочности его, использовали метод двуфотонной абсорбциометрии и созданный на его основе дихроматический костный денситометр фирмы "Норланд" (США). При расшифровке механизмов,лежащих в основе костеобразования, методом радиоиммунологического анализа определяли концентрацию остеотропных гормонов, а циклических нуклеотидов- радиоконкурентным методом.
Контролем служили эти же показатели, но полученные при замещении посттравматических дефектов кости. Сроки наблюдения были аналогичными. Показатели исследуемой группы сравнивали с показателями контрольной.
Статистическая обработка результатов исследования проведена по критерию Стьюдента.
При замещении дефекта после удаления опухоли в период дистракции и фиксации накопление меченого технефора больше в регенерате, что указывает на то, что в нем много незрелого коллагена и меньше содержание минеральных веществ. Сравнение данных на этих стадиях остеосинтеза показало, что процесс регенерации у онкологических больных протекает медленее.
Динамика минерализации на этапах остеосинтеза представлена на рис.3. Насыщение регенерата минеральными веществами у онкологических больных происходило медленее, а величины, близкие к норме, при замещении
дефекта после резекции опухоли наблюдали на 1 месяц позже.
В связи с различиями в минерализации регенератов в контроле и у онкологических больных нас заинтересовал вопрос о причинах этого явления. Поэтому была изучена концентрация следующих гормонов в крови: паратирина, кальцитонина, соматотропина.
При определении концентрации паратирина выявлено, что у онкологических больных его больше на этапах остеосинтеза. Различия становились недостоверными только с 100-го дня фиксации аппаратом.
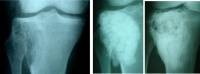
Паратирин, наряду с деминерализацией, вызывает резорбцию органического матрикса. Как следствие этого на рентгенограммах были видны проявления остеопороза.
Существенно меньшей в процессе дистракции и первой половине фиксации оказалась концентрация кальцитонина в исследуемой группе больных . Кальцитонин тормозит активность остеокластов, усиливает насыщение регенерата минеральными веществами и ослабляет распад коллагена, способствуя увеличению массы регенерата. Это доказано с помощью меченого пирофосфата . В связи с меньшей концентрацией кальцитонина у онкологических больных формирование и структурная перестройка регенерата происходила медленее.
Содержание соматотропина в течение первых двух месяцев дистракции возрастало, но было ниже, чем в контрольной группе.
В связи с тем, что уменьшена концентрация паратирина и соматотропина пролиферация костномозговых клеток, в том числе и остеогенных, происходит медленее, что доказано в наблюдениях с меченым серным коллоидом .
Клетки – предшественники медленее превращаются в остеобласты, снижена их биосинтетическая активность.
С учетом изложенного было интересно получить представление об активности клеточной пролиферации по отношению циклического аденозинмонофосфата (цАМФ) к циклическому гуанозинмонофосфату (цГМФ).
Обнаружено первоначальное повышение концентрации цАМФ, что отражало напряжение адренергетических механизмов. Это одна из первых ответных реакций организма на травму.
При этом ингибируется деление клеток, замедляется прохождение их через фазу митоза .
При увеличении цГМФ подключались холинергические механизмы, повышающие устойчивость организма к травме. Он инициировал пролиферацию, а также цепь реакций, ведущих к митозу. Поэтому уменьшение отношения цАМФ/цГМФ характеризует активность репаративного процесса.
В наших наблюдениях активная регенерация по величине этого отношения начиналась одновременно в обеих группах при значениях меньше единицы и была однонаправленной, однако у онкологических больных более низкие значения сохранялись дольше (в течение всего периода дистракции), следовательно, длительнее протекал процесс органотипической перестройки регенерата.
Таким образом, репаративный процесс при замещении дефекта методом чрескостного остеосинтеза после удаления гигантоклеточной опухоли протекает аналогично, но менее интенсивно, чем у больных с посттравматическими
дефектами костей нижней конечности.
Проведенное нами исследование позволило определить дополнительные критерии в обосновании целесообразности применения метода чрескостного остеосинтеза в ортопедическом лечении больных онкологического профиля.
Теги: конечность, опухоль, остеосинтез
234567 Начало активности (дата): 21.01.2016 18:14:00
234567 Кем создан (ID): 645
234567 Ключевые слова: конечность, опухоль, остеогенез
12354567899



